MOFs材料研究進展
屈靜 李秦偉

摘 ?????要:金屬有機框架化合物MOFs材料,由金屬中心與橋連配體構成。構成框架的金屬中心及有機配體同簡單的配合物、高分子聚合物相比,有著非常顯著的差異,因此,MOFs材料的物理化學性質根據金屬中心和有機配體的變化而具有明顯的多樣性。概述了MOFs材料的產生過程,總結了MOFs材料的多孔性、大的比表面積、結構的多樣性及具有不飽和金屬配位點的特點,綜述了其在燃氣存儲、熒光性能方面的研究進展,并概述了其在其他領域的研究進展。
關 ?鍵 ?詞:MOFs; 多孔; 燃氣; 熒光性能
中圖分類號:TB383 ??????文獻標識碼: A ??????文章編號: 1671-0460(2019)04-0819-06
Abstract: Metal-organic frameworks, MOFs materials are composed of metal centers and bridged ligands. The metal centers and organic ligands in the frameworks are significantly different from those of simple inorganic complexes or organic polymers, therefore, the physical and chemical properties of MOFs materials have obvious diversity according to the change of metal centers and organic ligands. In this paper, the production process of MOFs materials was outlined. Characteristics of MOFs materials were summarized, such as porous property, large specific surface area, the diversity of structure and unsaturated metal coordination sites. The research progress of MOFs materials in gas storage, fluorescence property and other application areas was reviewed.
Key words:MOFs; porous; fuel gas storage; fluorescence property
金屬有機框架化合物(Metal-Organic Frame- works) ,簡稱MOFs材料。它是由金屬離子或金屬簇構成的金屬中心與橋連配體通過自組裝方式相連接,形成的擁有周期性結構的一類多孔晶態材料。構成框架的金屬中心及有機配體同簡單配合物、高分子聚合物相比,有著非常顯著的差異,因此,MOFs材料的物理化學性質根據金屬中心和有機配體的變化而具有明顯的多樣性。近年來,化學合成方法如水(溶劑)熱、微波法等的使用,使得MOFs材料迅速發展,已由設計金屬有機框架合成向實用性研究轉變。
1 ?MOFs材料的產生
MOFs材料是由配位聚合物發展而來的,合成色素普魯士藍是早期發現的一種配位聚合物, 1977年由X-射線衍射確定了它是混合價態Fe(II)/Fe(III)的網狀結構[1]。隨后,由Hoffman等發現,Powell等通過X-射線研究,得出了與普魯士藍的結構因子相似的配位聚合物Ni(CN)2(NH3)·C6H6[2]。Iwamoto等使用聯二苯替換Ni(CN)2(NH3)·C6H6的客體分子苯,在一定范圍內拓寬了配位聚合物的范圍[3]。Robson等[4]發現的金屬中心Cu(I)與四氰基四苯基甲烷連接形成的配合物材料,表明配位聚合物除了與氰根外還可與有機配體橋連。之后,配體的多樣性不斷增加,從氰化物到有機腈再到基于吡啶的供體。20世紀90年代中期,在Kitagawa等[5]使用4,4′-bpy構筑了具有穩定結構的多微孔材料之后,多孔材料的合成研究便獲得了很大的關注,Yaghi等[6]使用多羧酸合成的多孔結構就是一個典型的例子。相較于之前的配位聚合物,這些多孔材料配合物具有周期性網絡結構,可以可逆的吸收-釋放氣體,被稱為金屬-有機框架材料(MOFs材料)。
2 ?MOFs材料的特點
2.1 ?多孔性
研究表明,MOFs材料一般均具有多孔性和永久性孔隙,孔徑范圍較小的MOFs材料與典型的沸石的直徑相當,多數大孔直徑MOFs材料的最低骨架自由體積大于50%[7-11]。MOFs材料是通過連接體作為支架構筑內部空間,相比于傳統多孔材料并沒有器壁結構。另一方面,采用連接體作為支架構筑內部空間會提高孔體積及比表面積,且孔結構根據骨架結構的不同而變化。
2.2 ?大的比表面積
在氣體吸附分離和存儲中比表面積具有重要意義,高比表面積的物質在多孔材料研究領域具有重要的應用價值。
研究表明,相比于具有有序結構的沸石,一些MOFs材料的比表面積較大。Yaghi等[10]設計的MOFs材料由金屬和具有多齒型的羧基配體配合而成,Zn4O(BDC)3(MOF-5)的Langmuir比表面積為2 900 m2·g-1, Zn4O(BTB)2·(DEF)15·(H2O)3 (MOF-177)的Langmuir比表面積可達到4 500 m2·g-1,有超大空隙可鍵合多環有機大分子[11]。
2010 年,Yaghi等[12]對多齒型羧基有機配體進行了拓展,合成出了BET比表面積為6 240 m2·g-1,Langmuir比表面積達到10 400 m2·g-1的具有清晰孔道的三維晶體結構MOF-210。
2.3 ?結構的多樣性
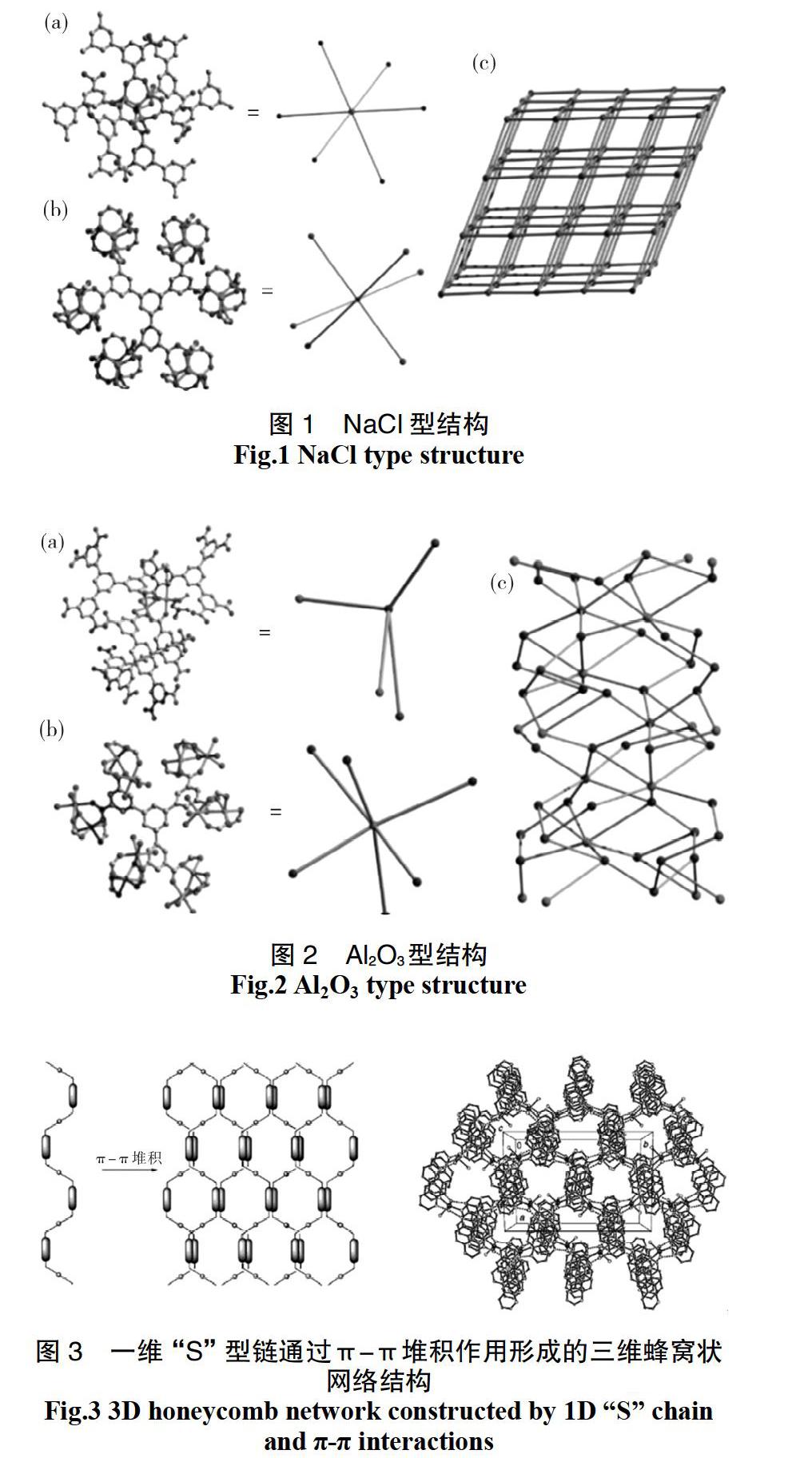
MOFs材料結構的多樣性取決于金屬離子和有機配體的配位能力多樣性,也與配體環境和金屬離子的配位方式有關,因此配位模式多種多樣。而一些基團如羧基基團本身配位模式較多,且根據不同程度的去質子化其配位模式更加多樣化。2011年Crystal Growth&Design上報道的使用3,3',3'',5,5',5''-苯基-1,3,5-三-苯六甲酸合成出的NaCl型、Al2O3型MOFs材料就是MOFs結構多樣性的很好的例子(見圖1、圖2)[13]。
MOFs一般具有一維、二維和三維結構,而氫鍵、π-π堆積等弱相互作用力會使MOFs的維度結構發生由低向高的轉變[6,14,15]。1998年Yaghi等[6]使用對苯二甲酸合成的MOFs結構就是Zn2+與有機配體構成的二維結構在O—H…O氫鍵作用下形成的三維結構。圖3為Mingliang Tong等報道過的一個由π-π堆積構筑的三維蜂窩狀網絡結構,[Cu(4,7-phen)(H2O)3]n2n+陽離子和游離的鄰菲啰啉(4,7-phen)分子通過不同方向的π-π堆積作用,組裝成三維蜂窩狀網絡結構[14]。
2.4 ?具有不飽和金屬配位點
在合成MOFs材料時,金屬中心受空間位阻等原因的影響,除與有機配體配位外還會結合一些不穩定配體。
大部分情況下,不穩定配體為溶劑分子(如水、乙醇、甲醇、DMF等),它們通過與金屬離子的Lewis酸堿作用配合在一起,這些不穩定配體穩定性較低,在外界條件如溫度發生改變時,形成中性客體分子從MOFs結構中脫落,這些中性客體分子的脫落在較多情況下并不會對材料的骨架結構造成影響,反而會在材料的結構中形成開放的金屬點。這些金屬點在一定條件下形成的不飽和配位點會增強材料的吸附及存儲氣體性能,同時促進和底物間的相互作用,是材料催化性能的主要影響因素[16,17]。
3 ?MOFs材料在燃氣儲存方面的研究進展
隨著對新型燃料氣體的開發與利用,能源儲備材料的需求日益擴大,因而具有超低密度的多孔材料—MOFs材料在氣體吸附、燃氣儲存等方面引起了研究者的廣泛關注,目前,國內外研究者在MOFs材料儲存H2、CH4方面進行了大量的實驗和理論計算方面的研究工作。
3.1 ?MOFs材料在儲氫方面的研究進展
氫氣是一種理想能源,以其燃燒熱高及燃燒后主要產物是水的特點,贏得了人們的青睞。氫能安全性是影響其整個生產、存儲和使用過程以及實現工業化應用的重要條件。儲氫方式有壓縮儲氫、金屬氫化物儲氫、液化儲氫等。壓縮儲氫耗能高且對容器材質要求高。液氫存儲在能耗較大的前提下對容器要求較高且存儲過程伴隨一定的蒸發損失。金屬氫化物在存儲過程中易受儲氫密度低和放氫速度慢等問題的限制。近幾年,MOFs材料因具有較大的比表面積和孔體積,成為了一種新型的儲氫材料,其儲氫性能得到了普遍的關注及探索[18]。
相比于一般MOFs材料,儲氫MOFs材料的比表面積更大,1999年,Yaghi等[10]報道了Zn2+與對苯二甲酸合成了具有儲氫功能的MOF-5:Zn4O(BDC)3,并在之后報道了其在77K、1bar下的氫氣儲存量為1.3%(wt)[19]。MOF-5的儲氫量雖然較低但具有一定的指導意義,研究表明,當MOF-5的有機配體或有機配體和金屬離子同時改變,可合成新的、具有類似結構的MOFs材料,如使用1,3,5-三對羧苯基苯(BTB)、2,5-二羥基苯-1,4-二羧酸(DHBDC)、均苯三甲酸(H3BTC)替換MOF-5的有機配體,或向有機配體的苯環上引入-Br、-C2H4-等官能團。通過儲氫性能的對比,研究者們發現大的有機配體對氫具有更強的親和力,但配體的存在對基體材料的儲氫性能無明顯作用,而對儲氫性能主要表現為有機配體分子連鎖效應的作用(骨架結構通過物理作用貫穿或交織在一起形成一個分子整體的現象)及其引起的孔直徑及孔體積的變化[19,20]。
Yildirim等[21]研究了不同的金屬離子對有機配體為2,5-二羥基-1,4-苯二甲酸二甲脂(DHTP)的MOFs材料M2(DHTP)(M= Mg, Co, Ni, Mn, Zn)儲氫性能的影響。結果表明在77K、1bar的條件下,此類MOFs材料儲氫量的大小順序為(以金屬離子表示):Ni2+ > Co2+ > Mg2+> Mn2+ > Zn2+。將理論計算的各金屬與氫之間結合鍵長、鍵能以及庫侖力與實驗測得的吸附能進行了比較分析,結果表明骨架內的八面體金屬結構的儲氫性能主要受金屬與氫之間的庫侖作用力影響。
研究者們還通過向MOFs結構中引入橋聯溢出結構、將堿金屬離子摻雜到MOFs材料中等方法,在一定程度上提高了原MOFs材料的儲氫能力[22,23]。此外,國內外研究者從理論計算的角度對MOFs材料的儲氫性能也進行了大量的研究工作,有很多預測、模擬結果都得到了實驗結果的驗證[24]。
目前,MOFs 材料在儲氫領域的研究進展迅速,但仍存在較多的關鍵性問題尚需解決,研究MOFs材料的儲氫機理及結構對儲氫性能的影響以及如何改善并提高對儲能材料的發展具有重要意義。
3.2 ?MOFs材料在儲存CH4方面的研究進展
甲烷作為一種清潔能源由于具有較高的碳氫比因此能釋放出較大能量的同時產生的二氧化碳較少。甲烷是有機物分解腐爛時形成的,比石油分布更廣也更容易獲取,因此在交通領域有巨大的潛在應用。而目前的使用現狀基本為采用壓縮天然氣的方法,這種高壓條件存儲的 (>200 atm)甲烷具有潛在的危險。美國 DOE為更好的發展甲烷存儲工業,把甲烷的存儲目標設定為室溫35 bar 壓力的條件下180 v/v[25],盡管一些碳材料符合要求但由于有限的填充密度而限制了在儲氣方面的進一步應用,因此發展具有高比表面積的多孔材料對氣體存儲的發展具有較大的應用價值。
雖然MOFs材料比表面積較大,但內部孔徑較小,難以容納甲烷分子,所以用于吸附CH4的MOFs材料需要有大的孔徑。近年來,Hongcai Zhou等[26]致力于研究合成擁有高儲甲烷性能的MOFs,他們為克服MOFs材料孔徑小不能容納甲烷分子的問題,用更多的苯環來增大MOFs材料的孔徑,合成出了具有納米級的孔洞的PCN-14,在 290 K和35 bar下,絕對吸附量為230 v/v(過剩吸附量為220 v/v),高出美國 DOE 目標的 28%。2016年,中山大學張杰鵬等[27]合成的MAF-38,此材料為八面體、類立方八面體籠狀結構,在298 K和65 bar條件下,它的體系吸附量為263 v/v。此材料與MOF-5和PCN-14具有相似的籠狀結構、孔隙體積和比表面積,但具有不同孔隙形狀和尺寸。通過計算、模擬,該材料的籠狀結構有非常合適的形狀、尺寸和吸附點,使得甲烷高效吸附與堆積。
各種多孔MOFs對甲烷的存儲數據表明,高的比表面積是甲烷存儲的必要條件但不是決定性因素。例如,上面提到的具有220 v/v 過剩吸附量的PCN-14的Langmuir 表面積為2176 m2/g,而 Langmuir 表面積為5 900 m2/g的MIL-101的甲烷過剩吸附容量僅為110 v/v,遠遠小于 PCN-14儲存性能[28]。為了進一步說明結構與甲烷儲存性能的關系,還需要系統性地研究孔洞尺寸、功能化配體等其它一些因素。
4 ?MOFs材料在熒光性能方面的研究進展
MOFs材料的金屬中心和有機配體均可為熒光的產生提供平臺,并且金屬和配體之間的電荷轉移也能導致熒光的產生,因此,利用金屬中心與有機配體自組裝形成的光功能MOFs材料成為了當下的一個研究熱點。目前構筑光功能金屬有機骨架結構的方法主要有引入熒光配體、引入有熒光發射功能的金屬離子、引入熒光客體、表面修飾熒光基團四種[29]。研究者們對前兩者的研究較多,但后兩種構筑方法是未來光功能MOFs材料的發展趨勢。
4.1 ?引入熒光配體的MOFs材料
由于剛性稠環大共軛有機分子如含氮雜環類、吡啶類及羧酸類等有利于增加分子的共平面性和電子的流動性以及減弱分子內振動,使得吸收和發射率較強,因此一般作為連接配體來設計具有熒光的MOFs結構。
當MOFs結構組裝時,熒光配體之間距離較小,相互之間的電子作用(包含MLCT(金屬到配體的電荷轉移)、LMCT(配體到金屬的電荷轉移)及LLMT(配體到配體的電荷躍遷))增強,使得MOFs的發光行為與組成該結構的配體的發光行為有所不同,具體表現在光譜的位移、發射光譜譜帶的變寬及熒光壽命的增強[28]。
前面提到的MOF-5的配體是典型的羧酸類熒光配體,MOF-5是由Zn(CH3COO)2結構單元和1,4苯二甲酸相連接構成的網絡立方體結構,有機配體1,4苯二甲酸的發射峰位于紫外區,而配合物MOF-5的發射峰位于525 nm處,發射出熒光,這是由于LMCT機理,即配體到金屬的電荷轉移機理產生的[29,30]。Qiangrong Fang等[31]合成了兩個含羧酸類熒光配體的MOFs結構Zn3(BTC)2(DMF)3 (H2O)·(DMF)(H2O)和Cd4(BTC)3 (DMF)2 (H2O)2·6H2O,它們分別在410和405 nm處顯示熒光發射,與單獨配體在370 nm處的熒光發射相比略有偏移,這是由于金屬離子微擾產生的。
基于含氮雜環類以及吡啶類等配位基團的配體也是常見的熒光配體, Yongqin Wei等[32]使用1-氫-苯并咪唑-5,6-二甲酸(H3BIDC)合成的Mn(HBIDC),它的最強熒光發射為在726 nm處的紅色熒光發射,單獨熒光配體1-氫-苯并咪唑-5,6-二甲酸的熒光發射在440 nm附近,此MOFs的熒光發射是基于Mn2+到熒光配體HBIDC2-的MLCT電荷轉移。Ming-Xing Li等[33]基于2,4,6-三(4-吡啶)-1,3,5-三唑(TPT)和Ag(I)、Cu(I)、Zn(II)的配位,合成出了一系列MOFs結構,TPT配體的發射峰出現在490 nm處,合成出的MOFs的發射峰出現在465~478 nm范圍內,發射出熒光,此熒光為金屬離子微擾熒光,屬于典型的基于熒光配體的發射。Antigoni Douvali等[34]以2,5-二羥基對苯二甲酸(H4dhtp)為配體,以N,Nˊ-二甲基甲酰胺,N-甲基吡咯烷酮、H2O為溶劑,合成出的一系列堿土金屬MOFs材料,在490~580 nm之間表面出強的熒光發射,此類MOFs的熒光發射是激發態分子中配體質子轉移所致。
4.2 ?引入具有熒光發射功能金屬離子的MOFs材料
過渡金屬離子具有未成對的電子,會發生熒光猝滅作用,而稀土元素除了La3+和Lu3+以外,其余所有Ln3+都可以形成從紫外光到可見光以及近紅外光范圍的f-f發射,因此具有較好的發光性質。但由于稀土離子的f-f躍遷禁阻,較低的光吸收率導致單個離子不易發射出特征熒光,因此需要能量傳遞來克服這個問題。而MOFs材料的結構可將能量傳遞給稀土離子,從而獲得更高的發光效率。
當有機配體的最低三線態能級與稀土離子的輻射能級相匹配時,可以發生T1-Ln3+的能量傳遞,稀土離子發生躍遷輻射出特征f-f光譜并回到基態,Eu3+、Sm3+、Tb3+、Tm3+的特征熒光分別為紅色、橙色、綠色、藍色,而Yb3+、Nd3+、Er3+發出的光則在紅外區附近[35-40]。
另外,能量也有可能直接從配體激發單重態傳遞到稀土離子輻射能級(主要是稀土Eu3+和Tb3+),然后輻射出特征光譜躍遷到基態能級[41]。因此,向MOFs材料中引入不同的稀土離子,可得到不同范圍的熒光發射。
4.3 ?引入熒光客體的MOFs材料
MOFs具有一定的孔洞,可以包裹客體分子,如熒光染料、稀土離子等發光物,從而表現出客體的特征熒光發射。2007年,Shilun Qiu等[42]成功將Rh6G染料分子包裹于含有一維六角形管狀通道的MOFs中,組裝后的新物質表現出與摻雜Rh6G染料的納米結構材料相似的黃色熒光。2010年,Feng Luo等[43]使用Eu3+和Tb3+替換[NH4]2 [ZnL]·6H2O (L=1, 2, 4, 5-苯四甲酸)1D孔道里的NH4+,替換后的新物質表現出稀土離子的特征熒光發射。
4.4 ?表面修飾熒光基團的MOFs材料
除了在MOFs中引入配體等前合成法外,還可采用后合成法即通過熒光功能基團與MOFs結構上的活性位點發生反應達到修飾的作用。到目前為止,活性位點主要有氨基、羧基等基團。Chunying Duan等[44]以吡啶和4,4′,4"-苯-1,3,5-三-苯甲酸為原料,合成出了一種MOFs結構BTPY-NH2,此MOFs結構具有三維大孔洞,在此基礎上,使FITC(一種熒光素)進入孔洞與MOFs結構中的氨基反應,實現了對MOFs的后合成熒光修飾。修飾后的結構在515 nm處有綠光發射(圖4)。
Suhyun Jung等[45]探索了對MOFs羧基基團的后合成熒光修飾。采用1-乙基-3-(3-二甲基氧丙基)碳二亞胺、二環己基碳二亞胺將MOFs結構表面的羧酸基團激活,然后再使用EGFP(一種共軛增強型綠色熒光蛋白)等生物材料或者蛋白質對激活后的MOFs機構進行修飾,通過熒光顯微鏡檢測,表現出的強烈綠色熒光表明EGFP的確修飾到了MOFs上。
5 ?MOFs材料在其他應用領域的研究進展
MOFs材料因具有大的比表面積和孔體積,對氫氣、甲烷等燃氣存儲具有很大的優勢,是新型的燃氣存儲材料,隨著對MOFs材料結構與燃氣存儲之間的研究,其作為燃氣存儲材料將會有更為實用的發展。由金屬中心與有機配體自組裝成的MOFs材料在修飾后由具有良好的發光性能,是獲得新型光學材料的有效途徑。MOFs材料除了在以上所提到的燃料存儲和熒光性能方面擁有廣泛的應用外,在化學、醫藥學、材料科學等其他領域也有很好的應用前景。
通過對MOFs材料及其合成方法、條件不斷深入的研究,更多種類的金屬用來構建MOFs材料,由于第Ⅷ族金屬如Fe、Co、Ni等金屬的引入,使得MOFs材料在磁學領域具有一定的應用價值。Fe、Co、Ni等第Ⅷ族金屬可與MOFs形成具有良好磁性和穩定性的配合物,進而有利于研究材料磁學性質與微觀結構之間的關系[46-48]。此外,由于MOFs材料的多孔性、大的比表面積、結構的多樣性及具有不飽和金屬配位點的特點,很多研究者正致力于MOFs材料在催化[49, 50]、化學傳感[51, 52]、藥物吸收與釋放[53]等領域的開發和研究。
參考文獻:
[1]Buser HJ, Schwarzenbach D, Petter W, et al. The crystal structure of Prussian Blue, Fe4[Fe(CN)6]3.xH2O[J]. Inorg. Chem., 1977, 16(11): 2704-2710.
[2]Rayner JH, Powell HM. J. Structure of molecular compounds. Part X. Crystal structure of the compound of benzene with an ammonia–nickel cyanide complex[J]. Chem. Soc., 1952,6(6):433-438.
[3]Iwamoto T, Miyoshi T, Sasaki Y. The Metal Cyanide Aromatic Clathrates. XIII. The Crystal Structure of the Hofmann-type Biphenyl Clathrate, Diammineickel(II) Tetracyanonickelate(II) Di-biphenyl: Ni(NH3)2Ni(CN)4·2C12H10[J]. Acta. Cryst., 1974, B30: 292-295.
[4]Hoskins BF, Robson R. Infinite polymeric frameworks consisting of three dimensionally linked rod-like segments[J]. J. Am. Chem. Soc., 1989, 111(15): 5962-5964.
[5]Kondo M, Yoshitomi T, Seki K, et al. Three‐Dimensional Framework with Channeling Cavities for Small Molecules: {[M2(4, 4′‐bpy)3(NO3)4]·xH2On (M ?Co, Ni, Zn)[J]. Angew. Chem., Int. Ed. Engl., 1997, 36(16): 1725-1727.
[6] Li HL, Eddaoudi M, Groy TL, et al. Establishing Microporosity in Open Metal?Organic Frameworks: Gas Sorption Isotherms for Zn(BDC) (BDC = 1,4-Benzenedicarboxylate)[J]. J. Am. Chem. Soc., 1998, 120(33): 8571-8572.
[22]Li YW , Yang RT. Hydrogen storage in metal-organic frameworks by bridged hydrogen spillover[J]. J. Am. Chem. Soc., 2008, 128(25): 8136-8137.
[23]Mulfort KL, Hupp JT. Alkali metal cation effects on hydrogen uptake and binding in metal-organic frameworks[J]. Inorg. Chem., 2008,47(18): 7936-7938.
[24]Getman RB, Bae YS, Wilmer CE, et al. Review and Analysis of Molecular Simulations of Methane, Hydrogen, and Acetylene Storage in Metal–Organic Frameworks[J]. Chem. Rev., 2012, 112(2): 703-723.
[25]Düren T, Sarkisov L, Yaghi OM, et al. Design of New Materials for Methane Storage[J]. Langmuir, 2004, 20(7): 2683-2689.
[26]Ma SQ, Sun DF, Simmons JM ,et al. Metal-organic framework from an anthracene derivative containing nanoscopic cages exhibiting high methane uptake[J]. J. Am. Chem. Soc., 2008, 130(3): 1012-1016.
[27]Lin XM, He CT, Liu Y et al. A Metal–Organic Framework with a Pore Size/Shape Suitable for Strong Binding and Close Packing of Methane[J]. Angew. Chem. Int. Ed., 2016, 55(15), 4674–4678.
[28]Llewellyn PL, Bourrelly S, Serre C, et al. High uptakes of CO2 and CH4 in mesoporous metal-organic frameworks MIL-100 and MIL-101[J]. Langmuir, 2008, 24(14): 7245-7250.
[29]武鵬彥. 光功能金屬有機骨架的構筑及其性能研究[D]. 大連理工大學, 2013.
[30]Bordiga S, Lamberti C, Ricchiardi G, et al. Electronic and vibrational properties of a MOF-5 metal-organic framework: ZnO quantum dot behavior [J]. Chem. Comm., 2004, (20):2300-2301.
[31]Fang QR, Zhu GS, Xue M, et al. Structure, Luminescence, and Adsorption Properties of Two Chiral Microporous Metal?Organic Frameworks[J]. Inorg. Chem, 2006, 45(9): 3582-3587.
[32]Wei YQ, Yu YF , Wu KC. Highly Stable Five-Coordinated Mn(II) Polymer [Mn(Hbidc)]n (Hbidc=1H-Benzimidazole-5,6- dicarboxy- late): Crystal Structure, Antiferromegnetic Property, and Strong Long-Lived Luminescence[J]. Cryst. Growth Des., 2008, 8(7): 2087-2089.
[33]Li MX, Miao ZX, Shao M, et al. Metal-Organic Frameworks Constructed from 2,4,6-Tris(4-pyridyl)-1, 3,5-triazine[J]. Inorg. Chem., 2008, 47(11): 4481-4489.
[34]Sava Gallis DF, Rohwer LES, Rodriguez MA, et al. Efficient Photoluminescence via Metal–Ligand Alteration in a New MOFs Family[J]. Chem. Mater., 2014, 26 (9):2943–2951.
[35]Chandler BD, Cramb DT , Shimizu GKH. Microporous metal-organic frameworks formed in a stepwise manner from luminescent building blocks[J]. J. Am. Chem. Soc., 2006, 128(32): 10403-10412.
[36]Sun YQ , Yang GY. Organic-inorganic hybrid materials constructed from inorganic lanthanide sulfate skeletons and organic 4,5-imidazoledicarboxylic acid[J]. Dalton Trans., 2007 (34): 3771- 3781.
[37]Song XQ, Liu WS, Dou W, et al. Structure variation and luminescence properties of lanthanide complexes incorporating a naphthalene- ?derived chromophore featuring salicylamide pendant arms[J].Eru. J. Inorg. Chem,. 2008, 11: 1908-1912.
[38]Cheng JW, Zheng ST, Yang GY. Diversity of crystal structure with different lanthanide ions involving in situ oxidation-hydrolysis reaction[J]. Dalton Trans., 2007, (36): 4059-4066.
[39]Douvali A, Papaefstathiou GS, Gullo MP, et al. Alkaline Earth Metal Ion/Dihydroxy-Terephthalate MOFs: Structural Diversity and Unusual Luminescent Properties[J]. Inorg. Chem., 2015, 54 (12): 5813–5826.
[40]Chen BL, Yang Y, Zapata F, et al. Enhanced near-infrared- luminescence in an erbium tetrafluoroterephthalate framework[J]. Inorg. Chem., 2006, 45(22): 8882-8886.
[41]Binnemans K. Lanthanide-based luminescent hybrid materials[J]. Chem. Rev., 2009, 109(9): 4283-4374.
[42]Fang QR, Zhu GS, Jin Z, et al. Mesoporous Metal–Organic Framework with Rare etb Topology for Hydrogen Storage and Dye Assembly[J]. Angew. Chem. Int. Ed., 2007, 46(35): 6638-6642.
[43]Luo F , Batten SR. Metal-organic framework (MOF): lanthanide (III)-doped approach for luminescence modulation and luminescent sensing[J]. Dalton Trans., 2010, 39(19): 4485-4488.
[44]Zhang LJ, Jian Y, Wang J ,et al. Post-modification of a MOF through a fluorescent-labeling technology for the selective sensing and adsorption of Ag+ in aqueous solution[J]. Dalton Trans., 2012, 41(34): 10153-10155.
[45]Jung S, Kim Y, Kim S-J, et al. Bio-functionalization of metal–organic frameworks by covalent protein conjugation[J]. Chem. Commun., 2011, 47(10): 2904-2906.
[46]Shiga T, ?kawa H, Kitagawa S, et al. Stepwise synthesis and magnetic control of trimetallic magnets [Co2Ln(L)2(H2O)4] [Cr(CN)6]·nH2O (Ln = La, Gd; H2L = 2,6-Di(acetoacetyl)pyridine) with 3-D pillared-layer structure[J]. J. Am. Chem. Soc., 2006, 128 (51): 16426-16427.
[47]Cheng XN, Zhang WX, Chen XM. Single crystal-to-single crystal transformation from ferromagnetic discrete molecules to a spin-canting antiferromagnetic layer[J]. J. Am. Chem. Soc., 2007, 129 (51): 15738-15739.
[48]Zheng YZ, Xue w, Tong ML, et al. A two-dimensional iron(II) carboxylate linear chain polymer that exhibits a metamagnetic spin-canted antiferromagnetic to single-chain magnetic transition[J]. Inorg. Chem., 2008, 47(10): 4077-4087.
[49]Yoon M, Srirambalaji R, Kim K. Homochiral Metal-Organic Frameworks for Asymmetric Heterogeneous Catalysis[J]. Chem. Rev., 2012, 112(2):1196-1231.
[50]Yang D,Han Y, Xu W, et al. A Series of Lanthanide-Based Metal–Organic Frameworks: Synthesis, Structures, and Multicolor Tuning of Single Component[J]. Inorg. Chem., 2017,56: 2345-2353.
[51]Kreno Le, Leong K, Farha OK, et al. Metal-organic framework materials as chemical sensors[J]. Chem. Rev., 2012, 112 (2): 1105-1125.
[52]Li H Y, Wei Y L, Dong X Y, et al. Novel Tb-MOF Embedded with Viologen Species for Multi-Photofunctionality: Photochromism, Photomodulated Fluorescence, and Luminescent pH Sensing[J]. Chem. Mater., 2015, 27(4): 1327-1331.
[53]Horcajada P, Serre C, Maurin G, et al. Flexible porous metal-organic frameworks for a controlled drug delivery[J]. J. Am. Chem. Soc., 2008, 130(21):6774-678.

