豬丹毒絲菌生產用菌種CVCC43005株最高擴繁代次的確定及疫苗佐劑的篩選
張 媛,魏財文,李 建,張一幟,辛凌翔,王秀麗,彭國瑞,劉 博,蔣玉文
(中國獸醫藥品監察所,北京 100081)
豬丹毒是由丹毒絲菌引起的一種嚴重威脅養豬業的重要傳染病,其臨床特征為高熱、急性敗血癥、皮膚疹塊、慢性心內膜炎,或皮膚壞死與多發性非化膿性關節炎,臨床上常與豬圓環病毒、豬細小病毒、豬肺炎支原體等病原混合感染,同時丹毒也是一種人和其它多種動物都能感染的共患病。接種豬丹毒疫苗是預防豬丹毒的一種重要手段,丹毒絲菌CVCC43005株是豬丹毒滅活疫苗的生產用菌株,由中國獸醫藥品監察所負責檢定、保管和供應,具有自主知識產權,該菌種毒力穩定、免疫原性好,是一株優良的疫苗株[1]。該菌種現有檢定依據為《中華人民共和國獸用生物制品規程》(二〇〇〇年版,第5次修訂)[2],該標準執行至今已近20年,其明確了CVCC43005株菌種基礎種子代數,但沒有明確生產種子最高擴繁代次,且菌種免疫原性是將其制備為氫氧化鋁膠佐劑疫苗后通過小鼠的免疫攻毒實驗予以評價。近20年來市場上已經出現多種新型佐劑,這些佐劑對菌種免疫原性是否有所影響不得而知。為研究該菌種作為生產用菌種的最高擴繁代次以及新型佐劑對該菌種免疫原性的影響,建立了豬丹毒絲菌CVCC43005株的種子批,并對不同佐劑進行篩選,為修訂菌種檢定依據奠定了基礎。
1 材料與方法
1.1 菌株 CVCC43005株F5、F10、F15、F20代凍干菌種,檢驗用CVCC43008株、CVCC43006株菌種,均由中國獸醫藥品監察所凍干、保存。
1.2 培養基及試劑 豬丹毒培養基、革蘭氏染色液,購自購自青島高科技工業園海博生物技術有限公司。TSA培養基,購自BD公司。TG培養基、TSB培養基、5%蔗糖脫脂牛奶,購自北京中海動物保健科技公司。馬血清,購自Gbico公司。細菌鑒定試劑盒,購自Biomerieux公司。裂解血細胞全血、豬丹毒分型血清、豬丹毒抗體陽性血清、豬丹毒抗體陰性血清、礦物質白油、氫氧化鋁膠、40%氫氧化鋁膠生理鹽水,由中國獸醫藥品監察所細菌制品檢測室提供。MONTANIDETMIMS1313VGNST佐劑、GEL01PR佐劑,購自法國賽比克公司。水溶性佐劑、水性復合免疫佐劑由洛陽賽威公司贈送。
1.3 實驗動物 16~18 g ICR小白鼠、18~22 g ICR小白鼠,購自北京維通利華實驗動物技術有限公司。
1.4 種子批的建立 以具有良好毒力、免疫原性、繁殖特性和純凈性的1986年凍干的CVCC43005菌株為原始種子,將原始種子用含4%馬血清及0.1%裂解血細胞全血TSA培養基連續傳代,每代于37 ℃培養24 h,各代命名為F1~F20。將生長純粹的F5、F10、F15、F20代菌分別用5%蔗糖脫脂牛奶洗下后分裝安瓿,凍干,抽真空后融封,用于后續檢定,依據檢定結果建立種子批。
1.5 形態 取菌種培養物進行革蘭氏染色,鏡檢。
1.6 生化特性 參照試劑的使用說明書檢定。
1.7 培養特性 菌種接種含4%馬血清及0.1%裂解血細胞全血TSA平板,37 ℃培養48 h,觀察細菌生長特性。
1.8 血清學特性 參照試劑的使用說明書檢定。
1.9 純粹 按《中國獸藥典》2015年版要求進行檢定[3]。
1.10 真空度 按《中國獸藥典》2015年版要求檢定[3]。
1.11 剩余水分 按《中國獸藥典》2015年版要求檢定[3]。
1.12 毒力 參照《中華人民共和國獸用生物制品規程》二〇〇〇年版[2]用小鼠進行最小致死劑量測定。將F5、F10、F15和F20代菌種分別用豬丹毒培養基制備成菌液后,皮下注射體重18~22 g小白鼠,根據菌液預數結果,將菌液稀釋為1、3、5、7、9、11、13、15 CFU/0.2mL,每個劑量組注射5只小鼠,每只小鼠注射0.2 mL,同時對菌液進行復數,根據復數結果計算每個劑量組小鼠實際注射的活菌數。7個觀察日內記錄小鼠死亡情況,結合每只小鼠實際注射的活菌數判定各代次菌種對于小鼠的毒力。
1.13 免疫原性 用小鼠進行免疫原性檢定。將F5、F10、F15、F20代菌種參照《中華人民共和國獸用生物制品規程》二〇〇〇年版[2]分別制備成氫氧化鋁膠滅活抗原。取100只16~18 g小白鼠分為12組。第1、2、3、4組,每組10只,分別皮下注射F5、F10、F15、F20代滅活抗原0.1 mL;第5、6、7、8組,每組10只,分別皮下注射F5、F10、F15、F20代滅活抗原40%氫氧化鋁膠生理鹽水4倍稀釋液0.2 mL;第9、10、11、12組,每組5只,不注射疫苗,作為對照組。免疫21 d后,每個免疫組各取5只小鼠,連同對照小鼠5只各注射1000 MLD(最小致死量,Minimum Lethal Dose) CVCC43008強毒菌液,另取5只對照小鼠注射1 MLD CVCC43008強毒菌液;每個免疫組剩余5只小鼠,連同對照小鼠5只各注射1000 MLD CVCC43006強毒菌液,另取5只對照小鼠注射1 MLD CVCC43006強毒菌液。攻毒后觀察10 d,統計保護率。
1.14 小鼠最小免疫劑量測定 將F5代菌株制備的菌液活菌計數后,經甲醛滅活,取滅活菌液40 mL,與8 mL氫氧化鋁膠充分混勻后置2~8 ℃靜置2 d后棄去上清28 mL,其作為抗原原液。用40%氫氧化鋁膠生理鹽水將抗原原液進行4倍、8倍、16倍稀釋,取各稀釋度抗原免疫16~18 g小白鼠,每個劑量免疫10只小鼠。免疫21 d后,每個免疫組各取5只小鼠,連同對照小鼠5只各注射1000 MLD CVCC43008強毒菌液,另取5只對照小鼠注射1 MLD CVCC43008強毒菌液;每個免疫組剩余5只小鼠,連同對照小鼠5只各注射1000 MLD CVCC43006強毒菌液,另取5只對照小鼠注射1 MLD CVCC43006強毒菌液。攻毒后觀察10 d,統計保護率。
1.15 不同佐劑疫苗的制備 分別將F5代菌株制備的甲醛滅活菌液用鋁膠佐劑、礦物質白油佐劑、洛陽賽威公司的水溶性佐劑、水性復合免疫佐劑以及法國賽比克公司的MONTANIDETMIMS1313VGNST、GEL01PR 6種佐劑按各自使用說明制備豬丹毒滅活疫苗。然后參照《中國獸藥典》2015年版要求進行性狀和無菌檢驗[3]。
1.15.1 鋁膠佐劑疫苗的制備 滅活菌液5份加滅菌的氫氧化鋁膠1份,充分混合均勻后,靜置沉淀3日,棄去上清,濃縮至全量的2/5,充分混合。用40%氫氧化鋁膠生理鹽水進行8倍、16倍、32倍稀釋,分別標記鋁1、鋁2、鋁3。
1.15.2 白油佐劑疫苗的制備 滅活菌液5份加滅菌的氫氧化鋁膠1份,充分混合均勻后,靜置沉淀3日,棄去上清,濃縮至全量的2/5,充分混合。用40%氫氧化鋁膠生理鹽水進行4倍、8倍、16倍稀釋,取稀釋后的抗原分別與吐溫-80混勻作為水相,再分別與等量的油相進行乳化,乳化后分別標記油1、油2、油3。
1.15.3 水溶性佐劑疫苗的制備 滅活菌液5份加滅菌的氫氧化鋁膠1份,充分混合均勻后,靜置沉淀3日,棄去上清,濃縮至全量的2/5,充分混合。用40%氫氧化鋁膠生理鹽水進行4倍、8倍、16倍稀釋,取稀釋后的抗原分別與等量的水溶性佐劑混勻,分別標記水1、水2、水3。
1.15.4 水性復合免疫佐劑疫苗的制備 滅活菌液5份加滅菌的氫氧化鋁膠1份,充分混合均勻后,靜置沉淀3日,棄去上清,濃縮至全量的2/5,充分混合。用40%氫氧化鋁膠生理鹽水進行4倍、8倍、16倍稀釋,取稀釋后的抗原分別與等量的水性復合免疫佐劑混勻,分別標記復1、復2、復3。
1.15.5 IMS1313VGNST佐劑疫苗的制備 滅活菌液5份加滅菌的氫氧化鋁膠1份,充分混合均勻后,靜置沉淀3日,棄去上清,濃縮至全量的2/5,充分混合。用40%氫氧化鋁膠生理鹽水進行4倍、8倍、16倍稀釋,取稀釋后的抗原分別與等量的IMS1313VGNST佐劑混勻,分別標記IMS1、IMS2、IMS3。
1.15.6 GEL01PR佐劑疫苗的制備 滅活菌液用PBS進行4倍、8倍、16倍稀釋,取稀釋后的抗原分別與GEL01PR佐劑按9∶1的比例混勻,分別標記GEL1、GEL2、GEL3。
1.16 疫苗安全檢驗 取180只18~22 g小白鼠,隨機分成18組,每組10只,分別于背部皮下注射標記為鋁1、鋁2、鋁3、油1、油2、油3、水1、水2、水3、復1、復2、復3、IMS1、IMS2、IMS3、 GEL1、GEL2、GEL3的滅活疫苗0.3 mL/只,觀察10日。
1.17 疫苗效力檢驗 取200只16~18 g小白鼠,隨機分成22組。其中1~18組,每組10只,分別于背部皮下注射標記為鋁1、鋁2、鋁3、油1、油2、油3、水1、水2、水3、復1、復2、復3、IMS1、IMS2、IMS3、 GEL1、GEL2、GEL3的滅活疫苗0.1 mL/只;第19、20、21、22組,每組5只,不注射疫苗,作為對照組。免疫21 d后,每個免疫組各取5只小鼠,連同對照小鼠5只各注射1000 MLD CVCC43008強毒菌液,另取5只對照小鼠注射1 MLD CVCC43008強毒菌液;每個免疫組剩余5只小鼠,連同對照小鼠5只各注射1000 MLD CVCC43006強毒菌液,另取5只對照小鼠注射1 MLD CVCC43006強毒菌液。攻毒后觀察10 d,統計保護率。
2 結果與分析
2.1 形態 經染色觀察,F5、F10、F15、F20代菌種均為革蘭氏陽性纖細小桿菌。
2.2 生化特性 F5、F10、F15、F20代菌種的生化特性均符合豬丹毒絲菌的特性。
2.3 培養特性 F5、F10、F15、F20代菌種在含4%馬血清及0.1%裂解血細胞全血TSA平板上均生長為形態完整的呈微藍灰色露珠狀小菌落,在低倍顯微鏡下觀察,菌落可呈光滑型或粗糙型,菌落中部含有黃褐色點狀顆粒。
2.4 血清學特性 F5、F10、F15、F20代菌種的血清型均為2型。
2.5 純粹 F5、F10、F15、F20代菌種均純粹,沒有雜菌生長。
2.6 真空度 將失真空的F5、F10、F15、F20代菌株淘汰,保留的菌株真空度檢查均呈現白色、粉色或紫色輝光。
2.7 剩余水分 F5、F10、F15、F20代菌株剩余水分測定結果見表1,各代次凍干菌株剩余水分含量均<3.0%。
2.8 毒力 F5、F10、F15、F20代菌株對小鼠最小致死劑量測定結果見表2,9~10 CFU活菌皮下注射體重18~22 g小白鼠,均于7日內5/5死亡。
2.9 免疫原性 F5、F10、F15、F20代菌株對小鼠免疫原性測定結果見表3,各代次菌株制備成滅活抗原后,按兩個劑量組免疫小鼠,每只小鼠分別免疫滅活抗原0.1 mL及滅活抗原4倍稀釋液0.2 mL。免疫小鼠攻擊1000 MLD強毒菌液全部健活,對照小鼠攻擊1000 MLD強毒菌液全部死亡, 攻擊1 MLD 強毒菌液C43-6株5/5死亡,C43-8株4/5死亡。各代次菌株免疫原性沒有變化,較為穩定。
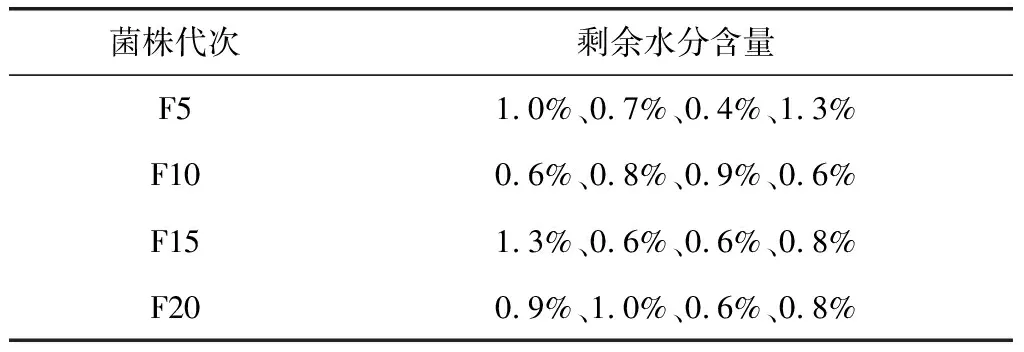
表1 不同代次菌株剩余水分含量Tab 1 The residual water content of differentgenerations of strains
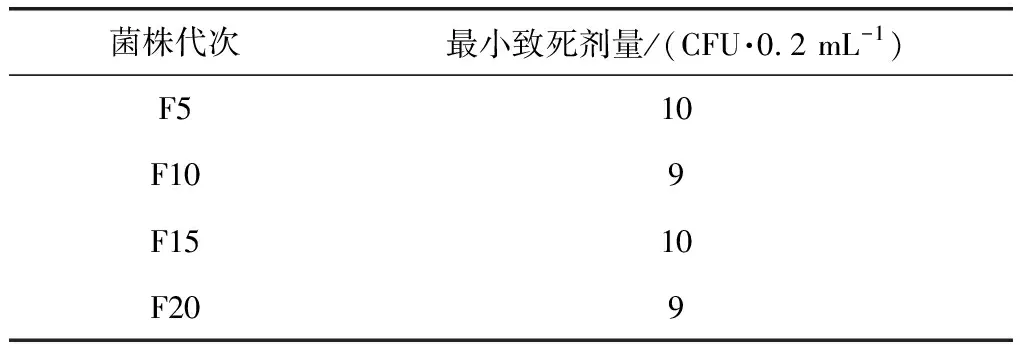
表2 不同代次菌株對小鼠的最小致死劑量Tab 2 The MLD to mice of different generations of strains

表3 不同代次菌株對小鼠的免疫原性Tab 3 The immunogenicity to mice of different generations of strains
劑量1為每只小鼠皮下注射滅活抗原0.1 mL; 劑量2為每只小鼠皮下注射滅活抗原40%氫氧化鋁膠生理鹽水4倍稀釋液0.2 mL
2.10 小鼠最小免疫劑量 F5代菌株制備的氫氧化鋁膠佐劑滅活疫苗對小鼠最小免疫劑量為2.1×108CFU/只(滅活前菌液含有的活菌數),攻擊1000 MLD CVCC43006及CVCC43008株免疫組小鼠均全部健活,對照組小鼠攻擊1000 MLD組均5/5死亡,攻擊1MLD組均4/5死亡。結果見表4。
2.11 疫苗性狀及無菌檢驗 6種疫苗均無菌生長,其性狀檢驗結果見表5。

表4 F5代菌株制備的氫氧化鋁膠佐劑滅活疫苗對小鼠的最小免疫劑量Tab 4 The minimum immune dose to mice of the inactivated aluminum hydroxide colloid vaccine

表5 不同佐劑疫苗性狀檢驗Tab 5 The appearance of the vaccines prepared by different adjuvants
2.12 疫苗安全檢驗 6種疫苗18個組注射的180只小鼠于10個觀察日內精神、采食均正常,但氫氧化鋁膠佐劑疫苗、IMS1313VGNST佐劑疫苗及礦物質白油佐劑疫苗注射的小鼠,注射部位會出現腫脹、硬結、破潰等不良反應,結果見表6及圖1。
2.13 疫苗效力檢驗 6種疫苗效力檢驗結果表明使用GEL01PR佐劑、鋁膠佐劑、礦物質白油佐劑制備的疫苗免疫效果最好(表7)。
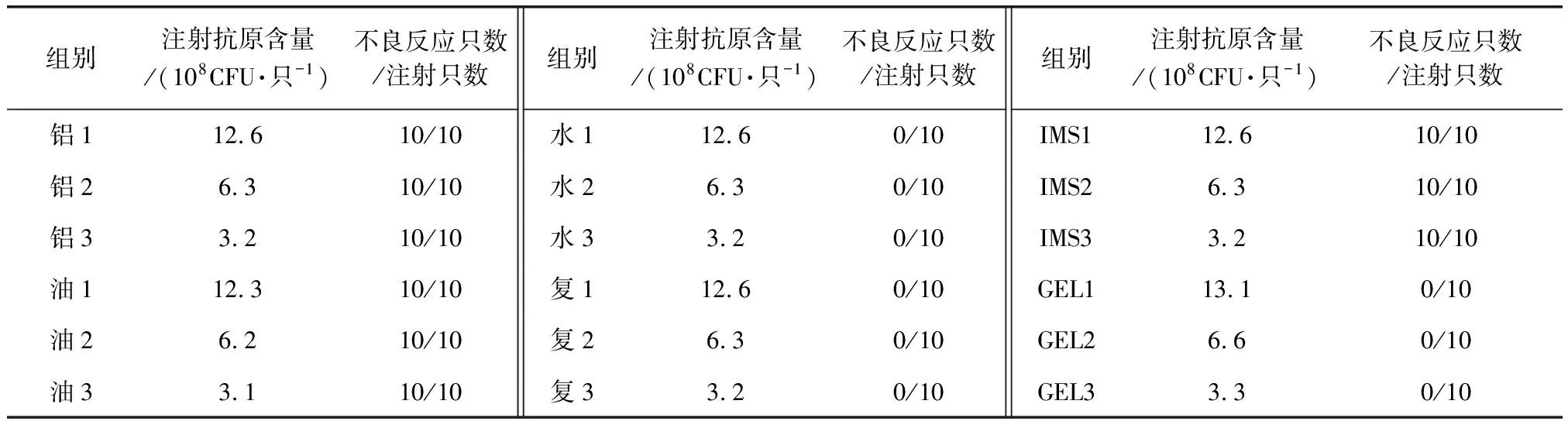
表6 不同佐劑疫苗注射局部反應Tab 6 The local reactions after injection of the vaccines prepared by different adjuvants
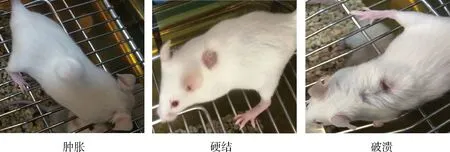
圖1 小鼠注射局部不良反應Fig 1 The local adverse reactions to mice after injection
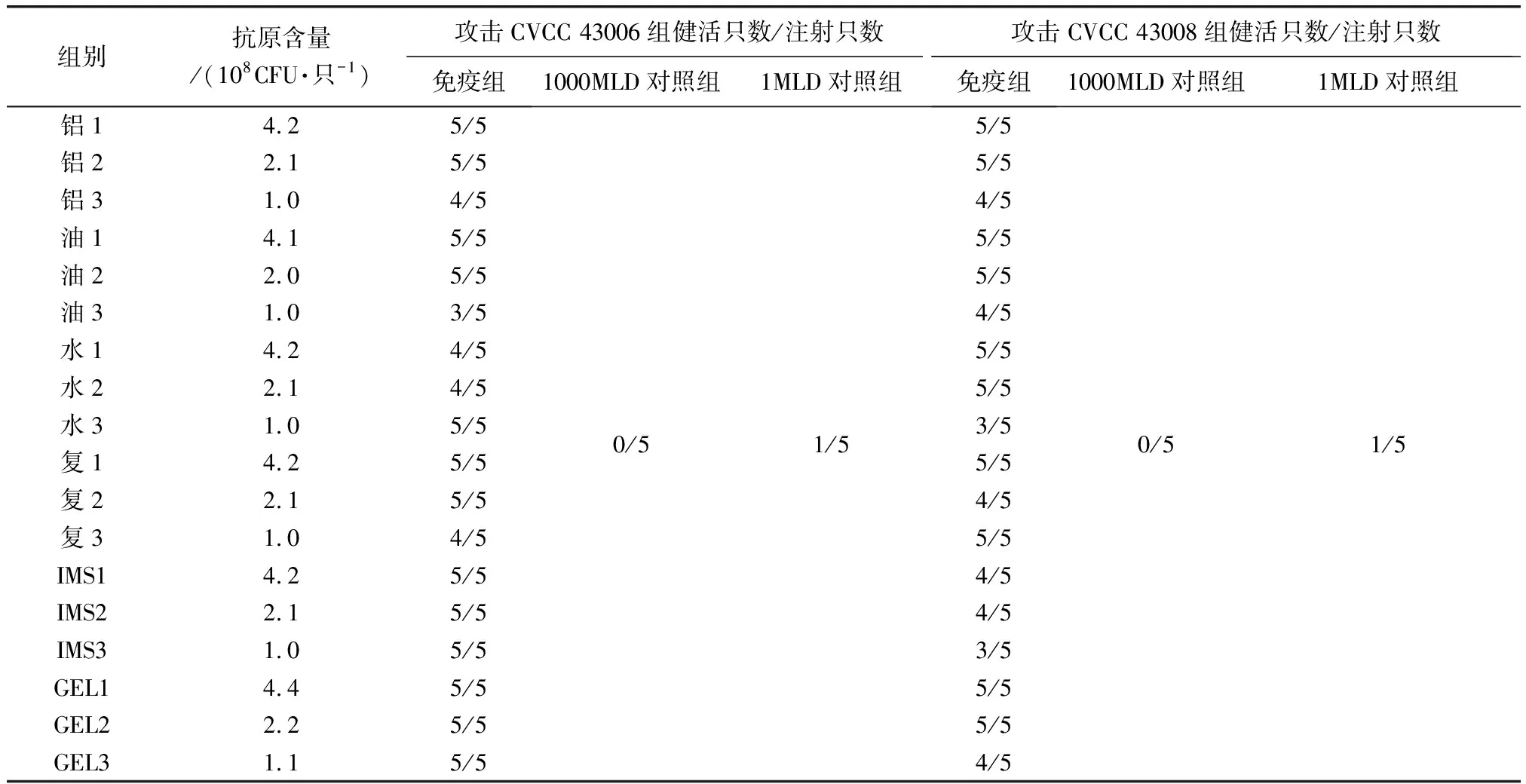
組別抗原含量/(108CFU·只-1)攻擊CVCC 43006組健活只數/注射只數攻擊CVCC 43008組健活只數/注射只數免疫組1000MLD對照組1MLD對照組免疫組1000MLD對照組1MLD對照組鋁14.25/5鋁22.15/5鋁31.04/5油14.15/5油22.05/5油31.03/5水14.24/5水22.14/5水31.05/5復14.25/5復22.15/5復31.04/5IMS14.25/5IMS22.15/5IMS31.05/5GEL14.45/5GEL22.25/5GEL31.15/50/51/55/55/54/55/55/54/55/55/53/55/54/55/54/54/53/55/55/54/50/51/5
3 討論與結論
小鼠對丹毒絲菌的毒力及免疫原性的反應是與豬的反應呈正相關的,目前國內市場上現有的豬丹毒產品均用小鼠來評價疫苗的安全性及效力,國外研究學者也是用小鼠來評價丹毒絲菌保護性抗原的免疫效果[4-6],用耗費資源更少的小鼠替代豬進行菌株毒力、免疫原性以及疫苗安全性和效力的評價,是遵循動物實驗3R原則的體現。
經一定途徑在一定時間內能使一組實驗動物全部致死的最小微生物劑量為1 MLD,但在實際操作過程中由于動物個體反應及菌液混合均勻度、注射劑量準確性等不確定因素的影響,有時注射1 MLD的對照動物組無法達到100%死亡,目前市場上現有的豬丹毒產品對于攻擊1 MLD強毒菌液對照組小鼠要求2/3死亡(即死亡率為66.7%)。本試驗中不論最小免疫劑量的測定、菌種免疫原性的測定還是疫苗效力檢驗,攻擊1 MLD強毒菌液對照組小鼠的死亡率均達到了80%以上,對照成立。
通過對CVCC43005株各代次凍干菌種的生化特性、培養特性、毒力、免疫原性等鑒定證明,各代次菌種傳代穩定;形態、生化特性、培養特性均符合丹毒絲菌的特性;凍干菌種純粹,沒有雜菌污染;真空度及剩余水分含量符合凍干菌種要求;各代次菌株毒力沒有明顯變化,9~10 CFU活菌可于7日內致死小鼠;各代次菌株制成滅活疫苗免疫小鼠后,均能夠產生完全的攻毒保護,以此為依據,建立了菌種的種子批,確定豬丹毒絲菌CVCC43005株基礎種子代數為F1~F10代;生產用菌種的最高擴繁代次宜控制在5代以內[7]。
疫苗的安全高效和副作用小是評價疫苗質量的重要指標,而適當的佐劑選擇對于疫苗安全性和效力至關重要。當18~22 g小白鼠背部皮下注射6種佐劑疫苗0.3 mL/只時,小鼠精神、食欲均無異常反應,但只有水溶性佐劑疫苗、水性復合免疫佐劑疫苗、GEL01PR佐劑疫苗注射的小鼠,注射部位沒有出現腫脹、硬結、破潰等不良反應,表明此三種佐劑具有良好的安全性。免疫16~18 g小白鼠,使用GEL01PR佐劑、鋁膠佐劑、礦物質白油佐劑制備的疫苗組表現最突出,皮下注射抗原含量2.0×108~2.2×108CFU的疫苗即可獲得對小鼠100%的免疫保護;水性復合免疫佐劑次之,需皮下注射抗原含量為4.2×108CFU的疫苗才可獲得對小鼠100%的免疫保護;MONTANIDETMIMS1313VGNST佐劑及水溶性佐劑最為不理想,即使皮下注射抗原含量為4.2×108CFU的疫苗,也只能獲得對小鼠90%的免疫保護。綜合評價疫苗的安全性及效力,GEL01PR佐劑為豬丹毒滅活疫苗的最佳佐劑。
本試驗種子批的建立、CVCC43005株作為生產用菌種最高擴繁代次的確定及疫苗免疫佐劑的篩選,為修訂菌種檢定依據奠定了基礎。

