不同穩定劑配制的三種精漿生化質控品的性能評價*
石漢振,陳雨薇,歐財文,王建兵,柯培鋒
(1.廣東省中醫院檢驗科,廣東廣州 510120;2.廣州市天河區中醫醫院檢驗科,廣東廣州 510120;3.南方醫科大學附屬里水醫院檢驗科,廣東佛山 528200)
精漿分析是一項用于評估男性生殖能力的重要的檢驗項目,其檢測的項目涵蓋許多用于診斷男性不育和男性生殖系統疾病的生化標志物[1]。精漿生化項目檢測的準確性對于臨床的診療判斷尤為重要。但是,精漿生化質控品價格昂貴和結果穩定性欠佳等原因導致精漿生化質控品尚未廣泛應用于臨床;缺乏相應的室內質控標準操作程序文件又導致臨床精漿生化分析標準化和質量控制工作難以開展[2]。同一實驗室內部或不同實驗室之間精漿生化分析結果存在很大的差異[3],結果的可信度備受懷疑。自2004年以來精漿生化分析標準化和質量控制引起國內外男科專家重視[4-6],國內外的男科實驗室一直致力于精漿生化分析標準化和質量控制研究,但國內尚未研制出均勻、穩定、價廉的質控品。有文獻報道,乙二醇、丙三醇是較好的質控品穩定劑、1,2-丙二醇是良好的防凍劑和除冰劑、氯霉素是良好的抑菌劑,因此常常作為臨床試驗中蛋白類項目質控品的穩定劑及抑菌劑[7-13]。但是這些試劑用于精漿生化質控品的配制尚未見報道,配制后精漿生化質控品的性能是否能滿足要求也不清楚。因此,本課題組采用乙二醇、丙二醇、丙三醇作為穩定劑配制精漿生化質控品,對其均勻性、穩定性以及實驗室常規質控監測進行評價,以期獲得配制精漿生化質控品的最佳配制方法,助力精漿生化室內質控工作的開展,提高結果的準確性。
1 資料與方法
1.1一般資料 采集2017年10月至2018年3月于廣東省中醫院進行體檢的健康男性的精液標本。要求受檢者禁欲2~7 d[14],于取精室手淫取精,收集一次射精的全部精液于清潔、無毒、密閉的容器內,置37 ℃水浴箱中待液化[15]。納入及排除標準:選取常見傳染病(乙型肝炎、丙型肝炎、梅毒、HIV)篩查結果為陰性的男性精液作為標本,剔除生殖道或泌尿道慢性炎癥、遺傳性疾病、生殖器質性疾病患者的標本。
1.2儀器與試劑 主要的檢測儀器為美國Awareness公司Chemwell BRED 2900型全自動精漿生化免疫分析儀。檢測試劑包括傳染病檢測試紙條(艾博生物醫藥公司生產)、氯霉素(青島海博生物公司生產)、乙二醇(國藥集團化學試劑廠生產)、丙二醇(無錫亞泰化工生產)、丙三醇(無錫亞泰化工生產)。
1.3方法
1.3.1提取精漿 將多份檢測后廢棄的精液標本用4 000×g離心15 min,取上層精漿。混合10~15份不同受試者的精漿用于制備質控品。為了避免精液液化不良對吸樣的影響,需剔除精液液化不良、嚴重黏稠的標本。離心后精漿不能有渾濁或絮狀沉淀。
1.3.2傳染病篩查 用乙肝表面抗原、丙肝抗體、梅毒螺旋體抗體、HIV抗體檢測試紙條(金標法)檢測混合后的精漿標本是否含有相關傳染病病毒的抗原或抗體。留取篩查結果陰性的標本待用。
1.3.3補體滅活處理 將傳染病篩查結果為陰性的精漿標本置于56 ℃的水浴中30 min,以期進一步滅活病毒[16-17]。
1.3.4實驗分組 根據實驗中待測精漿質控品中加入穩定劑的種類分成A、B、C三組,分別添加占精漿30%的乙二醇、丙二醇、丙三醇作為穩定劑,三組質控品中均加入5%的氯霉素溶液作為抑菌劑,然后立即用漩渦振蕩器將其充分混勻。
1.3.5分裝保存 將制好的精漿生化質控品分裝于子彈頭離心管中,每管400 μL,每次制作150個,置于-20 ℃冰箱冰凍保存。
1.3.6用全自動精漿生化分析儀進行檢測 檢測項目包括中性α-葡萄糖苷酶、檸檬酸、果糖、鋅。
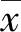
1.4統計學處理 (1)均勻性檢驗采用SPSS20.0軟件進行統計學分析,將測定結果進行單因子方差分析,若F小于自由度為(f1,f2)及給定顯著性水平α(通常α =0.05)的臨界值Fα(f1,f2),則表明質控品的均勻性良好。當測量數據樣品內均方MS2和樣品間均方MS1非常小,所計算出的F超過臨界值時,為獲得更客觀的統計結果,用SS≤0.3δ準則分析,若SS≤0.3δ,則表明質控品的均勻性良好。(2)穩定性檢驗采用SPSS20.0軟件進行統計學分析,將測定結果進行t檢驗,若t小于自由度為(n-1)及給定顯著性水平α(通常α=0.05)的臨界值tα(n-1),則表明質控品的穩定性良好。
2 結 果
2.1均勻性檢驗 A、B、C組精漿生化質控品F均大于2.39(臨界值),P<0.05,差異有統計學意義。進一步用SS≤0.3δ準則分析顯示,A組質控品中精漿中性α-葡萄糖苷酶SS>0.3δ,其余各組精漿生化質控品均SS<0.3δ。因此,只有A組質控品中的精漿中性α-葡萄糖苷酶存在明顯的瓶間差異。見表1、2。

表1 精漿生化質控品單因素方差分析結果
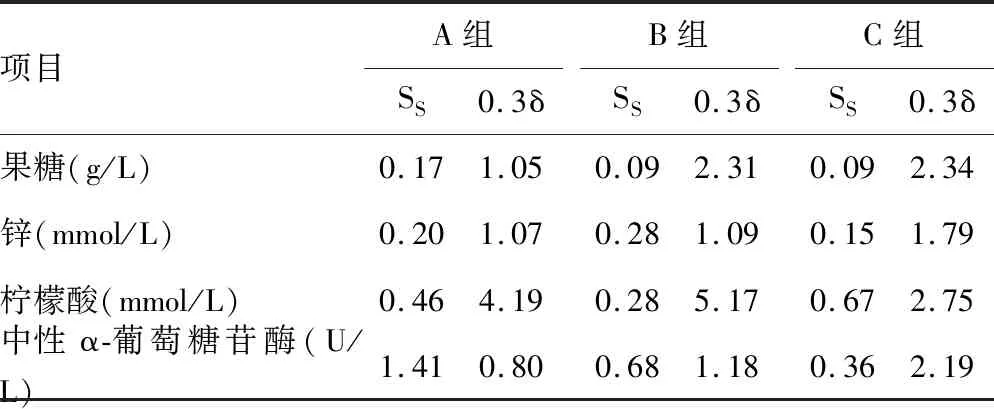
表2 精漿生化質控品SS≤0.3δ準則分析結果
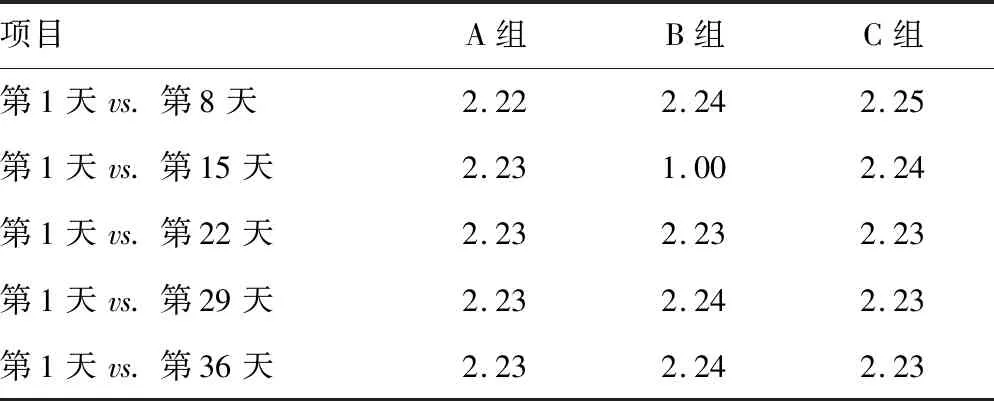
表3 精漿果糖質控品穩定性檢驗結果(t)
2.2穩定性檢驗 A、B、C組精漿生化質控品第8、15、22、29、36天的質控數據與第1天的質控數據進行t檢驗分析的結果均小于臨界值t0.05(5)(為2.57)。說明各組精漿生化質控品穩定性均符合要求。見表3~6。
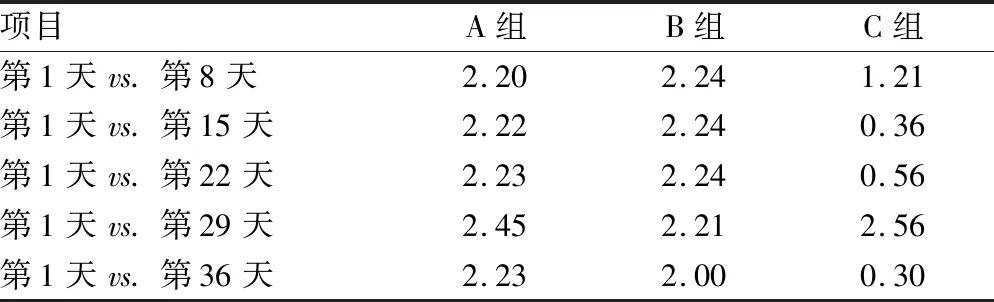
表4 精漿鋅質控品穩定性檢驗結果(t)

表5 精漿檸檬酸質控品穩定性檢驗結果(t)
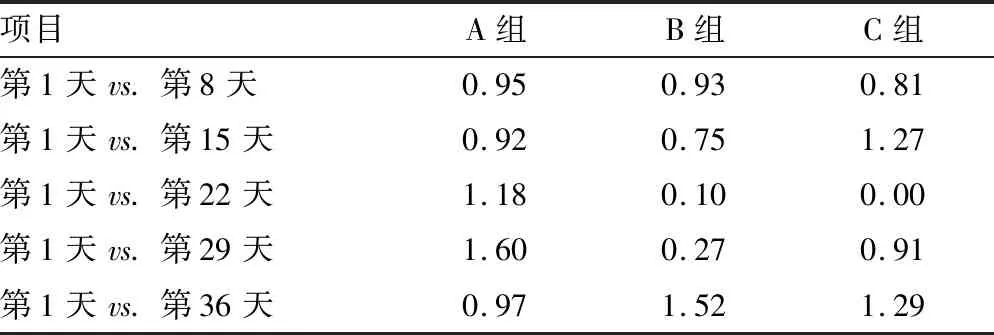
表6 精漿中性α-葡萄糖苷酶質控品穩定性檢驗結果(t)
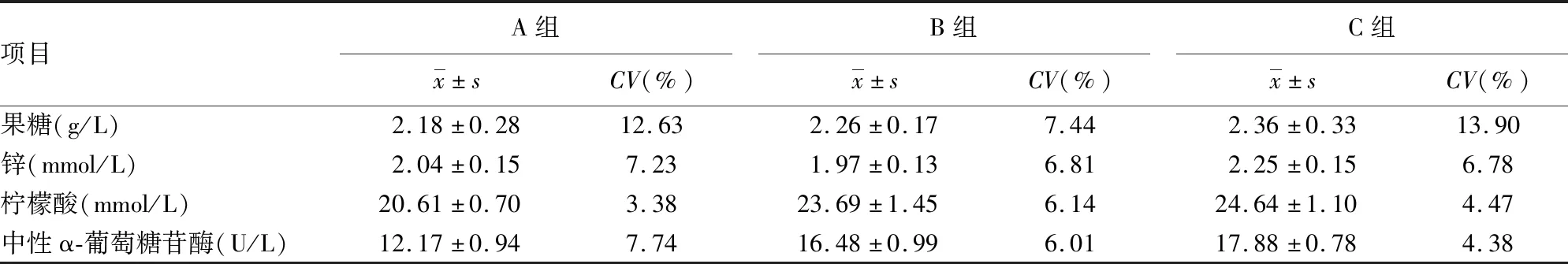
表7 精漿生化質控品常規質控監測
2.3常規質控監測 對自制精漿生化質控品連續進行3個月的常規質控監測,得到約20個質控數據,見圖1、表7。質控數據顯示,以乙二醇、丙二醇、丙三醇為穩定劑制備的精漿生化質控品結果均分布在±3s范圍內,CV值的變化均在15%以內。試驗發現B組的常規質控CV值均在10%以內,各個項目的穩定性最好。

圖1 各檢測項目的質控情況
3 討 論
目前男科實驗室質量控制措施薄弱,實驗室間精漿生化結果存在較大差異,主要原因是缺乏相應質控品或質控品正在研發過程中[22]。所以,積極開展精漿生化質控品的研究,不僅有利于提高精漿生化結果的準確度,為臨床提供準確可靠的結果,同時也可以減少實驗室質量控制成本,符合男科實驗室質量控制發展的迫切需求,具有巨大的社會和經濟價值。
大量研究顯示[7-13],乙二醇和丙三醇、1,2-丙二醇作為質控品穩定劑,氯霉素作為抑菌劑,常常被用于制備蛋白類檢測項目的質控品,而精漿生化項目恰好大多為蛋白類物質。本研究用文件CNAS-GL03提供的2種均勻性統計方法評價質控品均勻性。本實驗中單因素方差分析結果顯示,在 α=0.05 顯著性水平,配制的精漿生化質控品都存在瓶間差異。但是,由于測量數據的樣品內均方MS2非常小,應進一步用SS≤0.3δ準則進行均勻性分析。由于精漿生化項目為新開展的項目,實驗室目前尚無能力評價標準偏差目標值。為此,本研究參照生化項目的能力評價標準偏差目標值的計算方法[23]:總誤差(Tea)為參考生化項目的最大變異系數即30%,偏差(Bias)視為0,從而進行精漿生化項目的δ值計算,δ=(TEa-|Bias|)/CV。因此,可見以乙二醇為穩定劑配制的精漿質控品在中性α-葡萄糖苷酶項目上均勻性較差,而以丙二醇、丙三醇為穩定劑配制的精漿生化質控品在各項中均勻性良好。
精漿生化常規質控監測數據顯示,以乙二醇、丙二醇、丙三醇為穩定劑配制的精漿生化質控品測定的質控數據均均勻分布在±2s范圍內,CV值的變化均在15%[24]以內。但目前衛生部臨檢中心對精漿生化項目CV值沒有明確的規定,因此結合項目的特點參照類似的生化項目(按靶值±15%)進行評價,但下一步研究應根據不同的項目將不同CV值進行區分。因此,以乙二醇、丙二醇、丙三醇為穩定劑配制的精漿生化質控品用于果糖、鋅、檸檬酸、中性α-葡萄糖苷酶檢測的穩定性均良好。
自配質控品與商品化精漿生化質控品相比,其明顯優勢就是不受運輸條件影響,能有效避免運送過程中的不確定因素對質控品造成的影響。本研究對收集到的標本進行了56 ℃水浴加熱的處理,有效滅活了精漿中的病毒成分,確保了自制精漿生化質控品不含傳染性病毒[16-17]。
另外,在制作過程中用漩渦振蕩器充分混勻以盡量縮小瓶間差異,并以小劑量分裝保存,單次測定完可隨即丟棄,避免了由多次使用過程帶來的反復凍融造成質控品降解的情況。同時,自制精漿生化質控品均為人源精液,從而避免了額外的基質效應。但是,自制質控品并不能完全排除實際操作中的偶然誤差而導致的瓶間差增加,因此,為了保證較小的瓶間差異,在制備質控品時應嚴格按照實驗操作規程進行操作。
4 結 論
乙二醇組質控品精漿中性α-葡萄糖苷酶的檢測水平存在瓶間差異,可能是人員操作不當引起的。丙二醇組在精漿生化各項目質控中穩定性最佳,三種質控品性能評價結果均符合臨床要求,值得臨床實驗室推廣使用。

