流式熒光發光法聯合檢測肺癌患者血清CEA、CYFRA21-1、CA125及NSE的性能評價
趙 虹,紀秋野,王博揚
(吉林大學中日聯誼醫院,吉林 長春130033)
肺癌已經成為一種常見的癌癥類型,并被確定為中國癌癥死亡的主要原因[1],其發生、發展是一個多因素、多階段過程,伴隨著諸多分子及細胞生物學改變。有一系列的腫瘤標志物在肺癌的發生及發展過程中起到至關重要的作用,并且其在肺癌的診斷和后續治療監測中也顯得尤為重要[2]。例如神經元特異性烯醇化酶(NSE),即是小細胞肺癌(SCLC)患者的一種可靠的腫瘤標志物[3],而癌胚抗原(CEA)、癌胚抗原125(CA125)及細胞角蛋白19片段(CYFRA21-1)則被廣泛的應用于非小細胞肺癌(NSCLC)的研究中,而且CYFRA21-1的敏感性最強[4-9]。因此,選擇一種合理的腫瘤標志物的檢測方法,在癌癥患者疾病分型及后期用藥療效觀察方面均起到了至關重要的作用。目前常用的腫瘤標志物檢測方法主要有放射免疫法(RIA)、酶聯免疫吸附試驗(ELISA)、電化學發光法( ECLIA)等。本實驗采取的流式熒光發光法是一種基于熒光編碼微球和流式技術相結合的高通量發光檢測技術,對CEA、CA125、CYFRA21-1及NSE的血清表達水平進行檢測,并對檢測方法的準確性等方面其進行分析和評估。
1 材料與方法
1.1 檢測標本
選擇2018年3月至2018 年8月末,吉林大學中日聯誼醫院門診和住院的患者40例,用含分離膠和促凝劑的真空采血管采集各研究對象的空腹靜脈血3 mL,室溫靜置,3 500 r /min離心5 min,分離血清待檢。棄去溶血、脂血標本。本研究經醫院醫學倫理學委員會批準且患者知情同意。
1.2 試劑與儀器
多腫瘤標志物檢測試劑盒(上海透景生命科技有限公司),羅氏試劑盒(瑞士羅氏公司提供)、所用校準品、質控品均為各試劑盒原裝配套;Luminex多功能流式點陣儀(美國Luminex公司)、全自動流式熒光發光免疫分析儀(Tesmi F3999)羅氏電化學發光法檢測儀(Cobas e411Roche 公司,瑞士))、臺式低俗自動平衡離心機(北京時代北利DT5-2) 。
1.3 評價方法
按照美國臨床與實驗室標準化協會(CLSI)評價方案,在Luminex多功能流式點陣儀上評價本法的精密度、準確度(回歸實驗)、檢出限,并分析本法與電化學發光法檢測結果的相關性。
1.4 統計學分析
用SPSS 17.0 統計軟件進行數據統計分析。t檢驗和回歸分析,以P<0.05為差異有統計學意義。
2 結果
2.1 精密度驗證
本實驗選取上海透景腫瘤標志物質控品作為檢測標本,批號180601、180602。批內選取質控品各1份,各連續測定30次。批間選取質控品個1份,連續測定30天,每天測定1次。根據變異系數公式:C·V =(標準偏差SD /平均值Mean )× 100%,計算得知CEA、CA125、CYFRA21-1及NSE的批內變異系數(CV)均<10%,批間變異系數(CV)均<13%,見表1、表2。由結果可知,4種腫瘤標志物的批內及批間變異系數均較低,表明試劑在多次重復一次測定及多次測定中均有較高的重復性,數據準確度及精密度高。
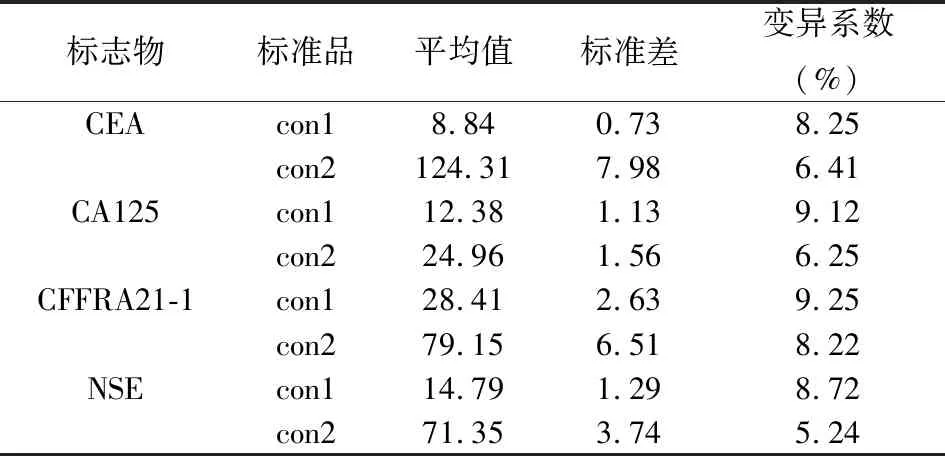
表1 流式熒光發光法精密度實驗批內結果
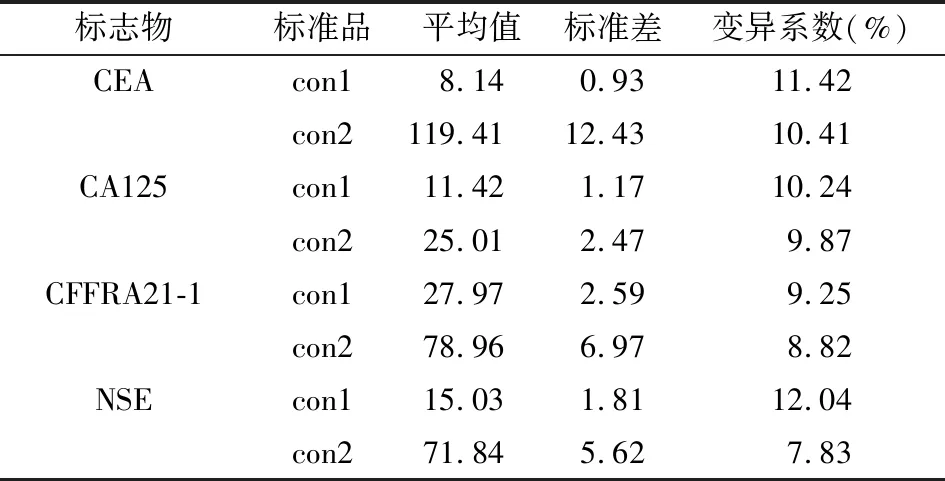
表2 流式熒光發光法精密度實驗批間結果
2.2 最低檢出限的測定
檢出限,是分析測定的重要指標之一,其對儀器的性能評價及方法建立都是重要的參數之一,本實驗將零號校準品作為空白對照,重復測定20次,計算平均值(X)與標準差(SD),以x±2s熒光信號值時對應的指標濃度作為各指標的最低檢測限。CEA、CA125、CYFRA21-1及NSE的最低檢出限值分別為0.5 ng/ml,10 u/ml,1 ng/ml和2 ng/ml。
2.3 流式熒光發光法參考區間的測定
利用流式熒光發光法測定一定數量的正常臨床樣本(n=300)的血清CEA、CA125、CYFRA21-1及NSE的表達水平,考慮到臨床檢測腫瘤標志物的檢測方法種類繁多,各檢測方法之間略有差異,本實驗根據百分位數法及結合經典文獻中的推薦值,建立4種腫瘤標志物的參考區間(表3)。對檢測數據進行正態性檢驗(Shapiro-Wilk 檢驗) 后,數據均呈非正態性分布。因此,采用百分位數法建立3 項腫瘤標志物的參考區間。表3所列為第95 百分位數(P95) 和第99 百分位數(P99) 的數值,以各標志物的P95作為參考區間的上限(臨界值)。
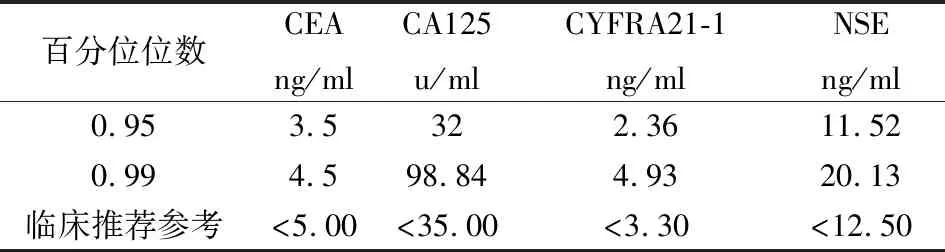
表3 腫瘤標志物臨床推薦參考值
2.4 不同檢測方法相關性的測定
選取40例臨床樣本,分別采用不同檢測方法對CEA、CA125、CYFRA21-1及NSE的表達水平進行檢測,進行方法學比對,其線性方程如圖1所示,結果列表見表4。結果顯示:透景試劑盒利用流式熒光發光法檢測的腫瘤標志物表達水平與羅氏電化學發光法檢測出的數據相關性良好(r>0.980)。
3 討論
本實驗利用Luminex多功能流式點陣儀,將多種不同熒光編碼的微球上分別以共價方式交聯針對CEA、CA125、CYFRA21-1及NSE這4種腫瘤標志物的單克隆抗體,并以一定數量混合,有效地提高了臨床檢測效率,顯著地降低了醫療成本。血清中各種腫瘤標志物會被對應的微球捕獲,然后加入生物素標記的針對上述各種腫瘤標志物配對的抗體及鏈親和素標記的PE混合物[10],以形成一種抗體-腫瘤標志物抗原-生物素標記的配對抗體-鏈親和素標記PE(藻紅蛋白)的混合物,從而通過多功能流式點陣儀判定出腫瘤標志物的種類及濃度,具有通量高、配套試劑多、應用領域廣、重復性好、既能檢測蛋白質又能檢測核酸等優點[11-13]。
本研究評估了流式熒光發光法檢測CEA、CYFRA21-1、CA125及NSE四種腫瘤標志物的精密度,由于FFA法對每種檢測指標最少進行100個微球的計數后取其平均值,從實驗結果分析上相當于對每個樣本額外重復了百次檢測,從而保證檢測結果的精密度和準確性。由結果可知,批內CV均<10%,批間CV均<13%,表明本法精密度較高。CEA、CA125、CYFRA21-1及NSE的最低檢出限值分別為0.5 ng/ml,10 u/ml,1 ng/ml和2 ng/ml,提示FFA法有較好的靈敏度。作者進一步以常規健康體檢患者血清水平的第95百分位數為參考區間上限,初步建立FFA法的CEA、CYFRA21-1、CA125和NSE的參考區間上限。最后,以金標準ECLIA為參考方法,通過與化學發光法比對試驗得知((rCEA) = 0.98917,(rCA125) = 0.99523,(r CYFRA21-1) = 0.99978,(rNSE) =0.99059),表明兩種方法檢測血清 CEA、CYFRA21-1、CA125和NSE具有較高的一致性及相關性。
綜上所述,FFA檢測 CEA、CYFRA21-1、CA125和NSE四種腫瘤標志物,僅需10 μl患者血清樣本,45 min便可得出結果,有效地提高了臨床檢測效率,可廣泛應用于急診患者的快速篩查。流式熒光發光法與常規免疫分析方法相比,具有靈敏度高,精密度好,檢測時間短,樣本用量少,醫療成本低等優勢,值得臨床推廣。

