犬特發性慢性肝炎病例報告
吳楚琳,張海霞,季玲西,呂艷麗,
(1.中國農業大學動物醫學院,北京 海淀 100193;2.中國農業大學動物醫院,北京 海淀 100193)
犬慢性肝炎(Chronic hepatitis,CH)的發病率較高,但該病的臨床癥狀、臨床病理學以及影像學檢查結果均不具有特異性,需依靠組織病理學檢查才能確診。臨床上,除了由銅蓄積或由部分藥物誘導所導致的CH以外,仍有一部分病例即使已進行了完整的檢查,但病因仍然不明的情況,認為是特發性CH。目前國內尚未見該病的病例報道。現報告一例犬特發性慢性肝炎如下。
1 病例情況
約克夏犬,9歲,雄性,已去勢,體重1.8 kg。家養,正常免疫、驅蟲。平日飼喂犬糧,排尿正常,大便成形。就診前一日進食后嘔吐成形犬糧。就診當日無飲食欲,無用藥史。患犬精神尚可,水合狀態尚可,黏膜淡粉色,未見黃染。
2 檢查
2.1 實驗室檢驗
2.1.1 血常規檢查 結果均在正常參考范圍內,未見明顯異常。
2.1.2 生化檢查 見表1,由表1可見ALT和AST輕度升高,提示輕度肝損傷或肝功能不全;白蛋白嚴重下降和球蛋白輕度下降,提示蛋白合成異常或蛋白丟失性疾病,肝功能不全的可能性較高;低血鈣可能與低白蛋白有關;總膽固醇降低,可能與肝功能異常相關。
2.1.3 尿液檢查 尿常規檢查未見明顯異常,UPC<0.20可排除蛋白丟失性腎病。
2.1.4 體腔液檢查 超聲引導下穿刺抽出5 mL微濁粉色腹腔液,有核細胞計數0.16×109/L,紅細胞總數為0.01×1012/L,比重為1.006,蛋白定量<2.0 g/dL,鏡檢未見明顯病原微生物,提示為漏出液。懷疑與低白蛋白血癥及早期肝功能不全相關。
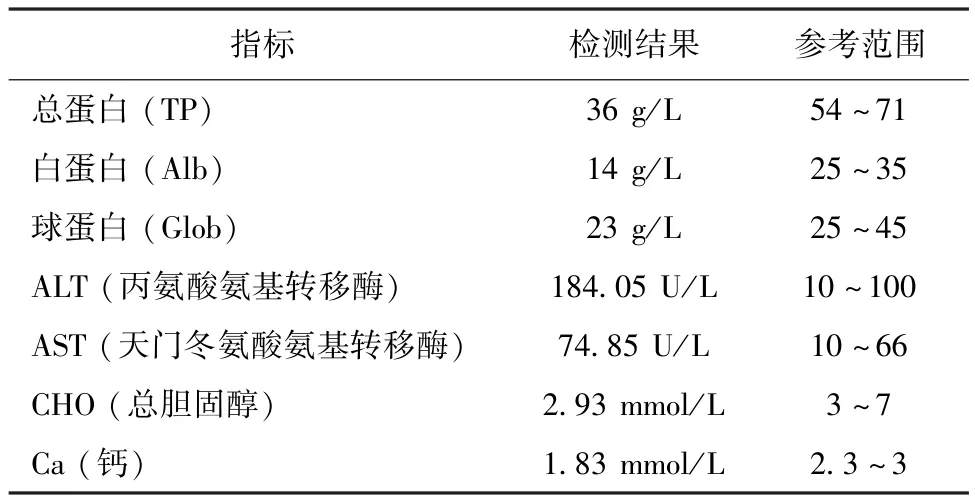
表1 血清生化檢查異常指標
2.2 影像學檢查 患犬胸部X線提示,右心輪廓輕度增大,心臟超聲未見明顯異常。腹部超聲則顯示胃腸道、肝膽、脾臟、胰腺形態亦未見明顯異常。僅見腹膜腔少量積液,可能與低白蛋白水平有關。
2.3 肝臟活組織檢查 鎮靜后,超聲介導下進行肝臟TRU-CUT活檢取4個樣本,送至德國納博科林實驗室檢查。行組織病理學檢查及H.E.、Azan和銅染色,結果診斷為門脈周混合型肝炎,伴有明顯的嗜中性粒細胞、淋巴細胞,門脈周纖維化和水腫性變性,提示病灶為慢性炎癥過程。
3 診斷
根據病史、癥狀及檢查結果,可排除蛋白丟失性腎病、心臟病和炎癥等導致的低白蛋白血癥。因患犬糞便一直成形,僅出現數次嘔吐,無其他明顯胃腸道癥狀,且胃腸道超聲未見異常,初步排除蛋白丟失性腸病。患犬血清ALT持續高于正常值,提示存在肝損傷。肝臟活檢證實存在慢性肝實質炎癥,銅染色未見陽性標記物進一步排除了銅蓄積性CH,故診斷該犬患有特發性CH。
4 治療
由于患犬低白蛋白血癥嚴重,先進行白蛋白作前期對癥治療,以800 mg/kg·d的劑量連續輸注3 d;同時使用保肝加強錠和口服蛋白片。待病理組織學結果確診特發性CH,每日1次使用潑尼松龍1 mg/kg·bw,19 d后用量減半。
5 轉歸及預后
發病初期僅以靜脈輸注白蛋白無法維持患犬血清白蛋白濃度,使用糖皮質激素治療后ALT一直下降至趨向正常,而血清白蛋白水平一直呈上升趨勢,最后穩定在正常水平。
6 討論
犬CH僅能通過病理組織學確診,臨床癥狀、臨床病理學及影像學檢查結果不具有特異性。世界小動物獸醫協會肝臟標準化組織(WSAVA Liver Standardization Group)已經發布了CH的定義及診斷標準。CH的特點是存在肝臟實質細胞發生纖維化、炎癥、凋亡和壞死[1]。CH的部分病因已知,包括銅蓄積以及部分毒/藥物誘導。大多數CH病因仍然不明,被定義為特發性CH。另外,不同于人類或其他動物,罕見由病毒或其他傳染性病原所導致的原發性犬CH[2]。一項相關研究中67例CH患犬經肝臟活檢后,36%確診為銅相關性CH,余下高達64%病因不明的特發性CH[3]。CH的確診需借助于組織病理學診斷,雖然據國外報道該病的發病率較高,但是由于國內獸醫和寵物主人對于取樣的認識不足,所以組織病理學檢查在臨床疾病診斷中的應用十分局限。本文所報道的病例亦為特發性CH,其肝臟活檢銅染色未見銅蓄積,且并無相關的傳染病史和毒/藥物接觸史。
不管何種病因的犬CH,任何品種、年齡及性別均可發病,且癥狀及臨床表現均不具有特異性。常見癥狀有厭食、嘔吐、多飲多尿、沉郁、腹瀉、體重減輕、腹水和肝性腦病等。研究指出,部分CH病例在就診時可能表現為亞臨床狀態,除肝酶活性增加以外不一定出現臨床癥狀[3],所以此時檢查血清白蛋白和膽汁酸等肝功能指標尤為重要。本病例患犬除肝指標稍有異常以外亦無明顯臨床癥狀。另外,若監測到ALT長期高于正常水平也有助于提示獸醫患犬可能存在持續的慢性肝損傷。
影像學檢查可提供肝膽系統病變的有用信息,并排查癥狀相似的其他疾病。如本病例患犬為約克夏犬,是蛋白丟失性腸病如腸淋巴管擴張癥的易發品種[4]。蛋白丟失性腸病與犬CH同樣會出現低白蛋白血癥,但早期腸道病變可能無明顯的癥狀及影像學形態改變,更何況目前在小動物臨床上無法檢測出經腸道糞便丟失的蛋白。因此,對于該犬,應注意觀察胃腸道癥狀,以及定期進行胃腸道超聲檢查以徹底排除蛋白丟失性腸病的可能。
雖然犬CH可基于品種、病史、癥狀和實驗室檢驗結果進行初步診斷,但只有肝臟活檢和組織病理學檢查才是正確診斷的關鍵,并有助于制定后續特異性治療的方案。肝臟活檢方法包括細針抽吸、TRU-CUT法、以及楔形活檢法(腹腔鏡或開腹術),其唯一的絕對禁忌癥是嚴重的凝血障礙[5],應在活檢前24 h內進行凝血試驗,并注意監測患犬出血情況。本病例選用了TRU-CUT法,它既不像楔形活檢需要在患犬全麻的情況下才能進行,也較細針抽吸更能得出準確的結果;但應注意肝臟 TRU-CUT活檢需在超聲引導下進行,并采集來自于不同肝葉的多個樣本,以提高活檢結果的準確性。
肝臟纖維化是犬CH發展中病理學變化的關鍵。CH患犬肝臟組織病理學均可見不同程度的纖維化和肝細胞凋亡/壞死,并出現炎性細胞浸潤[1]。已經有研究指出,部分血清標志物能提示肝纖維化的出現,但直接或間接血清標志物都不可能代替肝活檢標本的組織病理學評估[6],因為組織學才可對慢性肝炎進行明確的診斷,并查明是否出現銅蓄積,因此進行肝臟病理組織學檢查時必須進行銅染色。要注意的是,由于細菌性膽囊炎導致的臨床癥狀和病理學異常與CH十分相似,本病例中患犬的肝臟組織學檢查中發現炎性浸潤主要存在于門脈周圍區域,因此也應考慮行膽囊穿刺及膽汁培養以排除來源于膽管的感染性因素,這將有助于獸醫師進行正確的鑒別診斷。
除了針對銅蓄積的抗銅治療外,目前仍缺乏可針對犬CH的特異性治療。然而,非特異性治療能顯著提升CH患犬的生活質量。治療犬特發性CH的主要目的是抑制纖維化和治療肝病臨床癥狀,且飲食控制也是CH患犬治療方案中的關鍵。糖皮質激素是CH患犬最常用的免疫抑制藥物,在本病例中我們選用了1 mg/kg·bw的潑尼松龍作為主要用藥,多個研究指出,糖皮質激素具有抗炎、免疫調節和抗纖維化的作用[2-7],可延長生存期,改善及緩解肝細胞損傷,但應慎用于肝纖維后期或肝硬化患犬[5]。一旦患犬達到臨床緩解,劑量應逐漸降低至維持量。同時,建議使用熊去氧膽酸等抗氧化劑作為標準治療的輔助手段,可有助減少慢性肝炎犬的肝損傷和纖維化[7]。
肝細胞具有良好的再生能力,這意味著早期診斷和治療具有逆轉疾病機制的可能。獸醫應了解肝臟活檢對犬CH的必要及重要性,以目前對犬CH的研究進展為基礎,結合組織學、臨床表現和實驗室檢驗結果,合理進行肝臟活檢以確診疾病及評估其嚴重程度,以便開展適當的治療及選擇合適的治療藥物,以改善患犬的生活質量和預后。

