84Sr稀釋劑中鍶同位素組成的準確測定
張天睿,曾 遠,顏 妍,湯書婷,朱鍵銘
(核工業北京地質研究院,北京 100029)
同位素稀釋質譜法是國際公認的基準方法,在Rb-Sr、Sm-Nd定年方法中應用廣泛,采用同位素稀釋法分析可同時得到樣品中元素的同位素含量和比值,節省測量的時間,提高結果的準確度,但也給同位素測量過程中質量分餾校正帶來了困難。以稀釋法測定樣品中鍶同位素含量和比值測定為例,稀釋劑的加入,參考比值86Sr/88Sr不再為恒定的0.119 4,其比值隨混合稀釋比的不同而不同,使得常規質量分餾的校正方法 (如指數定律校正方法)不再適用。部分實驗室采用分樣的方法進行測定,即一份加稀釋劑測定含量,另一份不加稀釋劑測定同位素比值,兩次測定(加稀釋劑和原樣)限制了同位素稀釋法的廣泛使用[1]。 DZ/T 0184.4—1997 標準方法推薦使用稀釋分析法進行銣鍶同位素地質年齡的測定[2],沒有給出質量分餾的校正方法。因此采用稀釋法測定鍶同位素比值需要解決兩個問題:一是對84Sr稀釋劑中鍶同位素質量分餾如何進行校正以獲得稀釋劑鍶同位素的真實比值?二是稀釋劑和樣品混合溶液中鍶同位素比值如何進行質量分餾校正?
在同位素比值的測量過程中,常用的質量分餾校正模式包括線性定律校正方法、冪定律校正方法和指數定律校正方法三種[3-4]。質量分餾效應較小時,三種質量分餾校正模式得到的校正值是一致的[5],部分研究人員認為在單稀釋劑方法中冪定律和指數定律校正方法可得出相近的結果,但線性定律校正方法的校正結果與前兩種方法相比存在較大誤差,故很少應用。然而,在雙稀釋劑法[6-8]應用中常使用線性定律校正方法修正得出的指數近似模式質量分餾校正方法對測試結果進行質量分餾校正。
為了消除質量分餾效應的影響,使得稀釋法得到更為精準的同位素比值,Chu等[9]對熱電離質譜稀釋法分析釹同位素的分餾校正方法進行了詳細探討,采用冪定律校正模式建立了適用于靜態多接收和動態多接收的稀釋分析同位素分餾校正計算方法,同時介紹了稀釋劑同位素的質量分餾可采用數學迭代方法進行校正,但冪定律校正模式應用于稀釋法分析,其質量分餾系數計算公式過于復雜,應用時需忽略一些影響因素。Gioia[5]采用較為簡便的線性校正方法對Sm-Nd同位素的質量分餾進行校正,得到釹同位素比值的計算方法。
通過比較線性定律、指數近似模式和指數定律質量分餾校正方法對鍶同位素質量分餾校正結果,分析指數近似模式替代指數定律分餾校正方法,建立基于指數近似模式的質量分餾校正方法計算稀釋劑測量過程中的質量分餾校正因子,得到84Sr稀釋劑同位素的真實比值,以減少稀釋法測定鍶同位素比值測量過程中稀釋劑加入量對測量結果的影響,在此基礎上,以期得到混合樣品中鍶同位素比值的計算方法,提高稀釋法同位素測量的準確度。
1 質量分餾校正方法和同位素稀釋法的計算
同位素稀釋質譜法是基于同位素質譜測量與準確化學計量相結合的元素分析手段,其測量結果準確,不確定度小,該方法對樣品前處理要求較低,僅需保證稀釋劑與樣品混合均勻即可,回收率對測量結果幾乎無影響。但該方法受同位素比值測量準確度的影響較大,影響同位素比值準確度的因素主要來源于同位素測量過程中的質量分餾效應。離子的熱運動速率與它們的質量平方根成反比,在熱電離過程中隨測量時間的延續,輕質量同位素優先蒸發,重質量同位素逐漸被濃縮。所以,測量的同位素豐度比隨測量時間的延續不斷變化。導致測量結果與真值(參考值)有一定偏倚,故需對測量結果進行質量分餾校正。
1.1 常用的質量分餾校正方法
常用的質量分餾校正模式有線性定律校正方法、冪定律校正方法和指數定律校正方法三種,在雙稀釋劑法中常用對線性定律校正方法修正得出的指數近似模式校正方法。
線性定律校正方法[5]如下:

指數定律校正方法[4]如下:

冪定律校正方法[9]如下:

指數近似模式校正方法[10]如下:

式中:Rm—測量值;f—質量分餾校正系數;m1、m2—相對原子質量;Δm—相對原子質量數之差。
線性定律校正方法和指數近似模式校正方法與冪定律方法、指數定律方法相比,計算過程相對簡便,可以直接得到測量過程中的質量分餾校正因子。
1.2 同位素稀釋法比值的計算
同位素稀釋法是在樣品消解前,將稀釋劑加入樣品中與樣品一起消解,保證稀釋劑和待測樣品的化學性質相同,化學形式也必須一致,同位素豐度組成不同。在混合溶液中,待測樣品和稀釋劑必須混合均勻,充分交換達到化學平衡。以同位素稀釋法測定鍶同位素為例介紹稀釋分析同位素的計算方法:
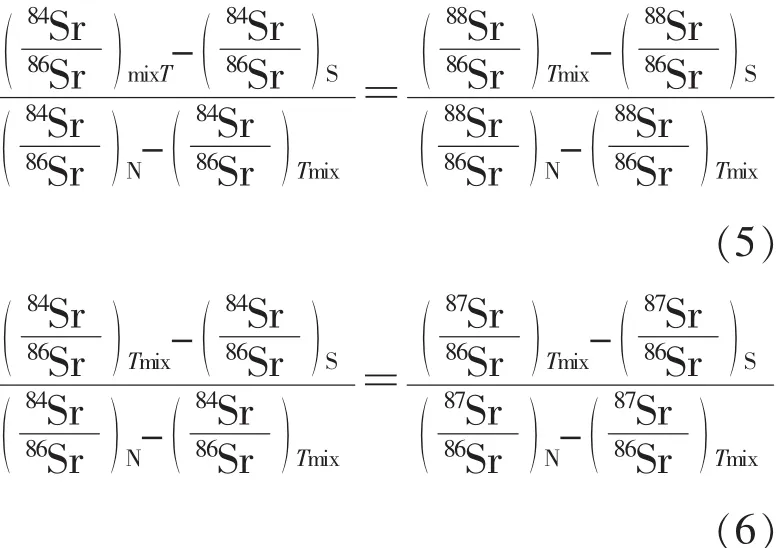
式中:N—樣品;S—稀釋劑;Tmix—樣品和稀釋劑的質量分餾校正的混合比值。
依據公式(6)可得出稀釋分析樣品中87Sr/86Sr的計算公式(7):

2 實驗部分
2.1 主要試劑及儀器
PHOENIX型熱電離質譜儀,英國GV儀器公司產品;十萬分之一分析天平;聚四氟溶樣罐;亞沸蒸餾純化MOS級HCl;鍶單元素標準溶液;84Sr稀釋劑。
2.2 鍶同位素比值的測定
使用Phoenix型熱電離質譜儀進行鍶同位素比值的測量,采用多接收測量,多個法拉第杯檢測器同時接收離子流,所以工作前需要進行法拉第杯之間的增益測量。測試流程包括:點樣、測試、數據處理等。開始鍶同位素測量前,應當清洗整個樣品盤,然后更換每個樣品位置的電離蓋。
2.2.1 點樣
取10 μL去離子水浸潤樣品杯底 (確保杯底全部被水浸潤),取6 μL溶液于錸金屬帶上,在1 000 mA電流烤干,加2 μL鉭發射劑于烤干的樣品上,于1 000 mA電流烤干,緩慢增加電流至樣品帶紅化后迅速關閉電源。
2.2.2 測試
按鍶測量升溫程序將樣品帶升溫至2 800mA,提高電流,使溫度升至1 550℃左右,停留約10 s以去除銣的干擾,電流迅速降回2 800 mA,打開隔離閥,調節聚焦參數,使88Sr離子流強度達到3 000 mV左右開始進行數據采集。
2.2.3 數據處理
非稀釋法鍶同位素比值校正至86Sr/88Sr=0.119 4。對稀釋劑、稀釋劑和鍶標準溶液混合溶液,測定84Sr/86Sr、87Sr/86Sr和88Sr/86Sr原始值。
3 結果與討論
3.1 不同質量分餾校正方法比較
對非稀釋法鍶同位素比值的測量,通常采用指數定律進行質量分餾校正,通過測定不同鍶豐度樣品,對采用線性定律、指數定律和指數近似模式的質量分餾校正結果進行對比,見表1。結果顯示,線性定律校正結果與指數定律校正結果存在較大差異,而指數近似模式校正結果與指數定律校正結果比較一致(δ<0.005‰)。
3.2 稀釋劑和樣品混合溶液中鍶同位素比值質量分餾校正因子的計算
由表1的結果可見,指數近似模式與指數定律校正結果一致,且計算相對簡單,故可替代指數定律校正方法對鍶同位素比值測量過程中的質量分餾效應進行校正。
以稀釋法分析測定鍶同位素為例介紹指數近似模式公式如下:
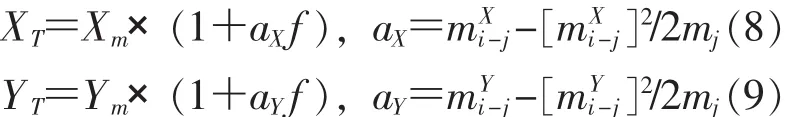

表1 不同質量分餾校正方法結果比較Table 1 Results of different mass fractionation correction methods
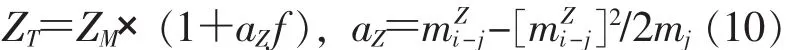
式中:X,Y,Z—84Sr/86Sr,88Sr/86Sr,87Sr/86Sr的同位素比值;T,M—校正值和測量值;f—質量分餾校正因子;a—質量差異系數的相對原子質量。
將公式(8)和公式(9)帶入公式(5)得稀釋分析同位素質量分餾校正系數f的計算公式(11):
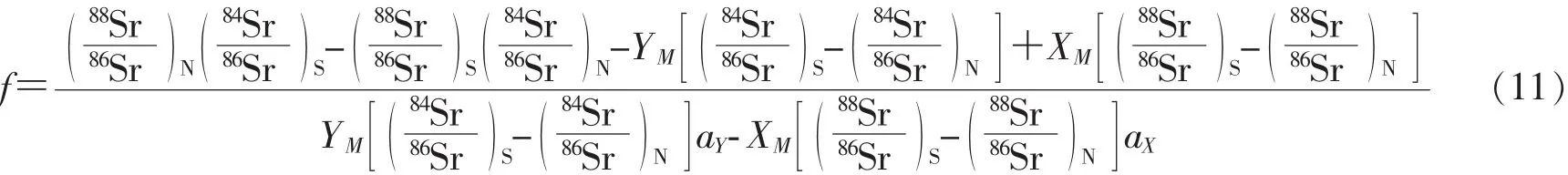
3.3 稀釋劑加入量對鍶同位素比值測量結果的影響
鍶單元素標準溶液(編號為a)和84Sr稀釋劑溶液按 1:0.5、 1:0.7、1:0.8、1:1、1:2、 1:5和1:10比例 (分別編號b、c、d、e、f、g和h)于潔凈的聚四氟溶樣罐中,充分混合后至于電熱板蒸干,加1滴1 mol·L-1HCl溶液,再次蒸干,以達到同位素平衡,得到不同稀釋比的樣品和稀釋劑混合溶液,按2.2.1點樣測試混合溶液鍶同位素比值 (84Sr/86Sr)Mmix、(87Sr/86Sr)Mmix、(88Sr/86Sr)Mmix, 同時測定84Sr稀釋劑溶液鍶同位素原始比值 (84Sr/86Sr)S、(87Sr/86Sr)S、 (88Sr/86Sr)S。

表2 不同混合稀釋比下稀釋分析鍶同位素比值結果Table 2 Sr isotope ratio result of spiked analysis using different mixture ratios
將上述比值的測量結果代入公式 (11)得到混合溶液中鍶比值的質量分餾因子。按公式(8)、 (9)、 (10)計算鍶混合樣品的比值校正結果。將校正的結果代入公式(7)中得到標準溶液中的 (87Sr/86Sr)N, 計算結果列于表2。 可以得出,隨著混合稀釋比增大,計算得到樣品的87Sr/86Sr與參考值(0.714 012)偏離越來越大,說明結果誤差來源于稀釋劑中鍶同位素比值的偏離。
3.4 84Sr稀釋劑中鍶同位素比值質量分餾的校正
稀釋劑中鍶的同位素比值的精確測定對提高稀釋法測定樣品中鍶同位素比值是非常重要的。但84Sr稀釋劑中鍶同位素比值不同于非稀釋法測定樣品中的鍶同位素可以利用參考比值86Sr/88Sr=0.119 4進行質量分餾校正。故需要引入新的方法對其進行校正。
設定84Sr稀釋劑鍶同位素質量分餾系數,按下列公式計算稀釋劑鍶同位素比值。

式中:X,Y,Z—稀釋劑中84Sr/86Sr,88Sr/86Sr,87Sr/86Sr的同位素比值,T和M—校正值和測量值,fS—稀釋劑的質量分餾校正因子,a—質量差異系數的相對原子質量。
假設84Sr稀釋劑的鍶同位素比值的初始質量分餾因子fS=0,計算得到表2結果。利用規劃求解函數進行數學迭代,通過改變fS值,使偏差值δ之和最小(小于萬分之三),從而得到稀釋劑鍶同位素的質量分餾系數fS=0.004 2,將fS按公式(12)、 (13)、 (14)計算得到稀釋劑同位素比值的校正值(84Sr/86Sr)S=22.153 38,(87Sr/86Sr)S=3.425 945,(88Sr/86Sr)S=0.426 076。不同混合稀釋比下稀釋分析鍶同位素比值校正結果見表3,可以看出不同混合稀釋比樣品中的鍶同位素比值在誤差范圍內與非稀釋鍶同位素測量的比值是一致的,說明該計算接近稀釋劑中鍶同位素的真實比值,可以消除測試過程中分餾效應的影響,提高稀釋法同位素測量的準確度。

表3 不同混合稀釋比下稀釋分析鍶同位素比值校正結果Table 3 Corrected Sr isotope results of spiked analysis using different mixture ratios
4 結論
在比較線性定律、指數定律和指數近似模式質量分餾校正方法對鍶同位素比值校正結果影響的基礎上,利用指數近似模式質量分餾校正方法取代指數定律校正方法,建立了稀釋法分析鍶混合樣品中鍶同位素的質量分餾因子和樣品中鍶同位素比值的計算方法。利用不同混合稀釋比下稀釋分析樣品中鍶同位素比值與非稀釋鍶同位素比值的差異,采用規劃求解函數進行數學迭代,計算出稀釋劑鍶同位素比值測量過程中質量分餾因子fS=0.004 2 和同位素比值 (84Sr/86Sr)S=22.153 38,(87Sr/86Sr)S=3.425 945, (88Sr/86Sr)S=0.426 076。采用校正后稀釋劑鍶同位素比值計算出不同混合稀釋比樣品中的鍶同位素比值在誤差范圍內與非稀釋鍶同位素測量的比值是一致的,說明該計算方法達到對稀釋劑同位素比值質量分餾效應進行校正的目的,消除了測試過程中分餾效應的影響,提高了稀釋法同位素比值的測定準確性。

