羊水細胞染色體檢測結果與產前診斷指征的關系研究
趙玨 孫娟 袁武鋒 李麗潔
出生缺陷指胎兒出生前已經存在的結構或功能異常,其產生原因包括遺傳、環境及兩者共同作用。據統計,由遺傳因素為主所致的出生缺陷占比約為20%~30%,由環境因素(如母體疾病、營養不良、感染、藥物等)所致的出生缺陷占比約10%,剩余的出生缺陷多是遺傳和環境共同作用的結果,故超過80%的出生缺陷與遺傳因素直接或間接相關[1]。隨著我國經濟的快速發展,醫療衛生水平的不斷提高,人們對優生優育日益重視,感染、藥物使用不當、營養不良等導致的胎兒發育異常比例下降,而遺傳因素引起的出生缺陷檢出率升高[2]。染色體病是導致出生缺陷的最常見原因之一,約0.5%新生兒患有染色體病[3]。染色體病目前尚無有效的治療方法,唯一可行的預防手段是及時進行產前診斷,防止嚴重的出生缺陷。故為了減輕患者、家庭及社會的經濟和精神負擔,應爭取對有指征的孕婦行產前診斷,必要時及時終止妊娠。
細胞染色體核型分析是目前公認的產前診斷的“金標準”,羊膜腔穿刺術是現今產前診斷最常用且最安全的取材方法。本文回顧性分析有產前診斷指征,即高齡、血清學篩查異常、無創性產前檢查(non-invasive prenatal testing,NIPT)高風險、超聲檢查異常、既往生育過缺陷兒、父母一方患有先天性或遺傳性疾病或有遺傳病家族史等的448例孕婦羊膜腔穿刺羊水細胞的染色體核型結果,以及根據不同穿刺指征選用的分子生物學技術,如染色體微陣列分析(chromosomal microarray analysis,CMA)750K基因組芯片、基于微陣列的比較基因組雜交(array-based comparative genomic hybridization,aCGH)及衍生技術 CGX 寡陣(CGX Oligo arrays)8×60K和細菌人工染色體微珠(bacterial artificial chromosome on beads BAC-on-Beads,BoBs)技術獲得的結果,探討羊水細胞染色體異常核型與產前診斷指征的關系,比較不同產前診斷指征的染色體異常檢出率,以及不同的遺傳學檢測技術在臨床的應用價值,為產前遺傳咨詢提供客觀的實驗數據和臨床參考資料。
1 對象和方法
1.1 對象 2016年11月至2018年11月在我院產前診斷中心接受羊膜腔穿刺產前診斷的妊娠婦女共448例,年齡20~46歲,孕周17~26周。其中瘢痕子宮87例,年齡≥35歲的高齡孕婦163例。將高齡組按年齡分為3組,A組年齡≥35歲,但<38歲,共57例;B組年齡≥38歲,但<40歲,共45例;C組年齡≥40歲,共61例。對具有以下至少1項產前診斷指征的孕婦,在知情同意后行超聲引導下羊膜腔穿刺術,行產前診斷。侵入性產前診斷的指征為:(1)妊娠年齡≥35歲;(2)孕婦血清學篩查高風險;(3)NIPT篩查高風險;(4)胎兒超聲篩查異常:結構異常、可疑畸形、2個及以上軟指標異常、頸項透明層(nuchal translucency,NT)厚度≥3mm等;(5)既往生育過缺陷嬰兒;(6)父母一方患有先天性或遺傳性疾病,或有遺傳病家族史;(7)其他高度懷疑染色體異常的情況。
1.2 方法
1.2.1 標本采集 簽署相關知情同意書,完善術前檢查后,所有孕婦接受B超引導下經腹羊膜腔穿刺術,抽取羊水25~30ml,其中20ml用于染色體核型分析,另5~10ml根據穿刺指征及患者的知情選擇,選擇產前BoBs、CGX 8×60k或CMA-750k等檢測。
1.2.2 胎兒染色體核型分析 將20ml羊水分裝至2支15ml離心管,1 200r/min離心后,棄去上清液,沉淀中加入廣州白云山拜迪生物醫藥有限公司的羊水細胞培養基(批號:20160902-20180502)4ml/瓶,接種 2 瓶,5%CO2培養箱中37℃培養6d后觀察細胞生長,有多個細胞集落生長即換液,每天觀察,視細胞生長情況擇機收獲。以胰蛋白酶消化法制片,Giemsa染色后G顯帶,按人類細胞遺傳學命名國際體系(ISCN,2005)描述異常核型。核型分析:每例取材需來自2個不同培養瓶,每瓶計數10~15個分裂相,采集3~5個核型圖,嵌合體計數適當增加,計算異常細胞比例。
1.2.3 產前BoBs及CGX 8×60k檢測 由蘇州Perkin Elmer醫學檢驗所完成,7~12個工作日出報告。
1.2.4 CMA-750k檢測 由浙江博圣生物負責完成,15個工作日出報告。
1.3 統計學處理 采用SPSS 17.0統計軟件。計數資料以例數和百分率(%)表示,組間比較采用χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 羊膜腔穿刺結果分析 448份羊水細胞中,檢出異常核型38例,檢出率8.48%,以高齡為穿刺指征的163例,與其他穿刺指征比,受檢人數占比最高,達36.38%,但異常核型檢出率只有9.82%;以血清學篩查21-三體高風險為穿刺指征的127例,受檢人數占比28.35%,異常核型檢出率3.94%;以超聲篩查異常為穿刺指征的78例,只占受檢人數的17.41%,但異常核型檢出率有11.54%,見表1。某些孕婦合并有多個羊膜腔穿刺指征,在統計歸類時造成了一定困擾,為避免重復計數,將合并有多個產前診斷指征的歸類到最常用(高齡)或風險值相對較高的穿刺指征(如超聲篩查異常)組,高齡合并超聲篩查異常的,若超聲提示為結構異常或畸形,歸為超聲組,若僅為多個軟指標異常,則歸入高齡組。
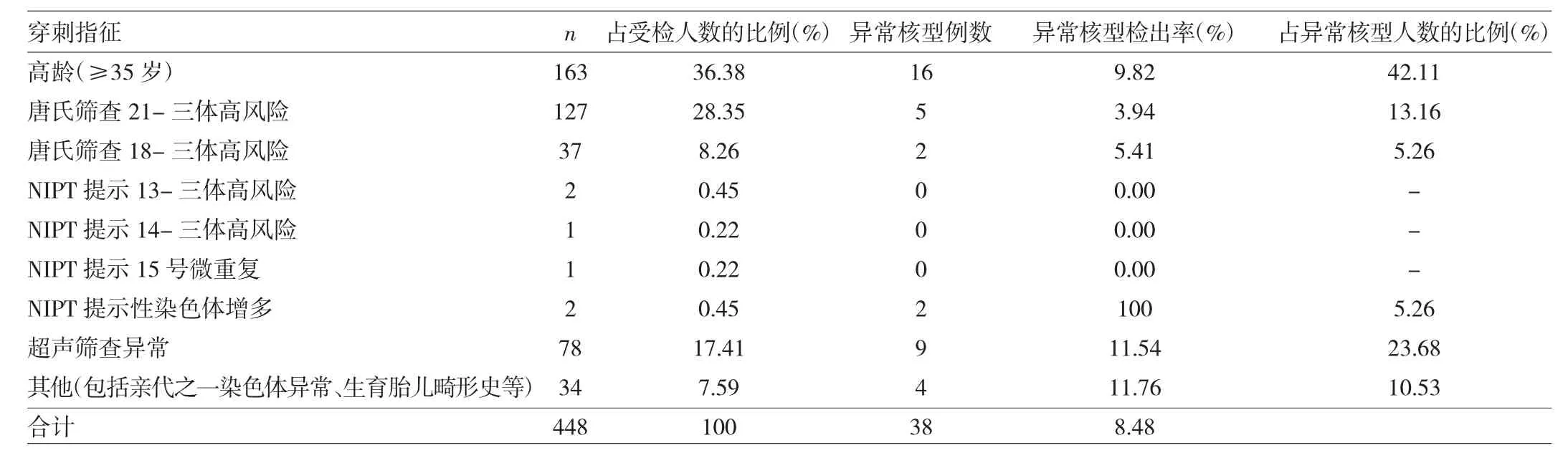
表1 羊膜腔穿刺結果分析
2.2 胎兒染色體異常核型分析 448例孕婦羊膜腔穿刺均成功,無一例出現流產、羊水滲漏、感染等并發癥而導致不良后果。羊水細胞培養成功率為99.78%(447/448),共檢出異常核型38例,包括染色體數目異常24例、結構異常12例和2例多態變異;其中21-三體8例,占異常核型比例21.05%;18-三體6例,占15.79%,21-三體和18-三體中均有1例為嵌合體。異常核型對應的穿刺指征中高齡和超聲篩查異常占比最高。因唐氏篩查21-三體高風險行產前診斷的發現核型異常5例,但其中核型確診為21-三體的只有2例,其余3例分別為21號和13號染色體平衡易位,47,XXX和46,XN,dup(9)(q12),唐氏篩查 18-三體高風險也存在同樣情況,見表2。
2.3 核型分析與分子生物技術檢測結果分析 核型分析與分子生物技術檢測結果分析見圖1。核型或分子生物技術檢測出異常的近三分之一伴有超聲異常發現。15例染色體核型分析異常,但未被當時同步進行的BOBs或CGX檢測所檢出。5例臂間倒位,其中4例發生在9號染色體,且有 3 例為 46,XN,inv(9)(p11q13);3 例臂內片段復制,也均出現在9號染色體,且有2例為46,XN,dup(9)(q12);1 例羅氏易位;1 例平衡易位;1 例臂內倒位;1例低比例的三倍體嵌合體;1例46,XN,1qh+,1號染色體長臂異染色質區增加;1例47,XN,+mar;1 例 46,XN,22ps+,一條 22 號染色體隨體偏大,B超提示消化道閉鎖可能。另有1例因胎兒水腫伴頸部水囊瘤形成行羊水細胞核型+CGX檢測,核型結果為46,X,+mar,分裂相少,CGX 檢測結果為 45,X。1例因 21三體高風險行羊水穿刺,BoBs提示17p11.2區域缺失,為Smith-Magenis綜合征,但核型提示正常。
2.4 不同遺傳學檢測方法檢出率比較 所有的羊膜腔穿刺均行羊水細胞培養染色體核型分析,告知患者各遺傳學檢測方法檢測范圍及局限性,若單純因高齡或血清學篩查高風險行產前診斷的一般選擇同步行產前BoBs檢測(患者選擇CGX檢測的例外);合并有超聲篩查異常的或合并有兩個及以上產前診斷指征的,2017年均選擇同步行CGX8×60k檢測,2018年選擇同步行CMA-750K檢測。不同遺傳學檢測方法染色體異常檢出率的差異無統計學意義(χ2=4.154,P=0.245),進一步兩兩比較,各方法間差異均無統計學意義(均P>0.05),見表3。2.5 高齡組不同年齡段染色體核型檢測結果比較 高齡組不同年齡段間染色體異常檢出率的差異無統計學意義(χ2=4.674,P=0.124)。進一步兩兩比較時,A 組染色體異常檢出率低于C組,差異有統計學意義(χ2=3.927,P=0.049),其余各組比較差異均無統計學意義(均P>0.05),見表 4。
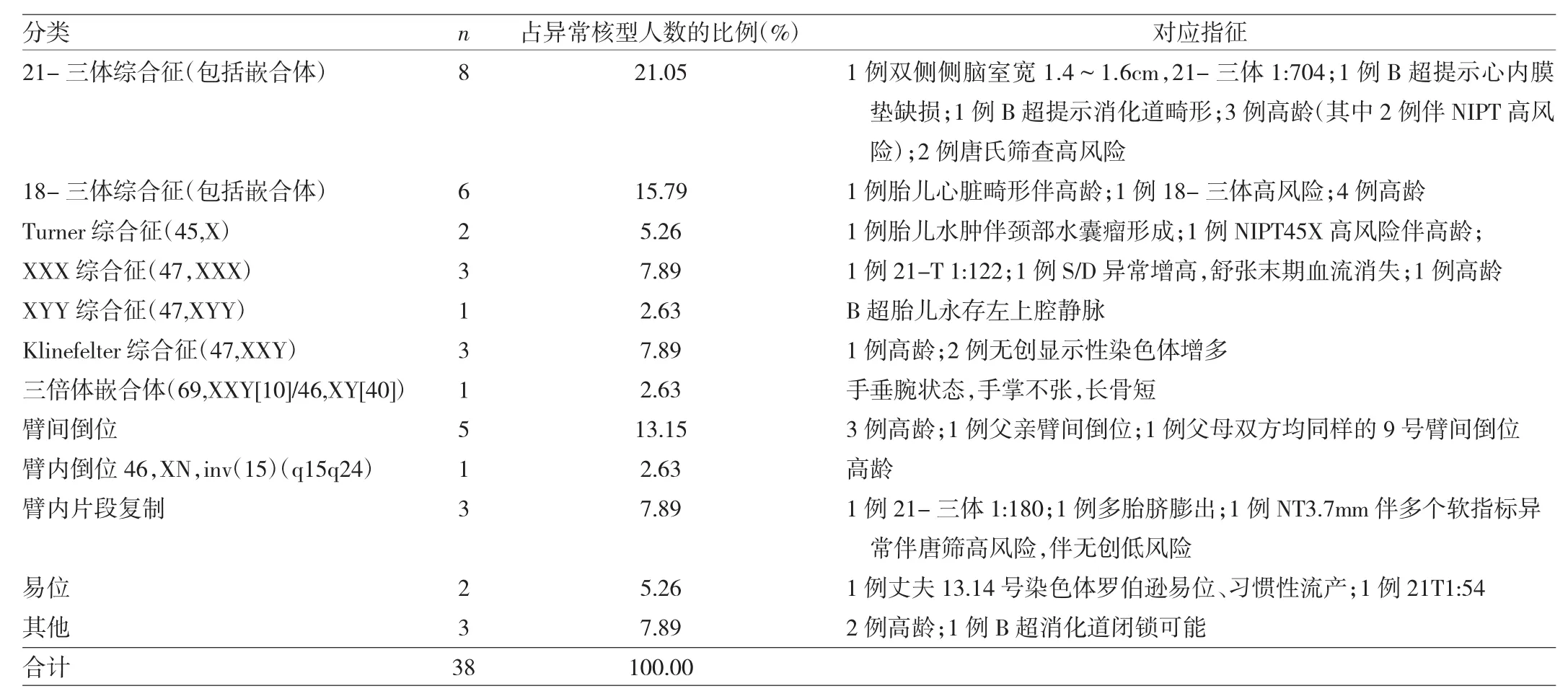
表2 胎兒染色體異常核型分析
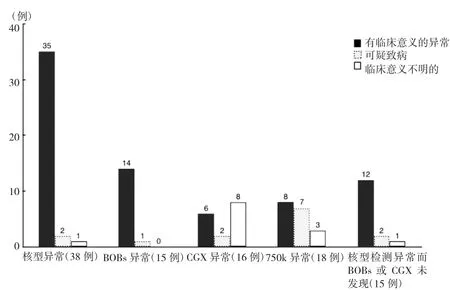
圖1 核型及分子生物技術檢測異常數據統計

表3 多種遺傳學檢測方法檢出率比較
3 討論
染色體異常是目前仍無法治療的先天性疾病,經過羊水細胞培養獲得胎兒染色體核型的準確性可達99%[4]。高質量的羊水細胞培養及收獲技術是進行羊水染色體分析診斷的關鍵[5]。本研究448例患者中,87例為瘢痕子宮,穿刺過程均順利,無不良后果產生。某些學者對于瘢痕子宮是否能進行侵入性產前診斷持謹慎態度,根據本研究結果,認為瘢痕子宮并非羊膜腔穿刺禁忌證。羊水細胞培養成功率為99.78%,發現38例染色體異常,檢出率為8.48%,高于相關文獻報道結果1%~6.7%[6-7]。究其原因,可能與以下幾方面相關:本研究將2例染色體多態性歸結為染色體異常;羊膜腔穿刺指征的嚴格把關;隨著2016年初“全面二孩”政策的開放,40歲以上孕婦進行羊水穿刺的比例增加。
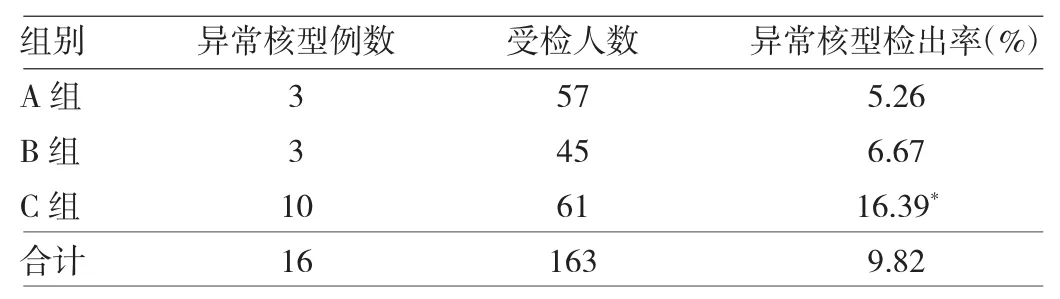
表4 高齡組各年齡段異常核型檢出率的比較
高齡妊娠是最早被提出的羊膜腔穿刺適應證。本研究中,高齡孕婦組胎兒異常核型的檢出率為9.82%,高于國內外文獻報道[8-9],與近2年進行羊膜腔穿刺的40歲以上孕婦所占比例明顯增多有關。眾所周知孕婦年齡越高,發生胎兒染色體異常的風險越大。另外,本研究將合并多個羊膜腔穿刺指征,比如高齡合并超聲軟指標異常、高齡合并NIPT高風險等都歸為了高齡組。近年國內專家對于單純高齡孕婦(≥35歲)進行產前診斷存在異議,有專家推薦以NIPT來替代有創產前診斷[10]。但根據本研究結果,高齡孕婦的染色體異常不僅僅是非整倍體異常,常常涉及染色體結構異常,這是目前NIPT檢測無法篩查的。有文獻佐證,高齡孕婦隨著年齡的增加,胎兒發生非篩查目標疾病的概率顯著增加[11]。且本研究以高齡為單一穿刺指征發現的染色體異常核型9例,占發現的異常核型比例23.68%,故應重視高齡孕婦的產前咨詢,并建議行產前診斷,以減少出生缺陷兒。但隨高齡孕婦的增多,對于35歲以上的高齡孕婦,是否根據年齡分層,采用不同的產前診斷策略,以盡可能避免侵入性操作造成的不良結果,改善孕婦體驗也是值得探討的問題。加拿大和英國等國家將單胎妊娠直接羊膜腔穿刺的最低年齡提高至40歲[12]。國內有報道在高齡孕婦中,年齡38歲以上異常核型陽性率顯著升高[13]。本研究將高齡孕婦根據年齡分為3組,統計結果發現,≥40歲的C組孕婦與≥35歲而<38歲的A組異常核型檢出率存在統計學差異,與≥38歲而<40歲的B組無統計學差異。雖樣本量少,但與國內文獻報道結果基本一致。國內還有文獻報道,同時采用孕中期血清學篩查可以將高齡孕婦羊膜腔穿刺率降低79.9%[14]。2007年美國婦產科醫師學會(American College of Obstetricians and Gynecologists,ACOG)提出不論孕婦年齡大小均進行產前篩查;高齡孕婦通過產前篩查進行胎兒異常風險分層,可以大大減少不必要的有創產前診斷。這些研究為不同年齡的高齡妊娠采用不同的產前診斷策略提供了參考。
血清學篩查受到多因素影響,假陽性率較高,本研究統計結果21-三體高風險組異常核型檢出率為3.94%,18-三體高風險組異常核型檢出率為5.41%,血清學篩查高風險總的檢出率為4.27%,均以血清學篩查高風險作為單一穿刺指征。NIPT是否可以取代產前血清學篩查也是近年的熱點議題。加拿大婦產科協會(Society of Obstetricians and Gynaecologists of Canada,SOGC)以及ACOG專家意見指出:血清學的產前篩查不僅針對21、18-三體、開放性神經管畸形,同時還可篩查其它染色體異常,高風險孕婦的胎兒即使染色體正常,但不良妊娠結局風險增高[15-16]。從本研究顯示,血清學篩查高風險通過產前診斷確認的7例染色體異常中非整倍體異常為4例,結構異常為3例,說明血清學篩查不僅僅局限于染色體非整倍體的篩查[17],還可篩查其他異常,這是NIPT目前無法完全替代的。故本文認為血清學篩查高風險仍應作為獨立的羊膜腔穿刺產前診斷指征。目前國內有些醫院在孕婦知情選擇下使用NIPT對血清學篩查高風險孕婦先行檢測,再根據檢測結果決定下一步檢測方案。綜上,此方法存在一定風險,需引起臨床醫師警惕。
針對超聲提示異常胎兒,染色體核型分析可檢出9%~19%的異常[18],胎兒有結構畸形的染色體異常核型檢出率常常更高[19]。作為穿刺指征,本研究將超聲檢查發現的胎兒結構畸形和軟指標異常(2個及以上)均歸為超聲異常。本研究78例因胎兒超聲檢查異常而進行羊膜腔穿刺的患者中,檢出染色體異常核型9例,染色體異常核型發生率達11.54%,與相關文獻報道相符。孤立的超聲軟指標是否應作為侵入性產前診斷指征尚存在爭議。本院選擇根據該指標的嚴重程度結合病史、年齡、NT、早中期唐氏篩查結果、患者本人意愿等綜合評估風險,有選擇地進行侵入性產前診斷,盡量減少漏診及價值不大的侵入性產前診斷。
分子遺傳學診斷技術與染色體G顯帶分析技術相比,各有長短,可為互補。染色體核型分析在可及的分辨率內,可以發現所有染色體的數目與結構異常,獲得的信息是全息的,但羊水細胞培養、染色體標本制備、核型分析等檢測費時長、人力耗費大;此外,該技術不能檢測單基因突變,也無法檢測染色體微小片段增減導致的微缺失微重復綜合征。熒光原位雜交技術(fluorescence in situ hybridization,FISH)、BoBs等在內的快速產前診斷技術,提高了診斷的分辨率、縮短了檢查時間,檢測效率高,但只能對試劑盒設定的目標疾病進行檢測,無法對染色體組的異常作全局分析。CMA技術能夠在全基因組水平進行掃描,可檢測染色體拷貝數變異(copy number variants,CNV),在檢出染色體微小片段的缺失和重復中相比核型分析具有突出優勢,但因為數據庫的不同或完整性尚欠缺,臨床意義不明的變異比例也較高,對臨床醫師解讀報告和臨床遺傳咨詢造成了一定的困擾。在本研究中CMA技術的異常檢出率高于傳統G顯帶分析技術,但其檢出率的差異無統計學意義,可能與樣本量較小及選用CMA時的穿刺指征不同等有關。
羊膜腔穿刺術是相對安全、穩定的,可被廣泛應用于產前診斷的一門技術。應重視產前診斷中心的咨詢工作,高齡孕婦及血清學篩查高風險都有進行產前診斷的必要性,尤其對伴有超聲檢查異常者,建議其行產前診斷;高齡孕婦可根據年齡進行風險再分層,采取不同的產前診斷策略,≥40歲的高齡孕婦不主張使用NIPT來替代產前診斷。胎兒染色體核型分析仍是金標準,但分子生物檢測技術可作為產前診斷有力的補充。

