球形密閉容器內氫氣濃度對混合氣體燃爆特性的影響?
任家帆 馮 偉 全樹新 常圣泉 彭 旭 曹衛國 饒國寧
①南京理工大學化工學院(江蘇南京,210094)②西安近代化學研究所(陜西西安,710065)③遼寧慶陽特種化工有限公司(遼寧慶陽,745000)④中北大學環境與安全工程學院(山西太原,030051)
引言
氫氣作為合成氨的基本原料之一,是煉油工業的重要原料;同時,氫氣因其清潔、效率高和可再生能力強等優點,是一種很有前途的新能源載體,得到了日益廣泛的重視和應用。但隨著社會發展和新能源的應用,由于對氫氣安全使用知識了解不足而造成的事故也越來越多。2001年2月27日,江蘇省鹽城市某化肥廠合成車間管道突然破裂,隨即大量氫氣泄漏發生燃爆;2015年6月28日,內蒙古鄂爾多斯市某公司發生一起氫氣泄露燃爆事故,造成大量的人員傷亡和財產損失。
國內外對氫氣燃爆的實驗研究主要集中在燃爆的傳播機理以及傳播影響等因素方面。孫從煌等[1]研究了點火條件對密閉管道內預混氫氣-空氣混合氣體燃爆特性的影響,研究表明:不同點火條件對密閉管內氣體的動能和內能的影響規律類似于其對管內氣體的流速和溫度的影響規律,而對渦量的影響不明顯;曹衛國等[2-5]采用20 L球形容器對粉塵燃爆的嚴重程度進行了評估,并利用Fluent軟件進行了數值模擬;Yang等[6]研究了導管長度和氫氣濃度對氫氣-空氣混合氣體燃爆后產生的最大超壓和火焰行為的影響;Tan等[7-10]通過側面帶有泄爆口的球形容器,研究了惰化條件下受限空間內部混合氣體燃爆及泄爆過程中的壓力變化規律;Zheng等[11]研究了可燃氣體燃爆火焰在不同長寬比封閉管道中的傳播規律。氫氣具有點火能低、燃燒極限范圍廣、層流燃燒和擴散速度快以及燃爆威力大等特點,因此其燃爆過程更有典型性[12]。
受實驗條件的限制,目前,對不同濃度的氫氣-空氣混合氣體燃爆壓力的研究主要集中在密閉空間中,通過壓力傳感器測量其燃爆的壓力特征,但在一個強約束的密閉空間中,其湍流預混火焰的火焰形態和火焰傳播規律也更加復雜,難以通過實驗手段獲取。
目前,數值模擬已經較為成熟,成為研究該類燃爆問題的一種有效手段。本文中,通過實驗和CFD(computational fluid dynamics,計算流體動力學)方法相結合,采用20 L球形燃爆系統對不同濃度的氫氣-空氣混合氣體燃爆結果進行實驗研究,然后對其燃爆過程進行模擬,并與實驗數據進行對比。仿真結果與實驗數據基本吻合,并揭示了詳細的三維流場參數,為理論研究提供了科學參考。
1 實驗設置
目前,對可燃氣體燃爆特性的研究沒有統一、標準、規范的研究方法。因此,本實驗中建立了針對于可燃氣體燃爆的20 L燃爆測試系統。該系統主要包括20 L燃爆球體、抽真空系統、配氣系統、點火系統、測試系統、控制系統和數據采集系統。
實物圖如圖1所示。

圖1 20 L球形燃爆裝置實物圖Fig.1 20 L spherical explosion device
示意圖如圖2所示。
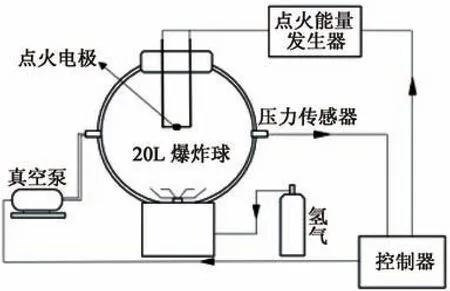
圖2 可燃氣體燃爆測試系統示意圖Fig.2 Schematic diagram of combustible gas explosion test system
在該實驗中,氫氣在20 L球中和空氣按不同的體積比預混進行反應。首先,對20 L球內部進行抽真空處理,此時抽真空的量取決于氫氣和空氣的體積比,通過狀態方程得出其壓強比,抽出一定比例的空氣;然后,由氣瓶向20 L球中注入氫氣,至球體內部壓力(表壓)為0。
通過壓力傳感器記錄燃爆過程中的動態壓力,并利用動態壓力的歷史數據來分析其最大燃爆壓力和壓力上升速率。
2 數學模型
2.1 物理模型
在以往的研究中,大多將20 L爆炸球簡化為一個二維的圓形或三維的球體,其內部結構并未很好地體現出來。為了更好地利用Fluent軟件進行流暢的分析,根據20 L爆炸球的實際尺寸,建立了三維幾何模型,并保留其點火電極、噴嘴和折流板等內部結構,對計算區域進行了細致的網格劃分,并對表面網格進行加密。示意圖如圖3所示。
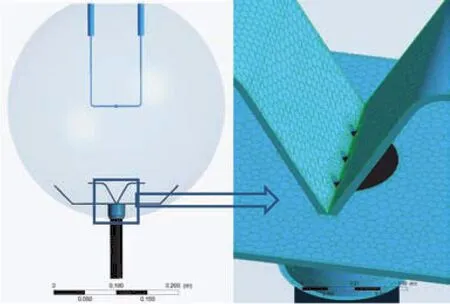
圖3 20 L球形燃爆裝置網格Fig.3 20L spherical vessel explosion device grid
2.2 控制方程
氫氣燃爆過程是復雜的湍流燃燒燃爆,對其燃爆過程采用標準k-ε模型來處理燃爆發生時產生的湍流,采用Arrhenius方程來描述可燃氣體的化學反應過程[13]。在迭代求解含化學反應的Navier-Stokes方程時,需要建立并求解一系列的控制方程[1]。
連續性方程
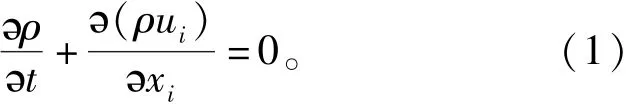
動量守恒方程

能量守恒方程
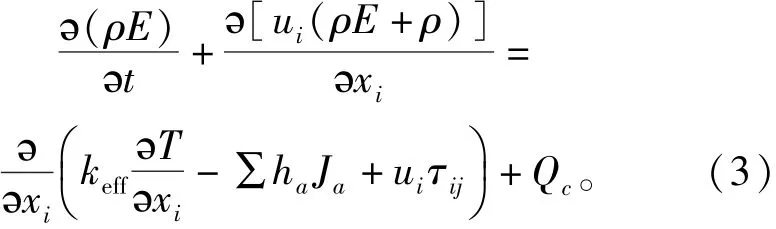
組分運輸方程
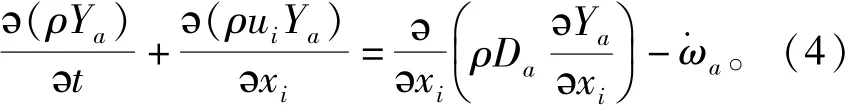
式中:ρ為密度;ui和uj為速度分量;p為靜壓;T為溫度,其中參考溫度為300 K;τij為應力張量,且τij=μ(?ui/?xj+?uj/?xi)-2/3(μ?ul/?xl)δij,δij為單位張量,μ為分子黏度;keff為有效熱導率;Qc為化學反應放熱的體積熱源以及輻射熱源的能量源項;E為內能,且E=h-p/ρ+μ2i;ha、Ja、Ya、Da、ωa分別為燃料組分a的比焓、質量擴散通量、質量分數、擴散系數和化學反應速率[14-15]。
3 結果與討論
3.1 壓力曲線分析
圖4記錄了不同體積分數(10%、20%、30%、40%、50%、60%)的氫氣燃爆壓力曲線;表1為不同體積濃度氫氣燃爆的最大壓力和最大升壓速率。
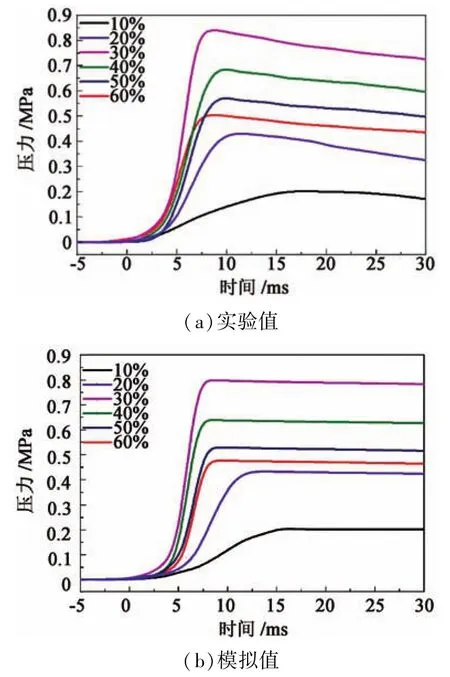
圖4 氫氣燃爆壓力曲線Fig.4 Combustion-explosion pressure curves of hydrogen
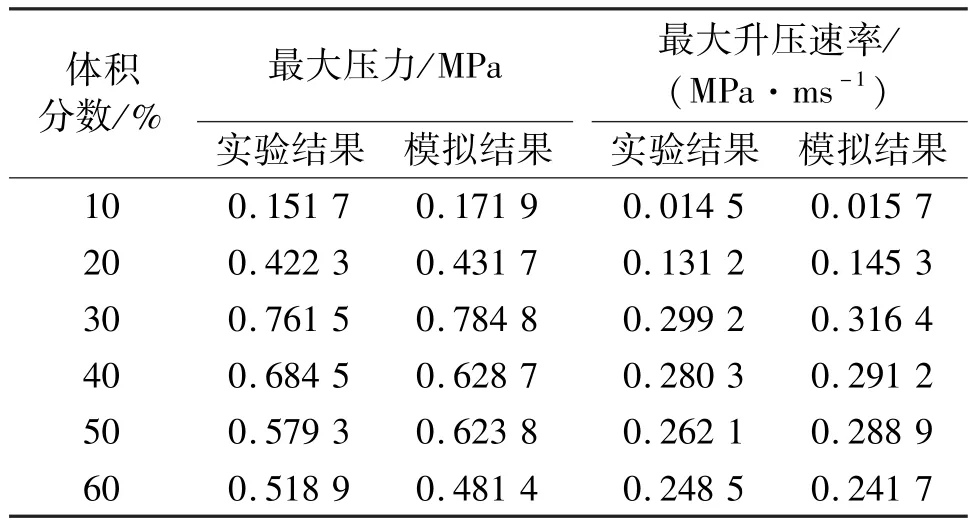
表1 不同體積分數氫氣燃爆的最大壓力及最大升壓速率Tab.1 Maximum pressure and pressure rising rate of hydrogen deflagration with different volume concentrations
從實驗結果可以看出,在6種氫氣體積分數下,氫氣燃爆的最大壓力先增加后減少,氫氣體積分數為30%時,達到的超壓最大。此時,氫氣和空氣中,氧氣的體積比接近化學計量比;因此,在該體積分數下,氫氣和氧氣的反應速率最快,即燃燒速率最大,火焰傳播速度也最大,爆炸時間相應地減少,對應的壓力上升速率也大于另外兩種情況。
由圖4(a)和圖4(b)的對比可以看出,數值模擬壓力曲線的上升階段與實驗結果基本吻合,但模擬的壓力曲線在到達最大壓力后卻并沒有像實驗結果一樣有較為明顯的下降。這是因為在模擬過程中,假設壁面是絕熱的,和外界沒有任何的熱傳遞,也不會造成熱量損失;因此,在反應完成后,20 L球中的壓力基本保持不變。但是在實驗條件下,20 L球不可能做到完全的絕熱條件,會與外界發生熱傳遞,造成熱量損失;因此,實驗結果中的壓力曲線在后期會有所下降。
3.2 數值模擬分析
運用Fluent軟件進行數值計算,通過標準k-ε湍流模型、化學反應模型和中心點火的方式來研究氫氣的燃爆過程。以30%氫氣體積分數為例,計算結果見圖5~圖7。
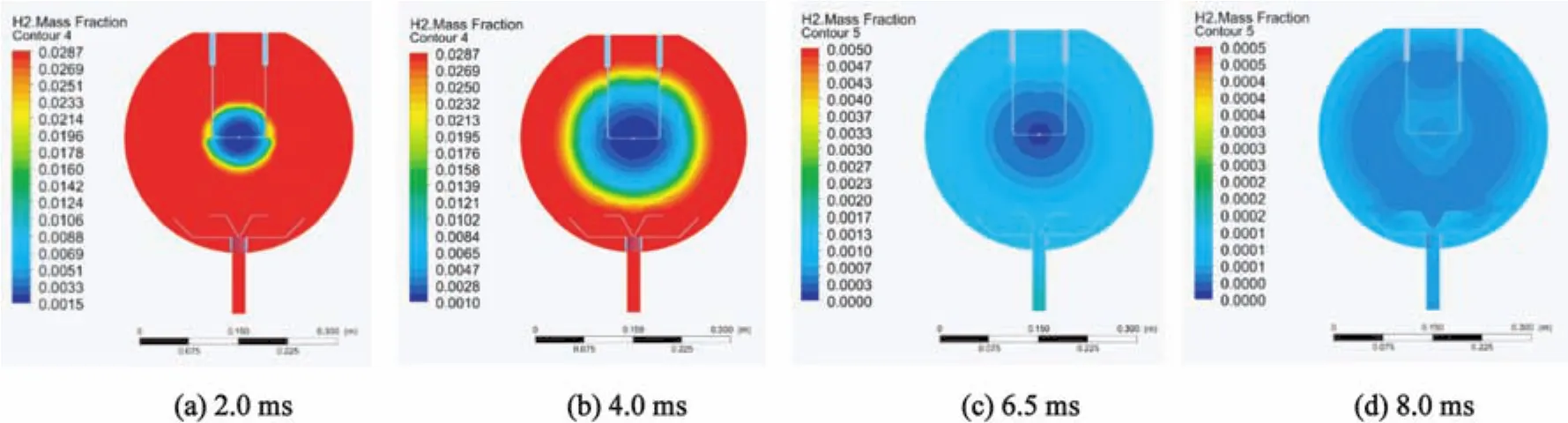
圖5 不同時刻氫氣的質量濃度Fig.5 Mass concentration of hydrogen at different times
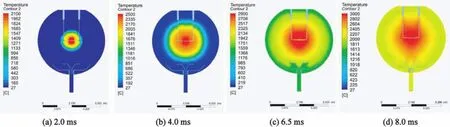
圖6 不同時刻系統中的溫度分布Fig.6 Temperature distribution in the system at different times
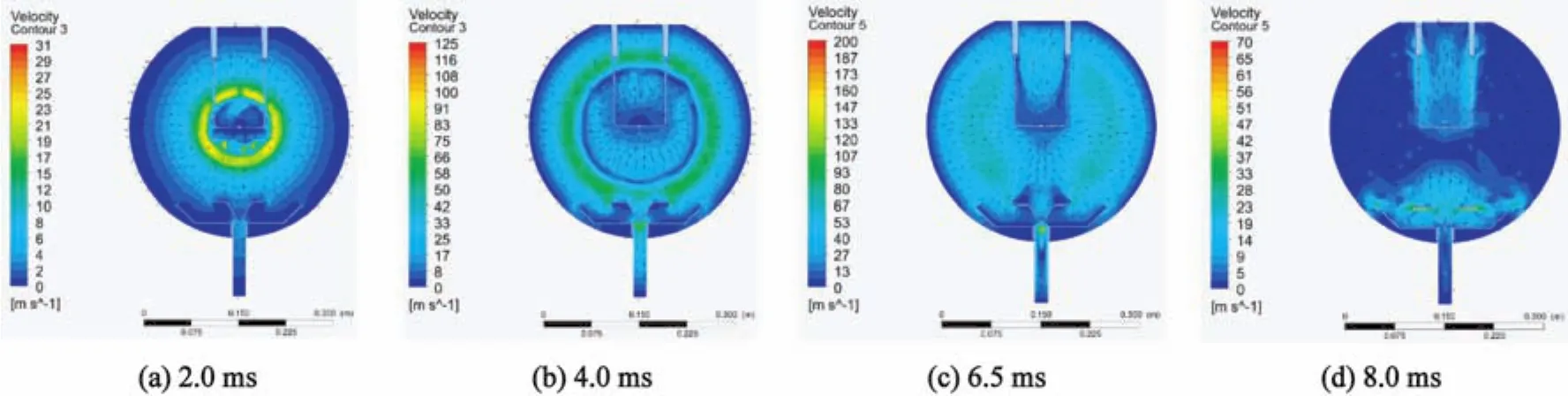
圖7 不同時刻球體中的氣流速度矢量Fig.7 Velocity vector in the sphere at different times
從圖5和圖6可以得出,氫氣低濃度區為已燃區,高濃度區為未燃區,已燃區和未燃區之間為預熱區;氫氣的質量分數沿著半徑方向升高,溫度則沿著半徑方向降低,即沿著半徑方向提供給氫氣反應的能量逐漸降低,因此吸收能量離解為自由基的氫分子數目越來越少,這也是越靠近未燃區氫氣質量濃度越高的原因。
從圖6可以看出,火焰是一個邊燃燒邊膨脹的過程,在反應初期(4.0 ms前),已燃區占比很小,使得未燃區氣體被壓縮的量可以忽略不計,從壓力曲線可以看出,其壓力變化也不劇烈;但隨著已燃區占比的增加,使得未燃燒氣體在燃燒前被壓縮,其單位體積內發生反應的分子數增多,反應速率加快,放熱量增加造成溫度的升高,同時,反應加快造成壓力的急劇上升。
圖7為反應的不同時刻氣流速度矢量圖。在數值模擬中,假定初始的氣流速度為0 m/s。隨著反應的繼續,中心氣流的速度減慢,這是由于在給予密閉容器內已燃區外部氣體壓力的同時,也承受外部氣體所帶來的阻力作用,導致已燃區氣流速度降低。在火焰傳播到達壁面之前,最大氣流速度不斷增加,并出現在火焰前緣位置。在點火后的6.5 ms,氣流到達壁面,此時容器內接近最大壓力。
4 結論
1)通過實驗和數值模擬相結合,對不同體積分數氫氣-空氣混合氣體的燃爆過程進行了深入研究。研究表明,在氫氣-空氣混合氣體的6種體積分數下,最大燃爆壓力隨著氫氣體積分數的增加呈現先增大、后減少的趨勢;且氫氣體積分數為30%時燃爆極限壓力最大,為0.761 5 MPa;升壓速率最快,為0.299 2 MPa/ms。
2)在點火開始后的4.0 ms內,火焰面擴張較慢;4.0 ms后,化學反應速率增大,火焰面迅速擴張。這是由于隨著火焰的擴張,使得未燃氣體在燃燒前被壓縮,單位體積內參與反應的分子數增加,化學反應速率加快。
3)建立了三維數值仿真模型,其模擬結果的壓力變化行為在上升階段和實驗結果基本一致,誤差不超過15%。因此,該數值模型可用于研究可燃氣體爆燃的最大壓力及其上升速率,為研究可燃氣體的爆燃機理和針對可燃氣體的防爆、抑爆提供了數據和理論基礎。

