糖尿病患者中上臂圍與SUDOSCAN預測的心血管自主神經病變風險的相關性
張 琦, 鄭杭萍, 季立津, 張元品, 孫婉婉, 朱小明, 張 爍, 劉曉霞, 鹿 斌, 陳 萱
1. 復旦大學附屬華山醫院內分泌科,上海 200040 2. 復旦大學內分泌糖尿病研究所,上海 200040 3. 上海市徐匯區湖南街道社區衛生服務中心,上海 200031
糖尿病心血管自主神經病變(diabetic cardiovascular autonomic neuropathy,DCAN)是易被忽視的糖尿病慢性并發癥之一[1]。其臨床表現較為復雜且缺乏特異性,易被糖尿病其他相關并發癥、合并癥所掩蓋。此外,DCAN也是糖尿病患者發生無癥狀心肌缺血及無痛性心肌梗死的重要原因之一,使糖尿病患者的心血管死亡率增加[2-4]。因此,應對DCAN進行早期診斷和治療。
DCAN的檢測方法較多,如Ewing心血管試驗、心率變異性分析、壓力反射敏感性分析等,但尚缺乏診斷金標準[5]。SUDOSCAN作為一種新型的電導分析儀,可以通過評估交感神經支配的泌汗功能評估DCAN的發病風險(SUDOSCAN風險評分)[6]。Yajnik等[7]對232例糖尿病患者的SUDOSCAN和Ewing心血管試驗檢查結果進行相關性分析,發現SUDOSCAN風險評分預測DCAN的受試者工作特征曲線(ROC)的曲線下面積為0.74,靈敏度為92%、特異度為49%。
DCAN與中心性肥胖關系密切。 Jang等[8]通過CT檢查發現,內臟脂肪面積的增加顯著降低了女性2型糖尿病患者對Valsalva動作的心率反應性,表明內臟脂肪的堆積影響糖尿病患者的自主神經功能,對DCAN具有一定的預測價值。但CT檢查不適合作為大規模篩查手段。中上臂圍(mid-upper arm circumference,MUAC)是評估中心脂肪含量和機體營養狀況的主要指標,臨床測量簡便[9]。研究[10-12]報道,MUAC與兒童及成人的全因死亡率或心血管死亡率負相關,可以用于預測兒童或成人的死亡風險。但目前鮮有研究報道MUAC與DCAN之間的關系。因此,本研究擬在社區糖尿病人群中探討MUAC與SUDOSCAN預測的DCAN風險之間的關系。
1 資料與方法
1.1 一般資料 2018年5月至8月從上海市靜安區石門二路社區衛生中心選擇324例2型糖尿病患者,最終納入316例臨床資料完整者。納入標準:(1)符合WHO 1999年糖尿病診斷標準,即空腹血糖水平≥7.0 mmol/L和(或)餐后2 h血糖水平大于或等于11.1 mmol/L;(2)年齡≥18歲。排除標準:(1)糖尿病急性并發癥患者(糖尿病酮癥酸中毒、高滲性高血糖狀態和乳酸性酸中毒);(2)伴有急性心肌梗死、腦出血、嚴重高血壓者或有心臟起搏器植入史;(3)嚴重甲狀腺、肝臟或腎臟疾病患者;(4)視網膜增生性損傷或視網膜出血者;(5)納入研究前1個月內服用地高辛、β-受體阻滯劑或抗抑郁藥者;(6)長期服用咖啡、濃茶、乙醇或其他含咖啡因的飲料者。所有納入者均簽署知情同意告知書,且本研究通過復旦大學附屬華山醫院倫理委員會批準。
1.2 病史及體格檢查 通過問卷調查收集納入者的年齡、性別和糖尿病病程等信息。所有納入者均由同一護理人員按標準進行體格檢查,包括身高、體質量、MUAC和靜息狀態血壓等。身高測量精確到0.1 cm,體質量測量精確到0.1 kg,體質指數(body mass index,BMI)= 體質量/身高2(kg/m2)。MUAC測量:受試者手臂自然下垂,使用軟尺緊貼皮膚,環繞肩峰與尺骨鷹嘴連線中點1周;測量精確到0.1 cm[13]。血壓測量由同一護理人員用水銀式血壓計測量3次并取平均值。
1.3 生化指標檢測 抽取納入者空腹靜脈血。空腹血糖(fasting blood glucose,FBG)以葡萄糖氧化酶法測定(儀器:Wako Pure 2756-01,Wako Pure Chemical Industries,日本);糖化血紅蛋白(glycated hemoglobin,HbA1c)以高效液相色譜法測定(儀器:HLC-723G7,Tosoh Corporation,日本)。丙氨酸氨基轉移酶(alanine aminotransferase,ALT)、天冬氨酸氨基轉移酶(aspartate aminotransferase,AST)、堿性磷酸酶(alkaline phosphatase,ALP)、血清肌酐(serum creatinine,SCr)、三酰甘油(triacylglycerol,TG)、總膽固醇(total cholesterol,TC)、低密度脂蛋白膽固醇(low density lipoprotein cholesterol,LDL-C)和高密度脂蛋白膽固醇(high density lipoprotein cholesterol,HDL-C)以酶比色法測定(儀器:Hitachi 7600-120,Hitachi High-Technologies, 美國)。
1.4 SUDOSCAN SUDOSCAN檢測儀(Impeto Medical,法國)由一臺電腦主機、手部和足部鍍鎳不銹鋼電極板連接組成。受試者雙腳站立于足部電極板上,雙手掌心朝下緊貼在手部電極板上,在啟動SCAN按鈕后,儀器自動對手部和足部的皮膚施加逐漸遞增的直流低電壓(<4 V);產生的電流穿過鍍鎳不銹鋼傳感器,通過反向離子電滲吸引來自手掌和足底汗腺中的氯離子。整個檢查持續2~3 min,儀器最終將產生的電流與電壓通過計時電流法繪制曲線計算斜率,測算并輸出手部和足部的電化學皮膚傳導率(electrochemical skin conductance,ESC),將足部和手部ESC值的平均值定義為ESC平均值。同時,SUDOSCAN根據內置的參數模型,將受試者的性別、年齡、身高、體質量、HbA1c等基本參數和測得的ESC值進行計算,得到DCAN風險評分[14]。所有受試者在SUDOSCAN檢測過程中無任何不適或不良反應出現。
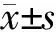
2 結 果
2.1 臨床特征 316例患者中,男性149例,女性167例,平均(68.81±7.99)歲,糖尿病病程(11.52±8.32)年;HbA1c平均(7.41±1.50)%,SUDOSCAN風險評分平均(42.90±9.91)%,MUAC平均(27.68±3.52) cm。將男性患者和女性患者分別分為低SUDOSCAN風險評分組(低SUDOSCAN組)和高SUDOSCAN風險評分組(高SUDOSCAN組)。結果(表1)表明:在男性患者中,高SUDOSCAN 組的年齡、收縮壓、體質量、BMI和SCr明顯高于低SUDOSCAN 組患者(P<0.01),但足部ESC值和ESC平均值低于低SUDOSCAN 組患者(P<0.05)。女性患者中,高SUDOSCAN 組的年齡、收縮壓、體質量、BMI和MUAC高于低SUDOSCAN 組患者(P<0.05),而身高、HDL-C、手部ESC值、足部ESC值和ESC平均值低于低SUDOSCAN 組患者(P<0.05)。
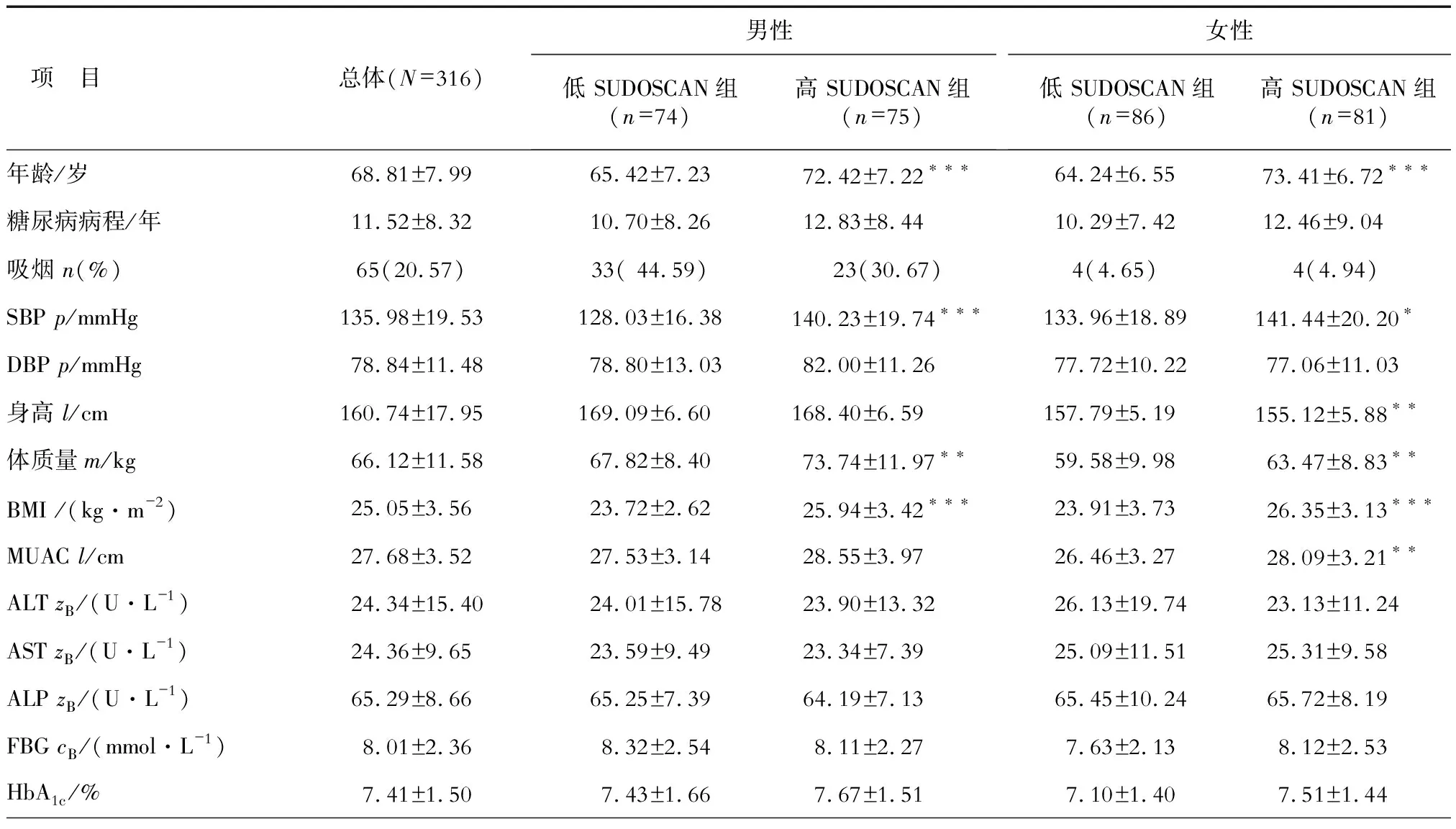
表1 納入患者的基本臨床資料
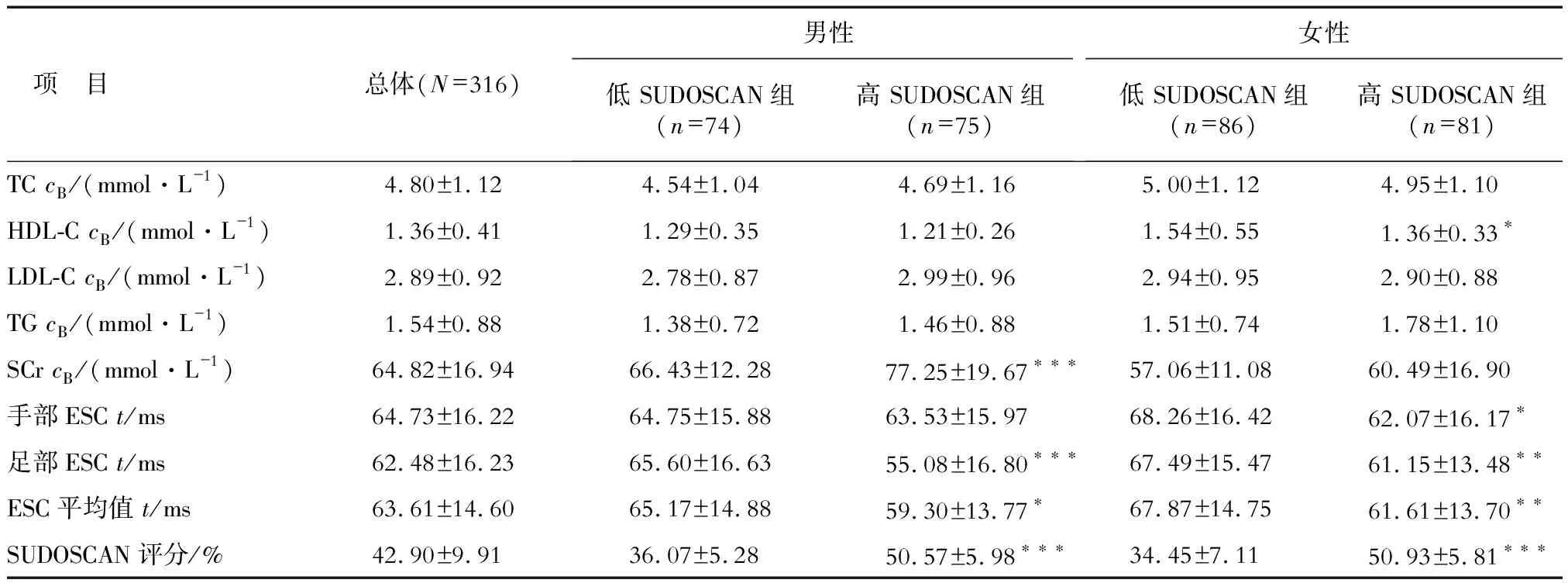
續表1
SBP:收縮壓;DBP:舒張壓;BMI:體質指數;MUAC:中上臂圍;ALT:丙氨酸氨基轉移酶;AST:天冬氨酸氨基轉移酶;ALP:堿性磷酸酶;HbA1c:糖化血紅蛋白;FBG:空腹血糖; TC:總膽固醇;HDL-C:高密度脂蛋白膽固醇;LDL-C:低密度脂蛋白膽固醇;TG:三酰甘油; SCr:血清肌酐;ESC:電化學皮膚傳導率.*P<0.05,**P<0.01,***P<0.001與低SUDOSCAN組相比
2.2 不同MUAC水平患者SUDOSCAN風險評分比較 將患者分為MUAC<26 cm組,26≤MUAC<29 cm組,MUAC≥29 cm組。結果(圖1)表明:隨著MUAC的增加,女性患者的SUDOSCAN風險評分增加(P<0.05),男性患者的SUDOSCAN風險評分未見明顯改變。
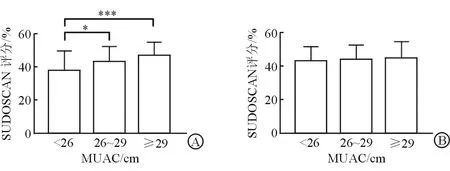
圖1 不同MUAC水平患者SUDOSCAN風險評分比較
2.3 MUAC與SUDOSCAN風險評分的相關性分析 Spearman相關分析結果(表2)表明:男性糖尿病患者中,MUAC與ESC平均值正相關(P<0.05),與SUDOSCAN風險評分無明顯相關性;女性糖尿病患者中,MUAC與ESC平均值和SUDOSCAN風險評分均正相關(P<0.05)。
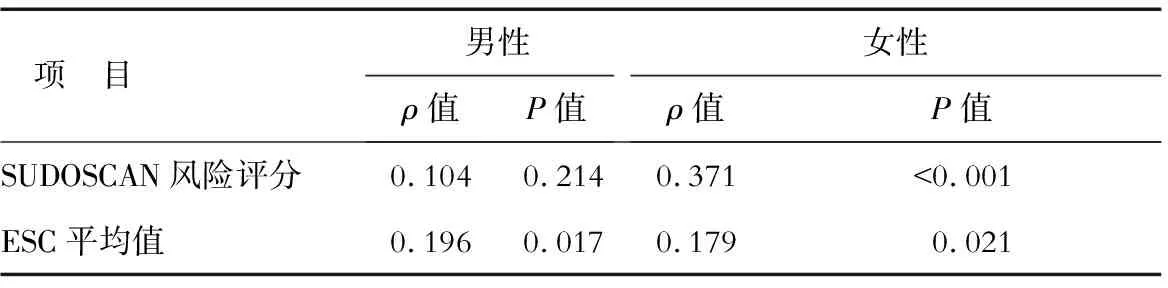
表2 MUAC與SUDOSCAN風險評分和ESC值間的相關性分析
2.4 MUAC與SUDOSCAN風險評分的線性回歸分析 結果(表3)顯示:未校正其他因素時(Model1),男性和女性患者的MUAC與SUDOSCAN風險評分均相關(P<0.001);校正年齡、糖尿病病程和吸煙后(Model2),男性和女性患者的MUAC與SUDOSCAN風險評分仍相關(P<0.001);校正年齡、糖尿病病程、吸煙、BMI和血壓后(Model3),僅女性患者的MUAC與SUDOSCAN風險評分相關(P<0.05);在Model3的基礎上,進一步校正患者的血糖、血脂和SCr水平后(Model4),女性患者的MUAC與SUDOSCAN風險評分仍獨立相關(P=0.026),且MUAC每增加1 cm,SUDOSCAN風險評分增加0.452%。
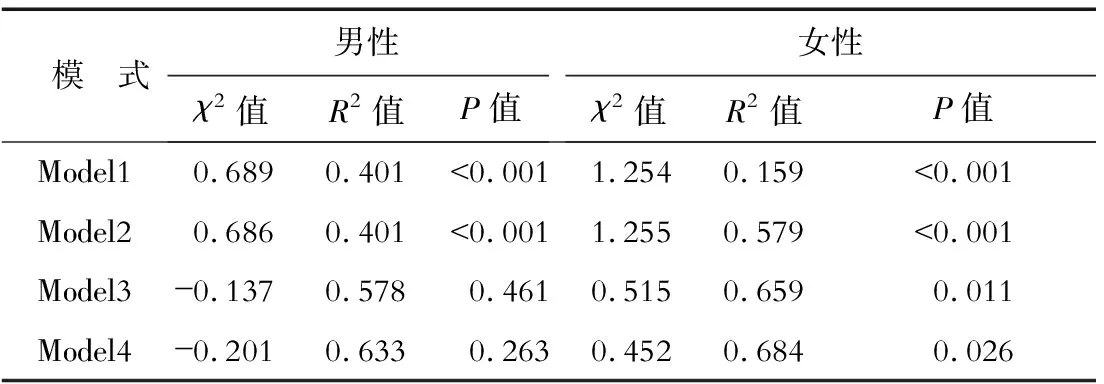
表3 MUAC與SUDOSCAN風險評分間的多重線性回歸分析
Model1:未校正其他因素;Model2:校正年齡、糖尿病病程和吸煙;Model3:校正年齡、糖尿病病程、吸煙、體質指數和血壓;Model4:校正年齡、糖尿病病程、吸煙、體質指數、血壓、血糖、血脂和血肌酐水平
3 討 論
MUAC是臨床上常用來評估中心脂肪含量和機體營養狀況的主要指標,臨床測量簡便,可作為多種疾病的預測信息,但目前鮮有研究報道其對DCAN的預測價值。本研究發現,在社區糖尿病人群中,女性患者的MUAC與SUDOSCAN風險評分顯著相關(P=0.026),且MUAC每增加1 cm,SUDOSCAN風險評分增加0.453%,男性患者的MUAC與SUDOSCAN風險評分則無明顯相關性。
中心性肥胖與DCAN的關系密切。Cho等[15]對253例初發1型糖尿病患者隨訪4年后發現,較大的腰高比是心率變異性損傷的重要預測因子,校正患者的血糖水平后,這種關系仍然存在,表明中心性肥胖與1型糖尿病患者心血管自主神經病變密切相關。此外,Laitinen等[16]對糖耐量受損患者隨訪2年后發現,副交感神經功能紊亂患者的腰圍大于副交感神經功能正常的患者(P<0.01),表明心血管自主神經病變在糖尿病早期就已發生,且中心性肥胖在DCAN早期病理過程中起到一定作用。本研究在社區2型糖尿病患者中也發現,MUAC與SUDOSCAN風險評分相關,并且校正DCAN常見的危險因素(年齡、糖尿病病程、吸煙)后,這種相關性仍然存在。中心性肥胖與自主神經功能紊亂之間的關系可能是兩者相互作用的結果:在瘦素等脂肪因子作用于下,丘腦引起交感神經輸出增加[17];由肥胖引起的低度慢性炎癥和氧化應激等也可以直接作用于自主神經系統[18],導致自主神經功能紊亂;自主神經功能紊亂又可以加重糖尿病患者的胰島素抵抗和肥胖[19]。
本研究校正各DCAN常見的危險因素后,僅在女性糖尿病患者中發現MUAC與SUDOSCAN風險評分相關,提示MUAC與DCAN的關系存在性別差異。流行病學研究認為,吸煙、血壓和血脂異常在心血管自主神經病變發生發展中發揮作用[20],這可能是造成這種性別差異的原因之一[21]。本研究人群中,男性患者吸煙的比例和舒張壓明顯高于女性患者(P<0.05),TC、TG和HDL-C水平明顯低于女性患者(P<0.05);校正吸煙、血壓、血糖和血脂水平后,女性患者的MUAC仍與SUDOSCAN風險評分相關(χ2=0.452,P=0.026),而男性患者中兩者無明顯相關性(χ2=-0.201,P=0.263),表明吸煙、血壓、血糖和血脂異常對男性患者MUAC和DCAN間的關系影響較大。此外,Yufu等[22]研究發現,2型糖尿病患者中,女性的壓力反射敏感性低于男性患者,表明女性患者的副交感神經反射能力低于男性患者。而副交感神經的反射能力的減弱可能影響MUAC與DCAN關系。Jang等[8]同樣僅在女性2型糖尿病患者中發現內臟脂肪面積與心血管自主神經病變有相關性,但Laitinen等[16]發現中心性肥胖在男性糖耐量受損患者中與心血管自主神經病變的關系更明確。因此,中心性肥胖與DCAN關系的性別差異仍需要多中心前瞻性的研究進一步闡釋。
DCAN檢測方法較多,其中以Ewing心血管試驗和心率變異性分析較為常用。本研究所使用的SUDOSCAN是一種新型的電導分析儀,目前還未被廣泛應用于評價心血管自主神經病變。SUDOSCAN可以通過評估交感神經支配的泌汗功能,并根據受試者的性別、年齡、身高、體質量、HbA1c等基本參數和測得的ESC值,計算得到DCAN風險評分,從而預測DCAN的發生風險[23-24]。Selvarajah等[25]以5項標準的心血管自主神經反射試驗結果作為金標準,發現SUDOSCAN風險評分診斷心臟自主神經病變的ROC曲線下面積為0.75,診斷的靈敏度和特異度分別為65%和80%。Yajnik等[7]在232例2型糖尿病患者中驗證了SUDOSCAN風險評分對自主神經病變風險的預測價值。相較于較為常用的Ewing心血管試驗和心率變異性分析,SUDOSCAN分析具有簡便、無創、省時、省力、靈敏度較高等優勢,更適用于DCAN的大規模早期篩查。上述研究表明,SUDOSCAN風險評分對DCAN具有良好的診斷價值,并可用于DCAN的早期篩查。
本研究存在一定的缺陷:(1)本研究為橫斷面研究,論證因果關系的能力較弱;(2)本研究采用的SUDOSCAN風險評分并不是心血管自主神經病變常用的檢測方法;(3)本研究納入患者的SUDOSCAN風險評分普遍較低[(42.90±9.91)%],僅5.4%的患者超過60%(心血管自主神經病變風險較高),較難進行亞組分析;(4)只對MUAC進行了單次測量。
綜上所述,本研究發現,女性2型糖尿病患者中,MUAC與SUDOSCAN風險評分相關;MUAC對早期發現DCAN具有重要價值。后續仍需較大規模的多中心前瞻性研究進一步進行SUDOSCAN風險評分分層,并多次重復測量MUAC,以更準確地分析不同程度的DCAN與MUAC的關系。

