電視胸腔鏡輔助小切口縱隔切除術與傳統開胸手術治療縱隔腫瘤患者的臨床效果比較
蔡迎玖
天津市武清區中醫醫院胸外科 (天津 301700)
縱隔位于兩側胸腔間、胸骨后、脊柱側面,上至頸部入口,下至膈肌,附近區域包含心臟、食管、胸腺、淋巴等多種組織,具有復雜的解剖關系,發生腫瘤的概率較高,即使體積很小也會對消化、呼吸、神經以及循環系統造成顯著影響,患者通常表現為氣短、胸悶、咳痰等[1]。臨床上主要以手術治療縱隔腫瘤患者,盡早切除病灶。本研究旨在比較電視胸腔鏡輔助小切口縱隔切除術與傳統開胸手術治療縱隔腫瘤患者的臨床效果,現報道如下。
1 資料與方法
1.1 一般資料
回顧性分析2017年6月至2018年12月醫院收治的81例縱隔腫瘤患者的臨床資料,根據手術方式的不同分為A組、B組。A組42例,經電視胸腔鏡輔助小切口縱隔切除術治療,B組39例,經傳統開胸手術治療。A組男24例,女18例;年齡20~70歲,平均(45.2±5.6)歲;腫瘤直徑2.8~10.4 cm,平均(6.4±1.3)cm;畸胎瘤13例,胸腺瘤12例,神經源性腫瘤6例,支氣管囊腫4例,心包囊腫5例,其他2例。B組39例,男23例,女16例;年齡19~71歲,平均(44.2±5.7)歲;腫瘤直徑2.5~10.8 cm,平均(6.7±1.2)cm;畸胎瘤12例,胸腺瘤12例,神經源性腫瘤5例,支氣管囊腫4例,心包囊腫4例,其他2例。兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。入選患者符合《現代腫瘤學》中縱隔腫瘤診斷標準[2],經胸部CT確診,符合手術指征,排除合并其他腫瘤、重要器官功能障礙、合并肺部疾病、手術禁忌證。
1.2 方法
A組經電視胸腔鏡輔助小切口縱隔切除術治療,患者保持側臥體位,全身麻醉,通常需置入3個Torcar,游離背闊肌并往后拉,于前鋸肌束間隙進行鈍性分離,切斷對應肋間肌,第1個置入位置為腋中線位置第6~8肋間,然后置入30° 10 mm硬質胸腔鏡進行探查,經電凝吸引器分離粘連,明確病變位置解剖關系與相連組織關系后,經直角鉗與圈鉗將組織與血管游離。在胸腔鏡直視下確定腫瘤位置,分離胸腔粘連,使用電鉤或電刀切開腫瘤表面的胸膜,順腫瘤外膜、周圍組織間隙對腫瘤組織進行分離,較細的滋養血管經電凝切斷,較大的血管在鏡下結扎,用標本袋存放切除的腫瘤組織,若腫瘤體積較大,難以經操作孔取出,可用旋切器分割后再取出。
B組經傳統開胸手術治療,常規全身麻醉,暴露胸腔,確定腫瘤位置,在胸骨正中做切口,切斷周圍腫瘤組織,逐步分離粘連,將腫瘤切除,常規縫合切口。
兩組均在胸腔積液每24小時少于500 ml時拔除引流管。
1.3 觀察指標
(1)比較兩組手術情況、術后疼痛情況、術后恢復情況。手術情況包括切口長度、手術耗時、手術失血;疼痛情況根據疼痛數字評價量表(NRS)評分進行評估,分數0~10分,分數越高,患者疼痛越嚴重,于術后3 d評價;術后恢復情況包括引流時間、住院時間。(2)比較兩組住院期間并發癥發生情況。
1.4 統計學處理
2 結果
2.1 兩組手術情況、術后疼痛情況、術后恢復情況比較
A組切口長度、手術耗時、引流時間、住院時間均短于B組,手術失血少于B組,NRS評分低于B組,差異有統計學意義(P<0.05)。見表1。
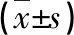
表1 兩組手術情況、術后疼痛情況、術后恢復情況比較
注:與B組比較,aP<0.05
2.2 兩組并發癥比較
A組并發癥發生率明顯低于B組,差異有統計學意義(P<0.05)。見表2。

表2 兩組并發癥發生情況比較[例(%)]
注:與B組比較,aP=0.031,χ2=4.636
3 討論
縱隔腫瘤起源于縱隔,包含淋巴肉瘤、支氣管囊腫、畸胎瘤、胸腺瘤等多個種類。大多數縱隔腫瘤為良性,僅需單純切除,操作并不復雜,因此盡量減小手術操作造成的創傷、減輕患者痛苦、縮短恢復時間是臨床研究人員關注的重點問題[3]。傳統開胸手術操作簡單,視野清晰,但切口長,對患者造成的創傷大,術后需要更長的恢復時間,且面臨較高的并發癥風險。現代微創理念與胸腔鏡的普及為縱隔腫瘤患者的治療提供了新的途徑。
本研究結果顯示,A組切口長度、手術耗時、引流時間、住院時間均短于B組,手術失血少于B組,NRS評分低于B組,差異有統計學意義(P<0.05),表明電視胸腔鏡輔助小切口縱隔切除術可促進手術情況、疼痛情況與恢復情況的改善。該術式在電視胸腔鏡引導下進行,可進一步明確腫瘤位置,獲取更加清晰的手術操作視野,有利于手術效率的提升,從而縮短手術耗時,減少出血量,減輕患者暴露應激與術后疼痛,恢復速度更快[4-5]。A組并發癥發生率明顯低于B組,差異有統計學意義(P<0.05),提示該手術可減少并發癥。電視胸腔鏡輔助小切口縱隔切除術切口長度更短,可縮短患者臥床時間,從而減少并發癥[6]。
綜上所述,與傳統開胸手術相比,縱隔腫瘤患者采用電視胸腔鏡輔助小切口縱隔切除術切口更小,手術耗時更短,出血量、并發癥更少,術后疼痛更輕,恢復速度更快。

