信號轉導和轉錄活化因子3通過趨化因子CX3C配體1促進血管內皮細胞增殖遷移
范麗娟,李慧,張慧敏,李含含,黃鳳,張子健,戴周彤,項園,姚奧,李佳蓬,廖興華
?
信號轉導和轉錄活化因子3通過趨化因子CX3C配體1促進血管內皮細胞增殖遷移
范麗娟,李慧,張慧敏,李含含,黃鳳,張子健,戴周彤,項園,姚奧,李佳蓬,廖興華
武漢科技大學 生命科學與健康學院,湖北 武漢 430000

范麗娟, 李慧, 張慧敏, 等. 信號轉導和轉錄活化因子3通過趨化因子CX3C配體1促進血管內皮細胞增殖遷移. 生物工程學報, 2019, 35(4): 677–686.Fan LJ, Li H, Zhang HM, et al. Signal transducer and activator of transcription 3 promotes vascular endothelial cell proliferation and migration by fractalkine. Chin J Biotech, 2019, 35(4): 677–686.
信號轉導和轉錄活化因子3 (STAT3) 與趨化因子CX3C配體1 (Fractalkine/CX3CL1) 在血管炎癥和損傷中起重要作用,為了探討STAT3是否通過CX3CL1促進血管內皮細胞增殖和遷移,在血管內皮細胞 (HUVEC) 中過表達或敲降STAT3,通過quantitative real-time PCR、Western blotting實驗確定STAT3對CX3CL1表達的影響。構建含有STAT3結合位點及突變STAT3結合位點的CX3CL1啟動子熒光素酶報告基因質粒,利用熒光素酶活性分析實驗研究STAT3對CX3CL1啟動子轉錄活性的作用。利用MTT實驗檢測過表達或敲降STAT3或CX3CL1對血管內皮細胞增殖率的影響。利用劃痕實驗檢測過表達或敲降STAT3或CX3CL1對血管內皮細胞遷移率的影響。結果顯示,過表達STAT3可以促進CX3CL1表達,敲降STAT3可以使CX3CL1表達下調。STAT3可以直接結合到CX3CL1的啟動子促進其轉錄激活,其促進作用依賴于CX3CL1啟動子上的GAS位點。敲降STAT3可以抑制血管內皮細胞的遷移,過表達CX3CL1拮抗該抑制作用。總結得出,STAT3通過結合到CXCL1啟動子促進CX3CL1轉錄與表達進而促進血管內皮的增殖與遷移。
人臍靜脈血管內皮細胞,CX3CL1,STAT3,增殖,遷移
動脈粥樣硬化 (Atherosclerosis,AS) 是許多心血管病形成的主要病理基礎,由多因素共同作用引起,發病機制復雜,目前尚未完全闡明。炎癥學說認為AS是一種慢性炎性反應,長期反復的內皮細胞 (Endothelial cells,EC) 損傷是其發生的病理基礎。在高脂血癥、高血壓、糖尿病或吸煙等危險因素作用下,EC發生形態改變及功能障礙,導致血管損傷[1]。關于信號轉導和轉錄活化因子3 (Signal transducer and activator of transcription 3,STAT3) 在參與動脈粥樣硬化炎癥機制方面的研究是目前的熱點。各種炎癥因子可能通過STAT3轉導的信號通路在血管炎癥中發揮作用。
細胞因子和生長因子識別表面受體后,受體偶聯的JAK激酶與STAT3相互作用發生磷酸化,形成同源或異源二聚體,并作為轉錄激活因子轉運到細胞核參與調控[2-3]。近年來JAK-STAT信號通路被發現與細胞因子刺激而形成的信號轉導過程密切相關,并通過這一形式參與許多重要生物學過程,該通路的異常會導致各種疾病的形成。炎癥因子IL-6就被報道通過激活JAK/STAT3通路參與了動脈粥樣硬化的病變[4]。
趨化因子CX3C的配體1 (Chemokine CX3C ligand 1,Fractalkine /CX3CL1) 是一種獨特的膜結合分子,在內皮細胞 (ECs) 中表達,分為可溶性 (游離型) 和膜結合性兩種形式。它是一種長蛋白質,具有擴展的粘蛋白樣莖和頂部的趨化因子結構域。粘蛋白樣莖可以使其與某些細胞表面結合。可溶性CX3CL1能有效地化學誘導T細胞和單核細胞[5],相對可溶性CX3CL1的趨化性而言,細胞結合趨化因子促進白細胞與活化的內皮細胞強烈粘附[6-7]。CX3C趨化因子受體1 (CX3C chemokine receptor 1,CX3CR1) 是CX3CL1的特異性受體,主要在某些白細胞群上表達[8-9],也被發現來源于血管壁損傷后平滑肌細胞分化的物質[10]。有研究報道CX3CL1和CX3CR1在血管炎癥和損傷中起重要作用,促進動脈粥樣硬化的形成[11]。
雖然由ECs表達,但CX3CL1和STAT3對內皮細胞的增殖遷移的影響并不清楚。根據生物信息學發現CX3CL1基因序列上有STAT3的作用位點,STAT3是否也同時與CX3CL1相互作用共同調節內皮細胞的增殖遷移情況也并不明確。這些問題的解決可能為動脈粥樣硬化不穩定斑塊里的血管新生機制提供依據。又根據其他研究表明,STAT3能夠上調平滑肌細胞中CX3CL1的表達[12]。因此本文創新性研究STAT3介導的CX3CL1對血管內皮細胞本身增殖能力的影響,為動脈粥樣硬化血管新生的研究奠定基礎。
1 材料與方法
1.1 材料
1.1.1 細胞
采用的人臍靜脈內皮細胞株來源于中國上海細胞庫。所用細胞系為EA.HY926,置于?80 ℃保存。在進行動脈血管內皮細胞實驗時,通常選用的細胞模型為人臍靜脈內皮細胞 (Human umbilical vein endothelial cells,簡稱HUVECs),因為臍靜脈內皮細胞具有干細胞的潛能,其特性與動脈血管內皮細胞相似,它們常被用作研究內皮細胞功能和病理學 (例如血管生成)[13]。
1.1.2 試劑
DMEM培養基 (Hyclone,美國);胰蛋白酶 (Biosharp,中國);胎牛血清FBS (Gibco,美國);雙抗/青鏈霉素合劑 (Gibco,美國)。培養細胞使用的完全培養基含10% FBS 1%的雙抗。PBS液、TBST (自配);RIPA裂解液;磷酸酶抑制劑 (Roche,瑞士);SDS-PAGE蛋白上樣緩沖液 (碧云天,中國);Trizol (Invitrogen,美國);熒光定量試劑盒 (TaKaRa,日本);人源STAT3抗體 (鼠抗人,STAT3 (124H6) (mAbs,CST),二抗使用羊抗鼠抗體;人源CX3CL1抗體 (兔抗人,(CX3CL1 (ab25088) (mAbs,Abcam)),二抗使用羊抗兔抗體;PVDF膜 (Bio-Rad,美國);SIRNA-STAT3及對照、SIRNA-CX3CL1及對照 (RIBOBIO,廣州銳博);一步法克隆試劑盒 (上海翊圣,中國);Western Bright ECL (Advansta,美國);熒光素酶報告基因檢測試劑盒 (Promega,美國)。
1.1.3 儀器
電泳儀 (BIO-RAD,美國),核酸蛋白凝膠圖像系統 (BIO-RAD,美國;酶標儀 (Leica,德國);熒光定量PCR儀 (BIO-RAD);冷凍超速離心機 (Beckman,美國);氣套式二氧化碳恒溫培養箱 (Astec,日本);倒置顯微鏡 (Olympus,日本)。
1.2 方法
1.2.1 質粒構建
在CX3CL1啟動子上發現有STAT3的結合元件GAS區,以人臍靜脈內皮細胞基因組為模板構建CX3CL1啟動子的熒光素酶報告基因質粒 pGL3-CX3CL1-WT,并構建其突變質粒pGL3- CX3CL1-MUT,空載為pGL3。同時以人臍靜脈內皮細胞的cDNA為模板構建STAT3、CX3CL1的表達質粒pCDNA3.1-STAT3、pCDNA3.1-CX3CL1,空載為pCDNA3.1。質粒構建引物設計采用上海翊圣一步法克隆試劑盒所提供的方法,原理為末端同源重組,引物序列見表1。實時熒光定量核酸擴增檢測所用的引物來源于PrimerBank,引物序列見表2。
1.2.2 細胞培養及轉染
為研究過表達和干擾CX3CL1和STAT3的表達對HUVEC細胞的增殖遷移作用,構建表達質粒和合成相應的SIRNA,由廣州銳博公司設計合成。合成的SIRNA要在無RNA酶環境下進行溶解分裝并置于?20 ℃保存。實驗分組:轉染STAT3過表達質粒 (STAT3組) 及其對照質粒pCDNA3.1 (NC組);轉染SIRNA-STAT3 (SI-STAT3組)干擾STAT3的表達及其對照SIRNA-STAT3-Control (SI-NC1組)。轉染CX3CL1過表達質粒 (CX3CL1組) 及其對照組pCDNA3.1 (NC組);轉染SIRNA-CX3CL1 (SI-CX3CL1組) 干擾CX3CL1的表達及其對照組SIRNA-CX3CL1-Control (SI-NC2組)。轉染前保證培養細胞處于對數生長期,此時轉染細胞狀態最好。應用FPF-g-PEI (Folate-poly (Ethylene glycol)-folate-grafted-polyethylenimine,PEI) 化合物作為轉染試劑進行轉染。根據6孔板1×106/2 mL、12孔板5×105/mL濃度種植細胞,用完全培養基培養細胞6 h后完全貼壁,準備轉染液配制。配制前提前半小時將細胞培養更換為無血清低糖DMEM培養基,然后按質粒∶PEI化合物=1∶3比例分別用無血清低糖DMEM培養基配置細胞轉染液200 μL,每100 μL中分別加轉染質粒和對應的轉染試劑,然后在室溫下放置5–10 min后混勻;混勻后37 ℃放置30 min。最后根據每個孔總培養基的量加入轉染液并補足無血清培養基,作好標記放置于37 ℃、5% CO2培養箱內培養8 h后棄掉轉染液更換為完全培養基繼續培養至48 h。

表1 質粒構建引物設計
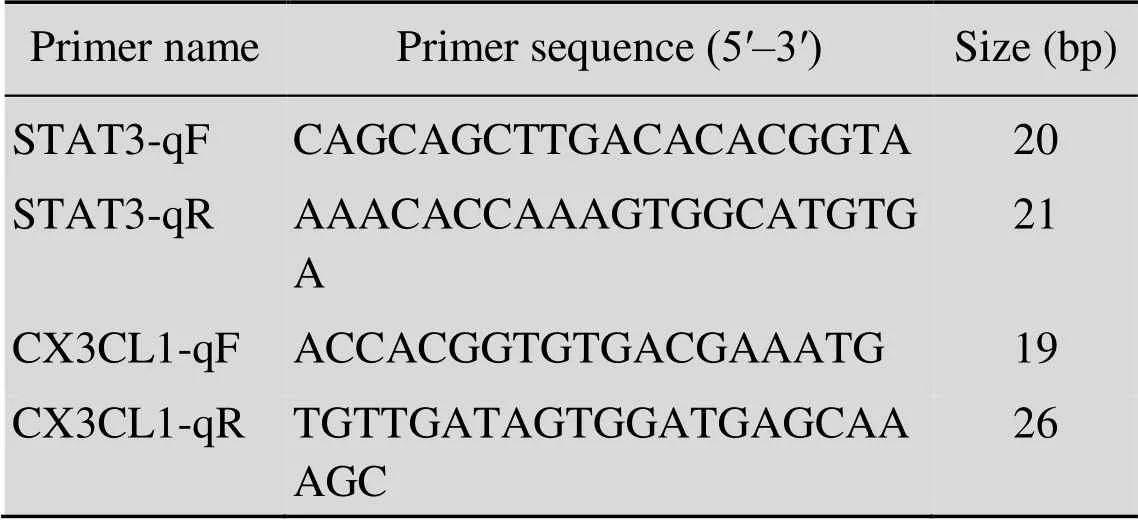
表2 實時熒光定量核酸擴增檢測引物序列
1.2.3 熒光素酶報告基因活性的測定 (Luciferase)
熒光素酶報告基因是指以熒光素 (Luciferin) 為底物來檢測螢火蟲熒光素酶 (Firefly luciferase) 活性的一種報告系統。熒光素酶可以催化luciferin氧化成oxyluciferin,在luciferin氧化的過程中,會發出生物熒光 (Bioluminescence)。先按pCDNA3.1+CX3CL1-WT組 (共轉pCDNA3.1和pGL3-CX3CL1-WT)、STAT3+CX3CL1-WT組 (共轉pCDNA3.1-STAT3和pGL3-CX3CL1-WT)、pCDNA3.1+CX3CL1-MUT組 (共轉pCDNA3.1和pGL3-CX3CL1-MUT)、STAT3+CX3CL1-MUT組(共轉pCDNA3.1-STAT3和pGL3-CX3CL1-MUT) 轉染細胞并進行培養。然后從孵育箱中取出經過處理好并培養48 h的細胞,棄去24孔板培養基,用PBS洗3次,動作輕柔避免細胞漂浮。后按150 μL/孔加入細胞裂解液,輕輕搖動讓裂解液完全覆蓋細胞后放冰上裂解30 min。小心刮下細胞,吸走裂解液轉到EP管,在冷凍超速離心機中于4 ℃、12 000 r/min離心20 min。離心后每個樣取上清和檢測底物,測20 s內的發光值。
1.2.4 MTT細胞增殖檢測
將對數期細胞均勻鋪在96孔板中,細胞濃度為1×104個/mL,每孔加100 μL。按照實驗分組,設6個復孔,37 ℃、5% CO2培養至24 h后,每孔加MTT溶液 (5 mg/mL,用pH 7.4的PBS緩沖液配制) 20 μL。繼續孵育4 h,終止培養,小心棄去孔內培養上清液,對于懸浮細胞,需要離心后再吸棄孔內培養上清液。每孔加150 μL DMSO,振蕩10 min,使結晶物充分溶解。后選擇490 nm波長,在酶聯免疫監測儀上測各組光密度 (Optical density,) 值。記錄測定結果。
1.2.5 細胞劃痕實驗檢測細胞遷移能力
將處理好的對數期細胞均勻鋪在12孔板中,待細胞貼壁并找到合適的密度開始劃線,劃線采用20 μL移液槍頭筆直地劃4條線,然后用PBS將漂浮的細胞洗滌3次。加入培養基放入37 ℃、5% CO2培養箱培養,針對同一視野選取不同的時間來拍攝記錄細胞增殖遷移情況。
1.2.6 實時熒光定量核酸擴增檢測 (qPCR)
將細胞培養并進行轉染處理后培養48 h,分別收集各組細胞至EP管中,離心后用Trizol裂解細胞快速提取RNA,提取時應防止污染導致RNA降解。然后進行逆轉錄合成cDNA。最后用熒光定量PCR試劑盒檢測基因的表達,獲取數據進行處理。
1.2.7 蛋白質印跡法檢測 (Western blotting)
在6孔板中種板細胞,待細胞進入對數生長期后,進行實驗分組并對細胞進行轉染。培養至48 h后分別收集細胞約5×106個,離心去上清,用裂解液裂解細胞,提取總蛋白進行定量,根據相應的實驗分組進行SDS-PAGE、300 mA轉膜 1 h。用5%奶牛封閉1 h,一抗 (一抗STAT3孵育濃度為1∶1 000,一抗CX3CL1孵育濃度為1∶1 500) 4 ℃孵育過夜,TBST洗膜5次, 5 min/次。用二抗37 ℃孵育2 h,洗膜后加化學底物發光試劑ECL,用核酸蛋白凝膠圖像系統顯影。用Origin 8軟件分析。
1.2.8 統計學方法
數據采用SSPS 13.0統計軟件單因素方差分析,以±表示,組間比較用檢驗或非參數檢驗,以<0.05為差異顯著,以α=0.05為顯著檢驗水準。
2 結果與分析
2.1 質粒構建及轉染效率圖
圖1A顯示PCR擴增出帶有CX3CL1啟動子片段、表達CX3CL1基因片段、表達STAT3基因片段以及構建成功的CX3CL1啟動子熒光素酶質粒和突變質粒、CX3CL1表達質粒和STAT3表達質粒。圖1B中紅色是轉染CY3后在熒光顯微鏡下觀察到的結果,代表SIRNA的轉染效率。綠色是轉染GFP后在熒光顯微鏡下觀察到的結果,代表質粒的轉染效率。CY3的轉染效率為70%左右,GFP的轉染效率為30%左右。
2.2 過表達STAT3上調CX3CL1的表達
Western blotting、QPCR檢測結果顯示,過表達STAT3組STAT3、CX3CL1水平比對照組高,SI-STAT3組STAT3、CX3CL1水平有所降低 (圖2A、2B)。
2.3 STAT3影響CX3CL1的啟動子活性
CX3CL1啟動子上TGCTGGGAA序列為GAS位點,為檢測STAT3與CX3CL1啟動子的相互作用,故將該位點序列突變為非GAS位點 (圖3A)。進行熒光素酶活性分析時,實驗組為共轉STAT3和野生型或者突變型CX3CL1啟動子熒光素酶質粒,共轉pCDNA3.1和CX3CL1啟動子熒光素酶質粒作為對照組。結果顯示,共轉STAT3和野生型CX3CL1啟動子熒光素酶質粒的實驗組熒光素酶活性明顯高于對照組 (<0.05),而共轉STAT3和突變型CX3CL1啟動子熒光素酶質粒的熒光素酶活性相比對照組變化不顯著 (圖3B)。

圖1 質粒構建和轉染效率
2.4 STAT3、CX3CL1促進HUVECs增殖
MTT檢測結果顯示,轉染STAT3、CX3CL1組HUVEC細胞在490 nm處測得的值與對照組相比明顯增高,而分別用SI-STAT3、SI-CX3CL1處理后的實驗組值明顯下降 (<0.05) (圖4A、4B)。
2.5 STAT3、CX3CL1對HUVECs遷移能力的影響
采用細胞劃痕試驗檢測各組細胞遷移能力。48 h后,觀察到STAT3、CX3CL1組相對于對照組細胞增殖遷移能力明顯增強,SI-STAT3和SI-CX3CL1組細胞遷移能力下降 (圖5A、5B)。表明STAT3和CX3CL1促進HUVECs遷移,而干擾STAT3以后,可能下調CX3CL1的水平從而抑制細胞遷移。
2.6 敲降CX3CL1時過表達STAT3對HUVEC的遷移能力的影響
為進一步驗證STAT3對HUVEC的遷移能力的影響是通過作用于CX3CL1來實現的,在敲降CX3CL1水平的同時過表達STAT3,通過圖6A可觀察到并沒有明顯地促進細胞遷移,而圖6B中敲低STAT3時過表達CX3CL1仍然能促進細胞遷移。這說明,CX3CL1可能作為STAT3的下游靶基因,對HUVEC的遷移有著更直接的影響。


3 討論
信號轉導子和轉錄激活子STAT3參與機體內多種生物學過程,包括細胞存活、增殖、纖維化、氧化應激、免疫功能改變及炎性反應等[14-15]。STAT3基因中的功能獲得性突變會引起多種疾病的產生。在與血管有關的疾病中,STAT3作為重要轉錄因子參與血管平滑肌細胞增殖過程[16-17]。JAK/STAT信號通路與CX3CL1密切相關,其調節異常可促使CX3CL1的表達[18]。CX3CL1是一種結構獨特的趨化因子,膜結合性CX3CL1被 2個肽酶ADAM10和ADAM17裂解后能形成可溶性CX3CL1[19]。CX3CL1-CX3CR1軸活性在不穩定性心絞痛和斑塊破裂或心血管疾病患者中表現增強[20-21]。據報道,CX3CL1和CX3CR1在動脈粥樣硬化中起重要作用,最有可能是通過促進血管壁炎癥[22]。在動脈粥樣硬化晚期的人動脈中觀察到高水平的CX3CL1 mRNA,在載脂蛋白基因apoE缺陷 (apoE-/-) 小鼠的動脈粥樣硬化病變中CX3CL1上調[23]。CX3CL1在正常的ECs中表達水平較低,由促炎因子如脂多糖、腫瘤壞死因子-α、白細胞介素-1和干擾素-α激活的EC中表達顯著增加[24]。腫瘤壞死因子-α和白細胞介素-1通過核因子kβ信號通路誘導CX3CL1的表達,而干擾素-β通過JAK/STAT1誘導CX3CL1的表達[25-26]。
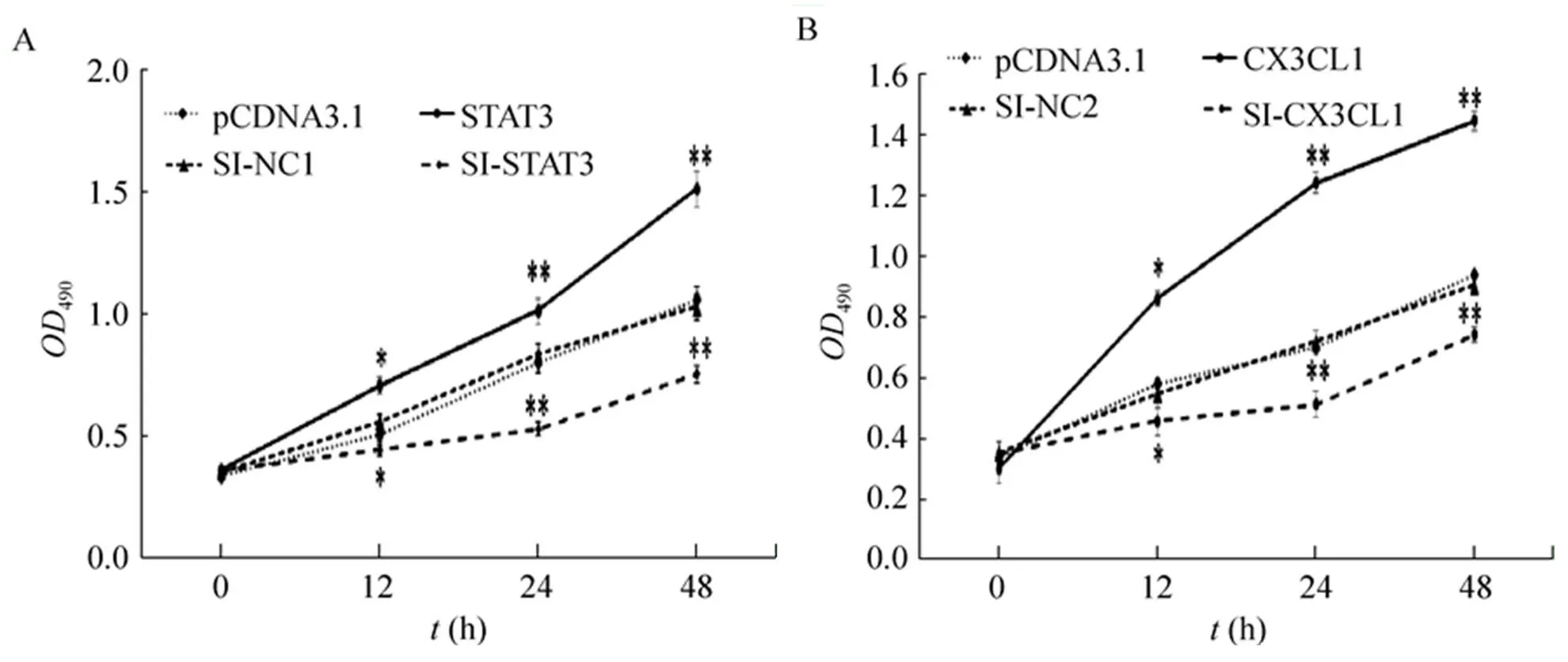
圖4 MTT測STAT3、CX3CL1對HUVEC細胞增殖的影響
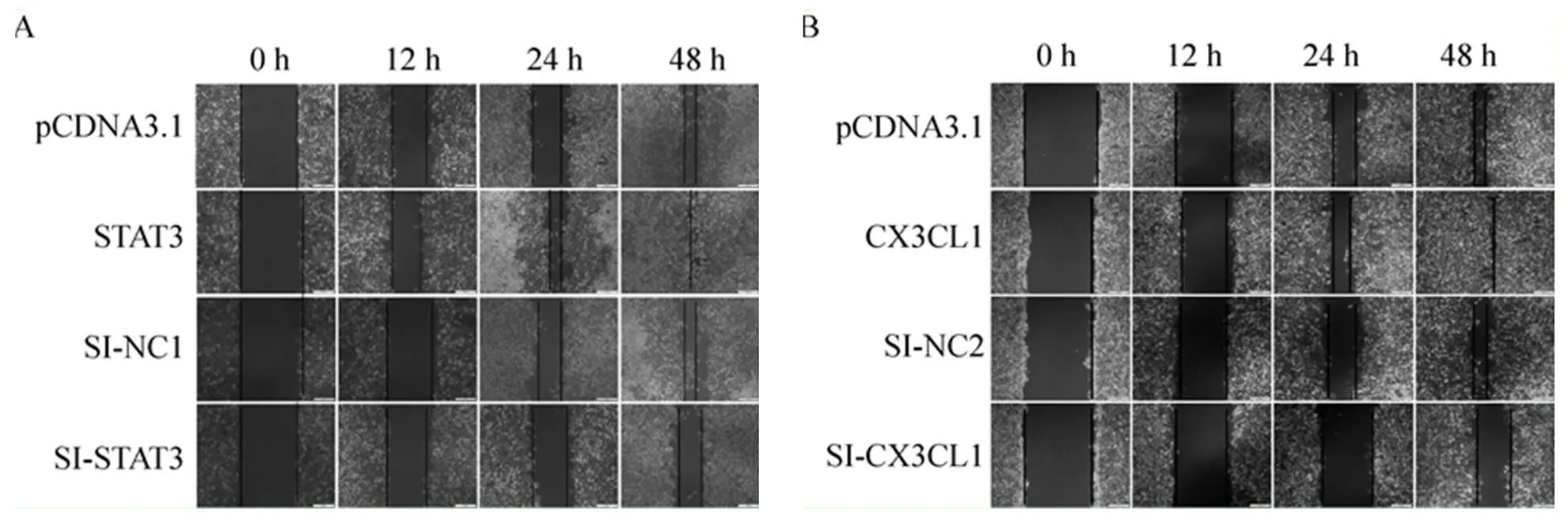
圖5 STAT3和CX3CL1對HUVEC的遷移能力的影響
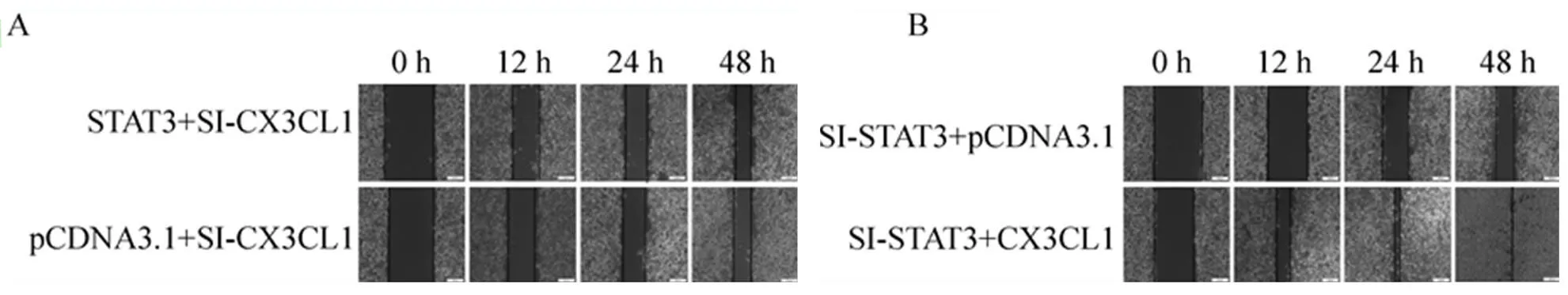
圖6 敲低CX3CL1時過表達STAT3對HUVEC的遷移能力的影響
為研究STAT3參與細胞的增殖過程是否通過調控CX3CL1來實現,以及探討在STAT3轉錄因子介導下CX3CL1對血管內皮細胞本身增殖能力的影響,本文針對STAT3對CX3CL1作用方式、STAT3對CX3CL1表達的調控以及其相互作用對內皮細胞增殖和遷移的影響也進行了初步的探索。結果表明STAT3可能通過作用于CX3CL1啟動子上的GAS區來調控CX3CL1水平,并且結果也顯示CX3CL1可以促進細胞增殖和遷移,STAT3能誘導血管內皮細胞CX3CL1表達上調。以上說明STAT3可能是通過直接作用于CX3CL1的啟動子上調CX3CL1的水平,從而促進細胞增殖和遷移。而干擾血管內皮細胞中STAT3的表達,則能下調CX3CL1的水平并能抑制血管內皮細胞增殖和遷移。這些結論對動脈粥樣硬化的機制研究具有重大意義,并且炎癥因子CX3CL1成為動脈粥樣硬化的治療靶點對尋找動脈粥樣硬化的治療藥物具有潛在的應用價值。
[1] Sorci-Thomas MG, Thomas MJ. Microdomains, inflammation, and atherosclerosis. Circ Res, 2016, 118(4): 679–691.
[2] Kiu H, Nicholson SE. Biology and significance of the JAK/STAT signalling pathways. Growth Factors, 2012, 30(2): 88–106.
[3] O’Shea JJ, Schwartz DM, Villarino AV, et al. The JAK-STAT pathway: impact on human disease and therapeutic intervention. Annu Rev Med, 2015, 66: 311–328.
[4] Zhao GB, Zhu GW, Huang YJ, et al. IL-6 mediates the signal pathway of JAK-STAT3-VEGF-C promoting growth, invasion and lymphangiogenesis in gastric cancer. Oncol Rep, 2016, 35(3): 1787–1795.
[5] postolakis S, Spandidos D. Chemokines and atherosclerosis: focus on the CX3CL1/CX3CR1 pathway. Acta Pharmacol Sin, 2013, 34(10): 1251–1256.
[6] Flierl U, Bauersachs J, Sch?fer A. Modulation of platelet and monocyte function by the chemokine fractalkine (CX3CL1) in cardiovascular disease. Eur J Clin Invest, 2015, 45(6): 624–633.
[7] Wong BW, Wong D, Mcmanus BM. Characterization of fractalkine (CX3CL1) and CX3CR1 in human coronary arteries with native atherosclerosis, diabetes mellitus, and transplant vascular disease. Cardiovasc Pathol, 2002, 11(6): 332–338.
[8] Furio E, García-Fuster MJ, Redon J, et al. CX3CR1/CX3CL1 Axis mediates platelet-leukocyte adhesion to arterial endothelium in younger patients with a history of idiopathic deep vein thrombosis. Thromb Hhemostasis, 2018, 118(3): 562–571.
[9] Ou D, He RZ. Research progress of cytokines in the pathogenesis of pulmonary hypertension. Guangzhou Med J, 2016, 47(2): 100–102 (in Chinese).歐東, 賀仁忠. 細胞因子在肺動脈高壓發病中作用的研究進展. 廣州醫藥, 2016, 47(2): 100–102.
[10] Rowinska Z, Koeppel TA, Sanati M, et al. Role of the CX3C chemokine receptor CX3CR1 in the pathogenesis of atherosclerosis after aortic transplantation. PLoS ONE, 2017, 12(2): e0170644.
[11] McDermott DH, Fong AM, Yang Q, et al. Chemokine receptor mutant CX3CR1-M280 has impaired adhesive function and correlates with protection from cardiovascular disease in humans. J Clin Invest, 2003, 111(8): 1241–1250.
[12] Gan AM, Butoi E, Manea A, et al. Functional analysis of the fractalkine gene promoter in human aortic smooth muscle cells exposed to proinflammatory conditions. FEBS J, 2015, 281(17): 3869–3881.
[13] Park HJ, Zhang YL, Georgescu SP, et al. Human umbilical vein endothelial cells and human dermal microvascular endothelial cells offer new insights into the relationship between lipid metabolism and angiogenesis. Stem Cell Rev, 2006, 2(2): 93–101.
[14] O'Shea JJ, Plenge R. JAK and STAT signaling molecules in immunoregulation and immune-mediated disease. Immunity, 2012, 36(4): 542–550.
[15] Matsui F, Meldrum KK. The role of the Janus kinase family/signal transducer and activator of transcription signaling pathway in fibrotic renal disease. J Surg Res, 2012, 178(1): 339–345.
[16] Li F, Xia K, Ali Sheikh MS, et al. Retinol binding protein 4 promotes hyperinsulinism-induced proliferation of rat aortic smooth muscle cells. Mol Med Rep, 2014, 9(5): 1634–1640.
[17] Lim S, Park S. Role of vascular smooth muscle cell in the inflammation of atherosclerosis. BMB Rep, 2014, 47(1): 1–7.
[18] Huang LY, Ma BW, Ma JW, et al. Fractalkine/CX3CR1 axis modulated the development of pancreatic ductal adenocarcinoma via JAK/STAT signaling pathway. Biochem Biophys Res Commun, 2017, 493(4): 1510–1517.
[19] Clark AK, Malcangio M. Fractalkine/CX3CR1 signaling during neuropathic pain. Front Cell Neurosci, 2014, 8: 121.
[20] Yin XY, Zhang SF, Yu D, et al. Circulating fractalkine levels predict the development of the metabolic syndrome. Int J Endocrinol, 2014, 2014: 715148.
[21] Zhang HL, Guo CF, Wu DJ, et al. Hydrogen sulfide inhibits the development of atherosclerosis with suppressing CX3CR1 and CX3CL1 expression. PLoS ONE, 2012, 7(7): e41147.
[22] Imai T, Yasuda N. Therapeutic intervention of inflammatory/immune diseases by inhibition of the fractalkine (CX3CL1)-CX3CR1 pathway. Inflammat Regenerat, 2016, 36: 9.
[23] Ebaid H, Salem A, Sayed A, et al. Whey protein enhances normal inflammatory responses during cutaneous wound healing in diabetic rats. Lipids Health Dis, 2011, 10(1): 235–235.
[24] Matsuura T, Ichinose S, Akiyama M, et al. Involvement of CX3CL1 in the migration of osteoclast precursors across osteoblast layer stimulated by interleukin‐1?. J Cell Physiol, 2017, 232(7): 1739–1745.
[25] Garcia GE, Xia YY, Chen SZ, et al. NF-κB-dependent fractalkine induction in rat aortic endothelial cells stimulated by IL-1β, TNF-α, and LPS. J Leukocyte Biol, 2000, 67(4): 577–584.
[26] Jang J, Yoon Y, Oh DJ. A calpain inhibitor protects against fractalkine production in lipopolysaccharide- treated endothelial cells. Kidney Res Clin Pract, 2017, 36(3): 224–231.
Signal transducer and activator of transcription 3 promotes vascular endothelial cell proliferation and migration by fractalkine
Lijuan Fan, Hui Li, Huimin Zhang, Hanhan Li, Feng Huang, Zijian Zhang, Zhoutong Dai, Yuan Xiang, Ao Yao, Jiapeng Li, and Xinghua Liao
College of Life Sciences and Health, Wuhan University of Science and Technology, Wuhan 430000, Hubei, China
Signal transducer and activator of transcription 3 (STAT3) and Chemokine CX3C ligand 1 (Fractalkine/CX3CL1) play important roles in vascular inflammation and injury. To study if STAT3 promotes vascular endothelial cell proliferation and migration through fractalkine, we overexpressed or knocked down STAT3 in vascular endothelial cells, and used quantitative real-time PCR and Western blotting to determine the effect of STAT3 on fractalkine expression. The wild type and STAT3 binding site mutantfractalkine promoter luciferase reporter plasmids were constructed, and luciferase activity assays were used to explore the effect of STAT3 on the transcriptional activity of the fractalkine promoter. MTT assays were used to detect the effect of overexpression or knockdown of STAT3 or fractalkine on the proliferation rate of vascular endothelial cells. Scratch assays were used to detect the effect of overexpression or knockdown of STAT3 orfractalkine on vascular endothelial cell migration. There results showed that overexpression of STAT3 could promote fractalkine expression, and knockdown of STAT3 could down-regulate fractalkine expression. STAT3 could directly bind to the promoter of fractalkine to promote its transcriptional activity via binding the GAS site of the fractalkine promoter. Knockdown of STAT3 could inhibit the migration of vascular endothelial cell, and overexpression of fractalkine antagonized this inhibition. Our data concluded that STAT3 promotes the proliferation and migration of vascular endothelial cell by binding the GAS site of the fractalkine promoter to promote fractalkine transcriptional activity and expression.
human umbilical vein endothelial cells, CX3CL1, STAT3, proliferation, migration
10.13345/j.cjb.180355
September 3, 2018;
December 20, 2018
National Natural Science Foundation of China (No. 31501149),Hubei Science and Technology Program Natural Science Fund General Project (No. 2017CFB537).
Xinghua Liao. Tel: +86-27-68893396; E-mail: xinghualiao@hotmail.com
國家自然科學基金 (No. 31501149),湖北省科技計劃自然科學基金 (No. 2017CFB537) 資助。
2019-02-19
http://kns.cnki.net/kcms/detail/11.1998.q.20190218.0956.002.html
(本文責編 陳宏宇)

