四味顆粒微生物限度檢查方法學(xué)驗(yàn)證*
胡 婧,鄧 莉,胡 斌,馬 攀,陳勇川
(陸軍軍醫(yī)大學(xué)第一附屬醫(yī)院藥學(xué)部,重慶 400038)
藥品的微生物限度檢查是控制藥品質(zhì)量的一項(xiàng)重要檢查項(xiàng)目,是制劑安全性檢查的重要組成部分[1]。自2005年版《中國藥典》開始,就對(duì)微生物限度檢查法的驗(yàn)證提出了具體要求:“當(dāng)進(jìn)行藥品無菌檢查或微生物限度檢查時(shí),應(yīng)進(jìn)行方法學(xué)驗(yàn)證,否則不能出具符合《中國藥典》規(guī)定的結(jié)論。”2015年版《中國藥典》相對(duì)于2010年版在非無菌產(chǎn)品微生物限度檢查方面做了較大改動(dòng),修訂后的微生物限度檢查方法與《美國藥典》要求基本一致[2-3],在中國制藥的國際化進(jìn)程上又向前邁進(jìn)了一大步。四味顆粒作為我院自制制劑,功能活血化瘀、軟堅(jiān)散結(jié)、鎮(zhèn)痛消脹,臨床運(yùn)用在各種乳腺增生性疾病的治療已多年,療效確切。為確保其微生物限度檢查質(zhì)量安全性達(dá)到要求[4],按照 2015年版《中國藥典(四部)》附錄 1105,1106,1107 項(xiàng)下要求[5],對(duì)四味顆粒的微生物限度檢查法進(jìn)行驗(yàn)證。由于四味顆粒為中藥復(fù)方制劑,其含有多種中藥成分,其中山楂對(duì)微生物具有抑菌作用,應(yīng)消除其抑菌性后再進(jìn)行檢查,故采用稀釋法和常規(guī)法相結(jié)合進(jìn)行四味顆粒的微生物限度檢查,以消除制劑中山楂的抑菌性。現(xiàn)報(bào)道如下。
1 儀器與材料
儀器:Thermo Scientific-1381 A2型生物安全柜(美國Thermo公司);BL-150型電子天平(梅特勒托利多儀器<上海 >有限公司);LRH-150F型生化培養(yǎng)箱(重慶四達(dá)實(shí)驗(yàn)儀器公司);MJ-180-Ⅱ型霉菌培養(yǎng)箱(上海躍進(jìn)醫(yī)療器械有限公司);LDZX-75KBS型、LDZF-30KB-Ⅱ型立式壓力蒸汽滅菌器(上海申安醫(yī)療器械有限公司)。
試藥:四味顆粒(醫(yī)院制劑,批號(hào)分別為180205,180319,180402,規(guī)格為每包 10 g);pH 7.0 氯化鈉 - 蛋白胨緩沖液(北京三藥科技開發(fā)公司,批號(hào)為170519);0.9%無菌氯化鈉溶液(西南藥業(yè)股份有限公司,批號(hào)為17034002)。
菌種:金黃色葡萄球菌[CMCC(B)26003]、枯草芽孢桿菌[CMCC(B)63501]、銅綠假單胞菌[CMCC(B)10104]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]、大腸埃希菌[CMCC(B)44102],均由中國食品藥品檢定研究院提供,試驗(yàn)所用菌株均為第3代。
培養(yǎng)基:胰酪大豆胨液體培養(yǎng)基(批號(hào)為161205),胰酪大豆胨瓊脂培養(yǎng)基(批號(hào)為1612192),沙氏葡萄糖液體培養(yǎng)基(批號(hào)為170815),沙氏葡萄糖瓊脂培養(yǎng)基(批號(hào)為1702134),麥康凱液體培養(yǎng)基(批號(hào)為161205),麥康凱瓊脂培養(yǎng)基(批號(hào)為161212),均由北京三藥科技開發(fā)公司提供。
2 方法與結(jié)果
2.1 計(jì)數(shù)培養(yǎng)基適應(yīng)性檢查[6]
分別取金黃色葡萄球菌、銅綠假單胞菌、枯草芽孢桿菌、白色念珠菌及黑曲霉菌的菌液,均不大于100 cfu,分別注入無菌平皿中,立即傾注胰酪大豆胨瓊脂培養(yǎng)基,每株試驗(yàn)菌平行制備2個(gè)平皿,混勻,凝固,置35℃培養(yǎng)3 d,計(jì)數(shù);分別取白色念珠菌、黑曲霉的菌液,均不大于100 cfu,分別注入無菌平皿中,立即傾注沙氏葡萄糖瓊脂培養(yǎng)基,每株試驗(yàn)菌平行制備2個(gè)平皿,混勻,凝固,置25℃ 培養(yǎng)5 d,計(jì)數(shù)。同時(shí),用相應(yīng)對(duì)照培養(yǎng)基替代被檢培養(yǎng)基進(jìn)行上述試驗(yàn)。結(jié)果見表1。
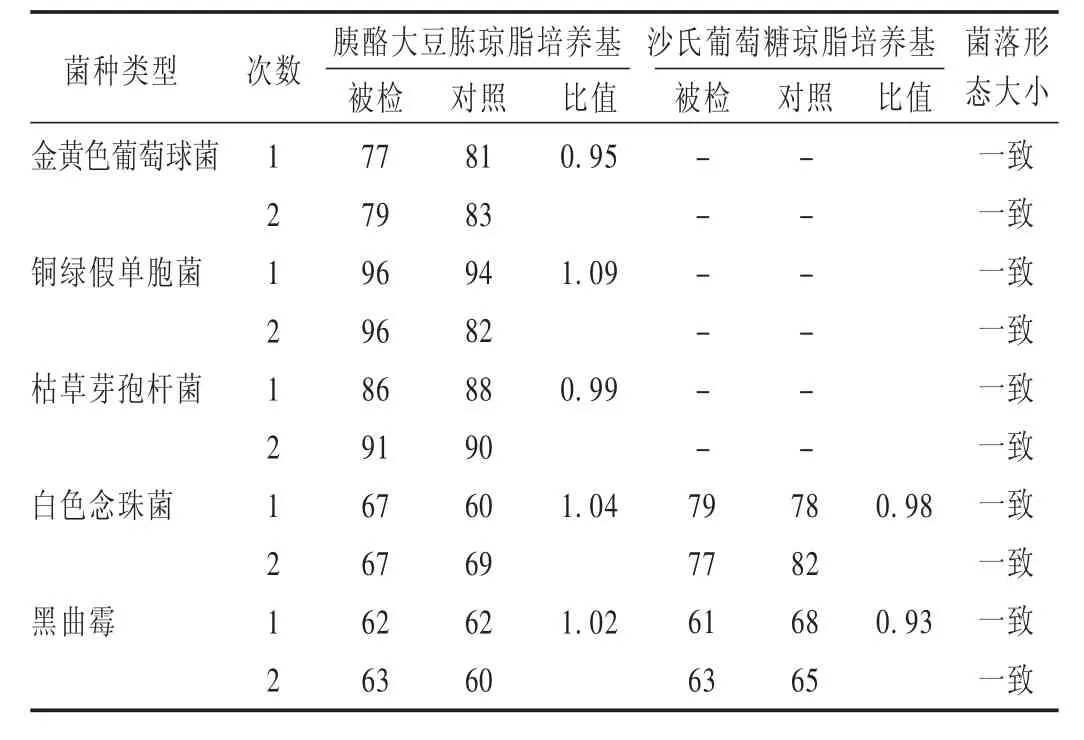
表1 培養(yǎng)基適用性檢查結(jié)果(cfu,n=2)
2.2 常規(guī)法適用性試驗(yàn)
2.2.1 菌液制備
取經(jīng)胰酪大豆胨液體培養(yǎng)基35℃培養(yǎng)24 h的金黃色葡萄球菌、枯草芽孢桿菌、銅綠假單胞菌、大腸埃希菌液體培養(yǎng)物,分別用0.9%無菌氯化鈉溶液稀釋成適宜濃度的菌懸液,作活菌計(jì)數(shù)備用。
取經(jīng)沙氏葡萄糖液體培養(yǎng)基25℃培養(yǎng)48 h的白色念珠菌液體培養(yǎng)物,用0.9%無菌氯化鈉溶液稀釋成適宜濃度的菌懸液,作活菌計(jì)數(shù)備用。
取經(jīng)沙氏葡萄糖瓊脂培養(yǎng)基25℃培養(yǎng)7 d的黑曲霉菌斜面培養(yǎng)物,加入含0.05%(mL/mL)聚山梨酯80的0.9%無菌氯化鈉溶液,將孢子洗脫,吸出孢子懸液(用管口帶有薄的無菌棉花或紗布能過濾菌絲的無菌毛細(xì)吸管),置無菌試管內(nèi),用0.9%無菌氯化鈉溶液制成適宜濃度的孢子懸液。
2.2.2 供試品溶液制備
取樣品(批號(hào)為 180205)10 g,加 pH 7.0 無菌氯化鈉-蛋白胨緩沖液至100 mL,搖勻,制成1∶10的供試品溶液。
2.2.3 回收率測定
試驗(yàn)組:取上述1∶10供試品溶液9.9 mL,共5份,每份分別加入金黃色葡萄球菌、銅綠假單胞菌、枯草芽孢桿菌、白色念珠菌及黑曲霉菌菌懸液各0.1 mL,使每1 mL含菌落數(shù)不大于100 cfu,混勻,吸取各染菌供試品溶液1 mL注入平皿中,每份平行制備2個(gè)平皿,傾注胰酪大豆胨瓊脂培養(yǎng)基,置35℃培養(yǎng)3 d,測定需氧菌總數(shù)。取上述1∶10供試品溶液 9.9 mL,共 2份,每份分別加入白色念珠菌和黑曲霉試驗(yàn)菌菌懸液各0.1 mL,使每1 mL含菌數(shù)不大于100 cfu,混勻,吸取各染菌供試品溶液1 mL置平皿中,每份平行制備2個(gè)平皿,傾注沙氏葡萄糖瓊脂培養(yǎng)基,置25℃培養(yǎng)5 d,測定霉菌及酵母菌總數(shù)。
菌液對(duì)照組:吸取pH 7.0無菌氯化鈉-蛋白胨緩沖液9.9 mL,共5份,每份分別加入金黃色葡萄球菌、枯草芽孢桿菌、銅綠假單胞菌、白色念珠菌、黑曲霉菌菌懸液各0.1 mL,使每 1 mL含菌落數(shù)不大于100 cfu,混勻,分別吸取1 mL置平皿中,每株試驗(yàn)菌平行制備2個(gè)平皿,傾注胰酪大豆胨瓊脂培養(yǎng)基;另取pH 7.0無菌氯化鈉-蛋白胨緩沖液9.9 mL,共2份,每份分別加入白色念珠菌、黑曲霉菌菌懸液各0.1 mL,使每1 mL含菌數(shù)不大于100 cfu,混勻,分別吸取1 mL置平皿中,每株試驗(yàn)菌平行制備2個(gè)平皿,傾注沙氏葡萄糖瓊脂培養(yǎng)基。
供試品組:吸取上述1∶10供試品溶液1 mL置平皿,平行制備4個(gè)平皿,其中2個(gè)傾注胰酪大豆胨瓊脂培養(yǎng)基,作為測定需氧菌總數(shù)的供試品組;另外2個(gè)傾注沙氏葡萄糖瓊脂培養(yǎng)基,作為測定基霉菌和酵母菌總數(shù)的供試品組。
稀釋液組:取相應(yīng)量稀釋液替代供試品溶液,同試驗(yàn)組操作,按試驗(yàn)組方法測定其菌落數(shù),平行制備2個(gè)平皿。
結(jié)果:依照公式計(jì)算加菌回收率。試驗(yàn)組菌比值=(試驗(yàn)組平均菌落數(shù)-供試品組的平均菌落數(shù))/菌液對(duì)照組的平均菌落數(shù)。按2015年版《中國藥典(四部)》附錄 1105,1106,1107項(xiàng)下[4]規(guī)定進(jìn)行結(jié)果判斷,回收率比值應(yīng)為0.5~2。需氧菌總數(shù)驗(yàn)證試驗(yàn)結(jié)果見表2,霉菌和酵母菌總數(shù)見表3。可見,常規(guī)法可用于霉菌和酵母菌的計(jì)數(shù),回收率為 0.5~2.0;而對(duì)于細(xì)菌的計(jì)數(shù),采用常規(guī)法檢查時(shí),供試品溶液對(duì)金黃色葡萄球菌、枯草芽孢桿菌的回收率均低于0.5,不符合規(guī)定。故本品對(duì)細(xì)菌的計(jì)數(shù)應(yīng)重新選擇適當(dāng)?shù)姆椒ǎ认湟志钚院笤龠M(jìn)行驗(yàn)證。
2.3 稀釋法(1∶50)適用性試驗(yàn)
2.3.1 菌液制備
制備方法同 2.2.1 項(xiàng)。
2.3.2 供試品溶液制備
取樣品10 g,加pH 7.0無菌氯化鈉-蛋白胨緩沖液至100 mL,搖勻,制成1∶10的貯備液;再取20 mL,加 pH 7.0無菌氯化鈉 -蛋白胨緩沖液至 100 mL,搖勻,制成1∶50的供試品溶液。
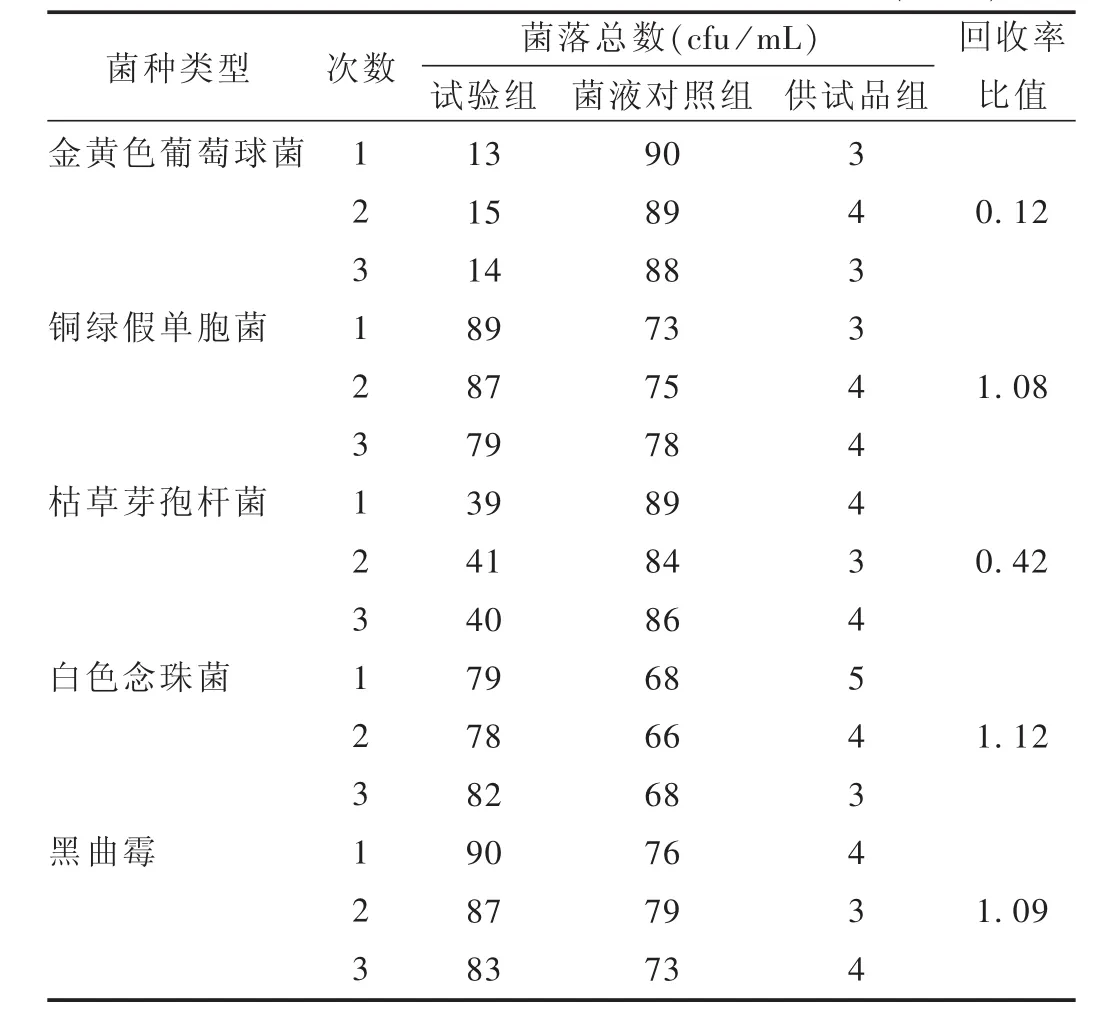
表2 1∶10供試品溶液需氧菌總數(shù)回收率比值(n=3)
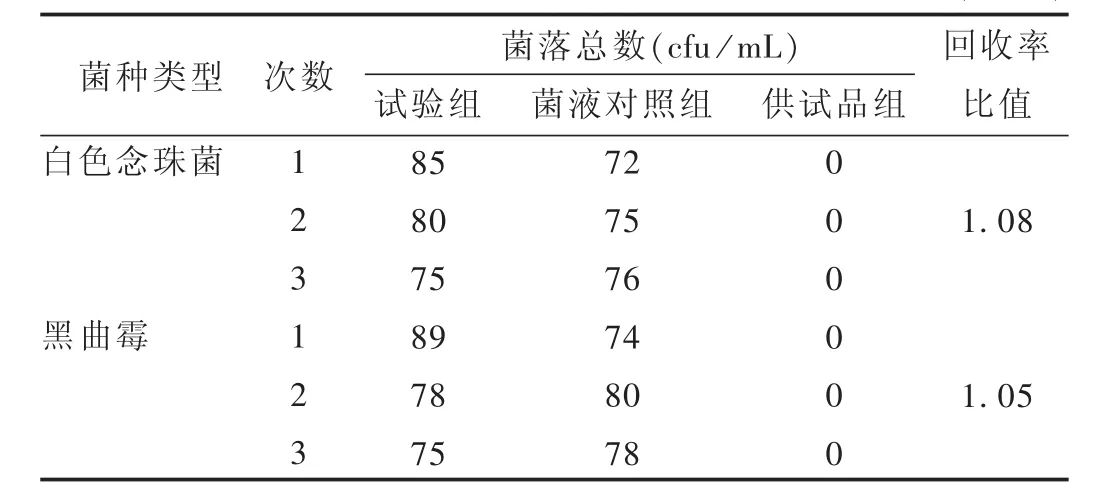
表3 1∶10供試品溶液霉菌和酵母菌回收率比值(n=3)
2.3.3 回收率測定
試驗(yàn)組:取上述1∶50供試品溶液9.9 mL,共5份,每份分別加入金黃色葡萄球菌、銅綠假單胞菌、枯草芽孢桿菌、白色念珠菌及黑曲霉菌菌懸液各0.1 mL,使每1 mL含菌落數(shù)不大于100 cfu,混勻,吸取各染菌供試品溶液1 mL置平皿中,每份平行制備2個(gè)平皿,傾注胰酪大豆胨瓊脂培養(yǎng)基,置35℃培養(yǎng)3 d,測定需氧菌總數(shù)。
菌液對(duì)照組:吸取pH 7.0無菌氯化鈉-蛋白胨緩沖液9.9 mL,共5份,每份分別加入金黃色葡萄球菌、枯草芽孢桿菌、銅綠假單胞菌、白色念珠菌、黑曲霉菌菌懸液各 0.1 mL,使每1 mL含菌落數(shù)不大于100 cfu,混勻,分別吸取1 mL置平皿中,每株試驗(yàn)菌平行制備2個(gè)平皿,傾注胰酪大豆胨瓊脂培養(yǎng)基。
供試品組:吸取上述1∶50供試品溶液1 mL置平皿中,平行制備2個(gè)平皿,傾注胰酪大豆胨瓊脂培養(yǎng)基,作為測定需氧菌總數(shù)的供試品組。
稀釋液組:取相應(yīng)量稀釋液替代供試品溶液,同試驗(yàn)組方法操作,依法測定其菌落數(shù),平行制備2個(gè)平皿。
結(jié)果:需氧菌總數(shù)稀釋法驗(yàn)證試驗(yàn)結(jié)果見表4。可見,采用常規(guī)法,控制菌能正常檢出,陰性對(duì)照未檢出。符合2015年版《中國藥典(四部)》微生物限度檢查控制菌檢查驗(yàn)證要求,所以常規(guī)法可用于四味顆粒的控制菌檢查。可見,金黃色葡萄球菌、銅綠假單胞菌、枯草芽孢桿菌、白色念珠菌、黑曲霉菌的回收率為 0.5~2.0,符合規(guī)定,本品細(xì)菌計(jì)數(shù)可采用稀釋法(1∶50)。

表4 1∶50供試品溶液需氧菌總數(shù)回收率比值(n=3)
2.4 控制菌(大腸埃希菌)檢查
試驗(yàn)組:取2.2.2項(xiàng)下 1∶10供試品溶液 10 mL及每1 mL含菌量不大于100 cfu的大腸埃希菌菌懸液,同時(shí)加入100 mL胰酪大豆胨液體培養(yǎng)基中,混勻,35℃培養(yǎng)24 h。取上述培養(yǎng)物1 mL接種至100 mL麥康凱液體培養(yǎng)基中,42℃培養(yǎng)24 h。取麥康凱液體培養(yǎng)物劃線接種至麥康凱瓊脂培養(yǎng)基平板上,35℃培養(yǎng)24 h,觀察結(jié)果。
菌液對(duì)照組:不加供試品溶液,其余操作與試驗(yàn)組相同。
供試品組:取2.2.2項(xiàng)下 1∶10供試品溶液10 mL,以稀釋液代替菌液,同試驗(yàn)組方法操作。
稀釋液組:以稀釋液代替供試品溶液,不加菌液,其余操作方法與試驗(yàn)組相同。
結(jié)果:觀察其菌落形態(tài)。驗(yàn)證結(jié)果見表5。

表5 大腸埃希菌檢查結(jié)果
2.5 樣品微生物限度檢查
采用稀釋法(1∶50)進(jìn)行需氧菌總數(shù)的檢查,常規(guī)法進(jìn)行霉菌和酵母菌總數(shù)及控制菌的檢查,對(duì)3批樣品進(jìn)行檢驗(yàn),結(jié)果見表6。可見,四味顆粒的微生物限度檢查方法為需氧菌總數(shù)檢查采用稀釋法(1:50),霉菌和酵母菌總數(shù)及控制菌檢查可采用常規(guī)法。結(jié)果表明,建立的檢查方法符合規(guī)定,可用于四味顆粒微生物限度的檢查。

表6 3批樣品微生物限度檢查結(jié)果(cfu/mL)
3 討論
中成藥組分復(fù)雜,劑型眾多,微生物檢測方法的適用性試驗(yàn)就顯得更為重要[6-8]。四味顆粒為我院治療乳腺增生類疾病的常用藥物,臨床用量極大,必須對(duì)制劑的安全性加以控制,而微生物限度檢查則是安全性檢查的重要環(huán)節(jié)。相對(duì)于前幾版藥典,2015年版《中國藥典》在微生物限度檢查方法和指導(dǎo)原則上均做出了較大修訂,增加了供試品制備中的稀釋液種類,采用胰酪大豆胨液體培養(yǎng)基和胰酪大豆胨瓊脂培養(yǎng)基取代了營養(yǎng)肉湯和營養(yǎng)瓊脂培養(yǎng)基;采用沙氏葡萄糖瓊脂培養(yǎng)基取代了玫瑰紅鈉培養(yǎng)基檢測霉菌與酵母菌總數(shù),相對(duì)于2010年版所采用的培養(yǎng)基具有良好的廣譜性,對(duì)目標(biāo)微生物的選擇性低,有利于微生物的修復(fù)與生長,提高了檢出率[9-10];在染菌方式上由試驗(yàn)菌最后加入改為配制樣品時(shí)即加入試驗(yàn)菌,充分模擬了樣品受微生物污染的狀態(tài),更能真實(shí)地體現(xiàn)樣品的受污染程度,從而減少實(shí)驗(yàn)室之間和檢驗(yàn)人員之間對(duì)結(jié)果的判斷誤差[11]。本研究中則是在原有微生物限度檢查方法基礎(chǔ)上按照新版指導(dǎo)要求重新建立四味顆粒的微生物限度檢查方法,并對(duì)其進(jìn)行驗(yàn)證,建立了符合規(guī)定的微生物限度檢查方法,以便在日常生產(chǎn)中更好地對(duì)藥物制劑質(zhì)量進(jìn)行監(jiān)督和把控,保證制劑質(zhì)量的安全性和穩(wěn)定性,保障廣大人民群眾的用藥安全。
四味顆粒由山楂、雞血藤、麥芽、通草4味中藥制成。山楂具有一定的抗菌活性,對(duì)多數(shù)致球菌和桿菌具有抑制作用,以山楂核提取物為主要?dú)⒕煞值钠つw消毒劑,對(duì)大腸桿菌,金黃色葡萄球菌、銅綠假單胞菌、白色念珠菌具有較好的殺菌效果,且穩(wěn)定性較好[12];在對(duì)14種中藥乙醇提取物對(duì)大腸桿菌的體外抑菌試驗(yàn)中,山楂表現(xiàn)出了良好的抑菌能力[13]。本研究中,采用常規(guī)法進(jìn)行需氧菌總數(shù)檢查時(shí),回收率均低于0.5,制劑顯示出了對(duì)金黃色葡萄球菌、枯草芽孢桿菌等需氧菌的抑菌作用,因此需抑制其抗菌活性。一般來說,中藥制劑采用稀釋法和薄膜過濾法以消除其抑菌活性[14-15],采用稀釋法(1 ∶20,1 ∶50,1 ∶100)3 個(gè)稀釋級(jí)考察,結(jié)果 1 ∶50的回收率可達(dá)到0.5~2.0,可消除其抑菌活性;而在進(jìn)行控制菌檢查時(shí),采用常規(guī)法制劑卻未顯示出對(duì)大腸埃希桿菌的抑菌活性,推測本制劑在制備過程中,抑制大腸桿菌的成分濃度未達(dá)到有效地最低抑菌濃度。由于中成藥大多為復(fù)方制劑,且經(jīng)過制備過程,藥理活性也會(huì)發(fā)生變化,因此個(gè)性化地對(duì)中藥制劑進(jìn)行微生物限度檢查方法的建立及驗(yàn)證顯得尤為重要,不僅能避免由于其本身的抑菌活性掩蓋了藥品制劑本身的受污染程度,還能簡化操作步驟,提高檢出效率。

