膠原肽聯合鈣爾奇D治療絕經后骨質疏松患者療效分析
王玉林 劉俊麗 李保成 王毅虎 楊國安 高黎明 葛根圖雅 王富榮 郭燕川
1.包頭醫學院第一附屬醫院,內蒙古 包頭 0140102.中國科學院理化技術研究所,北京 1001903.包頭東寶生物技術股份有限公司,內蒙古 包頭 014030
骨質疏松癥是一種代謝性疾病,其特征是骨形成不足、骨吸收過度而導致的骨量減少及骨微結構的惡化,其后果增加了骨脆性和骨折易感性[1],給患者及家庭和社會帶來了沉重的負擔[2]。目前用于骨質疏松癥的治療藥物主要以西藥為主,然而,這些藥物長期服用存在著安全隱患。例如,阿侖膦酸鈉是臨床治療骨質疏松的常規用藥,但不良反應會引起反酸、胃灼熱、腹痛等上消化道癥狀[3]。因此,有必要探索更安全、更有效的骨質疏松治療方案,以期解決這一問題。
膠原肽是膠原或明膠經蛋白酶降解處理后制成的富含人體需要的甘氨酸、脯氨酸、羥脯氨酸等氨基酸,具有較高的消化吸收性及安全性[4]。Kim等[5]的研究表明,100 μg/mL膠原蛋白肽能夠增加成骨細胞的增殖,以劑量依賴的方式促進堿性磷酸酶活性,促進膠原的合成,參與ERK/MAPK信號對COL1α1表達的轉錄影響。去卵巢大鼠每天服用150 mg/kg或500 mg/kg體重的膠原肽長達3個月后,與對照組相比,膠原蛋白肽能夠阻止去卵巢引起的骨丟失,并改善去卵巢大鼠椎骨組成及生物力學強度,顯著增加腰椎的骨小梁數目及骨體積比,從而顯示了較強的骨保護效果[6]。口服膠原肽或口服膠原肽聯合鈣能否治療絕經后骨質疏松癥,目前尚無文獻報道。因此,本研究篩選符合絕經后骨質疏松癥診斷標準患者202例,試驗組每日口服骨膠原肽10 g聯合鈣爾奇D600 mg,對照組口服鈣爾奇D600 mg,對絕經后骨質疏松患者進行為期6個月治療,通過骨密度(bone mineral density,BMD)及血清骨代謝指標評價,明確口服骨膠原肽聯合鈣爾奇D對絕經后骨質疏松患者BMD的影響。
1 對象與方法
1.1 研究對象
納入標準:選取2016年1年至2017年10月在包頭醫學院第一附屬醫院骨科門診就診的患者202例,符合WHO絕經后骨質疏松癥診斷標準即T≤-2.5SD,絕經3年以上,年齡為52~75歲,自愿參與并簽署知情同意書。
排除標準:任何非絕經后骨質疏松癥的骨病及其他代謝性骨病,如腎性骨營養不良、骨軟化、骨纖維病變;肝、腎功能明顯不全的患者;患有嚴重的心臟、血液、精神、神經系統疾病者;甲亢;患有癌癥和其他嚴重進行性疾病者;在近6個月接受雙膦酸鹽類抗骨質疏松癥藥物治療的患者;在近1個月內使用影響骨代謝藥物的患者(不包括補鈣和維生素D);對本藥、對照藥或其代謝成分過敏患者。
1.2 臨床評估及分組進行6個月干預治療
所有參加者均完成一份生活方式及醫學的綜合調查表,入選后對綜合調查表自行設計,分調查對象的一般情況和骨質疏松知識范圍具體問題兩大部分。其中一般情況包括性別、年齡、文化水平、身高、體重、生育史、絕經史、飲食習慣、運動習慣、陽光照射時間、煙齡和攝酒量;骨質疏松知識范圍包括有關骨質疏松知識掌握情況、獲取知識的途徑、具體預防措施實施情況和需求狀況。
入選者隨機接受鈣爾奇D(美國惠氏制藥有限公司)600 mg,或每日頓服骨膠原肽(包頭市東寶生物技術股份有限公司)10 g聯合鈣爾奇D600 mg/d,每日1次,干預治療6個月。
1.3 臨床疼痛癥狀療效評價
按照視覺模擬評分法(visual analogue scale,VAS)進行治療前后骨痛程度評價,根據疼痛強度分為4級:0級(0分),無疼痛;Ⅰ級(1~3分),有輕微疼痛,患者能忍受;Ⅱ級(4~6分),患者疼痛并且影響睡眠,但尚能忍受;Ⅲ級(7~10分),患者疼痛逐漸強烈,疼痛劇烈或難以忍受。療效評定:顯效,進步2級以上或疼痛消失;有效,進步1級但仍有疼痛癥狀;無效,疼痛無減輕或者加重。總有效率(%)=(顯效例數+有效例數)/總例數×100%。
1.4 骨密度測定及血清骨代謝指標檢查
在干預治療前及干預治療6個月后進行隨訪并檢測BMD、血清骨代謝指標。應用MEDIX DR骨密度測量儀(MEDILINK,France),利用雙能X線吸收法對所有入選者進行腰椎及髖部BMD檢測。利用全自動化學發光儀(Liaison,Italian)檢測血清總骨1型前膠原N端肽(N-propeptide of type 1 collagen,PINP)、β-I型膠原交聯羧基末端肽(C-terminal crosslinking telopeptides of type 1 collagen,β-CTX)、血清骨鈣素(N-MID osteocalcin,OC)、25-羥維生素D3[25 hydroxy vitamine D3,25(OH)D3]、甲狀旁腺素(parathyroid hormone,PTH)。
1.5 不良反應監測
治療前后分別監測所有患者的肝腎功能、血鈣、血磷水平及藥品不良反應發生情況。
1.6 統計學處理
BMD變化率=(治療后BMD-治療前BMD)/治療前BMD×100%。采用SPSS 17統計軟件進行數據分析,所有計量數據以均數±標準差表示。兩組間計量資料均數的比較采用兩獨立樣本的t檢驗;同組治療前后計量資料均數的比較采用配對t檢驗;以P<0.05為差異有統計學意義。
2 結果
2.1 兩組絕經后婦女患者一般資料比較
根據納入,試驗組、對照組受試者分別有102例、100例入選,各項指標如表1所示。兩組患者入組年齡、絕經年限、體重、身高、體質量指數(body mass index,BMI)及血糖水平差異均無統計學意義(P>0.05);入組前有脆性骨折史及合并慢性疾病的患者比例的差異在兩組間差異亦無統計學意義(P<0.05)(表1),所有患者完成 6個月的隨訪。

表1 兩組患者絕經后婦女一般資料比較 Table 1 Comparison of general characteristics between the two groups of postmenopausal women
2.2 兩組絕經后婦女患者治療效果比較
兩組治療后骨痛均有不同程度改善。試驗組與對照組治療6個月后治療顯效分別為67例、59例,有效分別為24例、30例,無效分別為7例、11例。因此,試驗組治療改善更明顯。
2.3 兩組絕經后婦女患者血清骨代謝水平比較
兩組患者治療前血清 PINP、β-CTX、PTH、25(OH)D3及OC水平比較差異無統計學意義(P>0.05)。治療6個月后,試驗組患者血清PTH、25(OH)D3及OC水平明顯高于治療前(分別增加45.92%、65.39%、16.18 %,P<0.01);對照組患者治療后血清β-CTX、PTH及25(OH)D3水平明顯高于治療前(分別增加100.00%、62.57%、78.84 %,P<0.01),總PINP水平明顯低于治療前(下降42.85%,P<0.01)。試驗組患者治療后血清總PINP、PTH、25(OH)D3及OC水平明顯高于對照組(分別增加84.81%、3.46%、7.16%、17.54 %,P<0.05),而β-CTX水平顯著低于對照組(降低1.18%,P<0.01)。詳見表2。
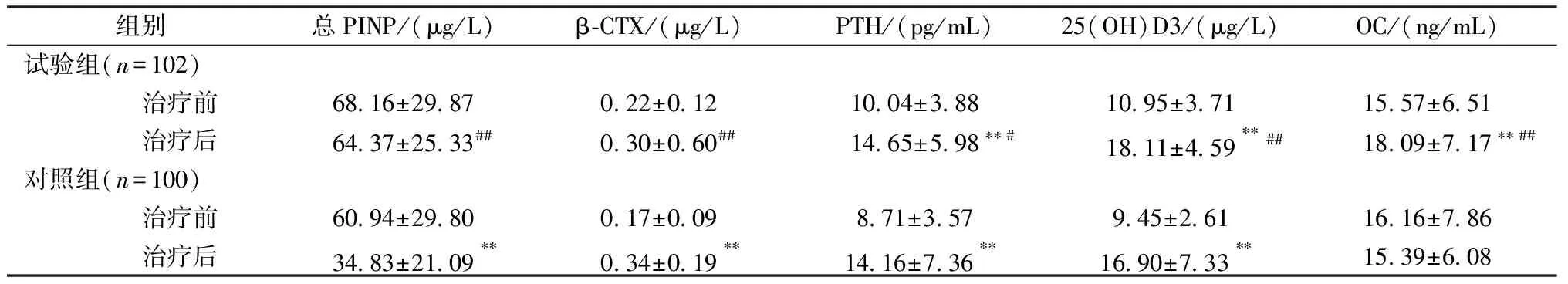
表2 兩組患者絕經后婦女治療前后骨代謝標志物水平比較 Table 2 Comparison of the levels of bone metabolic markers in the two groups of postmenopausal women before and after treatment
注:與治療前相比,*P<0.05,**P<0.01;與對照組相比,##P<0.01。
2.4 兩組絕經后婦女患者BMD比較
兩組患者治療前腰椎及股骨各部位BMD比較差異均無統計學意義(P>0.05)。治療6個月后,試驗組患者腰椎及股骨各部位L1~4、L1、L2、L3、L4,或股骨全髖、股骨頸、大粗隆、粗隆間BMD明顯高于治療前(分別增加4.41%、9.84%、7.69%、4.35%、4.35%和8.00%,或3.95%、4.48%、5.66%和6.67%,P<0.01);對照組患者治療后上述各指標差異無統計學意義(P>0.05)。試驗組患者腰椎L2、L4,或股骨頸、粗隆間BMD明顯高于對照組(分別增加9.38%、14.08% 或12.9%、11.63%,P<0.05)。詳見表3、4。
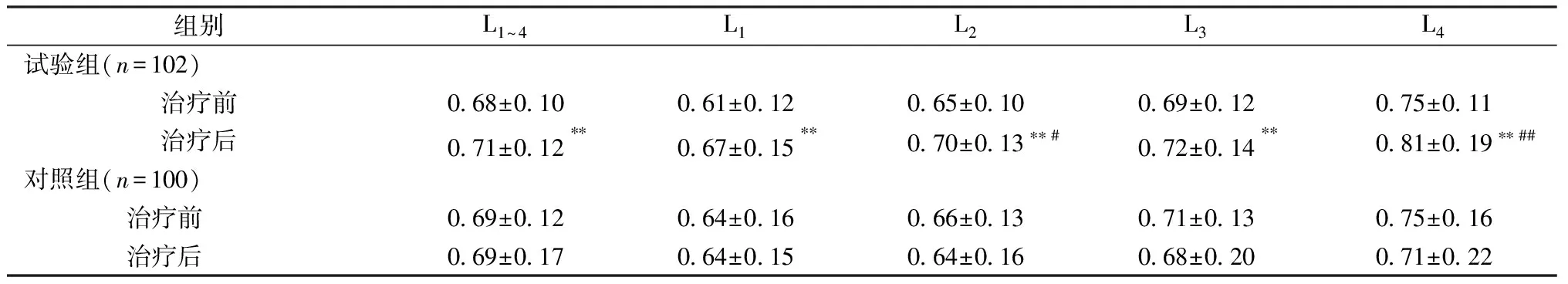
表3 兩組患者絕經后婦女治療前后腰椎BMD比較(g/cm2) Table 3 Comparison of lumbar spine BMD in the two groups of postmenopausal women before and after treatment(g/cm2)
注:與治療前相比,*P<0.05,**P<0.01;與對照組相比,##P<0.01。
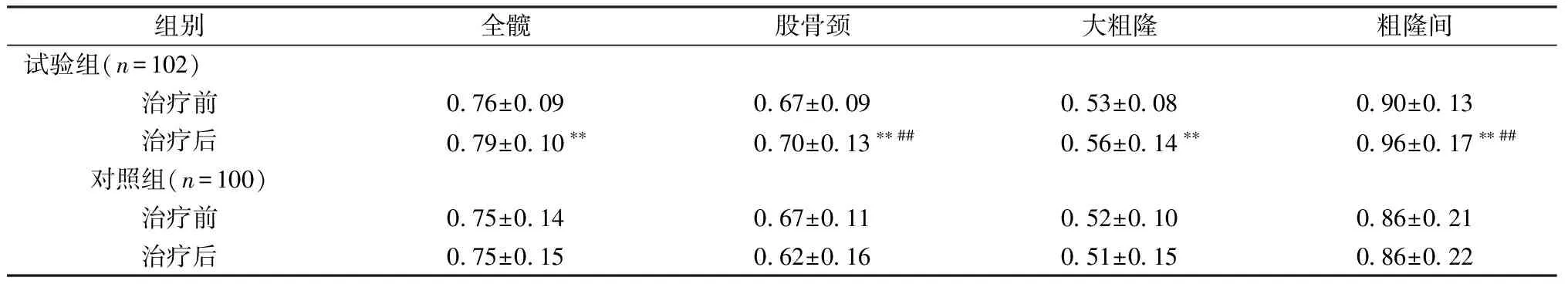
表4 兩組患者絕經后婦女治療前后股骨BMD比較(g/cm2) Table 4 Comparison of femur BMD before and after treatment in the two groups of postmenopausal women(g/cm2)
注:與治療前相比,*P<0.05,**P<0.01;與對照組相比,##P<0.01。
2.5 不良反應
治療前經檢測,兩組患者肝腎功能、血鈣、血磷水平等均無顯著變化,試驗組血鈣水平治療前為(2.16±0.40) mmol/L,治療后為(2.44±0.72) mmol/L,血鈣水平顯著升高(P<0.01);對照組血鈣治療前為(2.03±0.49) mmol/L,治療后為(2.24±0.94) mmol/L,血鈣水平顯著升高(P<0.01)。試驗組治療前血鈣水平與對照組相比顯著升高(P<0.05),治療后無顯著變化。試驗組治療后有2 例出現胃腸道不適癥狀,對照組中無不適癥狀,對癥處理后,上述癥狀均逐漸減輕至消失,最終所有患者均完成治療及隨訪。兩組患者不良事件發生率比較差異無統計學意義。
3 討論
據統計資料顯示,骨質疏松癥患病率在常見多發病中位居第7[7]。骨質疏松癥的患病人群以絕經后女性居多,由于絕經后女性的骨吸收速度大于骨質生成速度,導致了骨質丟失,進而引發骨質疏松。調查顯示,約25%的絕經后婦女都患有骨質疏松癥[8]。其臨床表現以腰膝酸軟、腰背疼痛為主,BMD的降低、骨質疏松的發生會增加患者的骨折風險。
人體內膠原蛋白三重螺旋分子結構隨著年齡增長遭到嚴重破壞而逐漸流失[9],鈣鹽無法有效沉積而造成骨礦物質流失增多,致使骨代謝異常[10]。鈣爾奇D所含鈣是骨礦化的底物,可及時補充機體對鈣劑的需求,提高了骨鈣內環境的穩定性,加快了骨的形成,緩解患者骨質疏松的癥狀,一定程度上降低了骨折的發生率,現已被臨床廣泛應用于治療骨折、佝僂病以及哺乳期、妊娠期婦女缺鈣等疾病[11]。筆者之前的研究結果表明去卵巢大鼠補充牛骨膠原肽能夠增加膠原合成,抑制膠原降解,并顯著增加BMD,改善骨微結構[12]。
骨痛是絕經后骨質疏松癥患者的主要癥狀之一,嚴重影響了患者的生活質量,迫使患者減少活動,進而加重骨質疏松[13]。本研究結果表明,試驗組與對照組患者治療后骨痛均有不同程度改善,且試驗組患者癥狀改善更為明顯,表明口服膠原肽能夠更有效地緩解骨質疏松導致的骨痛。
本研究檢測的血清總PINP、PTH、25(OH)D3、OC是骨形成標志物,β-CTX是骨吸收標志物[14]。P1NP和β-CTX對藥物治療的反應能作出快速預測,且具有個體內變異較小的優勢,被作為監測骨質疏松患者療效和依從性的首選。骨更新時Ⅰ型膠原降解,短肽片段進入血液,因此β-CTX為膠原降解標志物,是骨吸收和破骨細胞活性的標志。骨形成時,總PINP隨Ⅰ型膠原的合成而釋放入血,血清中的總 PINP的水平升高;而當成骨細胞合成減少時,血清總PINP水平下降,因此總PINP為膠原合成標志物,是成骨細胞活性的標志[13]。PTH對骨的形成具有雙向調節作用,持續性PTH刺激可引起重吸收增強;而小劑量、間歇性應用PTH則可促進骨形成[15]。VD可促進胃腸道對鈣的吸收,促進骨骼礦化,同時又可促進成骨細胞增生、分化,促進骨基質的形成、成熟與鈣化。VD 缺乏會導致骨質疏松,因此在骨質疏松癥患者中出現VD缺乏的概率更高[16]。OC由成骨細胞特異性合成、分泌的非膠原蛋白,是人體骨組織中的特異性蛋白,主要發揮調節、維持骨鈣的作用,通過檢測血液中OC的水平可直接反映出成骨細胞的活性[17]。本研究結果表明,治療6個月后,對照組血清PTH、25(OH)D3上升,表明鈣爾奇D通過提高血清PTH、25(OH)D3的表達水平而發揮其促骨活性,增加骨形成進而增加骨密度。此外,對照組血清總PINP顯著降低,而β-CTX顯著升高,表明鈣爾奇D的補充不能促進膠原的合成,反而促進了膠原的分解,該結果目前尚未有文獻報道,有待于進一步研究。試驗組患者血清總 PINP、PTH、25(OH)D3、OC水平明顯高于對照組,而β-CTX水平明顯低于對照組。表明膠原肽一方面能夠促進膠原的合成,體現出促成骨細胞的活性,與筆者以前的報道一致[4];另一方面能夠抑制膠原降解,體現出抑制破骨細胞的活性,在一定程度上改善了骨質疏松的癥狀。從骨代謝水平而言,試驗組療效顯著優于對照組。
雙能X線骨密度儀是臨床診斷骨質疏松癥的金標準,也是評估骨折風險的主要工具[18]。本研究采用雙能X線骨密度儀評價了絕經后骨質疏松患者腰椎部及髖部的骨密度。研究結果表明試驗組經過6個月的治療,能夠顯著增加絕經后骨質疏松患者各部位的BMD,與對照組相比,腰椎部L2、L4及髖部的股骨頸、粗隆間BMD療效明顯,進一步驗證了筆者之前的研究結果:去卵巢大鼠補充牛骨膠原肽能夠增加膠原合成,抑制膠原降解,并顯著增加BMD,改善骨的微結構[12]。絕經后骨質疏松癥患者血清骨形成指標表達水平顯著升高,表明膠原肽通過促進成骨細胞的活性而增加骨形成,進一步增加BMD。患者經6個月膠原肽治療后,骨痛癥狀改善明顯,并無明顯的不良反應,提示膠原肽有望在今后應用于絕經后骨質疏松癥患者治療,能夠降低骨折風險。
綜上所述,口服膠原肽聯合鈣爾奇D既能促進骨形成,又能抑制骨吸收,進一步增加BMD,并且可以緩解骨質疏松引起的疼痛,是一種切實可行的防治骨質疏松癥的臨床方案。

