水貂犬瘟熱活疫苗與水貂細小病毒性腸炎滅活疫苗制備及其聯合免疫效果研究
羅國良,王振軍,馮二凱,易立,郭利,程悅寧※,程世鵬,王守富,王宏正,張洪亮
(1.中國農業科學院特產研究所,長春 130112;2.吉林農業大學,長春 130118;3.長春西諾生物科技有限公司,長春 130012)
水貂犬瘟熱是引起水貂以雙相熱、白細胞減少、鼻炎和粘膜炎為特征的傳染病[1]。水貂病毒性腸炎是以出血和壞死、急劇下痢、白細胞高度減少為特征的急性病毒性傳染病[2]。2 種疾病均有較高的發病率和死亡率,是世界公認的危害水貂養殖業較嚴重的傳染病[3],一旦發生,損失巨大。疫苗免疫接種是目前預防這2種疾病的最主要的方法。目前,我國防治這2 種疾病的疫苗有水貂犬瘟熱活疫苗、水貂細小病毒性腸炎滅活疫苗以及水貂犬瘟熱、細小病毒性腸炎二聯活疫苗。聯苗具有“一針多防”、減少免疫次數、提高接種效率等優點,聯苗方式一般為活疫苗與活疫苗聯用或者為滅活疫苗與滅活疫苗聯用,而活疫苗與滅活疫苗聯用的情況在國內較少采用,在國外犬用多聯疫苗中較多采用滅活疫苗組分稀釋活疫苗組分的聯用方法,該方法有效地實現了聯苗中各組分的優勢組合。
本研究采用新型的制苗工藝,滅活疫苗采用新型滅活工藝,通過接種細胞和免疫動物實驗,評價2 種疫苗聯合免疫的效力,為進一步研制開發水貂犬瘟熱活疫苗與細小病毒性腸炎滅活疫苗二聯苗奠定基礎。
1 材料與方法
1.1 材料
1.1.1 病毒與細胞 水貂犬瘟熱CDV3-CL 株、水貂細小病毒MEVB株(中國農業科學院特產研究所特種動物病原與免疫團隊保存);F81 細胞、Vero細胞(中國科學院典型培養物保藏委員會細胞庫提供)。
1.1.2 主要試劑 MEM培養基、0.25%胰酶-EDTA消化液(Corning 公司);2-溴乙胺氫溴酸鹽(BEA)(Sigma-aldrich公司);甲醛(國藥集團);其它試劑為國產分析純。
1.1.3 實驗動物 水貂購自農業部長白山野生生物資源重點野外科學觀測試驗站,2~3月齡,雌、雄隨機,體況健康且未免疫水貂犬瘟熱疫苗和水貂細小病毒性腸炎疫苗,免疫前經采血檢測,犬瘟熱病毒中和抗體和水貂細小病毒HI 抗體均為陰性。
1.2 方法
1.2.1 水貂犬瘟熱活疫苗制備與檢驗 將CDV3-CL株用含MEM的細胞維持液作適當稀釋,按5%的比例接種于長成良好單層的Vero細胞轉瓶,37 ℃吸附1 h,加入含2%新生牛血清的細胞維持液,35 ℃旋轉培養,細胞病變(CPE)達到80%以上時收獲,20℃凍結,凍融后即為半成品。取樣檢驗無菌合格且病毒含量≥105.70TCID50/mL 的半成品作為制苗用病毒液。將檢驗合格的病毒液與明膠蔗糖凍干保護劑按適宜比例混合,同時用0.1 mol/L 的NaHCO3 調pH 值7.4,充分混合,定量分裝至100 mL玻璃凍干瓶內,凍干機凍干,凍干后軋蓋。按以上方法制備3 批疫苗,進行性狀、無菌檢驗、支原體檢驗、鑒別檢驗、外源病毒檢驗、真空度、水分測定以及效檢和安檢。
1.2.2 水貂細小病毒性腸炎滅活疫苗制備與檢驗 將MEVB 株按1%的比例接種于F81 細胞懸液轉瓶中。35 ℃旋轉培養,當細胞CPE達到80%以上時收獲,20℃凍結,凍融后即成半成品,取樣檢驗無菌合格且病毒含量≥106.00TCID50/mL的半成品作為制苗用病毒液。將病毒液用0.002 mol/L 二乙烯亞胺(BEI)滅活24 h,滅活后加入BEI 使用量的10%的1 mol/L 硫代硫酸鈉中和BEI。滅活檢驗合格后,按病毒液∶氫氧化鋁膠=9∶1 的比例制成水貂細小病毒滅活疫苗。按以上方法制備3批疫苗,進行性狀、裝量、無菌、效檢和安檢。
1.2.3 水貂犬瘟熱活疫苗與細小病毒性腸炎滅活疫苗聯合及聯合后犬瘟熱病毒含量的測定 在相同頭份數情況下,使用專用稀釋針頭將水貂細小病毒性腸炎滅活疫苗吸入犬瘟熱活疫苗凍干瓶內,將該狀態下產品組合稱之為水貂犬瘟熱、腸炎聯合疫苗(以下簡稱聯合疫苗)。
將聯合疫苗與同批次專用稀釋液稀釋的對照疫苗,分別置25 ℃條件下5 h,每小時取樣1 次,將樣品10 倍系列稀釋,接種長成單層的Vero 細胞培養板,測定兩種疫苗中犬瘟熱病毒含量。
1.2.4 聯合疫苗免疫試驗 犬瘟熱病毒中和抗體和細小病毒HI抗體均為陰性的水貂30 只,分為3 組,每組10 只。聯合疫苗組免疫聯合疫苗,每只水貂免疫各1頭份,犬瘟單苗組免疫水貂犬瘟熱活疫苗,每只水貂免疫1 頭份,腸炎單苗組免疫水貂細小病毒性腸炎滅活疫苗,每只水貂免疫1 頭份。免疫后21 d,采血分離血清,聯合疫苗組測定犬瘟熱病毒中和抗體和細小病毒HI 抗體,犬瘟疫苗組測定犬瘟熱病毒中和抗體,腸炎苗組測定水貂細小病毒HI 抗體。
2 結果
2.1 水貂犬瘟熱活疫苗制備與檢驗結果
3 批水貂犬瘟熱活疫苗半成品均合格,病毒含量均在105.70TCID50/mL 標準之上,且無明顯的批間差異。成品進行性狀檢驗、無菌檢驗、支原體檢驗、外源病毒檢驗、鑒別檢驗、剩余水分和真空度測定結果均符合現行《中國獸藥典》規定。3 批成品對水貂安全,病毒含量為104.50~104.70TCID50/mL,均符合產品質量標準(≥103.50TCID50/mL)。見表1、表2。
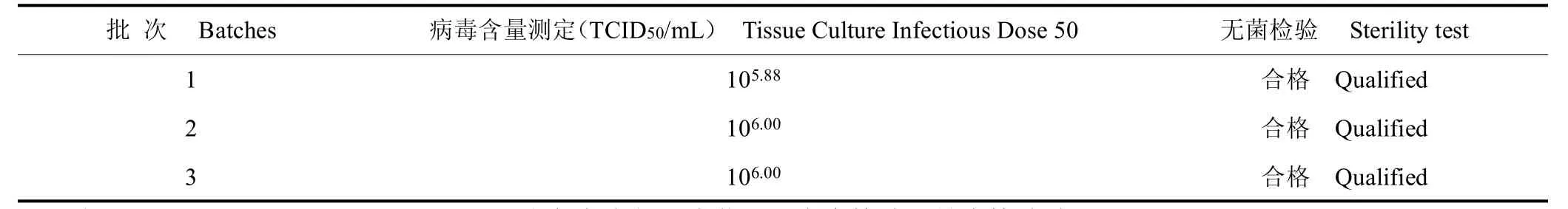
表1 水貂犬瘟熱活疫苗半成品檢驗結果Table 1 Results of semi-finished product test of mink distemper vaccine,live
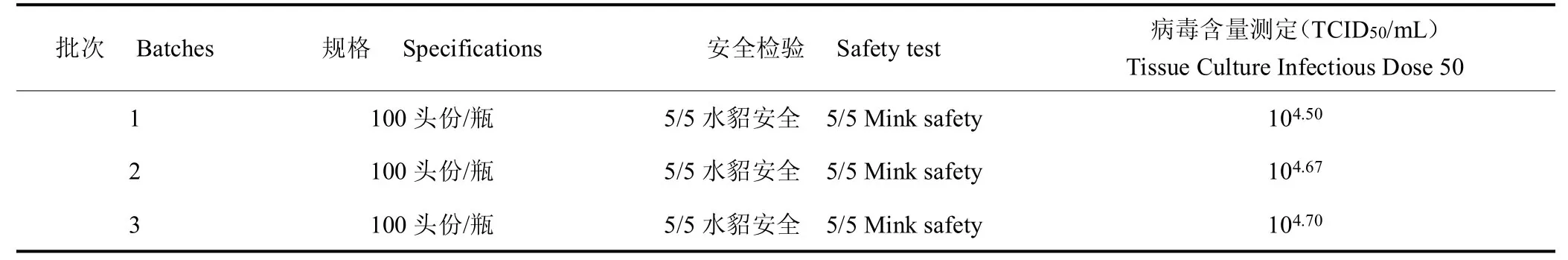
表2 水貂犬瘟熱活疫苗成品安全檢驗和效力檢驗結果Table 2 Safety test and efficacy test results of mink distemper vaccine,live
2.2 水貂細小病毒性腸炎滅活疫苗制備與檢驗結果
3 批水貂細小病毒性腸炎滅活疫苗半成品無菌檢驗與滅活檢驗均合格,病毒含量為106.67~106.80TCID50/mL,均符合質量標準(≥106.00TCID50/mL)。
成品進行檢驗,性狀、裝量、無菌檢驗結果均符合要求,對水貂安全,HI 抗體效價為1∶128~1∶1 024,均符合質量標準(≥1∶32)。見表3、表4。

表3 水貂細小病毒性腸炎滅活疫苗半成品檢驗結果Table 3 Results of semi-finished product test of mink parvovirus enteritis inactivated vaccine
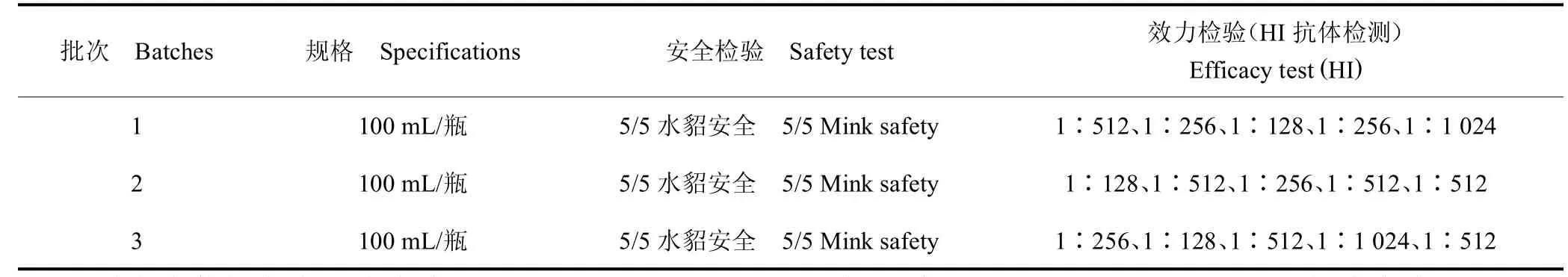
表4 水貂細小病毒性腸炎滅活疫苗成品安全檢驗和效力檢驗結果Table 4 Safety and efficacy test results of mink parvovirus enteritis inactivated vaccine
2.3 聯合疫苗的犬瘟熱病毒含量測定
將聯合疫苗組、犬瘟單苗組樣品25 ℃條件下不同時間取樣,測定的犬瘟熱病毒含量0~5 h 而略有下降(均下降100.30),但相同時間下兩者的病毒含量無明顯差異。見表5。

表5 水貂犬瘟熱活疫苗與細小病毒性腸炎滅活疫苗聯合后病毒含量結果Table 5 The TCID50 result of mink distemper vaccine live combined with parvovirus enteritis inactivated vaccine
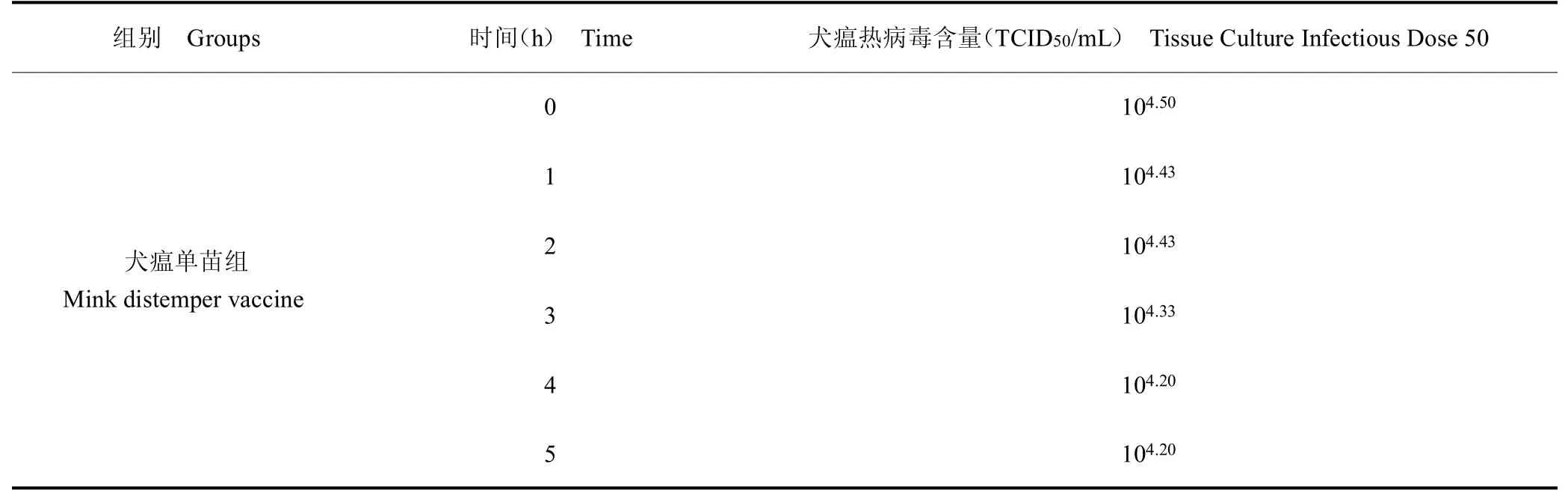
續表5
2.4 聯合疫苗動物免疫試驗
聯合疫苗組樣品產生的犬瘟熱中和抗體與犬瘟單苗組相比,兩者無明顯差異;聯合疫苗組產生的水貂細小病毒HI 抗體與腸炎單苗組相比,兩者亦無明顯差異。
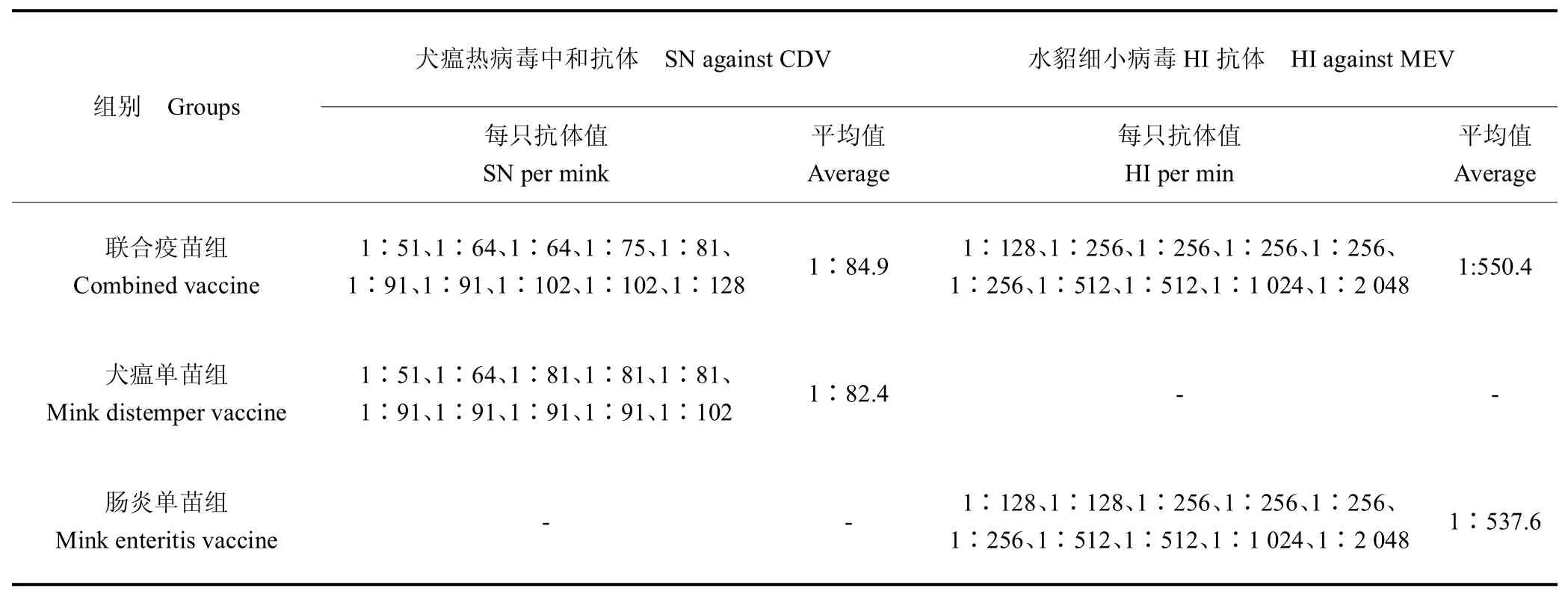
表6 聯合疫苗免疫抗體結果
3 結論與分析
目前,采用滅活疫苗稀釋活疫苗實現聯苗的方式在國外犬用苗上較常用,如法國梅理亞生產的犬瘟熱、腺病毒病、細小病毒病、副流感病毒2 型呼吸道感染癥4 聯活疫苗-犬鉤端螺旋體病、黃疸鉤端螺旋體病2 價滅活疫苗;碩騰公司的犬瘟熱、腺病毒2 型、副流感、細小病毒四聯活疫苗-犬鉤端螺旋體病(犬型、黃疸出血型)2 價滅活疫苗-犬冠狀病毒病滅活疫苗。能夠實現滅活疫苗與活疫苗聯用的前提條件是滅活疫苗與活疫苗聯合后對活疫苗中的病毒無滅活作用,兩者一起免疫后不降低各自的免疫效果。
本研究中,在水貂細小病毒性腸炎滅活疫苗的制苗過程中,為了降低滅活劑的殘留,優化了水貂細小病毒性腸炎的滅活工藝,采用BEI進行滅活,殘留的BEI采用硫代硫酸鈉進行中和,經檢驗水貂細小病毒滅活完全。半成品和成品的各項檢驗指標均符合要求,成品效力檢測抗體水平無明顯差異,生產工藝穩定。
犬瘟熱半成品、成品的檢測指標亦表明,采用100mL 玻璃凍干瓶凍干的犬瘟熱活疫苗的生產工藝穩定,成品病毒含量無明顯差異(104.50~104.70TCID50/mL);滅活疫苗組分對犬瘟熱病毒無明顯影響;犬瘟熱病毒、細小病毒抗體水平與單苗相比均無明顯影響。

