兩種不同胚胎移植策略對新鮮周期體外受精臨床結局的影響
陶林林,李國臻,楊志偉,段新崇,耿亞松,鄭波
(邢臺不孕不育專科醫院/邢臺生殖與遺傳專科醫院,邢臺 054000)
在體外受精-胚胎移植(IVF-ET)中,隨著促排卵技術及實驗室培養環境的改善,獲得胚胎的數量和質量都有了一定的提高,大多數周期能夠獲得可用胚胎進行移植,但部分周期移植后種植率較低[1],影響IVF的成功率[2]。在可用胚胎數目有限的情況下,如何選擇發育潛能更高的胚胎進行移植,即選擇怎樣的胚胎移植策略是目前生殖領域醫生共同關注的問題。大部分生殖中心在取卵后第3天(D3)卵裂胚階段或D5囊胚階段進行胚胎移植,有的生殖中心會為反復種植失敗的患者進行D2/D3或D3/D5的序貫移植[3]。D3移植和D5移植各有優勢和弊端,而D4移植鮮有報道,本研究回顧性分析了兩種不同的移植策略的妊娠結局,一種是僅進行D3移植;另一種是為了避免因得不到囊胚而取消移植,根據患者D3胚胎質量進行D3D4D5移植。探討不同移植策略對IVF-ET臨床結局的影響,為IVF助孕治療中移植胚胎的選擇提供參考。
資料與方法
一、研究對象與分組
回顧性分析本院生殖中心2017年1月至2018年5月行新鮮周期IVF/ICSI-ET患者的臨床資料,共1 048個周期。納入標準:(1)血清基礎FSH<10 U/L;(2)所有患者均采用黃體期長方案降調節,達到降調標準后,進行控制性促排卵;(3)均為第1次促排卵周期。排除標準:(1)卵巢功能減退、卵巢早衰;(2)HCG日E2≥29 280 pmol/L或P≥5.706 nmol/L;(3)合并遺傳性疾病者。
根據不同的移植策略分成兩組,A組(693個周期):D3移植組,新鮮移植周期全部行D3胚胎移植,剩余胚胎全部繼續培養囊胚。B組(355個周期):根據胚胎質量行D3、D4或D5移植,即D3D4D5胚胎移植組。D3可用胚胎數≤2枚,則D3移植;D3可用胚胎數≥3枚,則D4擇優移植2枚;若D3優質胚胎≥4枚,則全部胚胎培養囊胚行D5移植。再根據年齡的不同將A、B組各分為3個不同亞組,A1組(≤30歲,371個周期):D3移植組;B1組(≤30歲,207個周期):D3D4D5胚胎移植組;A2組(30歲<年齡≤35歲,187個周期):D3移植組;B2組(30歲<年齡≤35歲,108個周期):D3D4D5胚胎移植組;A3組(>35歲,135個周期):D3移植組;B3組(>35歲,40個周期):D3D4D5胚胎移植組。分別比較不同年齡段兩種移植策略對妊娠結局的影響。
二、研究方法
1.卵母細胞獲取及培養:所有患者采用常規長方案促排卵,B超監測卵泡發育情況,卵泡成熟時,注射HCG(珠海麗珠制藥)5 000~10 000 U,36.5 h經陰道超聲引導下穿刺取卵。卵丘復合物取出充分洗滌后置三氣培養箱(37℃、6%CO2、5%O2)中培養,取卵當日行常規IVF或ICSI授精。次日評估卵母細胞受精情況,并記錄原核(PN)數目:2PN為正常受精;受精后D2和D3評估卵裂期胚胎質量。
2.本中心可用優質胚胎評估標準:根據卵裂球數目、形態、碎片情況對卵裂期胚胎進行評分:1級:卵裂球大小均勻,形態規則,胞質均勻清晰,無碎片或碎片<10%;2級:卵裂球大小均勻或略不均勻,形態欠規則,無碎片或碎片10%~20%;3級:卵裂球大小不均,形態欠規則,碎片20%~50%;4級:卵裂球大小嚴重不均,碎片>50%。
D3可用胚胎標準:細胞數≥6個,評分為1級、2級和3級。D3優質胚胎標準[4]:D1為正常受精(2PN),6個≤細胞數≤10個,評分為1級和2級。
D4可用胚胎標準:胚胎開始出現部分融合。D4優質胚胎標準:胚胎已經完全融合或者開始出現囊胚腔。
可用囊胚標準:囊胚至少發育到囊胚腔完全擴張充滿整個胚胎;內細胞團細胞數目多而均勻,連接緊密或細胞數目相對較少或連接分散;滋養層細胞數目少或僅有少量大細胞即可。優質囊胚標準[4]:D1為2PN,囊胚腔及內細胞團達到可用囊胚標準,滋養層細胞數目多,大小均勻,呈鐮形,或細胞數目較多,但有大細胞或不均勻。
3.黃體支持方案:取卵后給予黃體酮(浙江仙琚制藥,20 mg/ml)80 mg,每天肌肉注射,行黃體支持。根據不同的移植策略于取卵術后D3、D4、D5移植,移植日視HCG日E2水平給予戊酸雌二醇(補佳樂,拜耳醫藥,德國)2~6 mg口服。
4.胚胎移植:用棉簽蘸取培養液清洗宮頸表面,若宮頸分泌物過多,則用卵圓鉗去除。按照常規操作進行胚胎移植:通過移植外管將含有胚胎的軟內管置入距宮底約1.0 cm處,緩慢推注留管30 s后輕輕取出,確認無胚胎殘留。胚胎移植后常規給予黃體支持。移植后14 d測血β-HCG水平,陽性者于第28日行陰道B超檢查,見到妊娠囊者確定為臨床妊娠。
5.觀察指標:治療周期移植率=移植周期數/取卵周期數×100%;種植率=B超下見到孕囊數/移植胚胎數×100%;妊娠率=妊娠患者數/移植患者數×100%;流產率=流產患者數/妊娠患者數×100%。
三、統計學分析
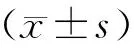
結 果
一、患者基本情況分析
≤30歲和30~35歲兩個亞組患者的年齡、不孕年限、基礎激素值、HCG日激素值、體重指數(BMI)、胚胎移植數量以及子宮內膜厚度和治療周期移植率等比較均無顯著性差異(P>0.05);>35歲中A3組的移植胚胎數顯著高于B3組(P<0.05),詳見表1。

表1 三個亞組患者的基本資料比較[(-±s),%]
注:與A3組比較,*P<0.05
二、不同亞組的妊娠結局比較
各個不同亞組的2PN受精率、2PN卵裂率、可用胚胎率及優胚率比較均無顯著性差異(P>0.05)。≤30歲年齡段中B1組的臨床妊娠率顯著高于A1組(P<0.05);兩組的種植率比較雖沒有顯著性差異(P>0.05),但B1組有高于A1組的趨勢;兩組的流產率比較無顯著性差異(P>0.05)。30歲<年齡≤35歲中兩亞組和>35歲兩亞組的臨床妊娠率、種植率和流產率比較均無顯著性差異(P>0.05),詳見表2。
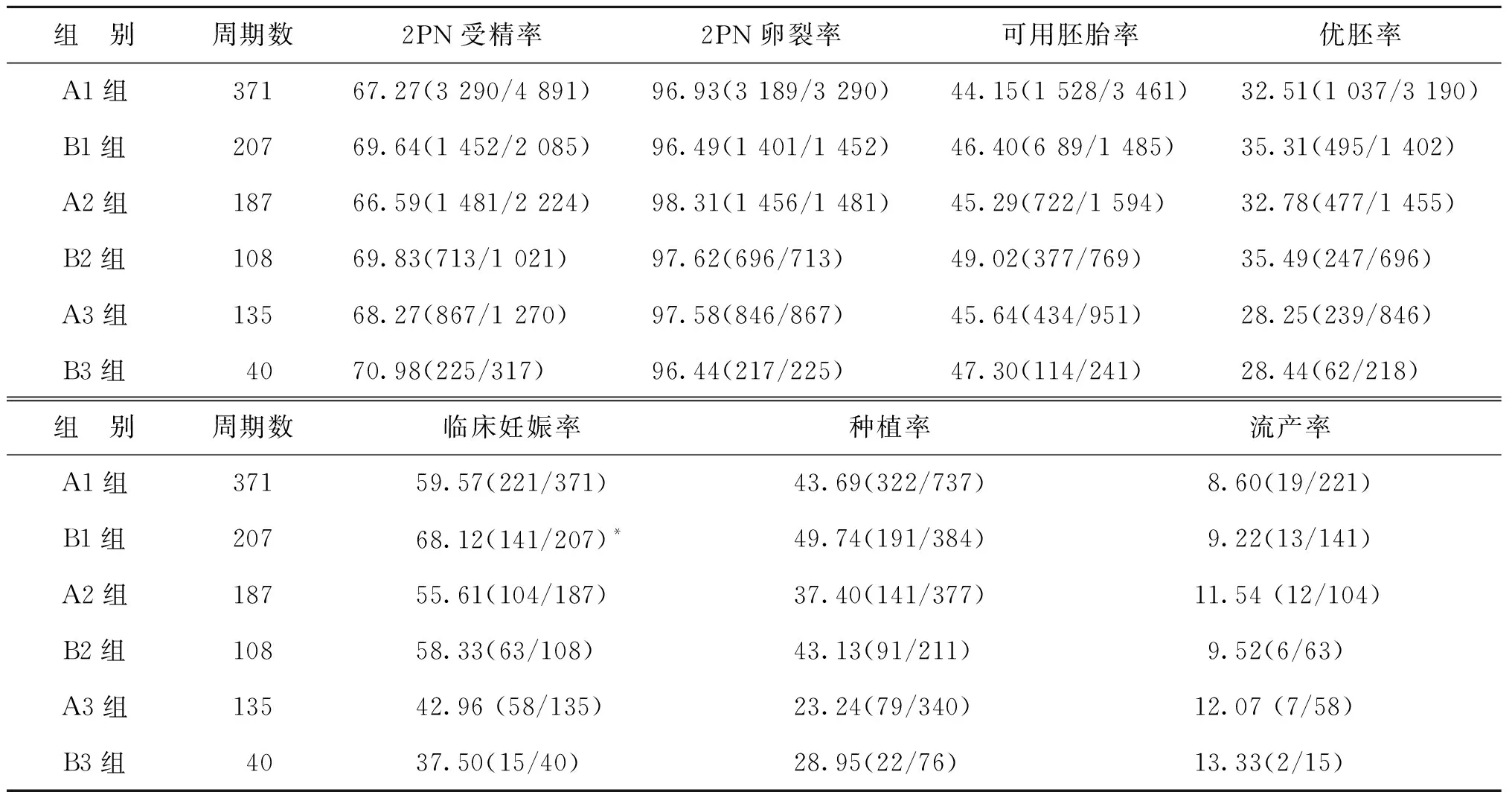
表2 各不同亞組妊娠結局比較 (%)
注:與A1組比較,*P<0.05
討 論
目前大多數的D3胚胎移植是根據形態學評分來挑選胚胎的,但大量研究表明形態學很難準確地評估胚胎發育潛能以選擇出較高發育潛能的胚胎進行移植[5]。在人類胚胎發育的早期階段,胚胎發育由儲存在卵母細胞內的母源基因所調控,當胚胎發育至D3(4~8細胞)階段時,胚胎基因組開始被激活,開始調控胚胎的繼續發育[6],發生致密化并形成囊胚。如果胚胎基因組無法正常激活或胚胎具有遺傳學異常,則胚胎會發生發育停滯、無法形成囊胚或凋亡。因此,在胚胎選擇中,具有激活胚胎基因組的桑椹胚與囊胚比卵裂階段胚胎具有更好的選擇價值,體外培養時間延長有助于判斷胚胎的質量[7],可以淘汰部分有遺傳缺陷及發育潛能差的卵裂期胚胎[8]。輔助生殖技術模擬體內胚胎發育的微環境,但與體內環境必然存在一定的差異,早期胚胎對于培養環境特別敏感,延長體外培養的過程中,實驗室的微環境如PH值、滲透壓、溫度等發生細微改變均可能影響胚胎質量,增加移植周期取消的風險[9]。什么時候是最合適的移植時間,目前尚沒有明確的定論。
大量研究證明與卵裂胚相比,囊胚移植能夠獲得較高的臨床妊娠率和活產率,所需移植數目較少,且能降低多胎妊娠率[10-11]。近年來,生殖領域專家們越來越傾向于囊胚移植。Kang等[12]報告,胚胎在哺乳動物受精后的3~4 d內移動到子宮腔,與卵裂期胚胎移植相比,D4桑葚胚/致密胚移植和囊胚移植與體內生殖過程更為同步。Li等[13]報道D4胚胎移植組的足月出生率顯著高于D5胚胎移植組,兩組的臨床妊娠率、持續妊娠率、流產率和活產率均無顯著差異,表明D4胚胎移植成功率與囊胚D5移植相似。有回顧性研究結果顯示,D4移植與D3移植相比能顯著提高胚胎種植率(46.4% vs. 21.4%,P<0.01),且D4移植胚胎數顯著低于D3移植胚胎數[14]。以上研究表明桑椹胚與囊胚具有相似的優勢,因為它們具有激活的胚胎基因組,且與D2、D3的卵裂期胚胎相比,它們與子宮內膜環境有更好的同步性[15]。但不是所有的患者都適合囊胚移植及D4移植,與D3移植相比,囊胚移植和D4移植會增加周期取消的風險,囊胚及D4胚胎培養能夠選擇出具有較高質量和發育潛能的胚胎,但有胚胎發育停滯及凋亡的風險,給患者帶來精神打擊和經濟負擔,不適合獲卵數較少及胚胎質量較差的患者,囊胚及D4胚胎培養的前提是要有一定數量的優質胚胎[16]。D4移植與D5移植相比,周期取消的風險要低一些,有研究表明59.2%的D3優質胚胎能夠發育成D4優質胚胎,47%的D3優質胚胎在D5發育成囊胚[12],在D3優質胚胎不夠多,沒有把握培養成囊胚而又有多于移植數目的胚胎的情況下,為了篩選發育潛能高的胚胎進行移植同時避免因得不到囊胚而取消移植,而進行D4移植;在優質胚胎足夠多的情況下可以繼續培養成囊胚后進行移植。Jones等[17]研究表明,囊胚形成數量與D3 8-細胞胚胎數量有關,D3 8-細胞胚胎≥3個時可避免因無囊胚形成而取消移植的風險。本研究中B組移植策略與其相似,D3可用胚胎數≤2枚,則D3移植;D3可用胚胎數≥3枚,則D4擇優移植2枚;若D3優質胚胎≥4枚,則全部胚胎培養至囊胚,D5移植。由于B組研究策略較靈活,根據D3胚胎質量行D3、D4或D5移植,對于優質胚胎較少可能養不成囊胚的情況則進行D3或D4移植,因此目前尚沒有因未形成囊胚而取消移植的周期;各亞組治療周期的移植率沒有顯著差異,提示D3/D4/D5移植策略并未增加取消移植周期,當然也可能是研究周期數較少的緣故。對于有多個優質囊胚的周期,本研究并沒有減少移植數目,少數周期只形成1枚囊胚則行單囊胚移植,本中心尚沒有全面開展單囊胚移植。
在本研究中,各個亞組的2PN受精率、2PN卵裂率、可用胚胎率和優胚率比較均沒有顯著性差異,提示繼續培養至D4、D5移植并沒有降低優質胚胎數量。≤30歲組行D3D4D5移植策略(B1組)比D3移植策略(A1組)臨床妊娠率有顯著提高(P<0.05),而31歲<年齡≤35歲和>35歲組中均沒有顯著性差異(P>0.05);各組的種植率D3D4D5移植策略比D3移植策略從數值上有增高趨勢,但亞組間的臨床妊娠率和種植率仍沒有顯著性差異(P>0.05),從另一個角度提示D3D4D5移植策略比單純D3移植可能有一定的優勢。這與其他研究者結果[18-19]相似,Blake等[18]的薈萃分析表明對年輕、預后較好的患者行囊胚移植能夠顯著改善妊娠結局。年齡是影響卵母細胞質量及妊娠結局的重要因素,也是卵巢反應性的獨立預測因子[20]。本研究數據表明不管是A組還是B組,隨著年齡增加,妊娠率呈降低的趨勢。年輕人群卵母細胞質量和胚胎發育潛能較高,繼續培養選擇胚胎的意義更大一些,因此,對于年齡≤30歲的年輕患者可根據D3胚胎質量靈活選擇移植天數,胚胎質量及數量較高時繼續培養篩選發育潛能較高的胚胎進行移植。≥35歲女性卵母細胞及胚胎非整倍體率增高,優質胚胎較少,妊娠率較低。朱靜等[21]研究表明對于≥35歲、卵巢功能較差的患者卵裂期胚胎在移植胚胎數、胚胎種植率及妊娠率等方面均高于囊胚期胚胎,本研究對>35歲患者卵裂期胚胎繼續培養后妊娠結局與D3移植沒有顯著差異,因此對>35歲患者仍建議卵裂期胚胎移植,但需要大樣本量進一步研究驗證。
綜上所述,對于年齡≤30歲的年輕且有足夠多胚胎的患者,可根據D3胚胎質量靈活選擇移植天數,其與單純D3胚胎移植相比能夠顯著改善臨床妊娠結局,且并不增加周期移植取消率。但對于30歲以上患者,該移植策略的優勢并不明顯。

