6 種中藥注射液聯合SOX 化療方案治療胃癌的網狀Meta 分析
吉躍進, 李紅曉, 陸為民?
(1. 南京中醫藥大學附屬醫院, 江蘇 南京210029; 2. 南京中醫藥大學醫學與生命科學學院, 江蘇 南京210023)
胃癌是世界上常見的惡性腫瘤之一, 為導致癌癥相關性死亡的重要因素。 就全球而言, 男性發病率通常是女性的2 倍, 而且各國差異很大[1], 2012年全球發病數為95.1 萬例(占總數的6.8%), 其中半數發生在東亞(主要在中國)[2]; 2015 年, 肺癌、 胃癌、 肝癌、 食管癌、 結直腸癌占中國所有癌癥相關性死亡的75%[3]。
替吉奧作為一種新型氟尿嘧啶衍生物口服抗癌劑, 于1999 年在日本被批準用來治療晚期胃癌,并于2009 年在中國上市, 因其能維持較高血藥濃度、 增強抗癌活性、 減少藥物毒性、 給藥便捷等優點被廣泛應用于臨床。 替吉奧聯合奧沙利鉑(SOX) 方案是目前晚期胃癌最常用的化療方案之一[4], 武惠麗等[5]研究表明, SOX 化療方案的療效略優于奧沙利鉑聯合氟尿嘧啶(FOLFOX)、 奧沙利鉑聯合卡培他濱(XELOX) 方案, 而且不良反應相對較低; 黃客增等[6]報道, 與表柔比星聯合順鉑及氟尿嘧啶(ECF) 方案相比, SOX 化療方案對胃癌根治術患者的化療效果更佳, 隨著該方案廣泛使用, 其優越性逐漸體現出來, 但不良反應依然不可忽視。
目前, 中藥注射液聯合化療治療胃癌已得到國內外廣泛關注, 在改善臨床癥狀、 提高生存質量、減輕放化療毒副作用、 延長生存期等方面具有明顯優勢, 楊旭平等[7-10]指出它在提高臨床療效及安全性方面的作用值得肯定。 本研究引入網狀Meta 分析, 在SOX 化療方案基礎上同時比較3 種或3 種以上中藥注射液輔助治療胃癌的臨床療效及安全性, 遴選出最優治療方案, 為相關臨床決策提供參考。
1 材料
1.1 研究類型 國內外公開發表的隨機對照試驗,無論是否采用盲法。
1.2 研究對象 符合經胃鏡聯合病理活檢確診的胃癌患者, 年齡、 性別不限。
1.3 干預措施 對照組均采用SOX 化療方案, 治療組在對照組基礎上加用中藥注射液。
1.4 結局指標 ①療效評價[11]: 采用WHO 實體瘤評價標準或RECIST 1.0 標準納入的研究, 包括完全緩解、 部分緩解、 疾病穩定、 疾病進展4 個等級, 有效率= [(完全緩解數+部分緩解數) /總例數] ×100%; ②生活質量指數[12]: 參照KPS 評分標準, 較治療前增加≥10 分為提高, 增加或減少<10 分為穩定, 降低≥10 分為降低, 改善率=提高例數/總例數×100%; ③安全性評價: 按照WHO化療藥物毒性反應分度標準Ⅰ~Ⅳ級的不良反應發生率, 主要包括白細胞減少、 惡心嘔吐、 肝損傷及周圍神經毒性等四個方面; ④無進展生存期(PFS): 腫瘤患者接受治療至疾病進展或死亡時的時間; ⑤中位生存期(MST): 當累積生存率為0.5 時所對應的生存時間[13]。
1.5 排除標準 ①非隨機對照試驗或半隨機對照試驗, 如綜述、 系統評價、 病例報道、 疾病證型限定、 按入院順序隨機等; ②非臨床試驗, 如動物、細胞實驗等; ③中藥注射液非靜脈使用, 如灌腸、腹腔灌注、 穴位注射等; ④中藥注射液劑型不符,如片劑、 膠囊等; ⑤無本研究結局指標或無法提取有效數據; ⑥研究對象合并其他腫瘤者, 如食管癌、 結直腸癌等; ⑦其他干擾治療者, 如放療、 中藥煎劑口服等; ⑧重復文獻, 選取時間較早的1 篇。
2 方法
2.1 檢索策略 檢索Pubmed、 Embase、 The Cochrane Library、 Wed of science、 中國知網、 萬方數據庫、 維普、 中國生物醫學文獻數據庫, 檢索策略以“中藥注射液及其相關自由詞+胃癌及自由詞+替吉奧及自由詞” 的方式進行構建, 檢索時間為建庫至2018 年3 月31 日。
2.2 文獻篩選及資料提取 由2 名研究人員根據納入、 排除標準分別獨立進行文獻篩選, 并交叉核對, 如有分歧, 則加入第3 名研究人員討論解決。文獻篩選完成后, 根據作者、 發表時間、 分配方法、 腫瘤分期、 病例數、 干預措施、 周期、 結局指標等方面將數據分別提取。
2.3 質量評價 采用Cochrane 推薦的“偏倚風險評估工具” 進行質量評價, 主要項目有7 個, 包括隨機序列產生、 分配方案隱藏、 對研究參與者采用盲法、 結局指標的盲法評價、 結果數據的完整性、 選擇性報告、 其他偏倚。
2.4 統計學分析 首先, 通過Stata14.0 軟件進行異質性檢驗及生存數據的Meta 分析, 若P>0.1 且I2≤50%, 表明各研究間具有同質性或異質性較小, 采用固定效應模型, 并在一致性模型下進行網狀Meta 分析; 若P<0.1 或I2>50%, 表明各研究間異質性較大, 查找分析其來源, 采用隨機效應模型, 并在不一致性模型下進行網狀Meta 分析。 然后, 通過ADDIS 1.16.8 軟件進行網狀Meta 分析[14], 以P<0.05 和95%CI (不包括1) 作為有統計學差異的標準; 計數資料應用比值比OR 及其95%CI 表示效應量, 并繪制各干預措施的網狀關系圖和排序圖。 有效率、 生活質量改善率、 無進展生存期、 中位生存期歸為有益結局, 概率排序在Rank 1 最好, Rank N 最差; 白細胞減少、 惡心嘔吐、 肝損傷、 周圍神經毒性歸為不利結局, 概率排序Rank N 最好, Rank 1 最差。 ADDIS 軟件主要采用潛在的標尺縮減參數(PSRF) 來評價結果收斂性, 當PRSF 接近或等于1 時, 表明結果有很好的收斂效能, 分析可信度高。
3 結果
3.1 文獻檢索 初檢得到文獻369 篇, 其中CNKI 57 篇、 VIP 63 篇、 萬 方117 篇、 CBM 46 篇、PubMed 25 篇、 Embase 42 篇、 Web of science 9 篇、Cochrane Library 10 篇、 手工檢索0 篇, 經NoteExpress 文獻管理軟件剔除重復文獻137 篇, 閱讀題目和綜述后排除文獻159 篇, 初步納入30 篇, 再通過閱讀全文剔除不適合文獻, 最終納入22 篇,均為公開發表。 流程見圖1。

圖1 文獻檢索與篩選流程Fig.1 Literature retrieval and screening process
3.2 基本特征 共納入22 項隨機對照試驗, 包含6 種中藥注射液, 分別為艾迪注射液(6 篇)、 參芪扶正注射液(6 篇)、 消癌平注射液(4 篇)、 康艾注射液(3 篇)、 康萊特注射液(2 篇)、 復方苦參注射液(1 篇); 共納入病例數1 419 例, 其中治療組722 例, 對照組697 例; 所有納入文獻中治療組均為中藥注射液+SOX 化療方案, 對照組均為單用SOX 化療方案; 20 項研究以有效率為結局指標, 9 項研究報道了KPS 評分, 14 項研究報道了白細胞減少, 12 項研究報道了惡心嘔吐, 9 項研究報道了肝損害, 15 項研究報道了周圍神經毒性, 5項研究報道了PFS, 7 項研究報道了MST。 見表1。
3.3 質量評價 所有研究均提出隨機分配, 但均未實施盲法, 其中9 項為隨機數表法, 1 項[26]為信封法隨機, 僅有2 項[26,28]對隨機方法進行具體描述; 10 項描述隨訪情況; 2 項[19,22]未對主要結局指標有效率進行報道。 然后, 根據Cochrane 推薦的“偏倚風險評估工具” 對納入研究進行質量評價, 結果見圖2。
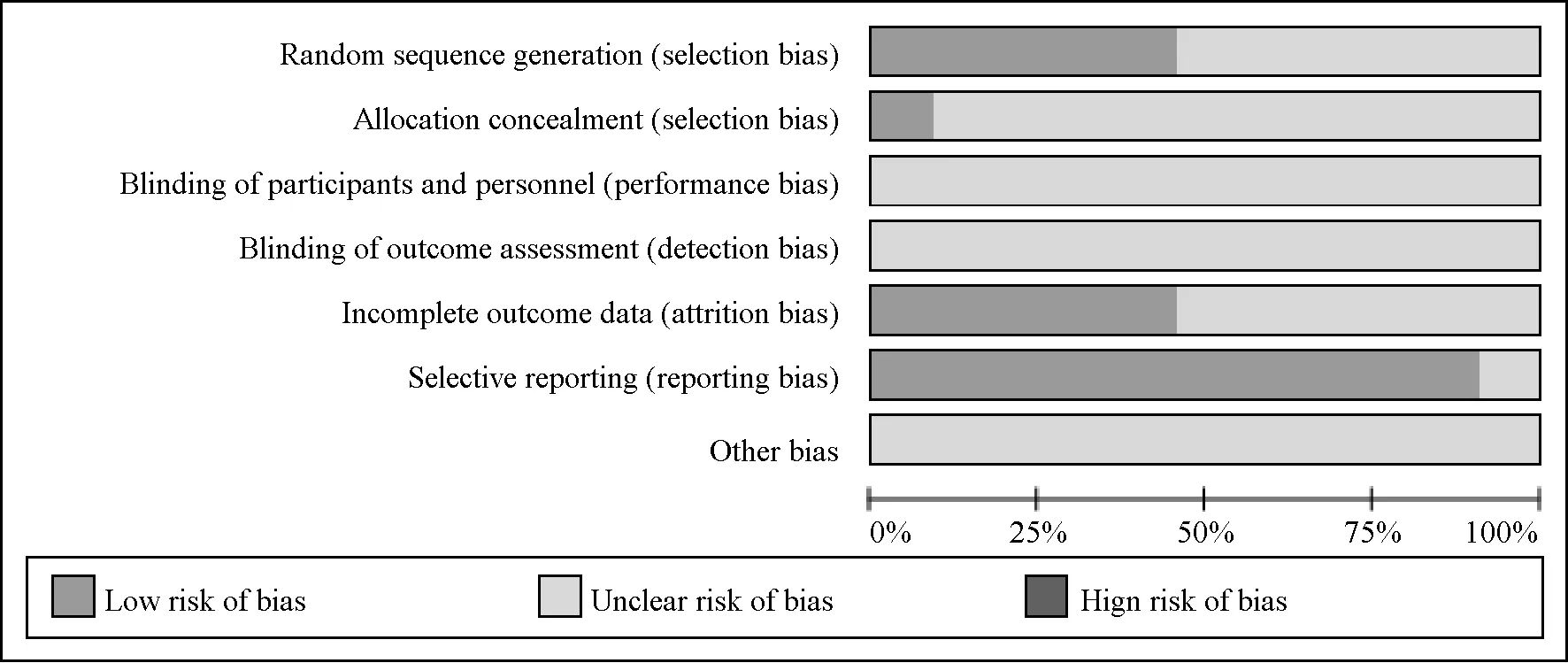
圖2 納入研究質量評價Fig.2 Quality evaluation of included studies
3.4 網狀Meta 分析 所有研究均為中藥注射液聯合SOX 化療方案與單用SOX 化療方案的直接比較, 并均為雙臂(總臂數為44), 干預措施關系見圖3。 各研究結局指標PSRF 均<1.02, 表明收斂性良好, 分析可信度高。
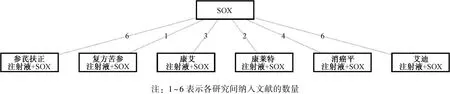
圖3 納入研究干預措施關系Fig.3 Relationships of intervention measures in included studies
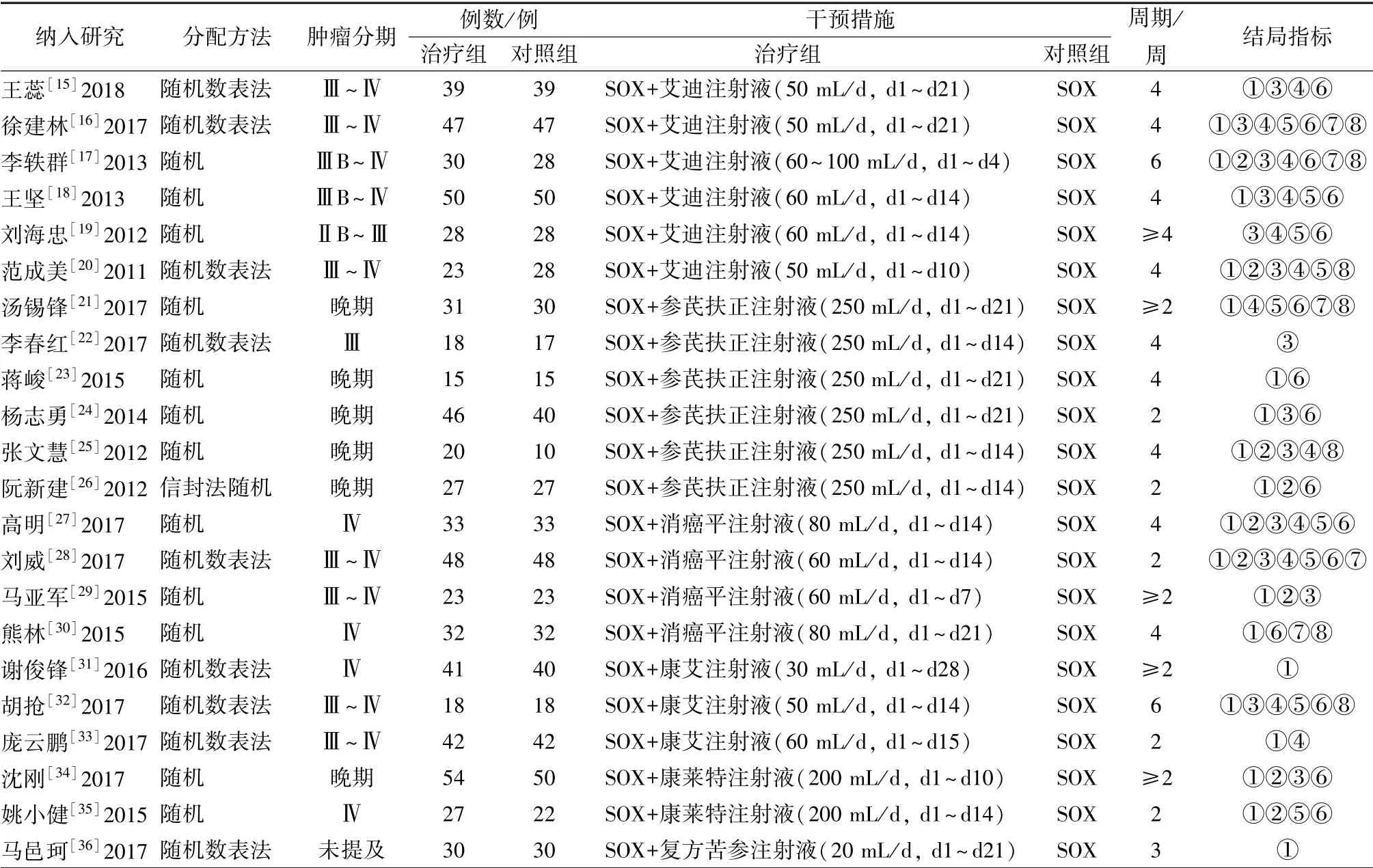
表1 納入研究基本特征Tab.1 Basic characteristics of included studies
3.4.1 有效率 20 項研究報道了有效率, 包括艾迪注射液、 參芪扶正注射液、 復方苦參注射液、 康艾注射液、 康萊特注射液、 消癌平注射液。 異質性檢驗(表2) 顯示, 中藥注射液聯合SOX 化療方案較單用SOX 化療方案的組內研究間異質性較小,故采用一致性模型進行網狀Meta 分析(表3)。結果顯示, 與單用SOX 化療方案比較, 艾迪注射液+SOX、 參芪扶正注射液+SOX、 康艾注射液+SOX、復方苦參注射液+SOX 差異有統計學意義, 其余無統計學意義, 并且6 種聯合用藥兩兩比較差異也無統計學意義。 Rank 1 ~7 概率排序顯示, 復方苦參注射液+SOX(50%) >康艾注射液+SOX (35%) >參芪扶正注射液+SOX (27%) >艾迪注射液+SOX(27%) >消癌平注射液+SOX (26%) >康萊特注射液+SOX (20%) >SOX (88%)。
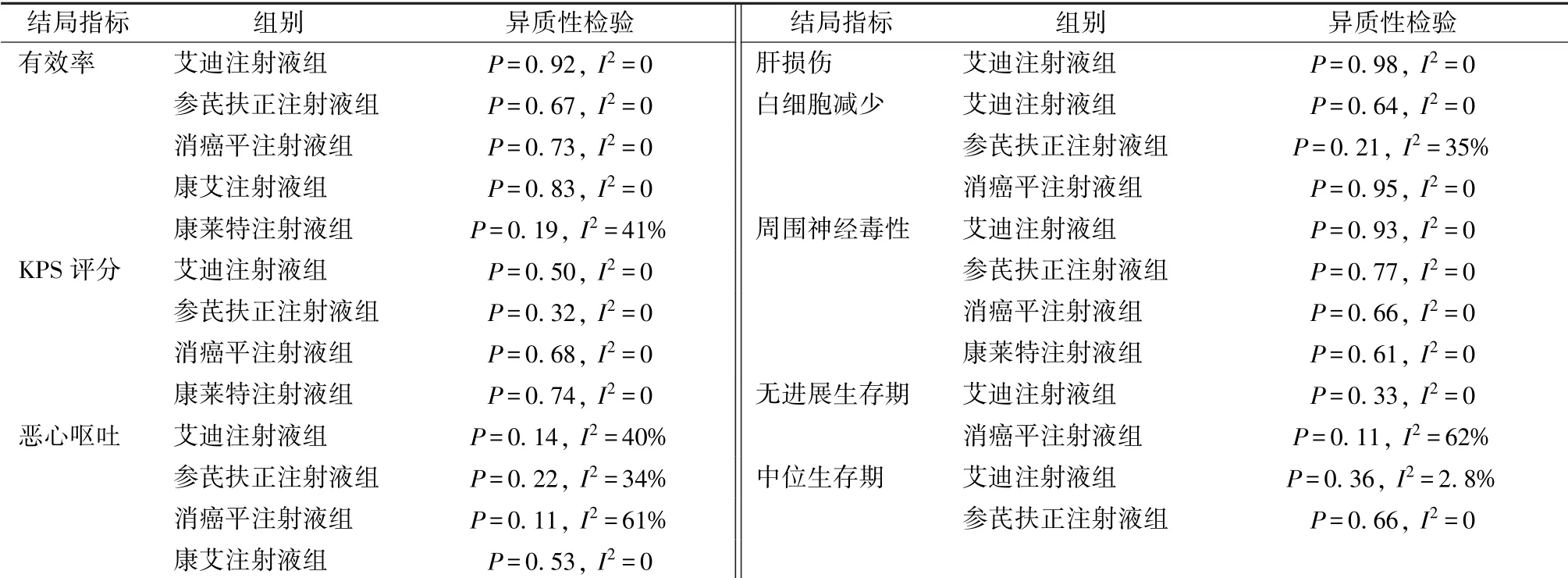
表2 納入研究異質性檢驗結果Tab.2 Results of heterogeneity tests for included studies
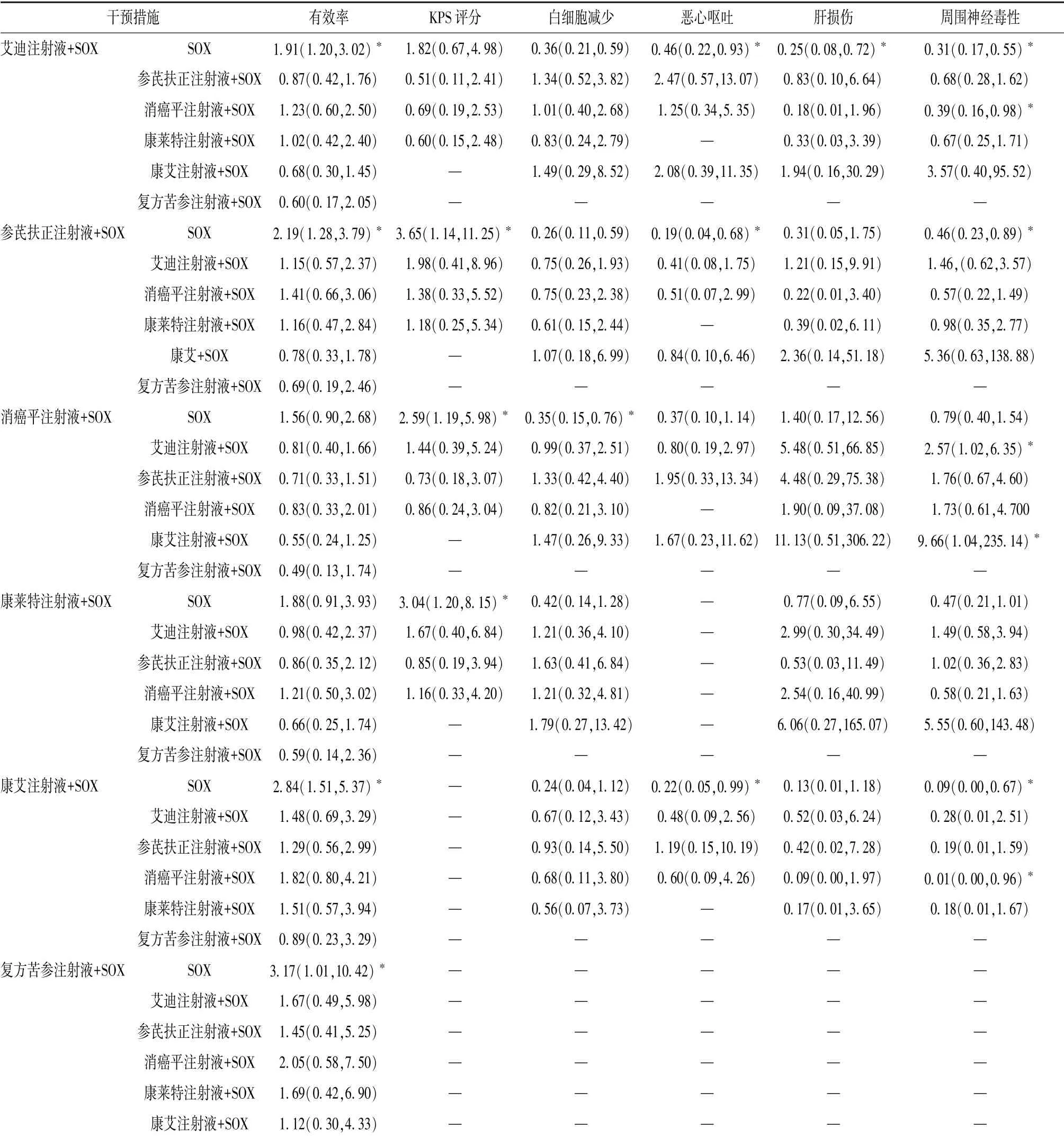
表3 網狀Meta 分析結果[OR (95%CI)]Tab.3 Results of network Meta-analysis[OR (95%CI)]
3.4.2 生活質量改善率 9 項研究報道了生活質量改善率, 包括艾迪注射液、 康艾注射液、 參芪扶正注射液、 消癌平注射液。 異質性檢驗(表2) 顯示, 中藥注射液聯合SOX 化療方案較單用SOX 化療方案的組內研究間具有同質性, 故采用一致性模型進行網狀Meta 分析(表3)。結果顯示, 與單用SOX 化療方案比較, 參芪扶正注射液+SOX、 消癌平注射液+SOX 差異有統計學意義, 其余無統計學意義, 并且4 種聯合用藥兩兩比較差異也無統計學意義。 Rank 1~5 概率排序顯示, 參芪扶正注射液+SOX(49%) >康萊特注射液+SOX(34%) >消癌平注射液+SOX(37%) >艾迪注射液+SOX(49%) >SOX (86%)。
3.4.3 白細胞減少 14 項研究報道了白細胞減少, 包括艾迪注射液、 參芪扶正注射液、 消癌平注射液、 康萊特注射液、 康艾注射液。 異質性檢驗(表2) 顯示, 中藥注射液聯合SOX 化療方案較單用SOX 化療方案的組內研究間異質性較小, 故采用一致性模型進行網狀Meta 分析(表3)。結果顯示, 與單用SOX 化療方案比較, 艾迪注射液+SOX、 參芪扶正注射液+SOX、 消癌平注射液+SOX差異有統計學意義, 其余無統計學意義, 并且5 種聯合用藥兩兩比較差異也無統計學意義。 Rank 6 ~1 概率排序顯示, 康艾注射液+SOX (44%) >參芪扶正注射液+SOX (31%) >艾迪注射液+SOX(29%) >消癌平注射液+SOX (26%) >康萊特注射液+SOX (37%) >SOX (91%)。
3.4.4 惡心嘔吐 12 項研究報道了惡心嘔吐, 包括艾迪注射液、 參芪扶正注射液、 消癌平注射液、康艾注射液。 異質性檢驗(表2) 顯示, 消癌平注射液+SOX 組內研究間異質性較大(P =0.11, I2=61%), 故采用不一致性模型進行網狀Meta 分析(表3)。結果顯示, 與單用SOX 化療方案比較,艾迪注射液+SOX、 參芪扶正注射液+SOX、 康艾注射液+SOX 差異有統計學意義, 其余無統計學意義, 并且4 種聯合用藥兩兩比較差異也無統計學意義。
3.4.5 肝損傷 9 項研究報道了肝損傷, 包括艾迪注射液、 參芪扶正注射液、 消癌平注射液、 康萊特注射液、 康艾注射液。 異質性檢驗(表2) 顯示, 中藥注射液聯合SOX 化療方案較單用SOX 化療方案的組內研究間具有同質性, 故采用一致性模型進行網狀Meta 分析(表3)。結果顯示, 與單用SOX 化療方案比較, 艾迪注射液+SOX 差異有統計學意義, 其余無統計學意義, 并且5 種聯合用藥兩兩比較差異也無統計學意義。 Rank 6 ~1 概率排序顯示, 康艾注射液+SOX (61%) >艾迪注射液+SOX (41%) >參芪扶正注射液+SOX (33%) >康萊特注射液+SOX (29%) >SOX (51%) >消癌平注射液+SOX (53%)。
3.4.6 周圍神經毒性 15 項研究報道了周圍神經毒性, 包括艾迪注射液、 參芪扶正注射液、 消癌平注射液、 康萊特注射液、 康艾注射液。 異質性檢驗(表2) 顯示, 中藥注射液聯合SOX 化療方案較單用SOX 化療方案的組內研究間具有同質性, 故采用一致性模型進行網狀Meta 分析(表3)。結果顯示, 與單用SOX 化療方案比較, 艾迪注射液+SOX、 參芪扶正注射液+SOX、 康艾注射液+SOX 差異有統計學意義, 其余無統計學意義; 艾迪注射液+SOX、 康艾注射液+SOX 顯著優于消癌平注射液+SOX, 其余無統計學意義。 Rank 6 ~1 概率排序顯示, 康艾注射液+SOX (85%) >艾迪注射液+SOX(59%) >參芪扶正注射液+SOX (36%) >康萊特注射液+SOX(36%)>消癌平注射液+SOX(52%) >SOX (72%)。
3.4.7 無進展生存期 5 項研究報道了無進展生存期, 包括艾迪注射液、 參芪扶正注射液、 消癌平注射液。 異質性檢驗(表2) 顯示, 消癌平注射液+SOX 組內研究間異質性較大(P =0.11, I2=62%),其余異質性較小, 由于數據缺失, 聯系作者后仍無法獲取標準差, 故只能進行生存數據Meta 分析。結果顯示, 艾迪注射液+SOX、 消癌平注射液+SOX、 參芪扶正注射液+SOX 的無進展生存期分別是對照組的1.184、 1.196、 1.422 倍, 差異有統計學意義[P =0.037, 95%CI (1.010, 1.388); P =0.024, 95%CI (1.024, 1.396); P =0.006, 95%CI (1.106, 1.828) ]。
3.4.8 中位生存期 7 項研究報道了中位生存期,包括艾迪注射液、 參芪扶正注射液、 消癌平注射液、 康艾注射液。 異質性檢驗(表2) 顯示, 中藥注射液聯合SOX 化療方案較單用SOX 化療方案的組內研究間異質性較小, 由于數據缺失, 聯系作者后仍無法獲取標準差, 故只能進行生存數據Meta分析。結果顯示, 艾迪注射液+SOX、 參芪扶正注射液+SOX、 康艾注射液+SOX 的中位生存期分別是對照組的1.224、 1.406、 1.467 倍, 差異有統計學意義[P =0.004, 95%CI (1.066, 1.404); P =0.001, 95%CI (1.145, 1.726); P =0.022, 95%CI (1.058, 2.033) ]; 消癌平注射液+SOX 的中位生存期是對照組的1.202 倍, 差異無統計學意義[P =0.141, 95%CI (0.941, 1.536) ]。
4 討論
網狀Meta 分析顯示: ①有效率方面, 復方苦參注射液成為最佳措施的概率最大; ②生存質量方面, 參芪扶正注射液成為最佳措施的概率最大; ③白細胞減少、 肝損害、 周圍神經毒性等不良反應方面, 康艾注射液成為最佳措施的概率最大; ④惡心嘔吐方面, 艾迪注射液、 參芪扶正注射液、 康艾注射液能改善相關癥狀; ⑤兩兩比較方面, 艾迪注射液、 康艾注射液在改善周圍神經毒性方面均優于消癌平注射液, 其余兩兩比較差異均無統計學意義。生存數據Meta 分析顯示, 艾迪注射液、 參芪扶正注射液均能延長無進展生存期和中位生存期, 消癌平注射液能延長前者, 康艾注射液能延長后者。
然而, 本研究僅納入6 種中藥注射液, 尚未納入其他品種, 無法將其聯合SOX 化療方案治療胃癌的有效性及安全性進行間接比較。 僅有1 項研究[36]報道了復方苦參注射液; 在白細胞減少、 肝損害、 周圍神經毒性、 中位生存期等結局指標下,康艾注射液均只有1 項研究[32]被納入; 在無進展生存期方面, 僅有5 項研究[16-17,21,28,30]納入, 包括3 種中藥注射液。 納入研究數量不足, 增加了偶然性, 從而降低最終結果的穩定性和可靠性。
質量評價結果顯示, 納入研究均屬中低質量隨機對照試驗, 其中12 項未提及隨機數列的產生方法, 19 項未對分配方法進行詳細說明; 所有研究均未對參與者實施盲法, 在實施過程中容易受到干擾; 所有研究均未對評價者實施盲法, 容易受陽性結果易發表等觀念的影響, 對結果評價缺乏客觀性; 12 項研究未明確提及隨訪/失訪, 不能排除結局數據缺失可能。 有效率為最主要的結局指標, 納入研究中有2 項[19,22]未作報道, 不能排除選擇性報道可能; 所有研究均在不同醫療中心進行, 患者身體素質、 醫療水平、 醫生能力等方面存在不同程度差異, 均可能導致偏倚產生。
在惡心嘔吐、 無進展生存期2 個結局指標中,消癌平注射液組內研究間異質性均較大, 涉及的3項研究[27-28,30]均采用相同評價標準和統計學方法,分析其異質性來源發現, 高明等[27,30]均為胃癌Ⅳ期, 劉威等[28]為胃癌Ⅲ~Ⅳ期; 高明等[27,30]均采用隨機, 但具體方法未描述, 劉威等[28]采用隨機數表法, 并描述了具體方法; 高明等[27,30]均為4個治療周期, 劉威等[28]為2 個治療周期; 高明等[27,30]均為80 mL/d 劑量, 劉威等[28]為60 mL/d劑量。 從目前所得資料來看, 腫瘤分期、 分配方法、 治療周期、 劑量是異質性的主要來源, 但實際操作中參與者主觀意識、 實驗客觀條件等方面也均有可能是其來源。
本研究發現, 消癌平注射液在肝損傷方面成為最佳措施的概率最小, 并低于單用SOX 化療方案;消癌平注射液中有2 項研究[27-28]以肝損傷為結局指標, 其中高明等[27]研究表明2 組均無明顯肝損傷的發生, 劉威等[28]發現治療組和對照組肝損傷發生例數分別為4、 3 例, 且均為Ⅰ度。 檢索文獻發現, 消癌平注射液并不能增加肝損害發生率[37-39]; 但李妮等[40]報道消癌平注射液聯合化療在肝損傷方面優于單純化療。 異質性分析表明, 2項研究[27-28]可能是異質性主要來源, 加上納入文獻過少, 樣本量小, 所得結果缺乏足夠的穩定性及可靠性, 須謹慎對待。
綜上所述, 6 種中藥注射液聯合SOX 化療方案治療胃癌時, 在提高有效率、 改善生存質量、 降低不良反應發生率、 延長中位生存期和無進展生存期等方面均能取得更好的臨床療效。 但限于本研究納入文獻偏少, 方法學質量不高, 今后有待更多前瞻性、 高質量、 大樣本、 多中心隨機對照試驗證實。

