3D打印技術輔助腹腔鏡下腎腫瘤冷凍消融術*
曹 健 朱 帥 葉明佶 皮碩煌 劉 侃 韓惟青 謝 宇
(湖南省腫瘤醫院泌尿外科,長沙 410006)
【內容提要】 2016年4月~2017年4月,對4例單發腎透明細胞癌(上極1例,腎門1例,下極2例,最大徑2.4~3.8 cm,平均3.13 cm),術前通過3D圖像輔助模擬冷凍消融治療,設計需要的進針數及進針的深度和角度,術中對照3D打印模型實施手術。4例手術順利,術后無并發癥。隨訪8~16個月,平均13.3月。復查泌尿系統CT平掃加增強,冷凍區域均無強化表現。
中國泌尿外科診療指南[1]顯示,外科手術是局限性腎癌的首選治療方法,但是對于需要盡可能保留腎單位、有嚴重合并癥、腎功能不全且腫瘤<4 cm的腎癌可以選擇冷凍消融。歐洲泌尿外科診療指南[2]同樣推薦具有嚴重合并癥的老年患者可選擇冷凍消融治療小腎癌。經皮穿刺在CT、MR或超聲引導下完成,或在腹腔鏡下直視完成,主要依靠術者經驗決定冷凍針使用數量、進針角度及深度,很難根據腫瘤形態精準適形形成冰球冷凍腫瘤,如用針過多則并發癥多,對正常組織損傷大,用針過少則有可能難以達到良好的腫瘤治療效果。
3D打印技術已用于輔助各種外科操作,包括復雜手術的術前規劃及手術操作訓練,可打印患者特異的手術輔助模型、手術替代物及外科手術器械等[3,4]。在保留腎單位的手術中,通過3D打印技術可以在術前打印出患腎的3D模型,清晰顯示腫瘤大小、位置、浸潤深度及其與腎血管、集合系統的關系,對術者的術前規劃及術中指導具有重要的意義。基于3D技術在保留腎單位手術中的優勢,我們認為3D技術可指導冷凍消融治療,讓術者可實施精準冷凍,從而最大限度保留腎單位。2016年4月~2017年4月,我們對4例單發腎透明細胞癌,且具有嚴重合并癥或腎功能損害需要最大限度保留腎功能者,利用3D打印技術輔助術前規劃,術中指導冷凍消融,為國內首次3D打印技術輔助腹腔鏡下冷凍消融治療的報道(教育部科技查新工作站Z11,201836000Z110173),報道如下。
1 臨床資料與方法
1.1 一般資料
本組4例,男2例,女2例。年齡50~75歲,平均62.8歲。1例有腰痛癥狀,其余3例無明顯癥狀,均為體檢超聲發現。均行泌尿系統CT平掃、增強、三維重建,提示腎惡性腫瘤,左側2例,右側2例,均為單發,位于上極1例,腎門1例,下極2例,最大徑2.4~3.8 cm,平均3.13 cm。1例孤立腎(因腎癌已行一側腎切除),1例因盆腔黏液性腺癌化療5周期,1例對側腎結石腎重度積水,1例對側腎囊腫合并高血壓。2例術前行腎穿刺活檢,2例術中行腎腫瘤穿刺活檢,病理診斷為腎透明細胞癌。臨床分期均為T1aN0M0。術前血肌酐正常(70.7~80.1 μmol/L,平均75.5 μmol/L,正常值57.0~111.0 μmol/L)。
根據歐洲泌尿外科協會指南[2]及中國泌尿外科疾病診斷治療指南[1],病例選擇標準:臨床分期為T1aN0M0期,病理診斷為腎細胞癌,且具有嚴重合并癥,或腎功能損害嚴重,或孤立腎,需要最大限度保護腎功能。
1.2 方法
1.2.1 儀器設備 3D打印技術采用醫學影像控制系統MIMICS18.0(比利時Materialise公司),HS402P 3D打印機(湖南華翔增量制造技術有限公司),打印材料為尼龍材料(FS3200PA Nylon Powder,湖南華翔增量制造技術有限公司)。冷凍消融治療采用美國氬氦刀系統(Cryocare Surgical System,美國加利福尼亞州Endocare高科技公司)。
1.2.2 3D打印技術 采用醫學影像控制系統對雙側腎CT平掃加增強的影像數據進行分析處理,對患腎進行三維重建,使用軟件在電腦上進行模擬穿刺,根據腫瘤的大小和位置,模擬計算用針數,進針角度及深度,優化出最佳方案,即用最少的針數使冰球完全覆蓋腫瘤(圖1A)。用3D打印機制作出患腎3D模型,輔助指導術中操作(圖1B)。
1.2.3 腹腔鏡下腎腫瘤冷凍消融術 根據3D打印模型的指導,選擇經腹膜后途徑手術。游離暴露患腎,根據3D打印技術輔助制定的最優方案,在腹腔鏡下使用17G探針穿刺,針尖最終溫度設置為2 min下降至-140 ℃,持續冷凍10 min,彩超監測使冰球超出腫瘤邊緣1 cm以上,解凍復溫10 min,解凍溫度42 ℃,共進行2個循環的冷凍復溫,第2次解凍復溫后緩慢退出探針。
1.2.4 隨訪和療效評價 術后定期門診隨訪,詢問癥狀,進行雙腎CT平掃加增強掃描、胸片、腹部彩超檢查、肝腎功能、電解質及尿常規檢驗,若發現問題則進一步檢查。術后泌尿系統增強CT檢查,冷凍治療區域無腫瘤強化作為治療成功的標準[5]。
2 結果
4例手術時間106~118 min,平均111 min,術中出血量50~100 ml,平均66.7 ml。術后血肌酐均正常(術后1周68.5~84.4 μmol/L,平均76.5 μmol/L;術后1個月70.5~85.6 μmol/L,平均74.8 μmol/L)。
隨訪時間8~16個月,平均13.3月。復查泌尿系統CT平掃加增強,冷凍區域均無強化(圖2),全身無明顯遠處轉移。
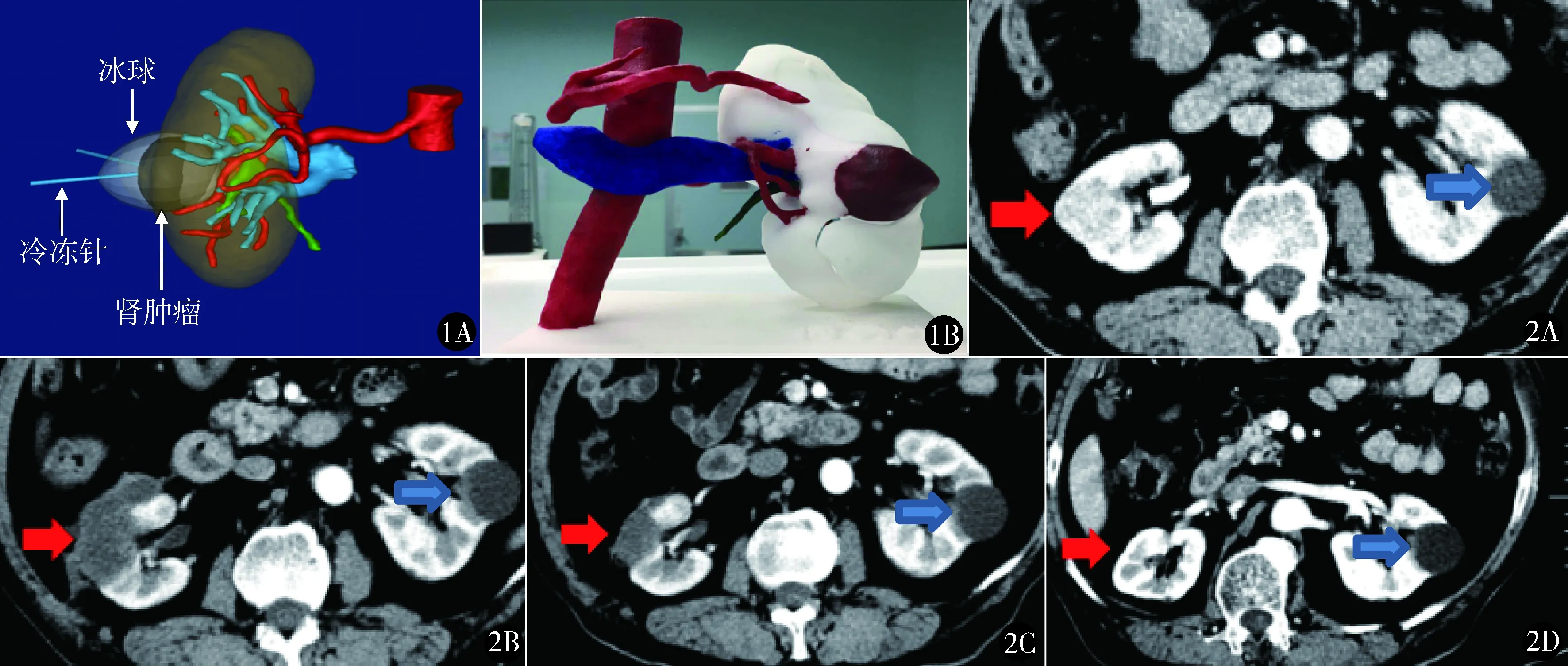
圖1 3D打印技術 A:提取患腎CT掃描數據進行三維重建,模擬冷凍消融進針數量、角度及深度,計算最佳方案;B:打印出模型輔助指導術中操作 圖2 冷凍消融前后增強CT對比 A.術前左腎腫瘤(紅箭頭),直徑3 cm,可見明顯不均勻強化,對側腎囊腫(藍箭頭),直徑2 cm;B.術后1個月冷凍區域可見大片低密度影,無強化,為冷凍后腫瘤壞死組織;C.術后6個月治療區域無明顯強化,腫瘤壞死組織減少;D.術后12個月治療區域幾乎無壞死組織,且未見明顯異常強化
3 討論
3D打印技術在臨床的運用絕大部分是打印出患者特異性的解剖模型輔助手術操作[4]。在泌尿外科中,3D打印技術用于輔助保留腎單位的腎部分切除術[6]、腎上腺部分切除術[7]、經皮腎鏡取石術[8]、前列腺穿刺活檢[9]等。在腎部分切除術中,術前3D打印出患腎模型,精準顯示腫瘤的大小、位置、浸潤深度及與腎動脈、腎靜脈、集合系統的位置關系,有助于術者進行術前手術規劃,術中參照指導,減少術中并發癥,提高手術成功率及精度[6,10]。
腹腔鏡冷凍消融是一種治療腎癌的新型微創手段,與傳統腹腔鏡腎部分切除術治療局限性腎癌相比具有自身的優勢,尤其適合于孤立腎癌、術前腎功能不全者[11],而且可以達到很好的腫瘤治療效果,在保留腎功能方面也有其優勢[12~14]。腹腔鏡下腎部分切除術是目前保留腎單位手術中運用廣泛、效果肯定的方法,但是對術者技術要求較高,需要阻斷腎臟血供,而腹腔鏡下冷凍消融治療技術相對簡單。冷凍消融的優勢在于相對安全,手術風險小,容易實施,無熱缺血損害,無需切開及縫合腎實質,可以更好地保留腎單位,因此對于身體條件差及腎儲備功能不足需要最大限度保留腎功能的患者意義尤為重大。Klatte等[15]的meta分析顯示,與腹腔鏡腎部分切除術相比,腹腔鏡下冷凍消融治療可較好地保護腎功能,減少并發癥,但局部復發率(OR=13.03)及遠處轉移率(OR=9.05)顯著高于腹腔鏡腎部分切除術。但作者同時指出,腹腔鏡下冷凍消融治療選擇的患者一般情況較差,年齡顯著高于腹腔鏡腎部分切除術,且孤立腎比率更高,因此在手術方式的選擇上仍需非常謹慎,根據患者特點選擇最利于患者的手術方式,對于那些年齡大、具有嚴重并發癥者,冷凍消融治療是一種很好的選擇。我們聯合3D打印技術輔助冷凍消融的方法可以進一步發揮冷凍消融的優勢,對于適合接受冷凍消融治療者可提供更加精確的腎功能保護。
本研究在國內首次探索了3D打印技術輔助腹腔鏡下冷凍消融治療進行精準腎功能保護的可行性,雖然這兩種技術都已經分別運用于腎腫瘤的治療,但是我們首次實現了聯合此兩種技術進行腎腫瘤治療。經過4例手術,我們的經驗如下:第一,在病例選擇上,嚴格遵照國內外指南,選擇因其他疾病腎功能損害較嚴重,如對側腎重度積水、糖尿病腎病、高血壓腎病者,或患者一般情況差不能耐受腎部分切除術,且腎腫瘤<4 cm。本研究1例孤立腎(因腎癌已行一側腎切除),1例因盆腔黏液性腺癌化療5周期,1例對側腎結石腎重度積水,1例對側腎囊腫合并高血壓,都需要最大限度保護腎功能。第二,術前可通過3D重建模型在電腦上模擬冷凍消融治療,模擬進針位置、深度及角度;還可打印出患腎的3D模型,增加對腎臟解剖、腫瘤位置、與血管比鄰關系的深入了解;可以為術者提供術中指導,在完整覆蓋腫瘤的情況下,盡可能多地保留腎單位。需要注意的是,整個操作過程需與麻醉師密切配合,在進針時降低潮氣量,減少呼吸運動引起的臟器移動,防止探針偏移。
我們認為,3D打印技術和腹腔鏡冷凍消融技術已分別成熟運用于腎腫瘤治療,二者聯合使用有利于冷凍消融更加精準,盡可能保留腎單位,值得進一步推廣。但本研究僅4例,是對此方法的初步探索,尚需進行大樣本前瞻性隨機對照研究證實其可行性及有效性。

