非缺失型α-珠蛋白生成障礙性貧血基因檢測簡化方法的研究*
涂志華,周 知,馬 寧,吳 忠,黎業娟,王安國,阮海玲,趙立強,胡嘉嘉,王 潔
(海南省婦幼保健院:1.生殖醫學中心;2.檢驗中心,海口 570206)
珠蛋白生成障礙性貧血(thalassemia)是由于珠蛋白基因發生缺失或突變而導致的一組溶血性貧血,可遺傳;以α-珠蛋白生成障礙性貧血和β-珠蛋白生成障礙性貧血為主要類型[1]。α-珠蛋白生成障礙性貧血又根據其基因改變類型的不同,分為缺失型α-珠蛋白生成障礙性貧血和非缺失型α-珠蛋白生成障礙性貧血[2]。地中海沿岸國家及東南亞各國、非洲均是珠蛋白生成障礙性貧血高發區,就十年前WHO統計,全世界就有約3.5億人攜帶珠蛋白生成障礙性貧血基因[3]。聚合酶鏈反應-反向點雜交法(PCR-RDB)針對基因突變區域,設計特異性探針置于尼龍膜等介質上,PCR體外擴增基因突變DNA片段,同介質上的探針雜交并顯色,能夠進行多個靶基因并行檢測,可用于批量檢測,是臨床上檢測非缺失型α-珠蛋白生成障礙性貧血的主流方法。中國珠蛋白生成障礙性貧血人群Hb Westmead(Hb WS)、Hb Quong Sze(Hb QS)、Hb Constant Spring(Hb CS)3種常見非缺失型α-珠蛋白生成障礙性貧血大多采用PCR-RDB法檢測[4]。我國南方珠蛋白生成障礙性貧血高發,特別是廣西、廣東、海南,各級政府每年需支付數以億計的群體篩查費用。筆者希望可以建立一種針對珠蛋白生成障礙性貧血群體篩查的方法,基于PCR-RBD技術,將適量例數的DNA標本混合成1例檢測的非缺失型α-珠蛋白生成障礙性貧血基因批量檢測的方法,以縮減珠蛋白生成障礙性貧血群體防控經費,現報道如下。
1 資料與方法
1.1標本處理 取患者靜脈血3 mL,置入抗凝管內。采用全血DNA快速提取試劑盒(亞能生物技術有限公司),運用柱式分離法,提取抗凝血中的DNA。
1.2PCR-RDB 采用非缺失型α-珠蛋白生成障礙性貧血基因突變檢測試劑盒(亞能生物技術有限公司)進行檢測,儀器采用ABI 9700型PCR儀。嚴格按照說明書操作,每批設置陽性、陰性對照。檢測限相關最大標本數檢測實驗:隨機抽取臨床標本10例,分別稀釋3、6、12倍,經PCR-RDB檢測,觀察結果。
1.3干擾實驗 驗證非缺失型α-珠蛋白生成障礙性貧血基因DNA標本之間、與健康人標本之間會否相互干擾檢測結果。3種非缺失型α-珠蛋白生成障礙性貧血標本間干擾實驗:隨機選取Hb WS、Hb CS、Hb QS的DNA標本各1例,等量混勻,經PCR-RDB檢測后觀察結果,進行3次重復實驗。非缺失型α-珠蛋白生成障礙性貧血標本與正常標本間的干擾實驗:隨機選取Hb WS、Hb CS、Hb QS兩類標本各1例,與正常標本1例,等量混勻,經PCR-RDB檢測后觀察結果,進行3次重復實驗。健康人標本之間的干擾實驗:隨機選取健康人DNA標本3例,等量混勻,經PCR-RDB檢測后觀察結果,進行3次重復實驗。
1.4數學模型建立 設某地區初篩實驗α-珠蛋白生成障礙性貧血基因陽性預測值為K,初篩陽性批標本量為N,每例非缺失型α-珠蛋白生成障礙性貧血基因檢測費用為S,則該批標本標本常規檢測費用為SN。剔除雙缺失α-珠蛋白生成障礙性貧血DNA標本后,每次取A例DNA標本混成1例檢測,混合樣本有N/A例。每例混合標本為陽性的概率為KA(0≤KA<1),如有混合標本檢測出陽性,則需單獨檢測出現陽性的混合標本中的每1例,混合標本的檢測次數為A+1。則檢測結果陽性的批檢測費用為:F陽=N/A×KA×(A+1)×S,混合樣本檢測結果陰性的概率為1-KA,檢測結果陰性的批檢測費用為:F陰=N/A×(1-KA)×S,批檢測總體費用公式為:F總=F陽+F陰=N/A×KA×(A+1)×S+N/A×(1-KA)×S=SN×(KA2+1)/ASN、K相對穩定,F總隨A變化而變化,故F總有最小值,該最小值對應的A值即混合標本檢測費用最小的最適標本數。
1.5方法驗證實驗 選取2013年10月東方市珠蛋白生成障礙性貧血群體篩查中初篩為α-珠蛋白生成障礙性貧血陽性的標本50例,用建立的新非缺失型α-珠蛋白生成障礙性貧血批量檢測方法進行檢測,比對新方法與傳統方法的檢測費用。
2 結 果
2.1檢測限相關最大標本數檢測組結果 分別稀釋3、6、12倍后DNA標本能檢測出結果且與其確診結果相同(圖1)。
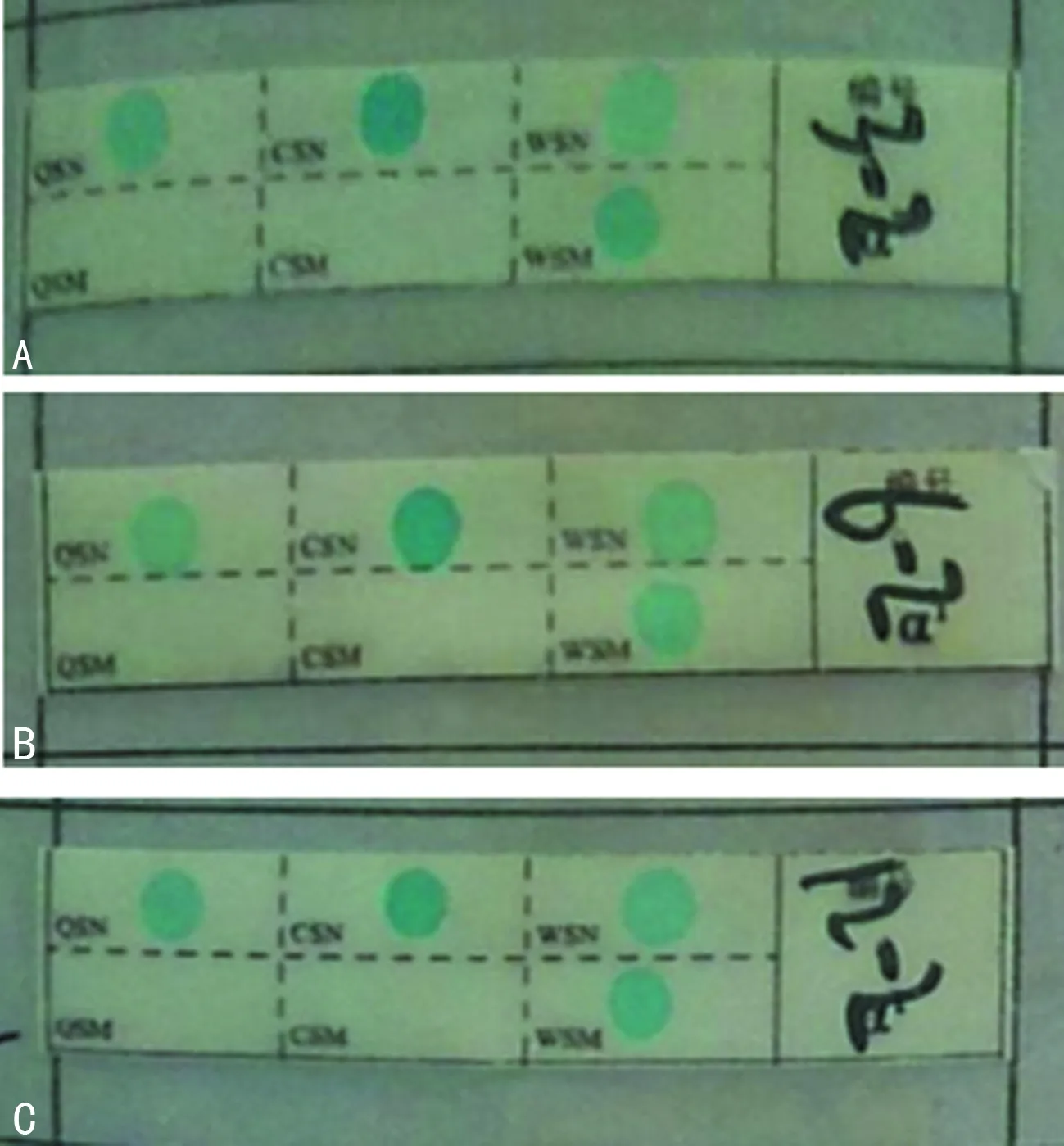
A:稀釋3倍;B:稀釋6倍;C:稀釋12倍
圖1稀釋后Hb WS雜合子標本DNA基因檢測結果
2.2干擾實驗檢測組結果
2.2.13種非缺失型α-珠蛋白生成障礙性貧血標本間干擾情況 Hb WS + Hb QS + Hb CS標本混合均能檢測出結果且結果為混合突變總和的結果,如圖2所示。

圖2 Hb WS+Hb QS+Hb CS純合子標本混合檢測結果
2.2.2非缺失型α-珠蛋白生成障礙性貧血標本與正常標本間的干擾情況 2種非缺失型α-珠蛋白生成障礙性貧血標本+健康人標本混合均能檢測出結果且結果為混合突變總和的結果(圖3~5)。

圖3 Hb WS純合子+Hb QS純合子+健康人標本混合檢測結果
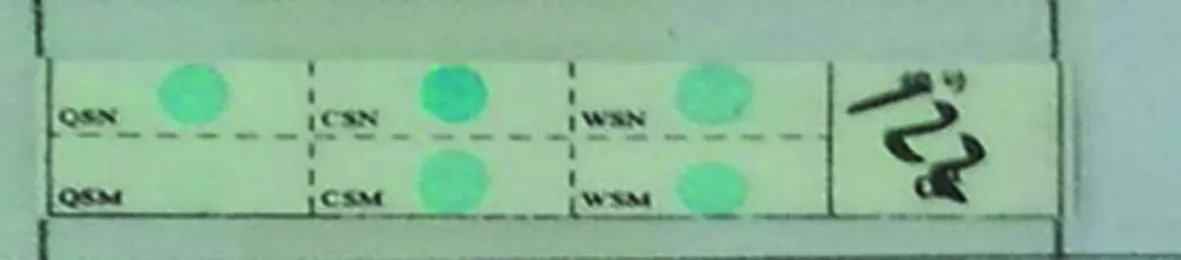
圖4 Hb WS純合子+Hb CS純合子+健康人標本混合檢測結果

圖5 Hb QS純合子+Hb CS純合子+健康人標本混合檢測結果
2.2.3健康人標本之間的干擾情況 健康人標本混合均能檢測出結果且結果不受干擾(圖6)。

圖6 3例健康人標本混合檢測結果
2.3新方法驗證結果 以海南省東方市婦幼保健院送檢標本驗證新方法可行性。2013年海南省東方市試行的珠蛋白生成障礙性貧血防控實驗室方案:育齡夫婦行血細胞分析、紅細胞滲透脆性實驗,血細胞分析結果紅細胞平均體積(MCV)<82 fL和/或紅細胞平均血紅蛋白含量(MCH)<27 pg、紅細胞滲透脆性實驗≤60%,符合其中一項即進行血紅蛋白毛細管電泳實驗,電泳結果HbA2 ≤2.5%或HbA2>3.5%為陽性,夫婦雙方只要一方血紅蛋白電泳結果陽性,則夫婦雙方定為高危人群,進行珠蛋白生成障礙性貧血基因檢測。該群體篩查實驗室方案下,海南省東方市珠蛋白生成障礙性貧血群篩初篩實驗平均陽性預測值為14.58%,代入上述公式,可知每3例標本混合后檢測,檢測費用最低,為傳統檢測費用的77.07%。2013年10月批次α-珠蛋白生成障礙性貧血初篩陽性病例50例,剔除3例雙重缺失型α-珠蛋白生成障礙性貧血病例,用新法檢測,費用為原來的78.72%,以三級醫院非缺失α-珠蛋白生成障礙性貧血基因檢測門診收費143元計算,該批α-珠蛋白生成障礙性貧血初篩陽性標本檢測可節約3 043.04元。
3 討 論
珠蛋白生成障礙性貧血又稱地中海貧血,是由于珠蛋白基因發生缺失或突變,珠蛋白鏈合成減少或缺失,導致血紅蛋白的α鏈/非α鏈比例失衡,而引起的一組隱性遺傳溶血性疾病。輕者可無臨床表現,重者以溶血性貧血為主要特征[5]。珠蛋白生成障礙性貧血早在1999年就被WHO人類遺傳病計劃列為在發展中國家開展人群預防的六大疾病之一。是我國最常見的遺傳性疾病之一。珠蛋白生成障礙性貧血目前尚無有效又廉價的治療方法,對該病進行群體篩查、降低珠蛋白生成障礙性貧血重癥胎兒出生概率有重要的意義。
根據珠蛋白肽鏈合成受到抑制的類型,珠蛋白生成障礙性貧血可以分為α-珠蛋白生成障礙性貧血、β-珠蛋白生成障礙性貧血、γ-珠蛋白生成障礙性貧血和δβ-珠蛋白生成障礙性貧血等,其中以α-珠蛋白生成障礙性貧血和β-珠蛋白生成障礙性貧血為主要類型[6]。α-珠蛋白生成障礙性貧血是由于α-珠蛋白基因突變而引起α珠蛋白肽鏈的合成受到抑制而導致[7],又可以根據其基因改變的不同,分為缺失型α-珠蛋白生成障礙性貧血和非缺失型α-珠蛋白生成障礙性貧血。缺失型α-珠蛋白生成障礙性貧血是由于α-珠蛋白基因大片段缺失引起,是α-珠蛋白生成障礙性貧血主要的類型;非缺失型α-珠蛋白生成障礙性貧血是由于α-珠蛋白基因發生了點突變或其調節序列發生突變如單堿基置換或一個或幾個核苷酸的缺失或插入所致,占α-珠蛋白生成障礙性貧血比例較少。目前發現至少有六十多種α珠蛋白基因點突變可以導致非缺失型α-珠蛋白生成障礙性貧血的發生,其中大部分突變點位于α2基因,少部分位于α1基因,及極少數位于α珠蛋白基因簇上α1和α2基因外的地方[8]。中國南方人群中常見的3種α點突變位點Hb WS、Hb QS、Hb CS位于α2基因。
非缺失α-珠蛋白生成障礙性貧血基因的檢測有基因測序、基因芯片、變性高效液相色譜技術(DHPLC)、單鏈構象多態性(SSCP),變性梯度凝膠電泳(DGGE)等技術,隨著各國政府對珠蛋白生成障礙性貧血的日益重視,學者們用新方法進行α-珠蛋白生成障礙性貧血篩查、診斷的嘗試多見報道[9]。而隨著PCR技術的發現,結合PCR技術的點突變分析鑒定非缺失型α-珠蛋白生成障礙性貧血的方法成為檢測技術的主流,1989年發明反向點雜交技術(RDB)后,該技術在檢測突變的確定性上僅次于基因測序。PCR-RDB-個雜交反應能同時分析一份標本中可能存在的多種點突變[10]。
雖然珠蛋白生成障礙性貧血篩查診斷技術有多種選擇,但大多檢測費用昂貴,多是一例標本一份試劑一次檢測操作,但每年有數以百萬計的珠蛋白生成障礙性貧血篩查人群,政府在珠蛋白生成障礙性貧血防治項目上所需費用過于龐大,珠蛋白生成障礙性貧血群體防控要更好地開展,需要大幅提高珠蛋白生成障礙性貧血醫療資源利用率[11]。
α-珠蛋白生成障礙性貧血檢測的主流產品多基于PCR-RDB技術,理論上只要模板DNA高于檢測限2 ng/μL,PCR過程不會相互干擾,RDB階段,PCR產物與探針結合有特異性,理論上也不會相互干擾。正常提取的DNA標本,濃度為10~50 ng/μL,2~5例標本混合,單個樣本濃度2~25 ng/μL,對基因擴增沒有影響。珠蛋白生成障礙性貧血篩查方法中初篩可以初分α-珠蛋白生成障礙性貧血和β-珠蛋白生成障礙性貧血,再經基因診斷,但是初篩不能區分α-珠蛋白生成障礙性貧血表型陽性標本為缺失型還是非缺失型,基因檢測時需α-珠蛋白生成障礙性貧血的兩種類型同時檢測,中國人群非缺失型α-珠蛋白生成障礙性貧血比例較小,因此非缺失型α-珠蛋白生成障礙性貧血檢測多為陰性,適量例數標本混成一例檢測非缺失型α-珠蛋白生成障礙性貧血相當于一次實驗可得出多例標本的結果,節省大量試劑、工時、儀器損耗、水電等。
現有的珠蛋白生成障礙性貧血篩查診斷技術,多是一例標本一次檢測操作,針對大樣本群體篩查批檢測的改進方法,罕見報道。筆者建立了一種應用于珠蛋白生成障礙性貧血群體篩查的非缺失型α-珠蛋白生成障礙性貧血批檢測方法,該法基于PCR-RBD技術,根據初篩實驗α-珠蛋白生成障礙性貧血陽性預測值均值,概率推算費用公式,建立數學模型,并依此將適量例數DNA標本混合成一例進行非缺失型α-珠蛋白生成障礙性貧血基因檢測。依據文獻報道,推測中國人群非缺失型α-珠蛋白生成障礙性貧血僅占α-珠蛋白生成障礙性貧血的2%~11%[12],珠蛋白生成障礙性貧血群體篩查時,理想狀態下,陽性預測值按此數據計,根據新的批檢測方法,套用費用公式,批檢測費用僅為常規檢測的30%~70%。
珠蛋白生成障礙性貧血群體篩查中應用該批檢測方法可大量減少基因檢測次數,縮減人工和試劑費用、儀器損耗等。中國每年珠蛋白生成障礙性貧血群體篩查人數以百萬計,而基因檢測費用昂貴,應用該法能大幅縮減珠蛋白生成障礙性貧血群體防控經費,極大提高醫療資源利用率和社會效益。

