PD-1靶向性腫瘤治療抗體藥物在消化道腫瘤中的應用價值
曹 焱 潘慧麗 張 超
流行病學研究發現,食管癌與民族、生活習慣、日常生活等明確相關[1-2]。放化療是目前臨床上用于治療晚期食管癌的主要手段,能很好地殺傷或者抑制食管癌腫瘤細胞的擴散和轉移,但是也都存在一定的缺陷[3-4]。免疫治療是當前極具前景的綜合治療策略,其中靶向于免疫調節檢查點程序性死亡蛋白(PD-1)通路的治療方法在多種腫瘤中取得了不錯的療效[5-6]。PD-1是一種免疫檢驗點受體,可以維持自身抗原的免疫耐受性,也可以阻止免疫反應的過表達[7]。抗PD-1抗體已經在腎臟腫瘤、黑色素瘤、肺癌、膀胱癌等腫瘤的治療中獲得了較好的療效,且不良反應可耐受[8-9],但是在消化道腫瘤中的應用還鮮有報道。本文具體探討了PD-1靶向性腫瘤治療抗體藥物在食管癌中的應用價值,現報告如下。
1 資料與方法
1.1 一般資料
采用隨機、對照與雙盲研究方法,選擇2013年1月至2016年12月在我院診治的食管癌晚期患者116例。納入標準:患者年齡大于18歲;研究得到醫院倫理委員會的批準;符合晚期食管癌的診斷標準;病灶局限在黏膜層至固有肌淺層;患者知情同意本研究。排除標準:妊娠與哺乳期婦女;合并其他嚴重消化道疾病等;精神疾病患者;心腦血管疾病者。根據隨機數字表法原則分為觀察組與對照組,各58例。2組患者一般資料無明顯差異(P>0.05)。見表1。

表1 2組一般資料對比
1.2 治療方法
對照組:給予常規化療,多西他賽5 mg/m2,靜脈滴注;表阿霉素75 mg/m2,靜脈推注;環磷酰胺500 mg/m2,靜脈推注;都是在周期的第1天進行給藥,1個周期包括3周,治療觀察4個周期。
觀察組:在對照組治療的基礎上給予PD-1靶向治療,接受PD-1單抗(Nivolumab)靜脈輸液治療,劑量為3 mg/kg,1個周期靜脈輸液1次。
1.3 觀察指標
①療效判定:完全緩解(CR)、部分緩解(PR)、穩定(MR)、無效(NR)。CR+PR為總有效。②記錄2組患者的不良反應,包括胃腸道反應、心臟毒性、皮疹等。③生活質量:在治療后采用WHO生活質量測量量表進行調查,包括社會關系、環境、生理、心理等4個領域,分數越高,生活質量越好。④所有患者隨訪至今,記錄患者的中位生存時間。
1.4 統計學方法
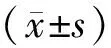
2 結果
2.1 總有效率對比
觀察組與對照組的總有效率為65.5%和48.3%,差異有統計學意義(χ2=6.159,P<0.05)。見表2。

表2 2組總有效率對比/例
2.2 不良反應情況對比
2組均有不同程度的不良反應,主要以心臟毒性、胃腸道反應、皮疹、白細胞減少等為主,但差異無統計學意義(P>0.05)。見表3。

表3 2組治療期間不良反應情況對比(例,%)
2.3 生活質量對比
治療后觀察組的社會關系、環境、生理、心理等領域評分都明顯高于對照組(P<0.05)。見表4。

表4 2組治療后生活質量評分對比分)
2.4 中位總生存期
隨訪至今,觀察組與對照組中位總生存期為25月(18~32月)、33月(27~40月),觀察組長于對照組(χ2=32.426,P<0.05)。
3 討論
現代研究表明惡性腫瘤的發生、發展與免疫系統密切相關,免疫調節檢查點對免疫系統起負性調節作用,可避免自身免疫性疾病的發生,以維持免疫自穩[10]。
PD-1主要表達于NK細胞、T細胞、B細胞等淋巴細胞,激活的PD-1/PD-L1通路通過抑制淋巴細胞的活化與增殖,從而負性調節免疫系統。本研究顯示觀察組與對照組的總有效率為65.5%和48.3%,觀察組的總有效率高于對照組(P<0.05);2組均有不同程度的不良反應,主要以心臟毒性、胃腸道反應、皮疹、白細胞減少等為主,對比無統計學意義(P>0.05),表明PD-1靶向性抗體藥物在食管癌中的應用具有比較好的安全性,且能提高治療效果。
PD-1/PD-L1抑制劑介導的抗腫瘤效應腫瘤生長微環境的形成,能夠通過某些信號通路,依賴其自身分泌的一些細胞因子,避免監視及調控,從而導致腫瘤的快速進展[11-12]。阻斷PD-1/PD-L1通路,可增加T細胞的活化,促進活化T細胞對腫瘤細胞的攻擊。本研究顯示隨訪至今,觀察組與對照組中位總生存期為25月(18~32月)、33月(27~40月),觀察組長于對照組,表明PD-1靶向性抗體藥物的應用能延長患者的生存時間。
國際公認的WHO生活質量測定量表簡表能夠對患者的生活質量進行針對性研究,能夠反映患者的生理與心理狀況;特別是從主觀感覺的角度來反映病情的變化,有助于臨床醫生全面地衡量病情和判斷療效[13]。本研究顯示治療后觀察組的社會關系、環境、生理、心理等領域評分都明顯高于對照組(P<0.05),也表明PD-1靶向性抗體藥物的應用能提高患者的生活質量。但是本研究也存在一定缺陷,比如病例數較少,存在其他混雜因素與主觀選擇偏倚等;免疫治療起效較慢,療效標準還有待進一步完善。
綜上所述,PD-1靶向性腫瘤治療抗體藥物在食管癌中的應用能提高治療效果,且不增加不良反應,可延長患者的生存時間,提高患者的生活質量。

