心臟術后重癥患者不同鎮靜方式比較的臨床研究
孟冬梅,齊玉娟,穆玉,李健,李培軍
心臟手術后的重癥患者,因血流動力學不穩定、心功能不全、嚴重低氧、二次手術、精神狀態異常、術后合并其他臟器衰竭等原因在術后短期內(36~48 h)無法脫離呼吸機,并常常需要主動脈內球囊反搏(IABP)、連續腎臟替代療法(CRRT)支持。因此,合適的鎮靜鎮痛治療有利于緩解治療期間患者的疼痛應激反應,減少躁動和非計劃性脫管的發生,是幫助患者度過難關的重要治療措施。近年來在重癥醫學領域,淺鎮靜既能發揮鎮靜治療的有益作用,縮短機械通氣時間,又可有效避免過度鎮靜、每日喚醒時循環氧合狀態的波動等弊病而被臨床廣泛接受。但心臟術后重癥患者的病因相對復雜,病情重且變化快,淺鎮靜是否能讓這些患者受益尚無定論,也沒有關于這方面的指南指導臨床工作。本文就淺鎮靜和傳統鎮靜方式(中度鎮靜加每日喚醒)對心臟術后重癥患者的早期循環指標和住院預后的影響進行比較。
1 對象與方法
1.1 研究對象及分組 選取2017年1月—6月于我院行心臟外科手術后轉入重癥監護病房(ICU)的患者。納入標準:成人心臟術后病情嚴重[術后出現嚴重情況需要延遲呼吸機輔助通氣時間,如血流動力學不穩定、需多種藥物或IABP、低心排出量綜合征(低心排綜合征)、精神狀態異常、出血、再次手術干預、腎衰引起的少尿,特別是氧合差或者呼吸功能差][1],預計48 h內不能脫離呼吸機的患者。排除標準:先天性心臟病患者;年齡<18歲;妊娠及哺乳期婦女;癡呆或精神疾病患者;嚴重心動過緩及Ⅱ、Ⅲ度房室傳導阻滯者;肝功能障礙者(Child評分C級);36 h內病情平穩脫離呼吸機者。按照納入和排除標準,共入組患者134例,男89例,女45例,平均年齡62.07(35~82)歲。入選患者按照隨機數字表法分入淺鎮靜組(65例)和傳統鎮靜組(69例)。2組患者術前性別、年齡、BMI、合并癥、心功能和手術方式比較差異均無統計學意義(P>0.05),見表1。
1.2 方法 所有患者術后當日轉入ICU,待患者清醒后,給予鎮靜鎮痛治療。鎮痛:依鎮痛評分給予0.2~0.3 μg/(kg·h)舒芬太尼充分鎮痛。鎮靜:淺鎮靜組隨機給予丙泊酚和/或右美托咪定鎮靜,右美托咪定從0.2 μg/(kg·h)開始泵入,無負荷劑量,調整右美托咪定的泵入劑量[0.2~1.0 μg/(kg·h)],丙泊酚先靜脈給予10~20 mg負荷量,繼以0.3~2.0 mg/(kg·h)的泵入劑量,單藥用量大時采用右美托咪定和丙泊酚聯合用藥;使患者Richmond躁動鎮靜量表(Richmond agitationsedation scale,RASS)評分達到-1~1分。傳統鎮靜組采用咪達唑侖先靜脈注射5 mg,繼以0.05 mg/(kg·h)開始靜脈泵入,調整劑量至RASS評分達到-3~-2分。每4 h進行一次RASS評分,待患者循環穩定、心功能恢復、氧合滿意、器官功能恢復滿意后逐步停用鎮靜藥物,評估患者脫離呼吸機指標,滿意者脫機拔管,視患者脫機后情況給予無創呼吸機輔助,必要時再次插管有創通氣治療。患者轉出ICU的標準包括氣道通暢、呼吸功能正常、血流動力學穩定、無需升血壓藥物。
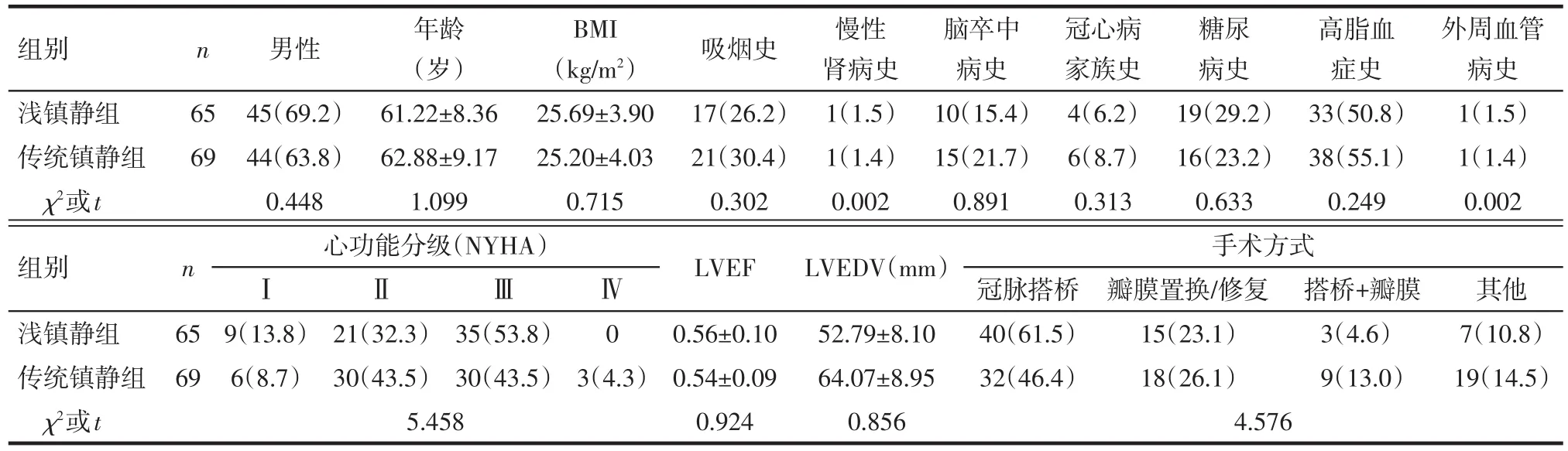
Tab.1 Comparison of the general clinical data and surgical methods before operation between two groups表1 患者術前一般臨床資料和手術方式比較
1.3 數據收集 記錄患者術前既往病史、心功能、手術方式等基線資料。所有低心排綜合征患者于術中或術后放置肺動脈漂浮導管以記錄混合靜脈血氧飽和度(SvO2)和心臟指數(CI),其他患者如術中未放置肺動脈漂浮導管,則留取中心靜脈血氣檢測中心靜脈血氧飽和度(ScvO2)。血流動力學指標采集:患者手術當日清醒后鎮靜前安靜狀態下和達到滿意鎮靜深度后0.5 h內分別記錄患者的血壓、心率、SvO2/ScvO2和CI。記錄患者術后的機械通氣時間、ICU停留時間、術后心臟功能、并發癥和出院存活情況。總機械通氣時間(h)=經氣管插管機械通氣時間+無創機械通氣時間。
1.4 統計學方法 采用SPSS 16.0進行統計學處理。符合正態分布的計量資料以均數±標準差(±s)表示,2組間比較采用t檢驗,組內鎮靜前后比較采用配對t檢驗;計數資料采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 患者術后臨床資料比較 2組患者術后心臟功能和低血壓、低心排綜合征、二次氣管插管、再次手術、術后心肌梗死、氣管切開、心包填塞、心臟驟停、腎功能衰竭、出院時死亡發生比例差異均無統計學意義(均P>0.05),見表2。
2.2 鎮靜前后血流動力學指標比較 淺鎮靜組中低心排綜合征12例,留置肺動脈漂浮導管30例,留取合格中心靜脈血氣24例;傳統鎮靜組中低心排綜合征患者10例,留置肺動脈漂浮導管31例,留取合格中心靜脈血氣19例。104例留取SvO2/ScvO2者中淺鎮靜組54例,傳統鎮靜組50例;61例留取CI者中淺鎮靜組30例,傳統鎮靜組31例。
2組內鎮靜后SvO2/ScvO2和CI均較鎮靜前有所上升(P<0.05),但2組間鎮靜前后SvO2/ScvO2、CI比較差異均無統計學意義(P>0.05),見表3。
非低心排綜合征患者中,淺鎮靜組和傳統鎮靜組組內鎮靜后SvO2/ScvO2較鎮靜前升高(P<0.05),但CI變化差別無統計意義(P>0.05);2組間鎮靜前后SvO2/ScvO2、CI差別均無統計學意義(P>0.05),見表4。低心排綜合征患者中,2組內鎮靜后SvO2/ScvO2和CI均升高(P<0.05);2組間鎮靜前后CI比較差異均無統計學意義(P>0.05),鎮靜前淺鎮靜組與傳統鎮靜組SvO2/ScvO2差別無統計學意義(P>0.05),但鎮靜后傳統鎮靜組SvO2/ScvO2較淺鎮靜組升高(P<0.05),見表5。
2.3 2組患者術后機械通氣時間、ICU停留時間比較 淺鎮靜組術后第1次脫機時間、總機械通氣時間和ICU停留時間均短于傳統鎮靜組,術后譫妄發生率低于傳統鎮靜組(P<0.05),見表6。
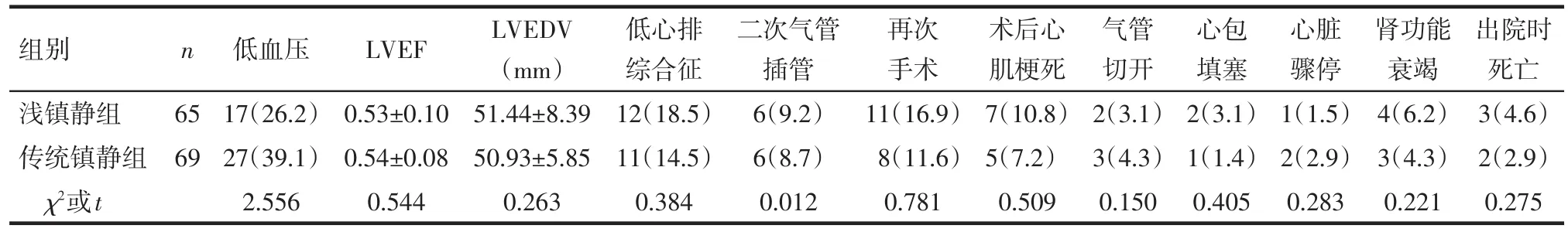
Tab.2 Comparison of the clinical data in postoperative hospitalization between two groups表2 患者術后臨床資料比較
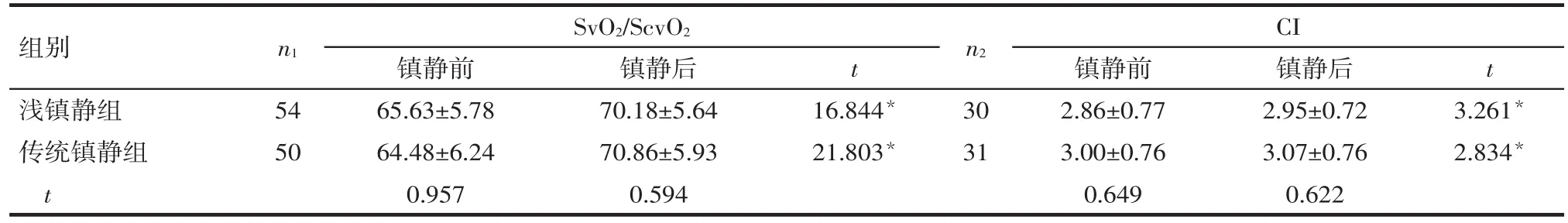
Tab.3 Comparison of postoperative hemodynamic indexes between two groups表3 2組術后血流動力學指標比較
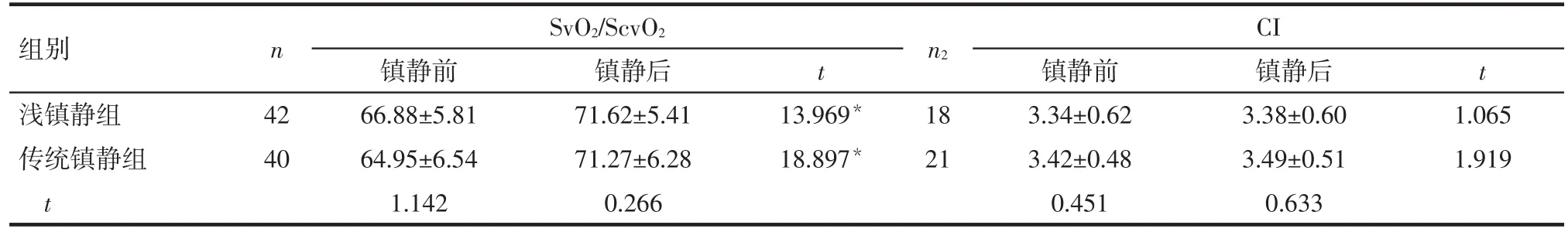
Tab.4 Comparison of the hemodynamic indexes in patients with non-low cardiac output syndrome between two groups表4 非低心排綜合征患者血流動力學比較
Tab.5 Comparison of the hemodynamic indexes in patients with low cardiac output syndrome between two groups表5 低心排綜合征患者鎮靜前后血流動力學比較 (±s)
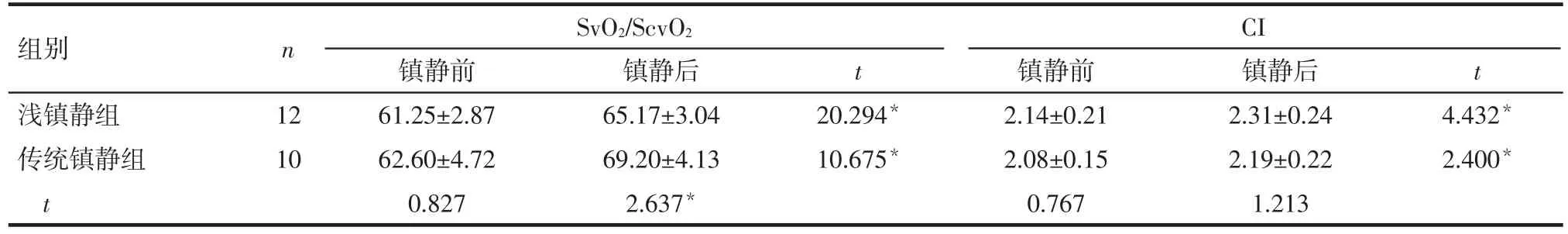
Tab.5 Comparison of the hemodynamic indexes in patients with low cardiac output syndrome between two groups表5 低心排綜合征患者鎮靜前后血流動力學比較 (±s)
*P<0.05
組別淺鎮靜組傳統鎮靜組t n SvO2/ScvO2 CI鎮靜前61.25±2.87 62.60±4.72 0.827鎮靜后65.17±3.04 69.20±4.13 2.637*t t 12 10 20.294*10.675*鎮靜前2.14±0.21 2.08±0.15 0.767鎮靜后2.31±0.24 2.19±0.22 1.213 4.432*2.400*
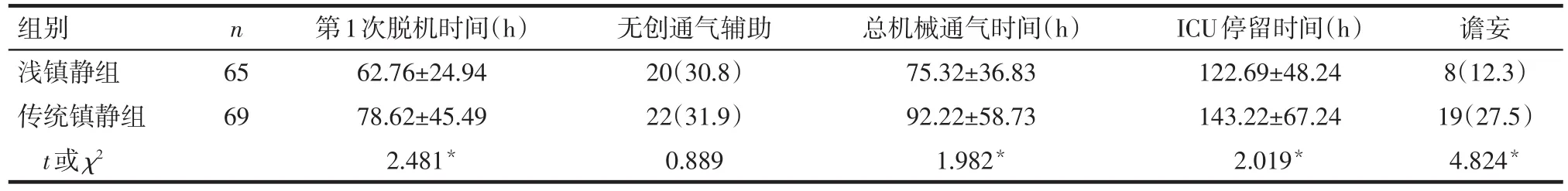
Tab.6 Comparison of the mechanical ventilation,time in intensive care unit,delirium ratio after operation in patients during hospitalization between two groups表6 術后住院期間機械輔助通氣、ICU停留時間、譫妄發生情況的比較
在非低心排綜合征患者中,淺鎮靜組的第1次脫機時間、總機械通氣時間、ICU停留時間均短于傳統鎮靜組(P<0.05),見表7;而在低心排綜合征患者中,淺鎮靜組和傳統鎮靜組間上述指標差異均無統計學意義(P>0.05),見表8。
Tab.7 Comparison of postoperative mechanical ventilation and the time in intensive care unit in patients with non-low cardiac output syndrome between two groups表7 2組中非低心排綜合征患者的機械輔助通氣、ICU停留時間比較 (h,±s)
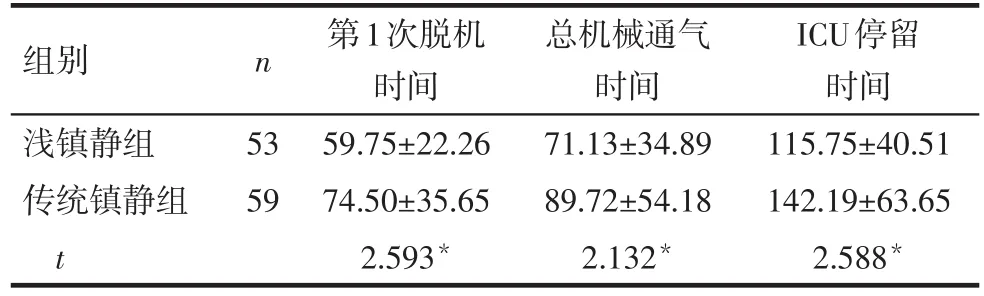
Tab.7 Comparison of postoperative mechanical ventilation and the time in intensive care unit in patients with non-low cardiac output syndrome between two groups表7 2組中非低心排綜合征患者的機械輔助通氣、ICU停留時間比較 (h,±s)
*P<0.05
n組別淺鎮靜組傳統鎮靜組t 53 59第1次脫機時間59.75±22.26 74.50±35.65 2.593*總機械通氣時間71.13±34.89 89.72±54.18 2.132*ICU停留時間115.75±40.51 142.19±63.65 2.588*
Tab.8 Comparison of postoperative mechanical ventilation and the time in intensive care unit in patients with low cardiac output syndrome between two groups表8 2組中低心排綜合征患者的機械輔助通氣、ICU停留時間比較 (h,±s)
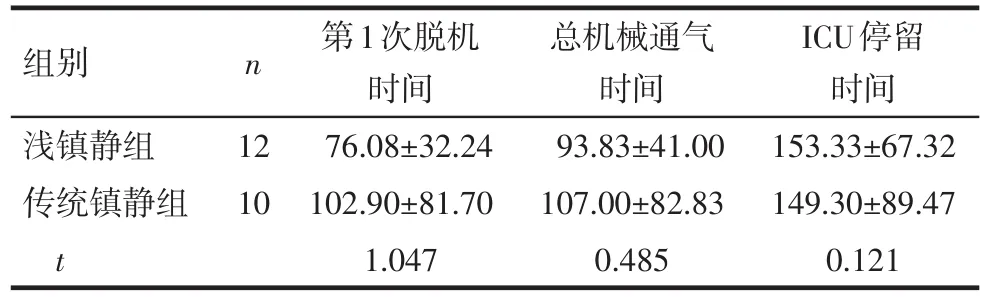
Tab.8 Comparison of postoperative mechanical ventilation and the time in intensive care unit in patients with low cardiac output syndrome between two groups表8 2組中低心排綜合征患者的機械輔助通氣、ICU停留時間比較 (h,±s)
均P>0.05
n組別淺鎮靜組傳統鎮靜組t 12 10第1次脫機時間76.08±32.24 102.90±81.70 1.047總機械通氣時間93.83±41.00 107.00±82.83 0.485 ICU停留時間153.33±67.32 149.30±89.47 0.121
3 討論
心臟外科成人患者普遍病情重、術前合并癥多、手術時間長、操作復雜、創傷大,多數手術還需要體外循環支持,術后心血管和其他并發癥的發生率較高,患者需要較長時間的呼吸機輔助支持。因此心臟術后機械通氣患者需要鎮靜鎮痛治療已形成專家共識[1]。2013年美國危重病醫學會頒布了《重癥監護病房成人疼痛、躁動和譫妄處理臨床實踐指南》,推薦如沒有臨床禁忌證,建議對危重癥患者實施淺水平鎮靜而非深度鎮靜[2]。故淺鎮靜策略被臨床廣泛接受并應用,對于心臟術后重癥患者的鎮靜方式亦引發了深入討論。
低心排綜合征是指心內直視術后早期原發心肌損害所致的心臟泵功能低下,伴有周圍組織低灌注狀態,是導致患者術后早期死亡的主要原因之一,因此有必要對低心排綜合征患者進行亞組分析。本研究顯示,淺鎮靜組和傳統鎮靜組術后血流動力學指標SvO2/ScvO2、CI鎮靜前比較沒有明顯差異。在亞組分析時,對于低心排綜合征患者,傳統鎮靜組鎮靜后的SvO2/ScvO2高于淺鎮靜組,而在非低心排患者中未發現此現象。SvO2/ScvO2是反映氧輸送和組織氧耗量的一個重要指標,連續監測對評估氧輸送和氧耗量的供需平衡很有幫助。如低容量狀態或心功能不全等原因導致心輸出量下降或嚴重貧血時,氧輸送下降,如氧耗量不變,則SvO2/ScvO2降低;在心輸出量平穩、氧輸送穩定時,減少機體氧耗量則SvO2/ScvO2上升[3]。既往研究發現,相比于淺鎮靜,鎮靜深度加強可能對患者的交感神經抑制更充分,更好地降低術后應激反應[4],減輕術后心肌細胞的缺血再灌注損傷,減少躁動和寒戰的發生率,降低機體耗氧量[5],提高SvO2/ScvO2。機體氧耗量的降低對心功能低下患者顯得更為重要。史春芝等[6]的研究顯示,短期深鎮靜策略(接受初始的12 h以深鎮靜RASS評分在-3~-4分之間)為目標的鎮靜治療,用于心臟術后早期是安全和有效的,并沒有增加低血壓、呼吸機相關性肺炎(VAP)發生的風險,也不會延長機械通氣和ICU治療時間[6],同時還降低了心房顫動的風險[7]。故適當加深鎮靜深度可能有利于低心排患者氧合功能的改善。
與傳統鎮靜方式比較,總體上淺鎮靜組顯示出更短的術后機械通氣時間和ICU住院時間,術后譫妄的發生率也更低,與文獻報道相似[8]。本研究亞組分析顯示,非低心排綜合征患者中淺鎮靜策略降低機械通氣時間和ICU住院時間,而在低心排綜合征患者中淺鎮靜策略未顯示出此種優勢。心臟手術后譫妄是一種常見的情況,有研究顯示合并譫妄的心臟手術患者住院時間明顯延長,跌倒發生率和再住院率明顯升高,預后更差[9]。本研究淺鎮靜策略降低心臟術后譫妄發生率可能是其獲益的重要原因之一。此外,有研究顯示機器人輔助下微創冠狀動脈旁路移植(CABG)術后應用右美托咪定更有利于術后血流動力學的穩定和撤離機械通氣[10]。在亞組分析的低心排綜合征患者中淺鎮靜并未顯示出這一優勢。除上述術后早期低心排綜合征患者較深程度鎮靜所帶來的益處外,可能還和淺鎮靜所選用藥物有關。丙泊酚對離體豬心肌收縮功能的研究表明,對正常心肌和起搏誘導的充血性心力衰竭心肌的收縮力,丙泊酚均有負性影響,并能降低β腎上腺素能反應,這些作用在衰竭心肌中表現更明顯[11]。丙泊酚對心肌細胞的抑制作用可能抵消了淺鎮靜所帶來的益處。
本研究顯示,心臟術后非低心排綜合征患者從淺鎮靜策略中受益明顯,術后機械通氣時間和ICU停留時間縮短;而適度地加深鎮靜可能有利于低心排綜合征患者早期心臟功能的恢復。但本組研究病例數量較少,并沒有做盲法研究,也沒有對淺鎮靜所使用藥物進一步區分比較,對于遠期預后的影響還需長期隨訪加以確認。
[1]中國心臟重癥鎮靜鎮痛專家委員會.中國心臟重癥鎮靜鎮痛專家共識[J].中華醫學雜志,2017,97(10):726-733.Chinese Committee of Experts on Heart-intensive sedation and analgesia.The consensus of Chinese experts on heart-intensive sedation and analgesia[J].Natl Med J China,2017,97(10):726-733.doi:10.3760/cma.j.issn.0376-2491.2017.10.003.
[2]Barr J,Fraser GL,Puntillo K,et al.Clinical practice guidelines for the management of pain,agitation,and delirium in adult patientsin the intensive care unit[J].Crit Care Med,2013,41(1):263-306.doi:10.1097/CCM.0b013e3182783b72.
[3]Ducrocq N,Kimmoun A,Levy B.Lactate or ScvO2as an endpoint in resuscitation of shock states?[J].Minerva Anestesiol,2013,79(9):1049-1058.
[4]Hu YF,Chen YJ,Lin YJ,et al.Inflammation and the pathogenesis of atrial fibrillation[J].Nat Rev Cardiol,2015,12(4):230-243.doi:10.1038/nrcardio.2015.101.
[5]Ji F,Li Z,Nguyen H,et al.Perioperative dexmedetomidine improves outcomes of cardiac surgery[J].Circulation,2013,127(15):1576-1584.doi:10.1161/CIRCULATIONAHA.112.000936.
[6]史春芝,孫立平,李玉偉,等.短期深鎮靜策略對心臟術后患者的有效性和安全性評價[J].心肺血管病雜志,2017,36(3):214-217.Shi CZ,Sun LP,Li Y,er al.Shod-course deep sedation strategy in patients aftercardiac surgery [J].Journalof Cardiovascular and Pulmonary Diseases,2017,36(3):214-217.doi:10.3969/j.issn.1007-5062.2017.03.017.
[7]Narisawa A,Nakane M,Kano T,et al.Dexmedetomidine sedation during the nighttime reduced the incidence of postoperative atrial fibrillation in cardiovascular surgery patients after tracheal extubation[J].J Intensive Care,2015,3(1):26.doi:10.1186/s40560-015-0092-5.
[8]李雙玲,王東信,楊拔賢.重癥加強治療病房成人患者淺鎮靜治療進展[J].中華危重病急救醫學,2016,28(1):89-93.Li SL,Wang DX,Yang BX.The progress of light sedation for critically ill adult patients in intensive care unit[J].Chin Crit Care Med,2016,28(1):89-93.doi:10.3760/cma.j.issn.2095-4352.2016.01.019.
[9]Mangusan RF,Hooper V,Denslow SA,et al.Outcomes associated with postoperative delirium after cardiac surgery[J].Am J Crit Care,2015,24(2):156-163.doi:10.4037/ajcc2015137.
[10]Torbic H,Papadopoulos S,Manjourides J,et al.Impact of a protocol advocating dexmedetomidine over propofol sedation after robotic-assisted direct coronary artery bypass surgery on duration of mechanical ventilation and patient safety[J].Ann Pharmacother,2013,47(4):441-446.doi:10.1345/aph.1S156.
[11]Hebbar L,Dorman BH,Clair MJ,et al.Negative and selective effects of propofol on isolated swine myocyte contractile function in pacing-induced congestive heart failure[J].Anesthesiology,1997,86(3):649-659.

