物質結構與性質(必修+選修)模擬試題
■鄭州外國語學校 劉俊可
1.短周期元素X、Y、Z、W在元素周期表中的相對位置如下所示。已知YW的原子序數之和是Z的3倍,下列說法正確的是( )。
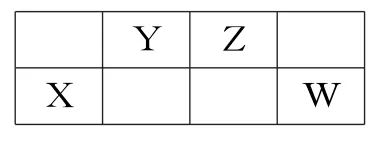
A.原子半徑:X<Y<Z
B.氣態氫化物的穩定性:X>Z
C.Z、W均可與Mg形成離子化合物
D.最高價氧化物對應水化物的酸性:Y>W
2.短周期元素X、Y、Z、W在元素周期表中的相對位置如下所示,其中W原子的質子數是其最外層電子數的三倍,下列說法不正確的是( )。
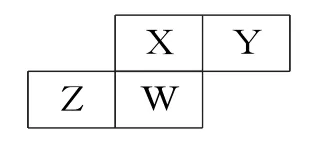
A.原子半徑:W>Z>Y>X
B.最高價氧化物對應水化物的酸性:X>W>Z
C.最簡單氣態氫化物的熱穩定性:Y>X>W>Z
D.元素X、Z、W的最高化合價分別與其主族序數相等
3.下列有關性質的比較,不能用元素周期律解釋的是( )。
A.酸性:H2SO4>H3PO4
B.非金屬性:Cl>Br
C.堿性:NaOH>Mg(OH)2
D.熱穩定性:Na2CO3>NaHCO3
4.碳酸亞乙酯是鋰離子電池低溫電解液的重要添加劑,其結構為。下列有關該物質的說法正確的是( )。
A.分子式為C3H2O3
B.分子中含6個σ鍵
C.分子中只有極性鍵
D.8.6g該物質完全燃燒得到6.72LCO2
5.a、b、c、d為短周期元素,a的M電子層有1個電子,b的最外層電子數為內層電子數的2倍,c的最高化合價為最低化合價絕對值的3倍,c與d同周期,d的原子半徑小于c。下列敘述錯誤的是( )。
A.d元素的非金屬性最強
B.它們均存在兩種或兩種以上的氧化物
C.只有a與其他元素生成的化合物都是離子化合物
D.b、c、d與氫形成的化合物中化學鍵均為極性共價鍵
6.短周期主族元素X、Y、Z、W原子序數依次增大,X原子最外層有6個電子,Y是至今為止發現的非金屬性最強的元素,Z在周期表中處于周期序數等于族序數的位置,W的單質廣泛用作半導體材料。下列敘述正確的是( )。
A.原子最外層電子數由多到少的順序:Y、X、W、Z
B.原子半徑由大到小的順序:W、Z、Y、X
C.元素非金屬性由強到弱的順序:Z、W、X
D.簡單氣態氫化物的穩定性由強到弱的順序:X、Y、W
7.中國科學技術名詞審定委員會已確定第116號元素Lv的名稱為鉝。關于v的敘述錯誤的是( )。
A.原子序數為116
B.中子數為177
C.核外電子數為116
D.Lv元素相對原子質量為293
8.不能作為判斷硫、氯兩種元素非金屬性強弱的依據是( )。
A.單質氧化性的強弱
B.單質沸點的高低
C.單質與氫氣化合的難易
D.最高價氧化物對應的水化物酸性的強弱
9.將 Na、Na2O、NaOH、Na2S、Na2SO4分別加熱熔化,需要克服相同類型作用力的物質有( )。
A.2種B.3種 C.4種 D.5種
10.下列有關物質性質的比較,錯誤的是( )。
A.溶解度:小蘇打<蘇打
B.密度:溴乙烷>水
C.硬度:晶體硅<金剛石
D.碳碳鍵鍵長:乙烯>苯
11.短周期元素甲、乙、丙、丁的原子序數依次增大,甲和丁的原子核外均有兩個未成對電子,乙、丙、丁最高價氧化物對應的水化物兩兩之間能相互反應。下列說法錯誤的是( )。
A.元素丙的單質可用于冶煉金屬
B.甲與丁形成的分子中有非極性分子
C.簡單離子半徑:丁>乙>丙
D.甲與乙形成的化合物均有氧化性
12.甲~庚等元素在周期表中的相對位置如下,己的最高氧化物對應水化物有強脫水性,甲和丁在同一周期,甲原子最外層與最內層具有相同電子數。下列判斷正確的是( )。
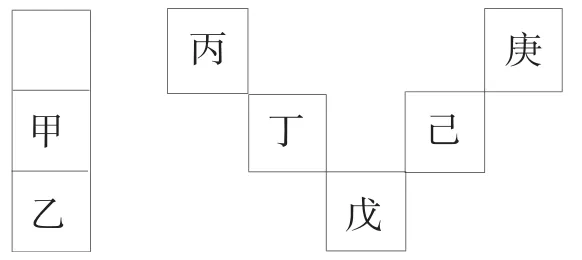
A.丙與戊的原子序數相差26
B.氣態氫化物的穩定性:庚<己<戊
C.常溫下,甲和乙的單質均能與水劇烈反應
D.丁的最高價氧化物可用于制造光導纖維
13.X、Y、Z均為短周期元素,X、Y處于同一周期,X、Z的最低價離子分別為X2-和Z-,Y+和Z-具有相同的電子層結構。下列說法正確的是( )。
A.原子最外層電子數:X>Y>Z
B.單質沸點:X>Y>Z
C.離子半徑:X2->Y+>Z
D.原子序數:X>Y>Z
14.中學化學中很多“規律”都有其適用范圍,下列根據有關“規律”推出的結論正確的是( )。
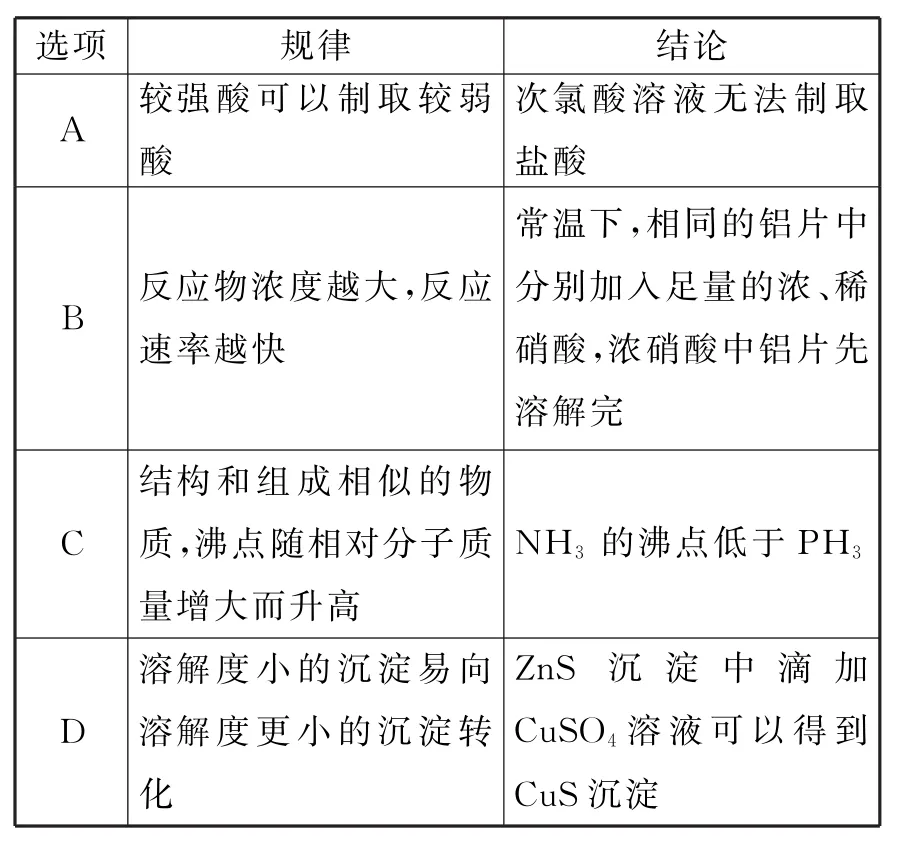
選項 規律 結論A較強酸可以制取較弱酸次氯酸溶液無法制取鹽酸B反應物濃度越大,反應速率越快常溫下,相同的鋁片中分別加入足量的濃、稀硝酸,濃硝酸中鋁片先溶解完C結構和組成相似的物質,沸點隨相對分子質量增大而升高NH3的沸點低于PH3D溶解度小的沉淀易向溶解度更小的沉淀轉化ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀
15.下面為元素周期表的一部分。
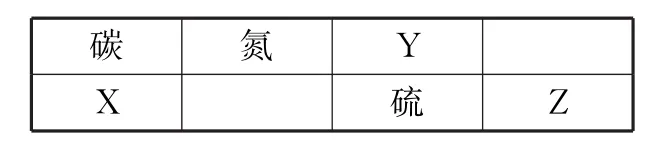
碳氮YX硫 Z
回答下列問題:
(1)Z元素在周期表中的位置為____。
(2)表中元素原子半徑最大的是(寫元素符號)____。
(3)下列事實能說明Y元素的非金屬性比S元素的非金屬性強的是____。
a.Y單質與H2S溶液反應,溶液變渾濁
b.在氧化還原反應中,1molY單質比1molS得電子多
c.Y和S兩元素的簡單氫化物受熱分解,前者的分解溫度高
(4)X與Z兩元素的單質反應生成1mol X的最高價化合物,恢復至室溫,放熱687kJ,已知該化合物的熔、沸點分別為-69℃和58℃,寫出該反應的熱化學方程式:____。
(5)碳與鎂形成的1mol化合物Q與水反應,生成2molMg(O H)2和1mol烴,該烴分子中碳、氫質量比為9∶1,烴分子的電子式為____。Q與水反應的化學方程式為____。
(6)銅與一定濃度的硝酸和硫酸的混合酸反應,生成的鹽只有硫酸銅,同時生成的兩種氣體均由表中兩種氣體組成,氣體的相對分子質量都小于50。為防止污染,將產生的氣體完全轉化為最高價含氧酸鹽,消耗1L 2.2mol·L-1NaOH溶液和1molO2,則兩種氣體的分子式及物質的量分別為____,生成硫酸銅物質的量為____。
16.鍺(Ge)是典型的半導體元素,在電子、材料等領域應用廣泛。回答下列問題:
(1)基態Ge原子的核外電子排布式為[Ar]____,有____個未成對電子。
(2)Ge與C是同族元素,C原子之間可以形成雙鍵、叁鍵,但Ge原子之間難以形成雙鍵或叁鍵。從原子結構角度分析,原因是____。
(3)比較下列鍺鹵化物的熔點和沸點,分析其變化規律及原因:___。
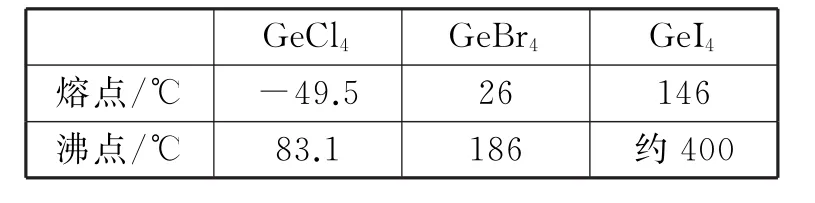
_____________GeCl4________________________________________G_e_B_r4_G_e_I4_熔點/℃_______-49.5____________________2_6_1_4_6_沸點/℃_______83.1________________________1_8_6_約4_0_0
(4)光催化還原CO2制備CH4反應中,帶狀納米Zn2GeO4是該反應的良好催化劑。Zn、Ge、O電負性由大至小的順序是____。
(5)Ge單晶具有金剛石型結構,其中Ge原子的雜化方式為____,微粒之間存在的作用力是____。
(6)晶胞有兩個基本要素:
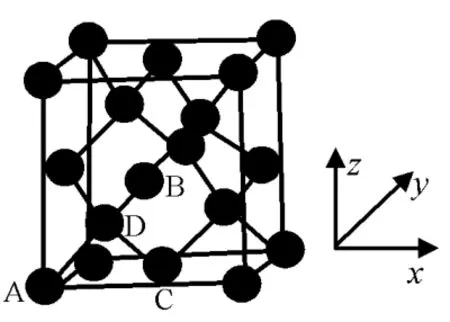
圖1
①原子坐標參數,表示晶胞內部各原子的相對位置,圖1為Ge單晶的晶胞,其中原子坐標參數A為(0,0,0),B為(),C為,0)。則D原子的坐標參數為____。
②晶胞參數,描述晶胞的大小和形狀,已知Ge單晶的晶胞參數a=565.76pm,其密度為____g·cm-3(列出計算式即可)。
17.A、B、C、D為原子序數依次增大的四種元素,A2-和B+具有相同的電子構型;C、D為同周期元素,C核外電子總數是最外層電子數的3倍;D元素最外層有一個未成對電子。回答下列問題:
(1)四種元素中電負性最大的是____(填元素符號),其中C原子的核外電子排布式為____。
(2)單質A有兩種同素異形體,其中沸點高的是____(填分子式),原因是____;A和B的氫化物所屬的晶體類型分別為____和____。
(3)C和D反應可生成組成比為1∶3的化合物E,E的立體構型為____,中心原子的雜化軌道類型為____。
(4)化合物D2A的立體構型為____,中心原子的價層電子對數為____,單質D與濕潤的Na2CO3反應可制備D2A,其化學方程式為____。
(5)A和B能夠形成化合物F,其晶胞結構如圖2所示,晶胞參數a=0.566nm,F的化學式為____:晶胞中A原子的配位數為____;列式計算晶體F的密度(g·cm-3):____。
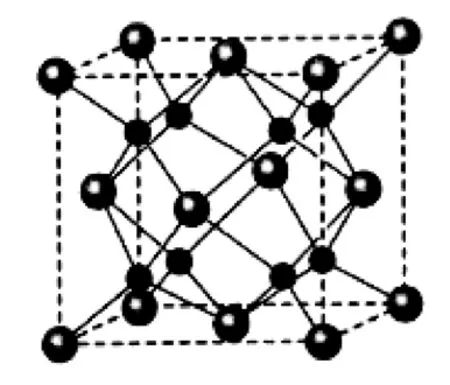
圖2
18.氟在自然界中常以CaF2的形式存在。
(1)下列關于CaF2的表述正確的是____。
a.Ca2+與F-間僅存在靜電吸引作用
b.F-的離子半徑小于Cl-,則CaF2的熔點高于CaCl2
c.陰、陽離子比為2∶1的物質,均與CaF2晶體構型相同
d.CaF2中的化學鍵為離子鍵,因此CaF2在熔融狀態下能導電
(2)CaF2難溶于水,但可溶于含Al3+的溶液中,原因是____(用離子方程式表示)。
已知AlF在溶液中可穩定存在。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子構型為____,其中氧原子的雜化方式為____。
(4)F2與其他鹵素單質反應可以形成鹵素互化物,例如ClF3、BrF3等。已知反應Cl2(g)+3F2(g)══2ClF3(g)ΔH=-313kJ·mol-1,F—F鍵的鍵能為159kJ·mol-1,Cl—Cl鍵的鍵能為242kJ·mol-1,則ClF3中Cl—F鍵的平均鍵能為____kJ·mol-1。ClF3的熔、沸點比BrF3的____(填“高”或“低”)。
19.下列反應曾用于檢測司機是否酒后駕駛:2Cr2+3CH3CH2OH+16H++13H2O--→4[Cr(H2O)6]3++3CH3COOH
(1)Cr3+基態核外電子排布式為____;配合物[Cr(H2O)6]3+中,與Cr3+形成配位鍵的原子是____(填元素符號)。
(2)CH3COOH中C原子軌道雜化類型為____;1molCH3COOH分子中含有σ鍵的數目為____。
(3)與H2O互為等電子體的一種陽離子為____(填化學式);H2O與CH3CH3OH可以任意比例互溶,除因為它們都是極性分子外,還因為____。
20.X、Z、Q、R、T、U分別代表原子序數依次增大的短周期元素。X和R屬同族元素,Z和U位于第ⅦA族,X和Z可形成化合物XZ4,Q基態原子的s軌道和p軌道的電子總數相等,T的一種單質在空氣中能夠自燃。
請回答下列問題:
(1)R基態原子的電子排布式是____。
(2)利用價層電子對互斥理論判斷TU3的立體構型是____。
(3)X所在周期元素最高價氧化物對應的水化物中,酸性最強的是____(填化學式);Z和U的氫化物中沸點較高的是____(填化學式);Q、R、U的單質形成的晶體,熔點由高到低的排列順序是____(填化學式)。
(4)CuSO4溶液能用作T4中毒的解毒劑,反應可生成T的最高價含氧酸和銅,該反應的化學方程式是____。
21.隨原子序數的遞增,八種短周期元素(用字母x等表示)原子半徑的相對大小、最高正價或最低負價的變化如圖3所示。
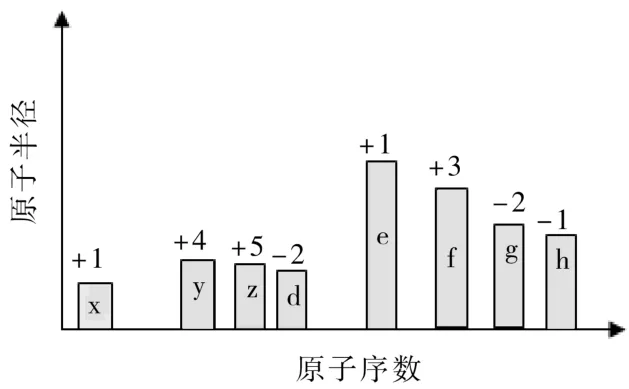
圖3
根據判斷出的元素回答問題:
(1)f在元素周期表的位置是____。
(2)比較d、e常見離子的半徑大小(用化學式表示,下同):___>____;g、h的最高價氧化物對應的水化物的酸性強弱:___>____。
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式:___。
(4)已知1mol e的單質在足量d2中燃燒,恢復至室溫,放出255.5kJ熱量,寫出該反應的熱化學方程式:___。
(5)上述元素可組成鹽R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的燒杯中滴加1mol·L-1NaOH溶液,沉淀的物質的量隨NaOH溶液體積變化如圖4所示。
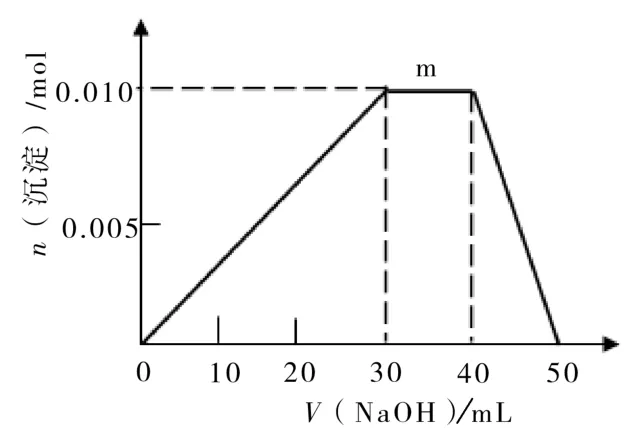
圖4
①R離子濃度由大到小的順序是____。
②寫出m段反應的離子方程式:___。
③若R溶液改加20ML1.2mol·L-1Ba(OH)2溶液,充分反應后,溶液中產生沉淀的物質的量為____mol。

