異煙肼對利福平單耐/多耐藥肺結核患者治療效果的分析
代曉琦 李仁忠 阮云洲 蘇偉 王忠東 王黎霞
耐藥結核病是指對一種或者多種抗結核藥物存在耐藥性的結核病,至少對利福平和異煙肼同時存在耐藥的結核病為耐多藥結核病(multidrug-resistant tuberculosis, MDR-TB)。我國因為MDR-TB患者絕對數大,居世界第二位,而被歸類為MDR-TB高負擔國家。2016年全球新發利福平耐藥結核病患者(rifampin-resistant tuberculosis,RR-TB)10萬例,其中45%的患者分布在印度、中國和俄羅斯,約25萬例患者死于MDR/RR-TB[1]。耐藥結核病尤其是MDR-TB的出現,在許多國家已成為重大的公共衛生問題[2]。2013年WHO提出將RR-TB與MDR-TB患者統一登記管理,使用MDR-TB治療方案進行治療[3]。
為了探索建立與社會基本醫療保險(簡稱“醫保”)相結合的醫療機構和疾病預防控制(簡稱“防控”)系統相合作的耐多藥肺結核患者的防控新模式,提高患者的發現率和治愈率,我國從2011年開始開展了中國衛生部-蓋茨基金會結核病防治合作項目——醫院與疾控系統合作管理耐多藥肺結核試點研究項目(簡稱“醫防合作子項目”)。2016年依托“醫防合作子項目”研究現場,在進行“MDR-TB患者治療轉歸影響因素的調查分析”的過程中發現,在RR-TB患者中有一類患者對利福平單耐(rifampicin mono-resistant tuberculosis,RMR-TB)/多耐藥(rifampicin poly-drug resistant tuberculosis,RPR-TB)[4],對異煙肼敏感,但這類肺結核患者的治療方案中卻有部分患者并未加用異煙肼。由于異煙肼是抗結核藥物中抗菌活性最強的藥物[5],對于此類肺結核患者在使用MDR-TB治療方案的同時加用異煙肼是否會提高治療成功率,相關研究及報道還較少。因此,本次研究依托于“醫防合作子項目”,探討異煙肼對利福平單耐/多耐藥肺結核患者治療效果的影響,為能夠有效地防控和治療耐藥結核病提供參考依據。
對象和方法
1.患者納入:收集2011年1月1日至2011年12月31日“醫防合作子項目”4個研究地區[內蒙古自治區呼和浩特市(華北)、河南省開封市(華中)、江蘇省連云港市(華東)和重慶市永川區(華西)]確診的利福平單耐/多耐藥的50例肺結核患者資料。50例患者中,治愈21例(42.00%)、完成治療1例(2.00%)、失敗12例(24.00%,1例無法使用有效治療方案)、死亡3例(6.00%)、丟失12例(24.00%)、未評估1例(2.00%)。
2.患者分組:50例利福平單耐/多耐藥肺結核患者中,剔除14例丟失、未評估、無法使用有效治療方案的患者,對其余36例患者的臨床資料進行分析。其中11例(30.56%)患者在接受治療后3~4個月時加用了異煙肼(治療方案:3~6Am-Lfx-H-PZA-EMB/9~12 Lfx-H-PZA-EMB;簡稱“異煙肼組”),25例(69.44%)未加用異煙肼(治療方案:6 PZA-Am (Cm)-Lfx(Mfx)-PAS(EMB)-Pto/18 PZA-Lfx(Mfx)-PAS(EMB)-Pto;簡稱“標準組”)。兩組患者的基本情況差異均無統計學意義(P值均>0.05),具體見表1。
3.兩組患者的耐藥情況:傳統藥物敏感性試驗(簡稱“藥敏試驗”)結果顯示,納入分析的36例肺結核患者中有8種耐藥譜,異煙肼組的患者中有6種耐藥譜系,標準組的患者中有8種耐藥譜系。異煙肼組耐藥率較高的分別為耐R(36.36%)、耐R+S+Ofx(18.18%)和耐R+EMB+S+Ofx(18.18%),無耐R+Ofx及耐R+S+Km者;標準組耐藥率較高的分別為耐R(48.00%)、耐R+S(12.00%)、耐R+EMB(12.00%)。具體見表2。

表1 研究對象基本信息在兩組患者中的分布情況
注a:采用Fisher精確概率法檢驗
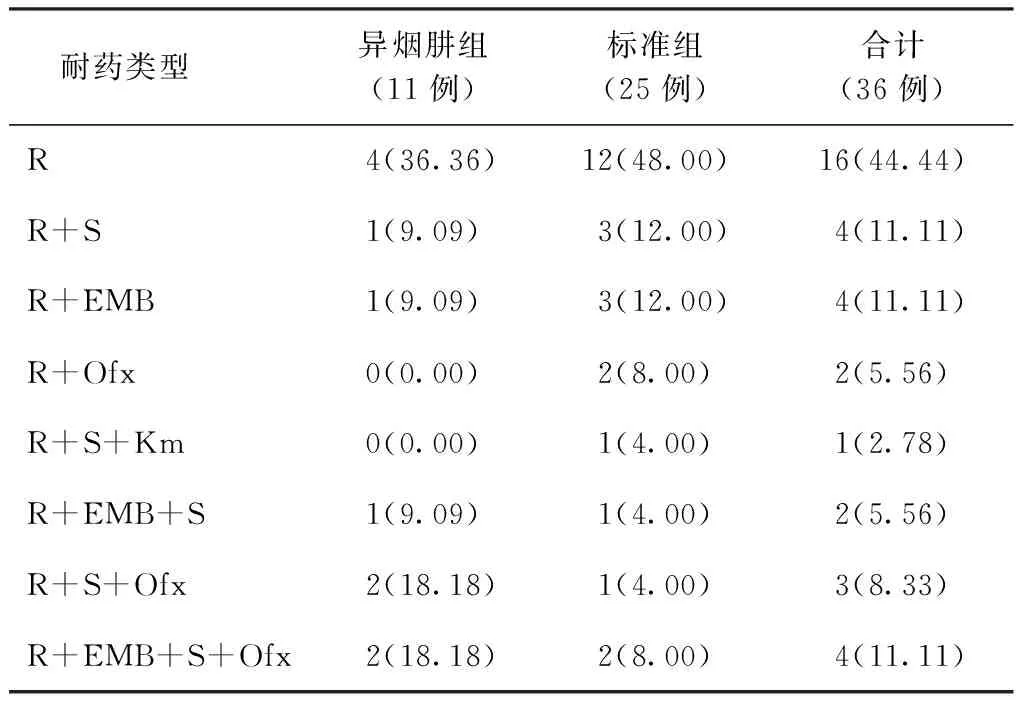
表2 不同耐藥譜在兩組患者中的分布情況
注括號外數值為“患者例數”,括號內數值為“耐藥率(%)”
4.調查設計及問卷調查:在對“醫防合作子項目”治療的所有患者進行“MDR-TB患者治療轉歸影響因素”的調查分析時,通過咨詢結核病防控領域、統計學領域專家和預調查,設計完成了《利福平耐藥肺結核患者治療情況調查表》,調查表內容包括患者基本信息、既往史、治療情況和藥物不良反應發生情況等,并使用該問卷收集患者隊列數據。選擇有結核病控制和臨床經驗的專業人員作為現場調查人員,在調查前統一進行培訓;調查過程中,及時核查漏缺項,并就患者治療期間治療情況與醫療機構信息系統中的記錄進行核對。問卷核對后,采用雙錄入的方式錄入EpiData 3.1數據庫,并抽取10%問卷進行復核。問卷有效率為100%,本研究中的利福平單耐/多耐藥的所有患者數據均來源于此問卷調查。
5. 利福平耐藥的診斷:應用基因芯片和傳統藥敏試驗對在疾病預防控制中心(簡稱“疾控中心”)和醫院診斷為涂片陽性的肺結核患者進行一線、二線抗結核藥物的耐藥性檢測。
6.患者的治療方案:若患者基因芯片快速診斷結果為利福平耐藥,則在傳統藥敏試驗結果報告之前,可以對耐多藥肺結核疑似患者采用由國產抗結核藥物組成的WHO推薦使用的MDR-TB標準化治療方案[6 PZA-Am (Cm)-Lfx(Mfx)-PAS(EMB)-Pto/18 PZA-Lfx(Mfx)-PAS(EMB)-Pto]進行治療,待傳統藥敏試驗結果報告后再進行治療方案的調整;但若兩者結果不一致,則需經國家參比實驗室復核后再行調整,如果證實為耐利福平肺結核患者,則改為加用異煙肼的治療方案(3~6Am-Lfx-H-PZA-EMB/9~12 Lfx-H-PZA-EMB)[2],如果治療3個月(注射期)痰菌陰轉(連續2次痰涂片和培養陰性,間隔至少30 d)則繼續9個月的非注射期治療;否則,需再次做痰培養、菌種鑒定和藥敏試驗,同時繼續注射期治療直至滿6個月,若此次藥敏試驗結果顯示異煙肼耐藥者,則再按MDR-TB方案處理;若為異煙肼敏感者,則仍按加用異煙肼的方案治療直至滿12個月。但由于傳統藥敏試驗結果報告和國家參比實驗室復核的時間較長,很多利福平單耐/多耐藥肺結核患者并未加用異煙肼治療,故本調查中此類患者的治療方案出現了加用異煙肼和未加用兩種現象。國產抗結核藥物的種類和劑量[6]詳見表3。
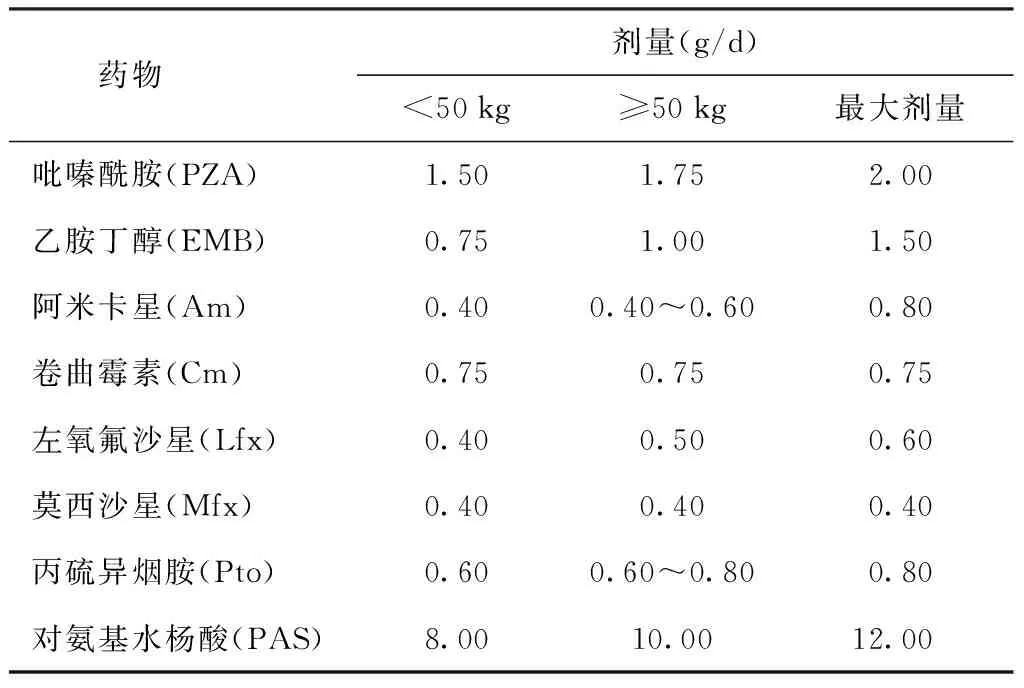
表3 研究對象所用國產抗結核藥物的種類和劑量
7.治療轉歸:截至2014年10月底,納入項目的患者全部完成治療療程。治療結果包括:治愈、完成治療、失敗、 死亡、丟失和未評估;治療結果定義見WHO發布的《結核病定義和報告框架(2013修訂版)》[7]。治愈和完成治療的患者視為治療成功。
8.統計學分析:建立EpiData數據庫,使用SAS 9.3軟件對數據進行統計分析。基本情況采用描述性分析,計數資料采用Fisher精確概率檢驗,檢驗水準為α=0.05。
結 果
1. 兩組患者藥物不良反應的發生情況:異煙肼組患者藥物不良反應發生率[54.55%(6/11)]低于標準組[60.00%(15/25)],但差異無統計學意義(Fisher精確概率檢驗,P=1.000),詳見表4。
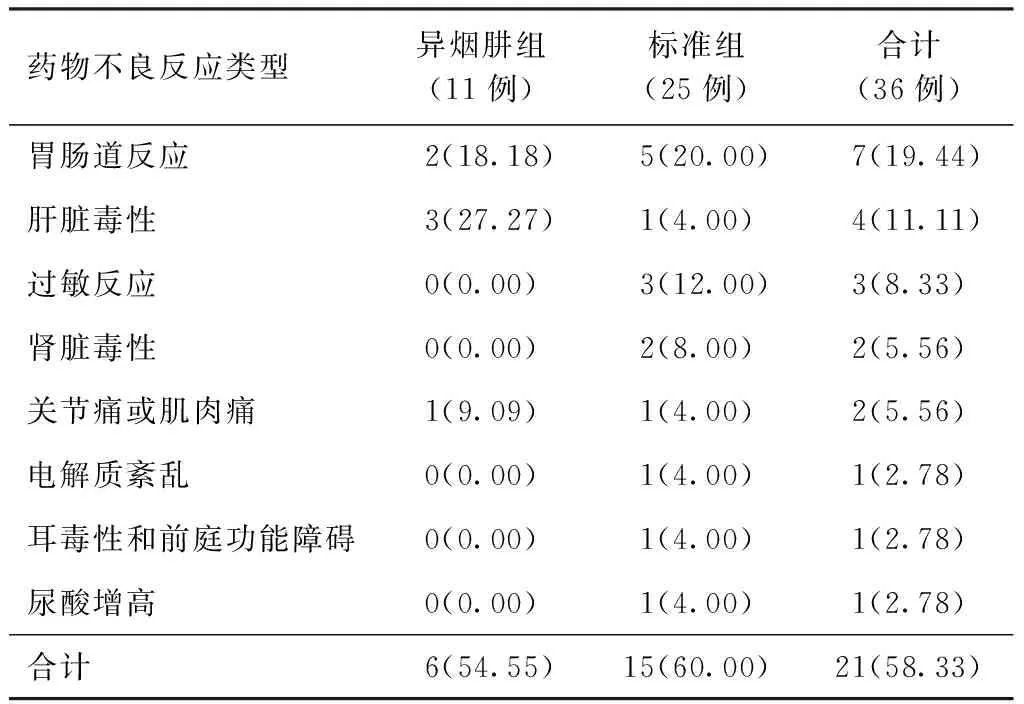
表4 藥物不良反應類型在兩組患者中的分布情況
注括號外數值為“患者例數”,括號內數值為“發生率(%)”
2.治療結果:36例患者中,治療成功患者22例(61.11%),其中治愈21例(58.33%)、完成治療1例(2.78%);失敗11例(30.56%)、死亡3例(8.33%)。異煙肼組與標準組患者的治療結果差異有統計學意義(P=0.016),異煙肼組患者治療成功的比率(90.91%)較高,見表5。
討 論
在2016年之前的全球結核病報告中,耐藥結核病負擔的估算多關注于MDR-TB。2016年開始,WHO指出RR-TB患者(包括了所有對利福平耐藥的情況,即單耐藥、耐多藥、多耐藥以及廣泛耐藥)[7],無論是否耐其他抗結核藥物,都需要使用MDR-TB治療方案[1, 7];加之WHO曾報道80%以上的RR-TB患者也同時對異煙肼耐藥,說明大多數的RR-TB患者為MDR-TB患者[8];同時我國耐藥基線調查報告也顯示,86%的RR-TB患者為MDR-TB[9];因此,MDR-TB患者和RR-TB關系緊密。根據2014年WHO伙伴手冊的相關內容[10],利福平耐藥與異煙肼耐藥呈明顯相關性,在快速診斷技術確定利福平耐藥后,可及時予以MDR-TB治療方案。但由于異煙肼是在抗代謝研究中發現的一種結構簡單的藥物,具有對結核分枝桿菌高特異性的抗菌活性,是抗結核藥物中抗菌活性最強的藥物[5],如果未能明確是否對異煙肼耐藥而直接舍棄使用,很可能會影響患者的治療效果;另外,對于利福平單耐/多耐藥肺結核患者在加用異煙肼后是否會提高治療成功率,相關研究及報道還較少。因此本研究針對此問題進行研究分析。

表5 兩組患者治療結果比較
注a:Fisher精確概率法檢驗;治療成功=治愈+完成治療
研究中使用基因芯片檢測發現的耐利福平肺結核患者在傳統藥敏試驗結果出來之前,首先作為耐多藥肺結核患者采用MDR-TB標準化治療方案,在確診為耐利福平肺結核患者后根據情況改用12~18個月的單耐利福平抗結核治療方案[2];本次研究中,異煙肼組和標準組的患者基本信息、藥物不良反應發生情況的差異均無統計學意義,說明兩組患者具有可比性,且治療過程中,是否加用異煙肼并不會增加藥物不良反應的發生。同時,研究數據顯示,在患者診斷為利福平單耐/多耐藥肺結核時,改用含有異煙肼的相應治療方案后,這部分患者的治療成功率(90.91%)明顯高于繼續使用MDR-TB治療方案的患者(48.00%),失敗率(0.00%)明顯低于未加用組(44.00%),提示加用異煙肼能夠明顯改善此類患者的治療效果,建議在不能確定患者是否對異煙肼耐藥的情況下,可以考慮加用異煙肼,或在患者確診利福平單耐/多耐藥時及時加用異煙肼進行治療,以確保治療效果。
有研究顯示,加大異煙肼的使用劑量,可以使患者單位體積內抗結核藥物的血藥濃度增加,殺菌和抑菌的效果也能隨之提升,改善治療效果[11];針對復治患者,由于之前已經接受過包括異煙肼的治療方案而未能成功,可能也與劑量不夠有關,提高藥物劑量是改善治療效果的一個研究方向[12-13];也有研究指出,因為異煙肼耐藥的水平低于標準方案用藥后的血清水平峰值,因此使用大劑量異煙肼對其治療有效[14],其效果依賴于使用劑量[15]。本研究未對患者使用異煙肼后的血藥濃度進行檢測是本次研究的一個局限,希望進一步研究在血藥濃度監測下提高異煙肼的治療效果,及增加可使用異煙肼的患者數量。
本研究中36例患者中有8種耐藥譜,耐藥譜結果顯示出多態性與復雜性。其中比例較高的有耐R(44.44%)、耐R+S(11.11%)、耐R+EMB(11.11%),與相關文獻相近[16]。異煙肼組耐藥率較高的為耐R(36.36%)、耐R+S+Ofx(18.18%)和耐R+EMB+S+Ofx(18.18%),無耐R+Ofx及耐R+S+Km者;標準組耐藥率較高的為耐R(48.00%)、耐R+S(12.00%)、耐R+EMB(12.00%)。提示兩組患者的耐藥譜還是存在一定的差異,可參考耐藥譜制定更有針對性的治療方案,以提高治療效果。
本次研究僅有36例患者的數據納入分析,例數偏少,代表性有一定局限,統計學分析可能出現偏差。且本次研究對象中僅11例患者的治療方案加用了異煙肼,加用時間集中在接受治療后的3~4個月,造成加用異煙肼的比例偏小、加用時間不夠及時,考慮與傳統藥敏試驗及國家參比實驗室復核后確診為單耐利福平的用時較長有關;還可能與菌株在運輸和保存過程中易造成污染或者損壞,無法最終確定耐藥情況有關。但由于目前相關研究還較少,本研究結果提示了應重視RR-TB患者治療方案的及時調整,在不確定是否耐異煙肼的情況下,可以考慮治療初期加用異煙肼,待明確耐藥譜后再調整,對于今后的研究具有參考價值。
[1] World Health Organization. Global tuberculosis report 2016. Geneva:World Health Organization, 2016.
[2] World Health Organization. Guidelines for the programmatic management of drug-resistant tuberculosis emergency update 2008. Geneva:World Health Organization, 2008.
[3] World Health Organization. Global tuberculosis report 2013. Geneva:World Health Organization, 2013.
[4] 顧瑾, 唐神結. 對利福平耐藥結核病診治的思考. 中國防癆雜志, 2015,37(11):1097-1101.
[5] 譚守勇, 丁秀秀, 譚耀駒, 等. 異煙肼和利福平治療方案對單耐異煙肼或利福平肺結核患者的治療效果. 中華結核和呼吸雜志, 2014,37(12):915-918.
[6] 王宇. 耐多藥肺結核防治管理工作方案. 北京: 軍事醫學科學院出版社, 2012.
[7] 世界衛生組織. 結核病定義和報告框架(2013修訂版). 日內瓦:世界衛生組織, 2014.
[8] World Health Organization. Anti-tuberculosis drug resistance in the world: Third global report. Geneva:World Health Organization, 2004.
[9] 肖東樓. 全國結核病耐藥性基線調查報告. 北京: 人民衛生出版社, 2010.
[10] World Health Organization. Companion handbook to the WHO guidelines for the programmatic management of drug-resistant tuberculosis. Geneva:World Health Organization, 2014.
[11] 陳瑜暉, 鐘球, 周琳, 等. 不同方案治療復治肺結核的療效評價. 廣東醫學, 2017,38(15):2355-2358.
[12] 杜建, 劉宇紅, 李亮, 等. 復治肺結核患者采用不同化療方案的效果評價. 中國防癆雜志, 2016,38(10):850-857.
[13] Chen L, Du J, Li L, et al. Low doses of rifampicin used in new tuberculosis patients correlated to increased frequency of rifampicin-resistance and poorer treatment outcomes. Open J Med Microbiol, 2015,5(2):76-84.
[14] Piubello A, Harouna SH, Souleymane MB, et al. High cure rate with standardised short-course multidrug-resistant tuberculosis treatment in Niger:no relapses. Int J Tuberc Lung Dis, 2014,18(10):1188-1194.
[15] Dooley KE, Mitnick CD, Ann DM, et al. Old drugs, new purpose: retooling existing drugs for optimized treatment of resistant tuberculosis. Clin Infect Dis, 2012,55(4):572-581.
[16] 張天華, 劉衛平, 李妍, 等. 陜西省肺結核耐藥性監測分析. 中國熱帶醫學, 2017,17(3):226-230.

