乙二醛雙氧水氧化萃取制備乙醛酸研究
王 萌,劉少文
(武漢工程大學 化工與制藥學院,湖北 武漢 430073)
乙醛酸(Glyoxylic acid,GA)是最簡單的酮酸,是重要的有機合成中間體。乙醛酸的工業生產方法有乙二醛硝酸氧化法、草酸電解還原法和順酐臭氧氧化法等[1-3]。目前國內多采用硝酸氧化法,國外多采用草酸電解還原法和順酐臭氧氧化法。草酸電解還原法對環境污染較小,但耗電量大,乙醛酸質量不穩定;乙二醛硝酸氧化法,雖然乙二醛價格便宜,但安全性差且設備腐蝕嚴重;順酐臭氧氧化法,雖產品質量好,但投資較大、電耗高。乙二醛雙氧水氧化法成本低、無污染、投資小,不失為生產GA的一種好的途徑。
因為乙二醛特殊的結構,易產生草酸等副產物,傳統方法合成乙醛酸的方法都選擇性較差。與傳統方法相比,反應萃取技術作為一種新興耦合技術能顯著提高選擇性,是一種高效、節能、清潔、安全、可持續發展的化工新技術[4]。通過查閱大量相關于草酸-乙醛酸的萃取分離技術,乙醇酸-乙醛酸的萃取分離技術等文獻,發現萃取劑對乙醛酸選擇效果較好,這充分證實了采用反應萃取合成乙醛酸的可行性[5-7]。利用反應萃取技術合成乙醛酸,其優點在于:可以及時將乙醛酸移出反應相不斷萃入萃取相,維持反應相中產物的濃度小于平衡濃度,就能打破化學平衡推動反應向右進行,提高平衡轉化率及乙醛酸收率;可以有效避免乙二醛過度氧化生成乙二酸,大大簡化后續分離工藝。
1 實驗
1.1 實驗裝置
實驗裝置見圖1。
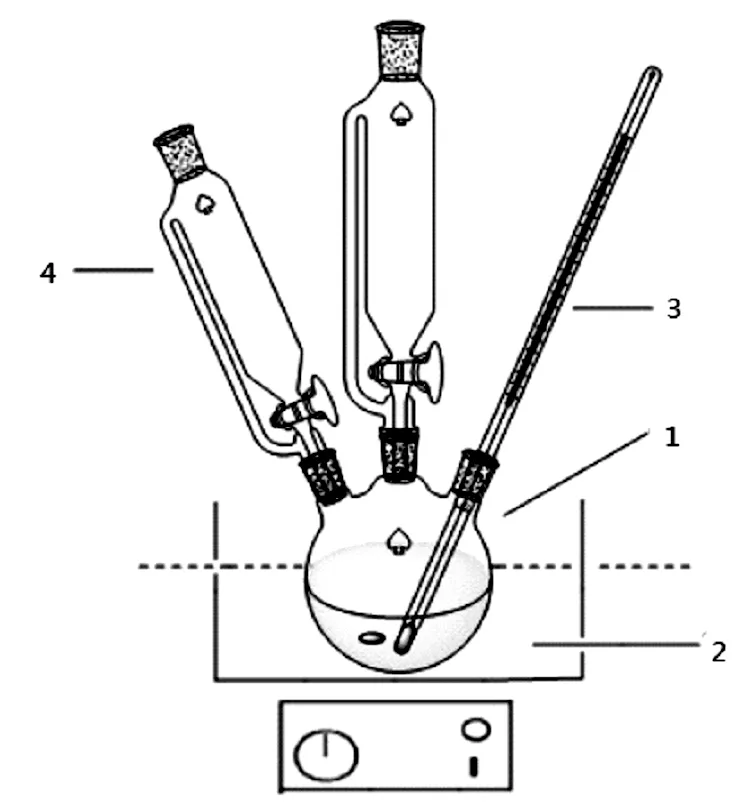
1.三口燒瓶;2.水浴磁力攪拌器;3.溫度計;4.恒壓滴液漏斗圖1 實驗裝置圖
1.2 實驗步驟
1.2.1 乙二醛雙氧水氧化制乙醛酸反應步驟
乙二醛雙氧水氧化反應是在是氮氣保護和無氮氣保護條件下進行的。稱取4.671g硫酸亞鐵,溶于50mL的蒸餾水,置于100mL的滴液漏斗中備用;稱取41.90g30%(質量分數)雙氧水置于另一個100mL滴液漏斗中備用。在四口燒瓶中加入60mL30%(質量分數)的乙二醛,用冰水冷卻,開始同時滴加硫酸亞鐵和雙氧水,保持反應溫度控制在3~8℃,滴加速度控制在2h內滴加完畢。滴加完成后繼續反應3h。在反應時間為10、20、30、60、90、120、180、240、300min時取樣送高效液相色譜進行分析,并計算各組分含量。
1.2.2 乙二醛雙氧水氧化萃取制乙醛酸反應步驟
按照上述的乙二醛雙氧水氧化反應步驟,在反應燒瓶中添加乙二醛的同時按體積比1∶1比例添加三辛胺萃取劑,并以萃取劑與稀釋劑的體積比分別為1∶1~3加入稀釋劑,用冰水冷卻,使其溫度保持在3~8℃。分別反應30、60、120、180min,取反應產物靜置分離,用乙醛酸溶液進行萃洗,再用水進行反萃取,分離,樣品用高效液相色譜進行分析,計算各組分含量。
2 實驗結果與討論
2.1 氧化氣氛對反應的影響
實驗考察了氧化氣氛(即氮氣保護和無氮氣保護)對反應的影響如圖2所示。

(a)主反應;(b)副產物草酸;(c)副產物乙醇酸;(d)副產物甲酸
圖2 氧化氣氛對反應的影響
從圖2可以看出,隨著反應時間的延長,乙二醛轉化率在有無氮氣保護時均呈現上升的態勢,且兩者的轉化率比較接近。但乙醛酸選擇性卻呈現較大的差異,反應開始時乙醛酸選擇性較高,隨著反應進行逐步降低,反應100min后選擇性逐步增加。在有氮氣保護的條件下乙醛酸選擇性比無氮氣保護時高5個百分點,這說明氮氣保護有利于乙醛酸的生成。
氧化氣氛對草酸選擇性的影響似乎不大,即有無氮氣保護時草酸選擇性變化不大,隨著反應時間增加,草酸選擇性先增加,反應100min后呈下降趨勢,這說明通過控制反應在較短或較長時間時可以抑制副產物草酸的生成。氮氣保護可以在一定程度上抑制乙醇酸的生成,但隨著反應時間的延長,有利于乙醇酸的生成,即乙醇酸選擇性明顯增加。氧化氣氛對甲酸選擇性的影響則比較復雜,反應時間較短時,氮氣保護有利于甲酸副產物的生成,反應時間較長時,氮氣保護可以抑制甲酸的生成。
2.2 萃取劑對反應的影響
氧化體系中各組分在三辛胺萃取劑中的分配系數如表1所示。
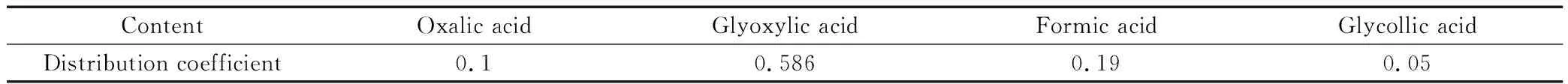
表1 各組分分配系數
由表1可以看出,三辛胺對羧酸的萃取效果乙醛酸>甲酸>草酸>乙醇酸,也印證了加入萃取劑能讓反應產生的乙醛酸進入有機相,避免其被氧化成其他副產物,這樣就能提高乙醛酸的選擇性和乙二醛的轉化率。
乙二醛雙氧水氧化反應體系添加三辛胺萃取劑的影響如圖3所示。
從圖3可以看出,當雙氧水氧化乙二醛添加三辛胺萃取劑時,乙乙二醛轉化率和乙醛酸選擇性顯著增加,反應180min后乙二醛轉化率由75.37%提高到79.61%,乙醛酸選擇性由56.07%提高到67.52%,萃取反應效果十分顯著。從前面的反應產物在三辛胺萃取劑中的分配系數可以得知,該萃取劑對乙醛酸具有較高的分配系數,隨著反應的進行,反應生成的乙醛酸進入有機相,一方面避免乙醛酸進一步氧化生成其它有機酸,另一方面在反應的同時進行了產物分離,這樣在提高轉化率的同時,也提高了乙醛酸的選擇性,同時大大減少了副產物的產生。
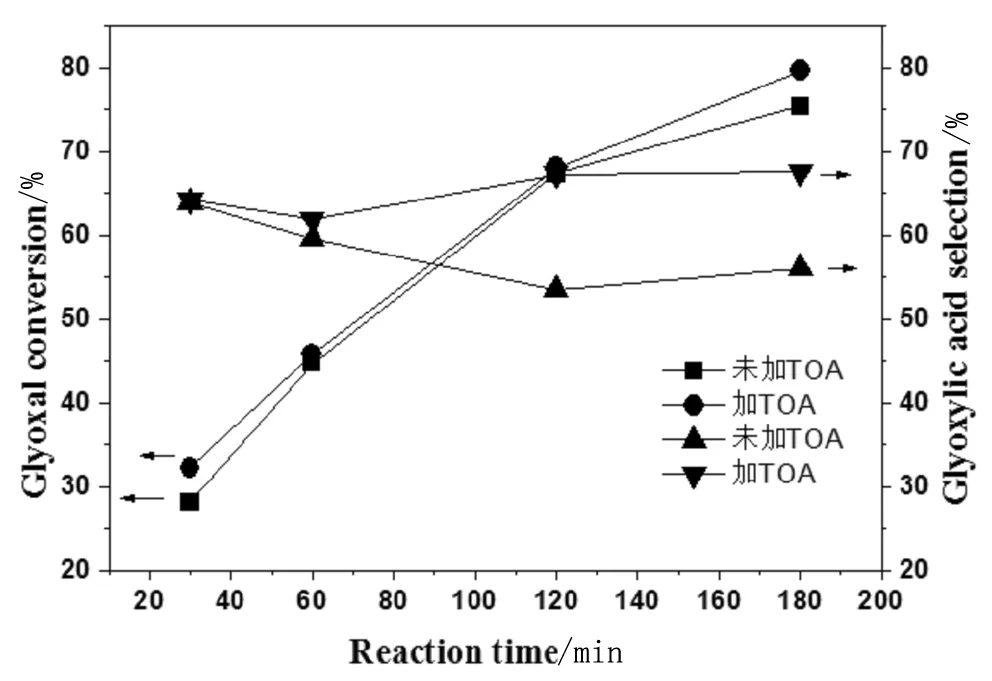
圖3 萃取劑對萃取氧化反應的影響
由于乙二醛雙氧水氧化萃取反應受氧化氣氛的影響,所以考察了氧化氣氛對萃取反應的影響如圖4所示。
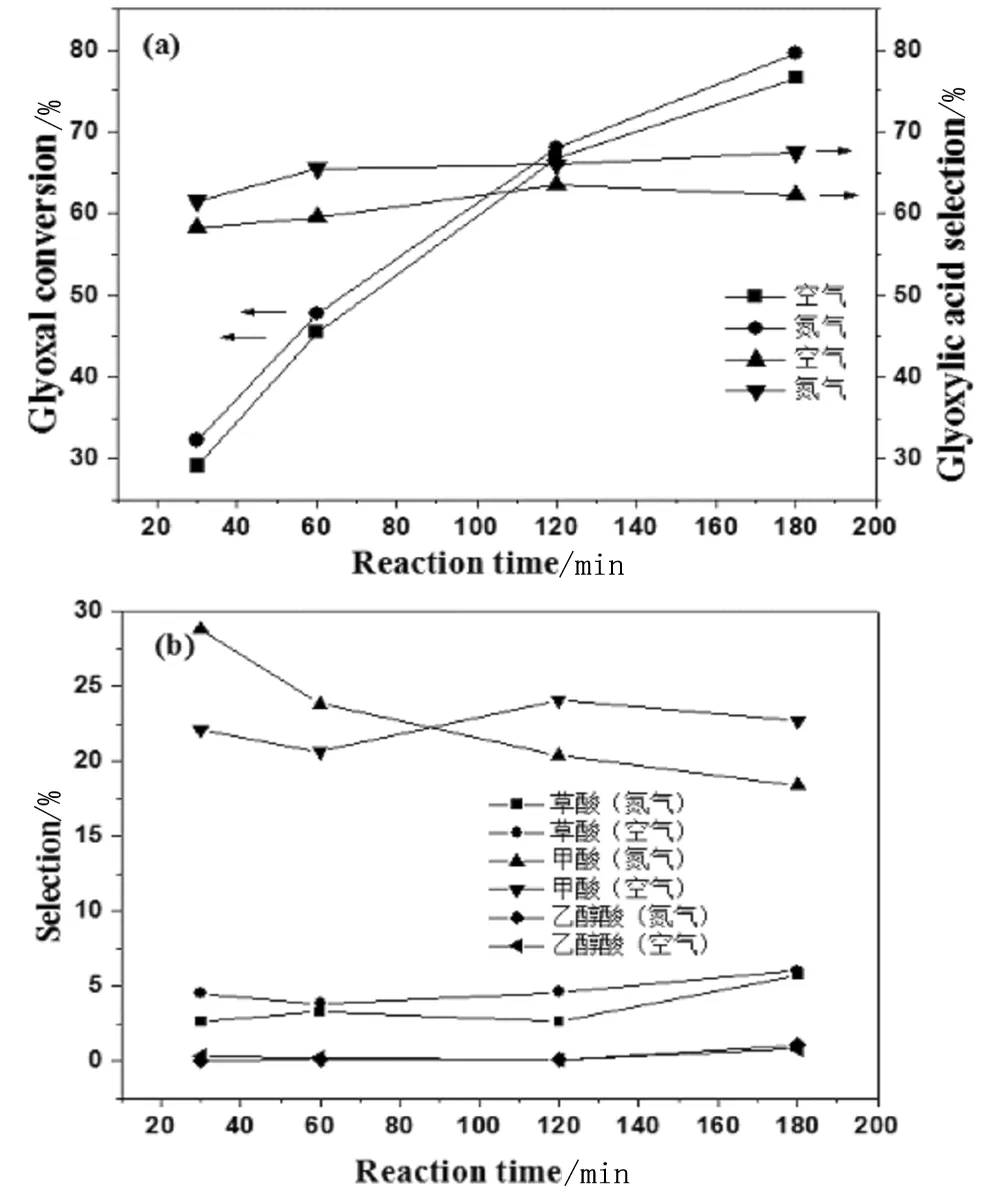
(a)主反應;(b)副反應;圖4 氧化氣氛對萃取反應的影響
由圖4可以看出,隨著反應時間的延長,乙二醛轉化率和乙醛酸選擇性在有無氮氣保護時均呈現上升的態勢,且在有氮氣保護的條件下乙二醛轉化率和乙醛酸選擇性都比無氮氣保護時高,這說明在雙氧水萃取氧化體系中氮氣保護也有利于乙醛酸的生成。
而在雙氧水萃取氧化體系中,有氮氣保護時草酸選擇性比無氮氣保護時低,說明氮氣會在一定程度上抑制副產物草酸的產生,且明顯抑制乙醇酸的生成。氧化氣氛對甲酸選擇性的影響則比較復雜,反應時間較短時,氮氣保護有利于甲酸副產物的生成,反應時間較長時,氮氣保護可以抑制甲酸的生成,這點與雙氧水氧化體系類似。
2.3 稀釋劑種類對反應的影響
稀釋劑種類對分配系數的影響如表2所示,對反應的影響如表3。
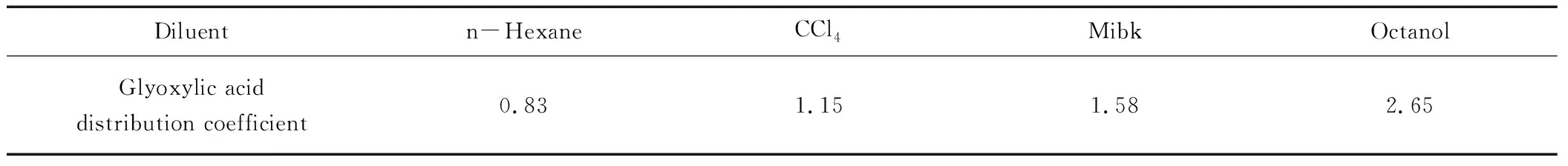
表2 反應萃取中稀釋劑對分配系數的影響
三辛胺∶稀釋劑=1∶1(V/V);T=3~8℃;通N2
由表2可以看出,在不同性質的稀釋劑中,三辛胺萃取乙醛酸的分配比相差很多,稀釋劑效應十分顯著。通過比較不同稀釋劑參加的氧化萃取反應參加萃取反應中乙醛酸的分配系數,可以發現稀釋劑的效果正辛醇>甲基異丁基酮>四氯化碳>正己烷。
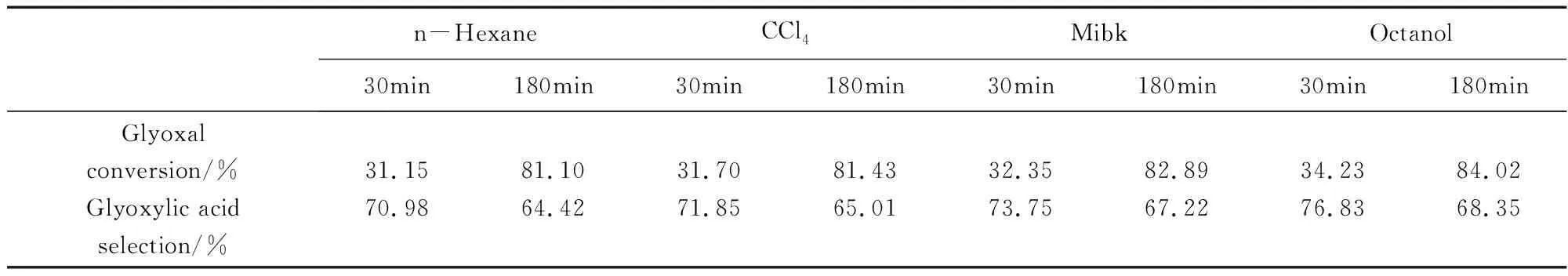
表3 稀釋劑種類對萃取氧化反應的影響
由表3可以看出,加入稀釋劑乙二醛轉化率和乙醛酸選擇性明顯增加。這是因為TOA是一種對羧酸比較有效的萃取劑,但由于其操作性能不夠好,需要加以稀釋,選擇一種好的稀釋劑可以改善萃取操作性能,還會產生很強的稀釋劑效應,改善萃取劑的的萃取性能,提高其萃取能力。一般認為稀釋劑的偶極矩、介電常數和溶解度參數是影響萃取平衡,產生稀釋劑效應的主要因素。通常都是用稀釋劑的極性參數、溶劑化作用、電子對的給予能力等來解釋。萃合物與稀釋劑的相互作用能力及其在稀釋劑中的疏溶作用是影響三辛胺萃取羧酸,產生稀釋劑效應的主要因素。通過比較不同稀釋劑參加的氧化萃取反應的乙二醛轉化率和乙醛酸選擇性可以看出反應30min時,正辛醇作為催化劑時,乙二醛的轉化率和選擇性最高;反應180min時,也是正辛醇作為催化劑時,乙二醛的轉化率和選擇性最高。但正辛醇作為稀釋劑反應30min乙二醛的轉化率太低了只有34.23%而反應180min時乙二醛轉化率很高的同時乙醛酸選擇性也不低,因此綜合考慮選擇正辛醇為稀釋劑反應180min為適宜的萃取反應條件。
2.4 萃取劑濃度對反應的影響
萃取劑和稀釋劑的不同配比對反應結果有很大影響,分別取三辛胺與正辛醇的體積比為1∶1,1∶1.5,1∶2和1∶3進行實驗,實驗結果對分配系數的影響如表4所示,對乙二醛轉化率和乙醛酸選擇性的影響如表5所示。

表4 反應萃取中萃取劑濃度對分配系數的影響
T=3~8℃;通N2
根據表4,乙醛酸分配系數隨著萃取劑濃度先升高后降低。這是因為,由于三辛胺是一種分子量高、憎水性很強的叔胺,當稀釋劑中含水量升高時,由于水和三辛胺萃合物的極大的不相溶性,溶解了水的稀釋劑不利于萃合物分子溶解到有機相,使得萃取能力下降,這種現象稱之為疏溶作用,這種疏溶作用越大越不利于萃取。萃合物與稀釋劑的相互作用能力越大及其在稀釋劑中的疏溶作用越小,稀釋劑效應越顯著,越有利于萃取。因此三辛胺濃度越大,其萃取能力越強。但隨萃取反應劑濃度的增大,草酸和乙醛酸的分配系數皆隨之增大,但隨著萃取劑濃度增到到一定程度時,草酸的變化幅度較乙醛酸的變化幅度大,即萃取劑對乙醛酸和草酸的分離能力就降低了,隨即分配系數降低。因此,乙醛酸分配系數隨著萃取劑濃度先升高后降低。
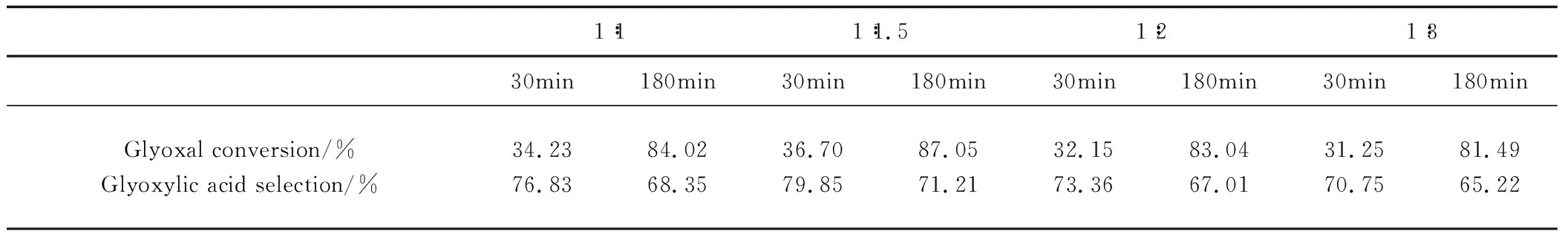
表5 萃取劑濃度對萃取氧化反應的影響
由表5可以看出,TOA與正辛醇的體積比依次為1∶3,1∶2,
1∶1.5和1∶1時,乙二醛的轉化率和乙醛酸的選擇性先增高后降低。這是因為乙醛酸分配系數隨著萃取劑濃度先升高后降低,乙二醛的轉化率和選擇性就隨之改變了。三辛胺與正辛醇體積比為1∶1.5時乙二醛的轉化率和乙醛酸的選擇性最高,當反應30min時乙醛酸的選擇性最高,但此時乙二醛的轉化率很低,而反應180min時,此時乙二醛的轉化率和乙醛酸的選擇性分別為為87.05%和71.21%,因此綜合考慮萃取劑TOA與稀釋劑正辛醇的配比為1∶1.5反應180min為較適宜的實驗條件。
3 結論
通過對乙二醛雙氧水氧化萃取制備乙醛酸過程的研究,考察了各因素對實驗結果的影響,可得出反應的優化實驗條件為:通N2條件下,選用三辛胺為萃取劑劑,正辛醇為稀釋劑,三辛胺與正辛醇的體積比為1∶1.5,在3~8℃下反應3h,乙二醛轉換率為87.05%,乙醛酸選擇性為71.21%。反應設備簡單經濟,反應副產物少,所得產物明顯優于其他傳統工藝,值得進一步推廣應用。
[1] 高會元.乙醛酸生產、應用研究新進展[J].上海化工,2002,27(15):51-54.
[2] 陸軍民.國內乙醛酸衍生產品的現狀與展望(一)[J].精細與專用化學品,2002(6):8-10.
[3] 陳銀生,張新生,戴迎春,等.乙醛酸合成方法最新進展[J].精細與專用化學品,2002,10(1):1617.
[4] 馮 霞,梁曉賢.反應萃取技術的研究現狀[J].精細與專用化學品,2012,32(4):301-304.
[5] 羅 津 A M.萃取手冊[M]. 袁承業,譯.北京:原子能出版社,1988.
[6] 秦 煒,張 英,羅學輝,等.草酸與乙醛酸的萃取分離[J].化工學報,2001(2):135-140.
[7] 張宏耀,秦 煒,戴猷元.乙醇酸與乙醛酸的萃取分離[J].化工學報,2003,54(11):1552-1557.
[8] Waghmare M, Wasewar K, Sonawane S,et al.Natural non-toxic solvents for recovery of picolinic acidby reactive extraction[J].Ind Eng Chem Res,2011,50(23):13526-13537.

