犬惰性角膜潰瘍新的治療分析
曹 悅,董 軼
(芭比堂動物醫院連鎖機構玉泉路總院,北京 石景山 100040)
惰性角膜潰瘍(SCCEDs)或慢性角膜上皮糜爛,是犬的不能通過正常創傷愈合過程的一種慢性角膜上皮缺損多發生于中老年犬,無明顯品種易感性。最早發現這種疾病是在拳師犬的角膜潰瘍中發現。此類角膜潰瘍未經過恰當治療可能會持續數月至1年,是臨床中常見且難治療的一種角膜疾病。
通過對北京芭比堂動物醫院接診的107例患病的犬進行金剛砂車針以及角膜格狀切開術的治療對比分析,我們發現金剛砂車針可以明顯高治愈率,且操作簡單。
1 實驗材料與方法
1.1 實驗樣本 樣本源自2012年1月至2015年7月北京芭比堂動物醫院的107例病例,其中進行金剛砂車針治療的病例50例,進行角膜格狀切開術的病例57例。
1.2 實驗方法 將患犬分為兩組,分別對損傷的角膜上皮進行金剛砂車針和角膜格狀切開術,并且同時進行自家血清與角膜上皮生長因子局部點眼的治療,每7天來院進行復查。
2 實驗結果
在治療的107例病例中,其中進行金剛砂車針治療50例,通過1~4次的治療,角膜潰瘍愈合47例,未愈合而最終進行結膜瓣遮蓋術3例,成功率為94%。對于通過金剛砂車針結合藥物治療而使角膜潰瘍愈合的病例,平均需要進行的金剛砂車針治療操作次數為1.4次,平均治療時間為14.6 d。
進行角膜格狀切開術治療57例,通過1~4次的治療,角膜潰瘍愈合47例,未愈合而最終進行了結膜瓣遮蓋術10例,成功率為82%。對于通過角膜格狀切開術結合藥物治療而使角膜潰瘍愈合的病例平均需要進行的角膜格狀切開術治療操作次數為1.51次,平均治療時間為14.94 d。
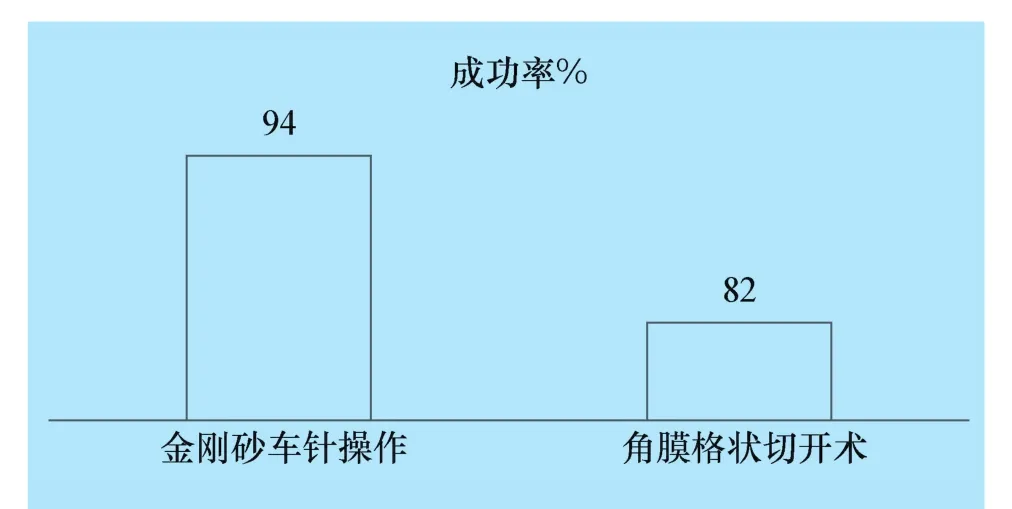
圖1 金剛砂車針與角膜格狀切開術治療頑固性角膜潰瘍的成功率對比
對患頑固性角膜潰瘍的動物的性別及年齡進行統計,107例犬患有頑固性角膜潰瘍的動物中,雄性68只,雌性39只,患犬平均年齡為10.26歲。
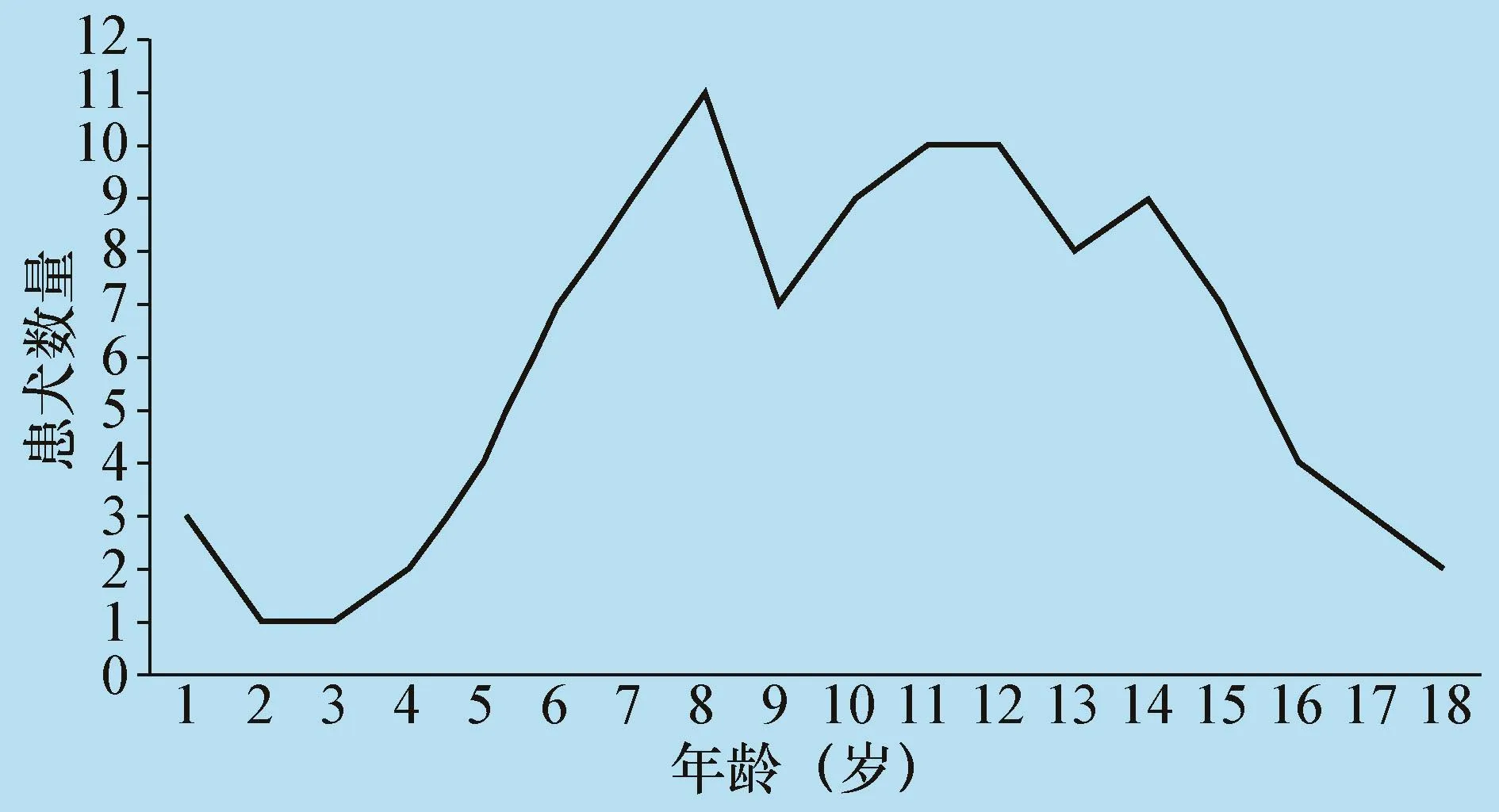
圖2 患有頑固性角膜潰瘍犬的年齡分布
3 討論
惰性角膜潰瘍(SCCEDs)是犬的不能通過正常創傷愈合過程的1種慢性角膜上皮缺損,多發生于中老年犬,無明顯品種易感性。最早發現這種疾病是在拳師犬的角膜潰瘍中。此類角膜潰瘍未經過恰當治療可能會持續數月,是臨床中常見且難治療的1種角膜疾病[1-4]。
3.1 病理學因素 SCCEDs的病理學還不十分明確,但是在一些形態學和功能學的異常已經在這類疾病中有過報道。病理研究顯示,角膜上皮層與基質層的連接處功能或形態異常與缺損[1-3]。在電鏡下看到角膜上皮基底膜與基質層連接的片段和纖維部分缺損,經常會出現一個由膠原纖維和異形纖維組織構成的一個薄且透明的非細胞層區域[1-3]。基質纖維素增生,血管化以及白細胞浸潤有時也會存在。在試驗中,患有SCCEDs的病例中,沒有發現在角膜的損傷中進一步發展到淺層基質透明化區域,這說明基質的改變可能也是發生SCCEDs的潛在病理性原因。
在患有SCCEDs的病例中,在缺損的角膜邊緣存在密集的異常P物質神經叢和與降鈣血素基因相關的免疫反應性肽神經纖維。而這個神經叢的改變在犬患有角膜上皮缺損的前4周中是不存在的,這提示了這些基質的改變可能是慢性角膜上皮缺失的原因。在患有SCCEDs的犬中,角膜上皮細胞中P物質神經叢水平被抬高[4]。
基質金屬蛋白酶(MMPs)表達的上升被認為是SCCEDs中潛在引起基底膜缺損的原因。但通過對比模型和實際的SCCEDs患犬中MMP-2和MMP-9的表達,并未發現與SCCEDs有任何明顯的關聯[5]。
在正常犬中,角膜創傷后,角膜上皮開始移行并覆蓋傷口,但在患有SCCEDs的犬中,創口邊緣因為細胞間聯系的缺損而無法遷移覆蓋傷口。研究發現,Slug是Snail家族中負責復制的因子,調節上皮間葉細胞的遷移,它的表達與細胞移行有關,包括細胞膜上皮細胞鈣粘蛋白和β-連環蛋白的內化作用和加強平滑肌α-肌動蛋白,原肌球蛋白和MMPs的表達。在正常犬角膜損傷時,角膜上皮細胞邊界進行移行中,Slug的表達在加強細胞移行上已經被證實,但是在SCCEDs中并未增強。TGFβ能夠增強nail家族的表達,而在SCCEDs的病例中,報道了淚液中的TGFβ的量有降低的現象[6]。總而言之,這些研究顯示,基質層的異常變化是導致SCCEDs病理變化的重要原因。而治療中通過移除異常的基質層而達到的良好療效更是驗證了這一理論。目前還沒有研究證明基底膜的退化是造成SCCEDs的病因,但在大齡犬出現SCCEDs時,需要考慮這種原因。
3.2 SCCEDs的診斷 SCCEDs總是淺表性的損傷。角膜新生血管程度在SCCEDs病例中各不相同,據統計報告顯示,約有58%~64%病例有新生血管的生成[7-8]。在角膜緣相對于角膜正中更容易形成新生血管。疼痛的程度會隨著時間的延長而趨于降低。SCCEDs發病的平均年齡為8~9歲[2,7-8]。同時,青年犬也應該小心排查。
3.3 SCCEDs的治療
3.3.1 角膜格狀切開術 治療SCCEDs最常用的方法是角膜清創術(Epithelial debridement)、角膜格狀切開術,有時單獨使用有時聯合使用。角膜清創術用棉簽從潰瘍中間向潰瘍的四周輻射方向擦拭,正常的角膜上皮組織時無法被擦拭掉的,所以清除掉所有的疏松的上皮,直到擦拭到正常的角膜組織。角膜格狀切開術用彎曲為30度的25 G無菌注射器針頭在角膜表面進行井字形切開。切開深度約0.2 mm左右[9]。
3.3.2 金剛砂車針 金剛砂車針治療在1983年最早報道用于人的角膜治療[10]。后來進一步試驗用于實驗動物兔子的角膜治療,發現其能夠移除角膜上皮細胞和部分基底膜[11]。有研究數據顯示,使用金剛砂車針治療 SCCEDs的治癒率能夠達到94%[12]。最近有研究報道金剛砂車針相對于角膜清創能夠有效降低SCCEDs的復發率。金剛砂車針對比角膜淺層切開術時也能夠有效的降低復發率并且輕度提高角膜愈合后的透明性[13]。
而金剛砂車針是如何提高SCCEDs治癒率的機理目前尚不清楚。之前的研究顯示,金剛砂車針能夠對基底膜造成一些小的創傷,就像拋光打磨了基底膜一樣,這樣使得新生的角膜上皮細胞能夠更好的貼合于基底膜而愈合創口。同時也有理論認為金剛砂車針促進了打磨區域內的蛋白的表達從而導致纖維素生產的增加進而更好的粘合新生的上皮細胞。而金剛砂車針治療的并發癥相對較少[14]。
在筆者對患有SCCEDs的犬進行治療中總結發現,對比金剛砂車針治療與格狀切開術,使用金剛砂車針的治愈率為94%,而進行格狀切開術的治愈率為82%,說明金剛砂車針治療對SCCEDs的治愈率具有明顯的優勢。這是由于角膜格狀切開術對操作者的操作技術要求更高,在角膜表面進行井字形切開時需要對角膜切開的面積和深度都需要更加均勻,如果在操作中切開角膜的深度過深時,可能會醫源性的加重了角膜潰瘍的問題。而金剛砂車針對于角膜的打磨要求的操作技術相對簡單,對于角膜上皮的打磨也更加均勻與光整。在金剛砂車針和角膜格狀切開術對于SCCEDs的治療中我們發現,對比治愈速率和治療操作次數上并無顯著差異。這可能跟我們要求動物主人復診的時間有關,通常來說我們要求在進行操作治療后7 d進行復查角膜上皮愈合情況。所以這可能在某些程度上人為的給統計數據中延長了治愈時間及治療操作次數的統計。
4 總結
上述結果表明,金剛砂車針治療為目前SCCEDs最有效的治療方法,該方法具有操作簡單,治療有效率最高等優勢。是值得在臨床治療中推廣的治療方法。
參考文獻:
[1] Murphy C J,Marfurt C F,McDermott A,et al.Spontaneous chronic corneal epithelial defects(SCCED)in dogs:clinical features,innervation,and effect of topical SP,with or without IGF-1[J].Investigative Ophthalmology and Visual Science,2001,42:2 252-2 261.
[2] Bentley E,Abrams G A,Covitz D,et al.Morphology and immunohistochemistry of spontaneous chronic corneal epithelial defects(SCCED)in dogs[J].Investigative Ophthalmology and Visual Science,2001,42:2 262-2 269.
[3] Kirschner S,Brazzell R,Stern M.The use of topical epidermal growth factor for the treatment of nonhealing corneal erosions in dogs[J].Journal of the American Animal Hospital Association,1991,27:449-452.
[4] Gelatt K N,Samuelson D.Recurrent corneal erosions and epithelial dystrophy in the boxer dog[J].Journal of the American Animal Hospital Association,1982,19:453-460.
[5] Carter R T,Kambampati R,Murphy C J,et al.Expression of matrix metalloproteinase 2 and 9 in experimentally wounded canine corneas and spontaneous chronic corneal epithelial defects[J].Cornea,2007,26:1 213-1 219.
[6] Chandler H L,Colitz C M,Lu P,et al.The role of the slug transcription factor in cell migration during corneal epithelialization in the dog[J].Experimental Eye Research,2007,84:400-411.
[7] Murphy C J,Marfurt C F,McDermott A,et al.Spontaneous chronic corneal epithelial defects(SCCED)in dogs:clinical features,innervation,and effect of topical SP,with or without IGF-1[J].Investigative Ophthalmology and Visual Science,2001,42:2 252-2 261.
[8] Stanley R,Hardman C,Johnson B.Results of grid keratotomy,superficial keratectomy and debridement for the management of persistent corneal erosions in 92 dogs[J].Veterinary Ophthalmology,1998,1 233-1 238.
[9] Champagne E,Munger R.Multiple punctate keratotomy for the treatment of recurrent epithelial erosions in dogs[J].Journal of the American Animal Hospital Association,1992,28:213-216.
[10] Buxton J N,Fox M L.Superficial epithelial keratectomy in the treatment of epithelial basement membrane dystrophy[J].A preliminary report Archives of Ophthalmology,1983,101:392-395.
[11] Aldave A J,Kamal K M,Vo R C,et al.Epithelial debridement and Bowman’s layer polishing for visually significant epithelial irregularity and recurrent corneal erosions[J].Cornea,2009,28:1 085-1 090.
[12] Wong V W,Chi S C,Lam D S.Diamond burr polishing for recurrent corneal erosions:results from a prospective randomized controlled trial[J].Cornea,2009,28:152-156.
[13] Aldave A J,Kamal K M,Vo R C,et al.Epithelial debridement and Bowman’s layer polishing for visually significant epithelial irregularity and recurrent corneal erosions[J].Cornea,2009,28:1 085-1 090.
[14] Gracia de silva E,Powell C C,Gionfriddo J R,et al.Histologic evaluation of the immediate effects of diamond bur debridement in experimental superficial corneal wounds in dogs[J].Veterinary Ophthalmology,2011,14:285-291.

