基于功能化銀納米粒子的表面增強(qiáng)拉曼法檢測水體中As3+
(大連大學(xué)環(huán)境與化學(xué)工程學(xué)院,大連 116622)
目前,我國最嚴(yán)重的重金屬水污染包括鎘、汞、鉛和砷污染。砷可以通過呼吸道、消化道及皮膚進(jìn)入人體,對(duì)各系統(tǒng)造成不同程度的損傷[1]。砷有無機(jī)砷和有機(jī)砷兩種形式,其毒性以無機(jī)砷最為顯著[2],在天然水體中,無機(jī)砷是主要的存在形式,多年來,世界不同地區(qū)的地下水受到不同程度的砷污染[3,4]。飲用含砷的水,會(huì)發(fā)生急性或慢性中毒,重金屬砷會(huì)在人體的肝、腎、肺、子宮、胎盤、骨骼、肌肉等部位蓄積,與細(xì)胞中的酶系統(tǒng)結(jié)合,抑制體內(nèi)許多酶的活性甚至使其失去活性,造成機(jī)體代謝障礙[5]。發(fā)展重金屬檢測技術(shù)對(duì)于控制環(huán)境污染、保護(hù)人體健康具有十分重要的現(xiàn)實(shí)意義。
目前用于重金屬檢測的方法有很多,常用的方法主要有原子光譜法、紫外-可見分光光度法、比色法、質(zhì)譜法和電化學(xué)分析法等。這些檢測技術(shù)大多存在耗費(fèi)耗時(shí)、依賴大型儀器、需要專業(yè)的技術(shù)人員,并且對(duì)某些重金屬離子的檢測不靈敏等問題,因此,發(fā)展簡單、快速、靈敏度高的重金屬檢測技術(shù)是十分必要的。
自從1974年英國科學(xué)家Fleishmann等人首次在粗糙的微納米結(jié)構(gòu)的銀電極表面發(fā)現(xiàn)增強(qiáng)的吡啶拉曼信號(hào)[6],1977年Van Duyne 和Creighton等人證實(shí)這一現(xiàn)象[7]并正式命名為表面增強(qiáng)拉曼散射(surfface-enhanced Raman scattering,簡稱SERS)以后,由于其具有簡單、快速、靈敏度高的優(yōu)點(diǎn),被迅速應(yīng)用于分析檢測。由于SERS效應(yīng)是發(fā)生在粗糙金屬表面上的孔洞或者間隙中的非常局域性的物理現(xiàn)象,對(duì)金屬本身的介電常數(shù)和金屬表面的形貌有著特別的要求,因此基底的制備成為這項(xiàng)技術(shù)發(fā)展的熱點(diǎn)[8]。隨著近年來納米技術(shù)的誕生[9]及發(fā)展,將納米金、銀顆粒具有表面等離子體共振的性質(zhì)應(yīng)用于光譜檢測[10],可發(fā)展基于金屬納米結(jié)構(gòu)的表面增強(qiáng)拉曼光譜方法,由于其可獲得大量的樣品分子結(jié)構(gòu)信息,可使探測靈敏度進(jìn)一步提高,在分析科學(xué)中得到了越來越多的應(yīng)用。Carron等利用鉻黑T作為SERS指示劑對(duì)重金屬離子進(jìn)行了測定[11],通過對(duì)不同離子的拉曼光譜進(jìn)行比較,得知離子半徑的不同能夠?qū)е吕鼒D譜的變化不同。基于這一原理實(shí)現(xiàn)了對(duì)不同離子的選擇性測定,該方法對(duì)鉛離子檢測的最低檢出限為270μg/L,對(duì)銅離子檢測的最低檢出限為85μg/L。Henrique E. Toma[12]課題組利用在有NaCl存在的條件下,金納米粒子能夠使修飾在其表面的2,4,6-trimercapto-1,3,5-triazine (2,4,6-三巰基-1,3,5-三氮雜苯)分子的拉曼信號(hào)顯著增強(qiáng),而2,4,6-trimercapto-1,3,5-triazine與Hg2+和Cd2+的結(jié)合方式不同,從而引起的拉曼圖譜的變化不同,進(jìn)而實(shí)現(xiàn)了對(duì)Hg2+和Cd2+的選擇性和靈敏性檢測。劉世勇[13]課題組利用設(shè)計(jì)合成的離子配體聚合物和拉曼報(bào)告分子共同修飾在金納米粒子的表面形成SERS探針,Cd2+通過與離子配體作用導(dǎo)致納米粒子發(fā)生團(tuán)聚進(jìn)而使拉曼報(bào)告分子的拉曼信號(hào)增強(qiáng),實(shí)現(xiàn)了對(duì)Cd2+的靈敏性測定。付秀麗[14]等基于抗聚集的4-巰基吡啶(4-MPY)功能化銀納米粒子以及聚陽離子魚精蛋白的SERS技術(shù)間接實(shí)現(xiàn)了對(duì)胰蛋白酶的檢測。本研究中基于功能化銀納米粒子的表面增強(qiáng)拉曼法實(shí)現(xiàn)對(duì)水體中As3+的檢測。
1 實(shí)驗(yàn)部分
1.1 儀器與試劑
DXR激光共焦顯微拉曼光譜儀:RFS100(美國Thermo Scientific公司),含顯微鏡、5mW的氦氖二極管泵浦激光源;透射電子顯微鏡:JEM-1230(日本JEOL公司); Zeta電位納米粒度儀:Zetasizer Nano ZS-90(英國Malvern公司);超純水系統(tǒng):CASCADE-BIO(美國Pall 公司)。
谷胱甘肽(GSH,99%)、4-巰基吡啶(4-MPY,95%)(美國Sigma-Aldrich 公司), As3+標(biāo)準(zhǔn)溶液(北京SCP科學(xué)有限公司),鹽酸羥胺(NH2OH·HCl)(天津市科密歐化學(xué)試劑有限公司),硝酸銀(AgNO3,99.8%)、氯金酸(HAuCl4·3H2O)、硼氫化鈉(NaBH4)、氫氧化鈉(NaOH,96%)、檸檬酸鈉(上海國藥集團(tuán)化學(xué)試劑有限公司),實(shí)驗(yàn)所用水均為超純水。
1.2 納米粒子的制備
(1)鹽酸羥胺為還原劑的銀納米粒子的制備
鹽酸羥胺為還原劑的銀納米粒子是根據(jù)室溫條件下利用鹽酸羥胺還原硝酸銀的方法并作必要的修改后合成的。制備方法如下:首先將1 mL的3×10-1mol/L氫氧化鈉(NaOH)水溶液加入89 mL的1.67×10-2mol/L鹽酸羥胺(NH2OH·HCl)水溶液中,使之pH值保持在堿性范圍內(nèi),在攪拌條件下將10 mL的1.11 mmol/L硝酸銀(AgNO3)水溶液滴加到上述混合液中,1 min滴加完成,繼續(xù)攪拌30 min,得到的黃色液體為納米銀顆粒,室溫下儲(chǔ)存待用。
(2)檸檬酸鈉為還原劑的銀納米粒子的制備
檸檬酸根穩(wěn)定的銀納米粒子是根據(jù)文獻(xiàn)報(bào)道的方法合成的[15]。將1.06 mL 0.10 mol/LAgNO3加入到100 mL 45°C的二次水中,磁力攪拌下迅速加熱至沸騰;加入2 mL 1%的檸檬酸鈉,在沸騰狀態(tài)下反應(yīng)45 min。所得溶液在室溫下冷卻待用。
(3)硼氫化鈉為還原劑的銀納米粒子的制備
硼氫化鈉為還原劑的銀納米粒子是根據(jù)文獻(xiàn)報(bào)道的方法并作必要的修改后合成的。首先將0.25 mL 0.1mol/LAgNO3和0.25 mL 0.1 mol/L檸檬酸鈉在攪拌條件下加入到100 mL 二次水中,然后將6 mL 5 mmol/LNaBH4加入到上述混合溶液中,繼續(xù)攪拌1 h后靜置,室溫下儲(chǔ)存待用。
(4)金/銀核殼納米粒子 (Au@Ag NPs)的制備
金/銀核殼納米粒子是按照Natan的方法,即在有金種存在下用檸檬酸鈉還原Ag+的方法并稍加修改后合成的。
種子溶液的制備:用檸檬酸鈉還原氯金酸的方法法制備13 nm粒徑的金納米粒子作為種子。具體過程如下:首先將100 mL 1 mmol/L的HAuCl4溶液加入三口燒瓶中加熱至回流,然后將10 mL 38.8 mmol/L的檸檬酸鈉迅速倒入HAuCl4溶液中,繼續(xù)回流,溶液逐漸由淡黃色變?yōu)榫萍t色,反應(yīng)約15 min后,停止加熱繼續(xù)攪拌冷卻至室溫。
金/銀核殼納米粒子的形成:將10 mL 13 nm的金納米粒子種子溶液稀釋到100 mL并加入三口燒瓶中重新加熱至回流,然后在劇烈攪拌下加入1 mL 38.8 mmol/L的檸檬酸鈉溶液,再加入5 mL 0.01 mol/L的AgNO3溶液,繼續(xù)回流反應(yīng)1 h。反應(yīng)完成后,冷卻至室溫并在4 °C條件下避光保存。
1.3 納米粒子的功能化
在攪拌條件下將10 μL的100 μmol/L的谷胱甘肽水溶液和10 μL的400 μmol/L的4-巰基吡啶水溶液同時(shí)加入到2 mL納米溶膠中,繼續(xù)攪拌30 min,即得谷胱甘肽和4-巰基吡啶同時(shí)功能化的納米粒子。
2 結(jié)果與討論
2.1 檢測原理
GSH/4-MPY功能化的AgNPs檢測水體中As3+的原理如圖1所示,GSH分子含有活潑的巰基-SH ,通過Ag-S化學(xué)鍵功能化到AgNPs表面[16,17]。一般來說,拉曼信號(hào)分子4-巰基吡啶主要通過3種不同的方式與銀納米粒子結(jié)合,即通過的硫(S)或氮(N)原子的孤對(duì)電子,或通過芳香族的π電子。Ag-S鍵的結(jié)合是4-巰基吡啶與銀納米粒子化學(xué)吸附的主要結(jié)合方式,Ag-N鍵的相互作用在吸附過程中起次要作用[18]。當(dāng)溶液中As3+與GSH/4-MPY功能化的AgNPs相遇,由于As3+對(duì)GSH配體有很強(qiáng)的親和力,每一個(gè)As3+離子可通過As-O化學(xué)鍵結(jié)合3個(gè)GSH功能化的AgNPs,導(dǎo)致銀納米顆粒發(fā)生聚集,產(chǎn)生許多拉曼活性位點(diǎn)(即熱點(diǎn)hot spots),從而使吸附在銀納米粒子表面的4-巰基吡啶的拉曼信號(hào)顯著增強(qiáng),間接達(dá)到了對(duì)As3+檢測的目的。
如圖2所示,新制備的AgNPs能夠很好的處于單分散狀態(tài)(圖2a),這是由于其表面由大量帶負(fù)電荷的羥胺氯離子保護(hù)著,防止了AgNPs發(fā)生聚集。通過調(diào)整加入的GSH和4-MPY的濃度,銀納米膠體的顏色仍保持明亮的黃色(圖2b),表明GSH/4-MPY功能化的AgNPs仍然處于單分散狀態(tài)。當(dāng)溶液中存在As3+時(shí),由于As-O化學(xué)鍵的形成而使銀納米顆粒發(fā)生聚集,結(jié)果是GSH/4-MPY功能化的AgNPs的表面等離子體共振光譜發(fā)生了紅移,溶液的顏色加深(圖2c)。由此得出,谷胱甘肽和4-巰基吡啶同時(shí)功能化的銀納米顆粒對(duì)As3+溶液具有一定的響應(yīng),這些響應(yīng)可以通過裸眼觀察。
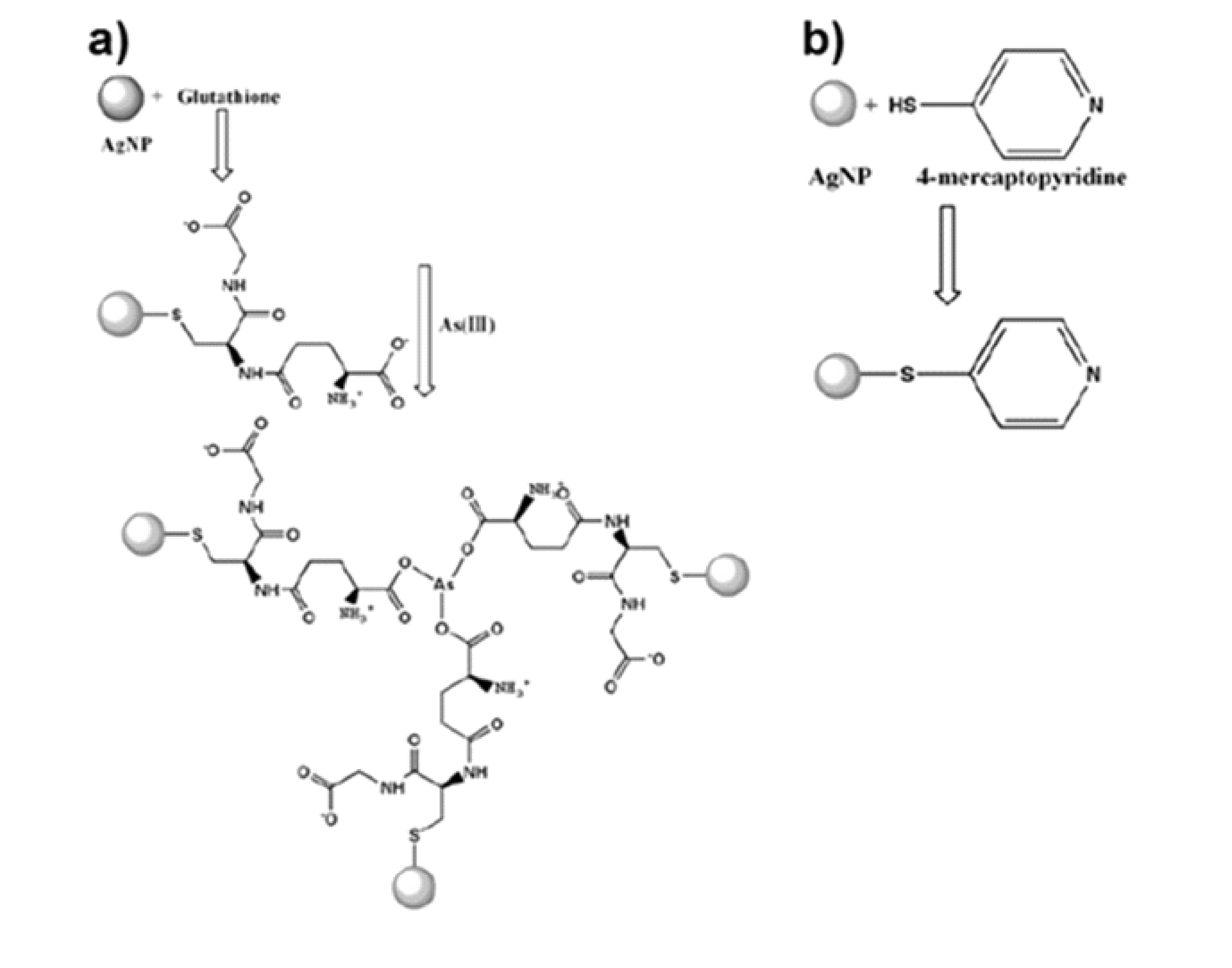
圖1 基于AgNPs的As3+檢測的結(jié)構(gòu)示意圖 a) .GSH功能化的AgNPs ;b). 4-MPY功能化的AgNPs

圖2 基于GSH/4-MPY功能化的AgNPs的As3+的SERS檢測示意圖、TEM及膠體顏色圖 (a).未功能化的AgNPs ;(b). GSH/4-MPY功能化的AgNPs ;(c).加入200μg/L As3+的GSH/4-MPY功能化的AgNPs溶液。
2.2 實(shí)驗(yàn)條件優(yōu)化
(1)納米粒子制備方法的選擇
分別用鹽酸羥胺、檸檬酸鈉、硼氫化鈉作為還原劑制備納米銀粒子(AgNPs),其中,鹽酸羥胺法用不同的藥品加入順序制備兩組,一組為硝酸銀加入到鹽酸羥胺中,一組為鹽酸羥胺加入到硝酸銀中。另外制備一組在有金種存在下用檸檬酸鈉還原Ag+制備的金/銀核殼納米粒子(Au@Ag NPs)。以上各組在相同條件下分別修飾500 nmol/L谷胱甘肽(GSH)和2 μmol/L4-巰基吡啶(4-MPY),攪拌30 min后各取90 μL,加入10 μL 2 mg/L的As3+,進(jìn)行拉曼檢測,每組平行測定3次,選擇1098 cm-1處特征峰做比較,從圖3中可以看出,用鹽酸羥胺作為還原劑,將硝酸銀加入到鹽酸羥胺中制備的AgNPs效果最好。
吸收峰由高到低分別為鹽酸羥胺法a(硝酸銀加入到鹽酸羥胺中)、鹽酸羥胺法b(鹽酸羥胺加入到硝酸銀中)、Au@Ag NPs、檸檬酸鈉法、硼氫化鈉法。
(2)硝酸銀加入速度的選擇
10.44 mg鹽酸羥胺溶解在89 mL二次水中,加入1 mL 0.30mol/L的NaOH,在磁力攪拌下,將10 mL 0.01mol/L硝酸銀溶液用注射泵調(diào)節(jié)不同速度加入到上述混合液中,速度分別為120、60、40、30、24 mm/min,相對(duì)應(yīng)的完成加入的時(shí)間分別為0.5、1、1.5、2、2.5 min,另外一組為硝酸銀快速倒入鹽酸羥胺混合液中。以上6組分別攪拌30 min,靜置30 min后修飾500 nmol/L GSH和2 μmol/L 4-MPY,攪拌30 min后各取90 μL,加入10 μL 2 mg/L的As3+,進(jìn)行拉曼檢測,每組平行測定3次。如表1所示,1.5 min組As3+濃度最高。

圖3 不同方法合成納米粒子功能化后檢測As3+的拉曼信號(hào)強(qiáng)度
表1完成時(shí)間對(duì)納米銀檢測As3+濃度的影響

完成時(shí)間(min)05115225快速As3+濃度(μg/L)532539803575469527
(3)合成納米銀攪拌時(shí)間的選擇
將硝酸銀在1 min內(nèi)加入到鹽酸羥胺與NaOH的混合液中,在相同轉(zhuǎn)速下分別攪拌30 min、45 min、60 min,靜置30 min后修飾500 nmol/L GSH和2 μmol/L 4-MPY,攪拌30 min后進(jìn)行拉曼檢測,每組平行測定3次。將以上各組修飾的AgNPs溶液各取90 μL,加入10 μL 2 mg/L的As3+,進(jìn)行拉曼檢測,每組平行測定3次。綜合考慮加入As3+前后的拉曼強(qiáng)度,選擇攪拌30 min為最佳條件(圖4)。


圖4 攪拌時(shí)間對(duì)納米銀檢測As3+信號(hào)強(qiáng)度影響A.200μg/L As3+時(shí)信號(hào)強(qiáng)度;B.不加As3+時(shí)信號(hào)強(qiáng)度。
(4)納米銀粒子的穩(wěn)定性
對(duì)納米銀溶膠在6天內(nèi)進(jìn)行連續(xù)測定,每次均進(jìn)行功能化然后對(duì)As3+檢測。在第4天時(shí),肉眼可見少許黑色顆粒析出,第6天無拉曼檢測信號(hào)(圖5)。

圖5 連續(xù)6天用功能化納米銀檢測As3+的信號(hào)強(qiáng)度曲線1~6分別為第1~6天拉曼響應(yīng)曲線
(5)4-巰基吡啶的溶劑對(duì)As3+探針的性能的影響
4-巰基吡啶作為拉曼信號(hào)分子修飾到納米銀顆粒上,在SERS檢測中起著非常重要的作用,用不同溶劑溶解4-巰基吡啶,對(duì)于As3+的測定具有一定影響。實(shí)驗(yàn)中考察了分別用甲醇、乙醇、水溶解的4-巰基吡啶修飾的AgNPs對(duì)水中As3+檢測的SERS信號(hào)強(qiáng)度,如圖6所示,用乙醇作為溶劑時(shí)SERS信號(hào)最強(qiáng)。

圖6 4-MPY的溶劑(水、甲醇、乙醇)對(duì)拉曼信號(hào)強(qiáng)度的影響其它實(shí)驗(yàn)條件為500 nmol/L的GSH和200μg/L的As3+
(6)4-巰基吡啶濃度的對(duì)As3+探針的性能的影響
實(shí)驗(yàn)中還考察了4-巰基吡啶的濃度對(duì)SERS 信號(hào)強(qiáng)度的影響,測試了3個(gè)不同濃度的4-MPY(1.0μmol/L, 2.0 μmol/L, 2.5 μmol/L ),其相應(yīng)的SERS光譜強(qiáng)度如圖7所示。從圖7中可以看出2.0 μmol/L的4-MPY產(chǎn)生最大的拉曼信號(hào)。
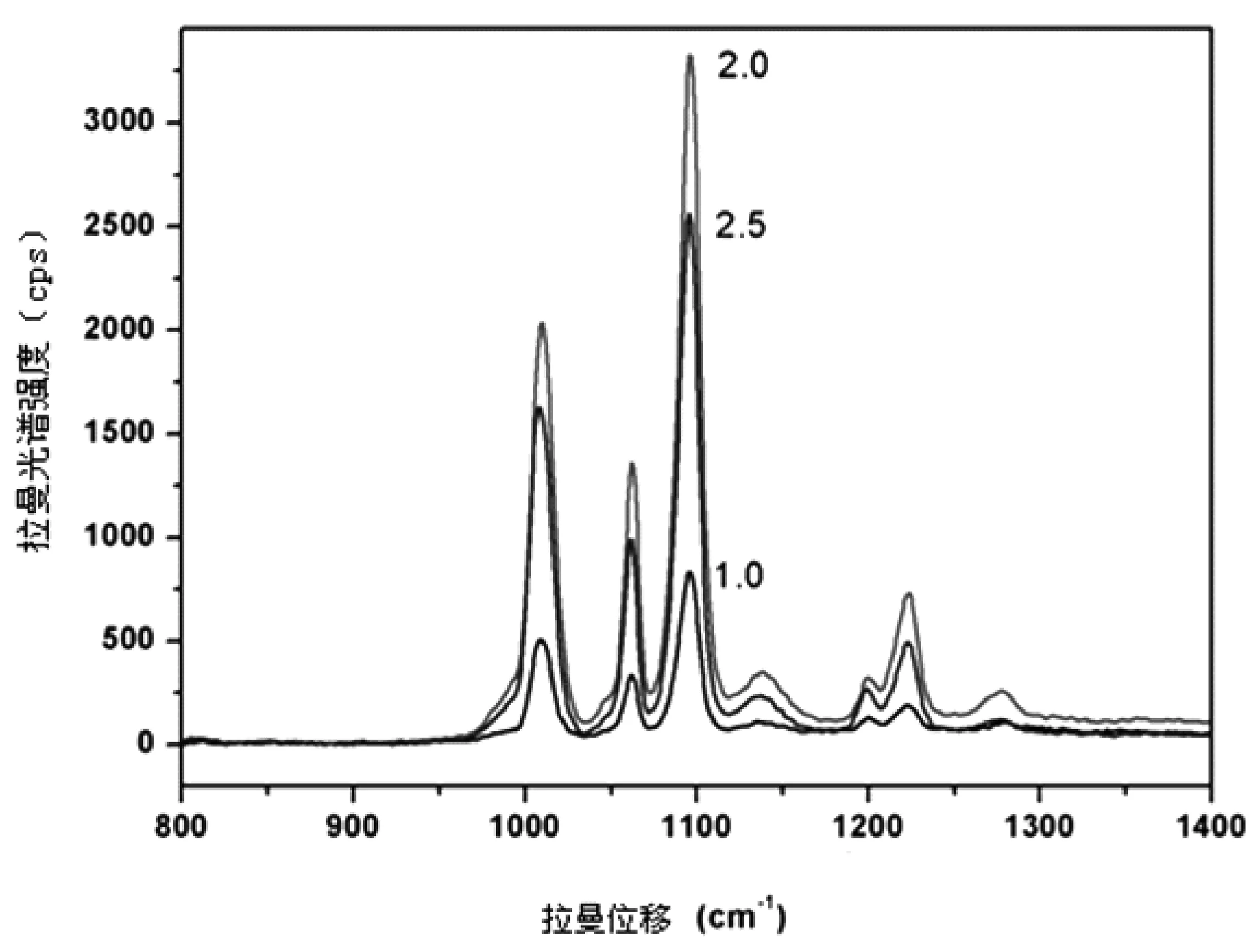
圖7 6 4-MPY的濃度對(duì)拉曼信號(hào)強(qiáng)度的影響濃度:1.0 μmol/L~2.5 μmol/L, 其它實(shí)驗(yàn)條件為500 nmol/L的GSH和500μg/L的As3+
2.3 檢測As3+的靈敏度和線性范圍
在最佳實(shí)驗(yàn)條件下,將不同濃度(0.01~3 mg/L)的As3+溶液分別加入到GSH/4-MPY同時(shí)功能化的AgNPs溶液中與其反應(yīng),對(duì)SERS譜圖進(jìn)行記錄,以確定本研究方法的靈敏度。如圖7所示,4-巰基吡啶呈現(xiàn)出許多特征峰,如位于710、1011、1062、1098、1224和1579 cm-1處的特征峰。其中,處于1098 cm-1的拉曼特征峰是對(duì)應(yīng)于苯環(huán)呼吸振動(dòng)/C-S伸縮模式,表明4-MPY是通過S原子功能化到AgNPs表面。從圖8中可以看出,所有的拉曼特征峰強(qiáng)度都會(huì)隨As3+濃度的增加而增強(qiáng),而1098 cm-1處拉曼特征峰最為顯著,其強(qiáng)度對(duì)As3+離子濃度最敏感。因此,選擇1098 cm-1處拉曼強(qiáng)度的變化來表示As3+引起的GSH/4-MPY功能化的AgNPs的聚集程度,從而作為定量分析As3+濃度的依據(jù)。如圖9、圖10所示,1098 cm-1處的拉曼強(qiáng)度與As3+的濃度在1~300μg/L范圍內(nèi)成良好的線性關(guān)系(相關(guān)系數(shù)R=0.9987),基于3 倍的信噪比計(jì)算得出最低檢測限為0.34μg/L。這一結(jié)果遠(yuǎn)遠(yuǎn)低于世界衛(wèi)生組織(WHO)關(guān)于飲用水中As3+濃度不應(yīng)高于10μg/L的規(guī)定。

圖8 As3+存在時(shí)GSH/4-MPY功能化的AgNPs的拉曼光譜

圖9 加入不同濃度(1~300μg/L)As3+溶液時(shí)GSH/4-MPY功能化AgNPs的SERS光譜

圖10 1098 cm-1波數(shù)處相應(yīng)于不同濃度As3+ 拉曼峰強(qiáng)度圖插圖為1~300μg/L的線性曲線(R2=0.9934), 誤差棒代表3次獨(dú)立實(shí)驗(yàn)的標(biāo)準(zhǔn)偏差
3 結(jié)論
研究了一種基于谷胱甘肽和4-巰基吡啶功能化的銀納米粒子的快速檢測水體中As3+離子的SERS方法。通過利用As3+與谷胱甘肽的結(jié)合作用及銀納米粒子對(duì)拉曼報(bào)告分子4-巰基吡啶顯著的SERS增強(qiáng)效果,本方法表現(xiàn)出了優(yōu)良的分析性能,如高的靈敏度(0.34μg/L)和寬的線性范圍 (1~300μg/L),有望在現(xiàn)場檢測中得以應(yīng)用。
[1]Wang S, Mulligan C N. Occurrence of arsenic contamination in Canada: Sources, behavior and distribution. Sci Total Environ, 2006,366: 701-721.
[2]Yokel R A, Lasley S M, Dorman D C. The Speciation of Metals in Mammals Influences Their Toxicokinetics and Toxicodynamics and Therefore Human Health Risk Assessment. Journal of Toxicology and Environmental Health, Part B: Crit Rev, 2006, 9: 63-85.
[3]Mohan D, Pittman C U. Arsenic removal from water/wastewater using adsorbents—A critical review. Journal of Hazardous Materials, 2007,142: 1-53.
[4]Jain C K, Ali I. Arsenic: occurrence, toxicity and speciation techniques.Water Res, 2000, 34(17): 4304-4312.
[5] 戴樹桂.環(huán)境化學(xué).北京:高等教育出版社,1997:18.
[6]Fleischmann M, Hendra P J, McQuillan A J. Raman spectra of pyridine adsorbed at a silver electrode. Chem Phys Lett, 1974, 26: 163-166.
[7]Albrecht M G, Creighton J A. Anomalously intese Raman spectra of pyridine at a silver electrode. J Am Chem Soc, 1977, 99: 5215-5217.
[8]Grabar K C, Freeman R G, Natan M J. Self-assembled metal colloid monolayers: An approach to SERS substrates. Science, 1995, 267: 1629-1632.
[9] 余海湖, 周靈德, 姜德生. 納米材料與自組裝技術(shù). 新技術(shù)·新方法, 2002, 24(4) : 216-218.
[10]Ghosh S K, Pal T. Interparticle coupling effect on the surface Plasmon resonance of gold nanoparticles: from theory to applications. Chem Rev, 2007, 107: 4797-4862. .
[11]Carron K, Mullen K, Lanouette M, et al. Selective-ultratrace detection of metal ions with SERS. Appl Spectrosc, 1991, 45: 420-423.
[12]Zamarion V M, Timm R A, Araki K, et al. Ultrasensitive SERS nanoprobes for hazardous metal ions based on trimercaptotriazine-modified gold nanoparticles. Inorg Chem, 2008, 47: 2934-2936.
[13]Yin J, Wu T, Song J B, et al. SERS-active nanoparticles for sensitive and selective detection of cadmium ion (Cd2+). Chem Mater, 2011, 23: 4756-4764.
[14]Chen L X, Fu X L, Li J H. Ultrasensitive 1 surface-enhanced Raman scattering detection of trypsin based on anti-aggregation of 4-mercaptopyridine-functionalized silver nanoparticles: an optical sensing platform toward proteases. Nanoscale, 2013, 5: 5905-5911.
[15]Lee P C, Meisel D. Adsorption and surface-enhanced Raman of dyes on silver and gold sols. J Phys Chem, 1982, 86: 3391-3395.
[16]Chen Z, He Y J, Luo S L, et al. Label-free colorimetric assay for biological thiols based on ssDNA/silver nanoparticle system by salt amplification. Analyst, 2010, 135: 1066-1069.
[17]Mo L X, Liu D Z, Li W, et al. Effects of dodecylamine and dodecanethiol on the conductive properties of nano-Ag films. Applied Surface Science, 2011, 257(13): 5746-5753.

