基于體外模擬消化的糖基化草魚魚鱗明膠抗氧化性研究
沙小梅 ,胡姿姿,涂宗財,*,李鑫,張露,王輝,鄭婷婷
1(江西師范大學 功能有機小分子教育部重點實驗室&生命科學學院,江西 南昌,330022)2(南昌大學 食品科學與技術國家重點實驗室,江西 南昌,330047)
草魚(Ctenopharyngodonidella),屬鯉形目鯉科雅羅魚亞科草魚屬,俗稱鯇、油鯇、草鯇、白鯇、草魚、草根(東北)、混子、黑青魚等[1]。2015年,我國草魚養殖年產量達到567.62萬t,為四大家魚產量之首[2]。除鮮銷外,大部分草魚被加工成魚制品,由此產生的大量廢棄物常被直接丟棄,造成環境污染和資源浪費。
魚鱗是魚制品加工過程中的主要廢棄物之一,富含膠原蛋白,是一種良好的明膠原料[3-7]。
魚明膠(魚鱗明膠、魚皮明膠等)是最具潛力的哺乳動物明膠替代物,許多類型的魚明膠,尤其是暖水魚魚明膠,有著良好的凝膠強度。然而,與哺乳動物明膠相比,魚明膠常常顯示出低膠融溫度。此外,包括魚明膠在內的所有明膠物質,有著相對較低的表面活性,尤其是乳化性和乳化穩定性明顯低于其他表面活性物質,例如球蛋白和阿拉伯膠[8-9]。因此,針對魚明膠的次優功能特性,科研工作者探尋了許多技術用于魚明膠改性,包括谷氨酰胺轉氨酶[10]、糖基化反應[11]、紫外線照射[12]等。
糖基化反應是一種改善食品蛋白質功能性質的有效方式,它甚至能賦予蛋白質新的功能特性[13]。糖基化反應已被應用于明膠改性,研究表明,糖基化反應會改變明膠膜的機械性能[14-15],改善明膠的表面活性[11]。此外,亦有報道顯示,蛋白鏈中賴氨酸和精氨酸殘基的修飾可能會阻礙明膠物理網絡結構的形成,進而降低其凝膠強度[16]。然而,鮮少有人報道糖基化修飾后的明膠降解成多肽后的生物活性。人體攝入的明膠會在體內經胃腸道消化形成肽,被人體吸收并產生生物學效應,因此,研究糖基化反應對明膠消化后生物活性的影響具有十分重要的意義。本文以草魚魚鱗明膠和葡萄糖為原料,以干熱條件促使其發生糖基化反應,通過模擬體外消化實驗,研究糖基化反應對明膠消化后多肽抗氧化活性(1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl, DPPH)自由基清除率,·OH 清除率以及 Fe2+螯合能力)的影響,豐富和完善明膠糖基化修飾體系,為糖基化修飾對明膠消化后肽的生物活性影響提供數據支撐。
1 材料與方法
1.1 材料與試劑
草魚魚鱗,于3月從南昌市天虹商場購買新鮮草魚后收集其魚鱗,清洗干凈后于-20 ℃保存,備用。
蛋白分子質量marker,北京索萊寶科技有限公司;胃蛋白酶(酶活力為1∶3000),江蘇銳陽生物科技有限公司;胰液素,美國Sigma公司;其他試劑都屬于分析純或更高的等級。
1.2 儀器與設備
Bio-Rad Mini-PROTEAN Tetra蛋白電泳儀,美國Bio-Rad公司;BioTek Synergy H1 全功能酶標儀,美國BioTek儀器有限公司;柯尼卡美能達CR-13色度儀,日本柯尼卡美能達控股公司。
1.3 方法
1.3.1魚鱗明膠的制備
將魚鱗置于組織搗碎機中搗碎5 min,以去除魚鱗表面的銀白色物質。接下來對魚鱗進行脫鈣處理,脫鈣工藝如下:HCl濃度0.5 mol/L、料液比1∶25(g∶mL)、脫鈣時間1 h。脫鈣后,進一步清洗魚鱗以去除殘存的酸液,直至溶液pH值偏中性。在WANGTUEAI[5]的基礎上進行適當的修改,魚鱗明膠的制備工藝如下:濕魚鱗和去離子水的比例為1∶5(g∶mL)、加熱溫度80 ℃、制備時間2 h。過濾去除魚鱗殘渣,將濾液濃縮凍干,備用。
1.3.2魚鱗明膠-葡萄糖體系的制備
參考那治國等[17]的實驗方法,并作一定修改。用磷酸鹽緩沖液(50 mmol/L,pH值 7.4)配制60 mg/mL的魚鱗明膠溶液,按明膠與糖質量比1∶1的比例加入葡萄糖,充分攪拌溶解混勻形成魚鱗明膠-葡萄糖混合溶液,進一步將其分裝成5份,凍干備用。
1.3.3魚鱗明膠-葡萄糖體系的糖基化反應
參考那治國等[17]的實驗方法,并作一定修改。將凍干的魚鱗明膠-葡萄糖混合物置于50 ℃培養箱中進行糖基化反應,借助飽和碘化鉀溶液控制相對濕度為65%,反應時間分別設置為0、3、6、9和12 h,反應結束后立即置于冰浴中終止反應。
1.3.4色澤的測定
將糖基化反應后的魚鱗明膠分別用色度計進行檢測,并記錄下L*、a*、b*值。色度計采用標準白板校正。
1.3.5游離氨基含量的測定
按照MARTINEZ-ALVARENGA等[18]的方法,采用OPA法測定反應產物中自由氨基的含量。OPA試劑現配現用,準確稱取80.0 mg的OPA溶解于1.0 mL甲醇中,再加入200 g/L的十二烷基硫酸鈉(SDS)5 mL,0.1 mol/L的硼砂50.0 mL,β-巰基乙醇200 μL,最后用蒸餾水定容到100 mL。測定時,取4.0 mL OPA試劑于試管中,加入200 μL樣品,混合均勻,放入35 ℃水浴中反應2 min后在340 nm下測吸光值A340,另取4.0 mL OPA試劑于試管中,加入200 μL水作為空白對照。用相同的方法,以賴氨酸代替樣品作出標準曲線,根據標準曲線計算樣品中游離氨基的含量。
1.3.6SDS-PAGE
參照BALTI等[19]的方法,經過微小修改,即濃縮膠和分離膠的濃度分別為5%和7.5%。配制魚鱗明膠濃度為5 mg/mL的樣品溶液,在95 ℃加熱5 min,再經離心機以5 000 r/min離心10 min,取10 μL溶液上樣。
1.3.7模擬胃腸道消化
綜合HIMAYA等[20]和YOU等[21]報道的方法,再進行適當的修改用于測定魚鱗明膠的體外消化性,即在37 ℃用胃蛋白酶酶解模擬胃部消化,再用胰液素酶解模擬腸道消化。采用1 mol/L的HCl將魚鱗明膠濃度為20 g/L的混合物溶液pH值調至2.0,按照酶與魚鱗明膠質量比為1∶100加入胃蛋白酶,在振蕩下酶解2 h。然后,用0.9 mol/L的NaHCO3溶液將pH值調至5.3,再用1.0 mol/L的NaOH進一步將pH值調至7.5,按照酶與魚鱗明膠質量比為1∶100加入胰液素,在振蕩下酶解4 h,中止酶解反應,即將試管置于沸水浴10 min。基于 KAYASHITA等報道的方法[22],并進行適當的修改,本文魚鱗明膠的體外模擬消化性能以體系中游離氨基數表示。
1.3.8胃腸道消化過程中魚鱗明膠抗氧化特性的測定
1.3.8.1DPPH自由基清除活性
參考ZHENG等[23]的方法進行DPPH·清除活性的測定。配制0.1 mmol/L的DPPH·溶液(以95%的乙醇溶解DPPH)。取酶解產物樣品溶液2.0 mL,加入DPPH·溶液2.0 mL,混合均勻后,在常溫下避光反應30 min,高速離心機10 000 r/min,離心10 min,在517 nm波長處測吸光度(A1),空白組為2.0 mL的體積分數95%乙醇溶液代替DPPH·溶液加入2.0 mL去離子水,在517 nm波長處測定其吸光度(A2),對照組為2.0 mL去離子水代替樣品與2.0 mL DPPH·溶液混合,在517 nm波長處測定其吸光度(A3),并以等體積去離子水和95%乙醇混合液空白調零。按公式(1)計算DPPH自由基清除率:
(1)
1.3.8.2·OH清除率的測定
參照ZUO等[24]的方法并略有改動,在反應體系中加入1 mL 9 mmol/L FeSO4,1 mL 9 mmol/L水楊酸-乙醇和50 μL水解液,最后加入1 mL 8.8 mmol/L H2O2啟動反應,37 ℃反應30 min,以蒸餾水為參比,在510 nm下測量吸光度Aj;取50 μL蒸餾水代替水解液,做空白對照,測得吸光度為A0,以蒸餾水代替雙氧水反應體系為本底測定吸收值Ai,采用下列公式計算·OH清除率:
(2)
1.3.8.3Fe2+螯合能力的測定
參考PHANAT等[25]的方法并略有改動,取0.5 mL的酶解液,加入1 mL 20 μmol/L FeCl2,混合均勻,然后加入1 mL 0.5 mmol/L菲洛嗪溶液,振蕩均勻,室溫下靜置10 min,在562 nm波長處測定吸光度(A樣品),以等體積去離子水代替樣品溶液作為參照測定吸光度(A參照)。金屬離子螯合率按公式(3)計算:

(3)
1.3.9數據的統計學分析
所有實驗數據都是來源于3個平行樣測得的結果取平均值,數據通過SPSS 17.0進行分析,選取Duncan's test用于顯著性分析(p<0.05)。
2 結果與分析
2.1 魚鱗明膠-葡萄糖體系的色澤變化
糖基化反應對魚鱗明膠顏色的影響如表1所示。其中,L表示黑白,+表示偏白,-表示偏暗;a表示紅綠,+表示偏紅,-表示偏綠;b表示黃藍,+表示偏黃,-表示偏藍;C=(a2+b2)1/2,用于表征外觀顏色的飽和度、純度和強度;E=(L2+a2+b2)1/2,用于表示2種顏色的差異程度。
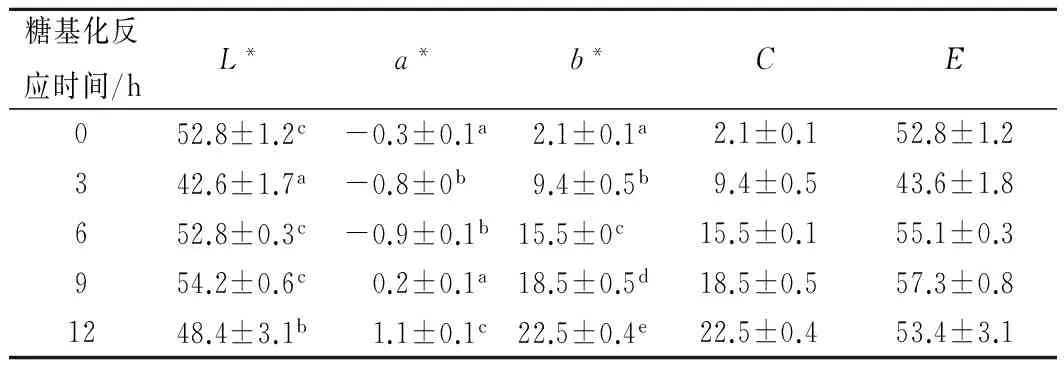
表1 糖基化反應對魚鱗明膠顏色的影響Table 1 Effect of glycation reaction on color valuesof fish gelatin
注:a,b,c,d,e表示數據間差異顯著性。
由表1可知,隨著糖基化反應時間的延長,反應終產物逐漸增多,這些終產物主要以類黑素為主[26],b*值越大(p<0.05),即黃色程度越深,美拉德褐變程度越高,C值也持續增加,說明魚鱗明膠經糖基化反應后黃褐色產物的生成并未達到飽和。本文還通過對魚鱗明膠糖基化產物的外觀顏色進行拍攝(圖片未展示),結果一致。糖基化反應時間越長,魚鱗明膠-葡萄糖體系的顏色越深。糖基化反應開始前,魚鱗明膠-葡萄糖體系呈白色;當反應時間為12 h,魚鱗明膠-葡萄糖體系已成為金黃色。
2.2 SDS-PAGE
魚鱗明膠-葡萄糖體系在不同反應時間的分子質量分布如圖1所示。經過糖基化(0、3、6、9、12 h)反應后的魚鱗明膠樣品有著相似的蛋白質條帶,即包含特征性的α鏈(α1和α2),β鏈(由2條α鏈共價交聯形成)和HMWP(高分子質量聚合物)。隨著糖基化反應時間的延長,魚鱗明膠的電泳條帶逐漸上移,可能是因為葡萄糖分子的引入使得魚鱗明膠的分子質量有所增加。當糖基化反應時間為12 h,魚鱗明膠的電泳條帶上移最為明顯,說明此時魚鱗明膠分子質量最大,糖基化反應程度最高。
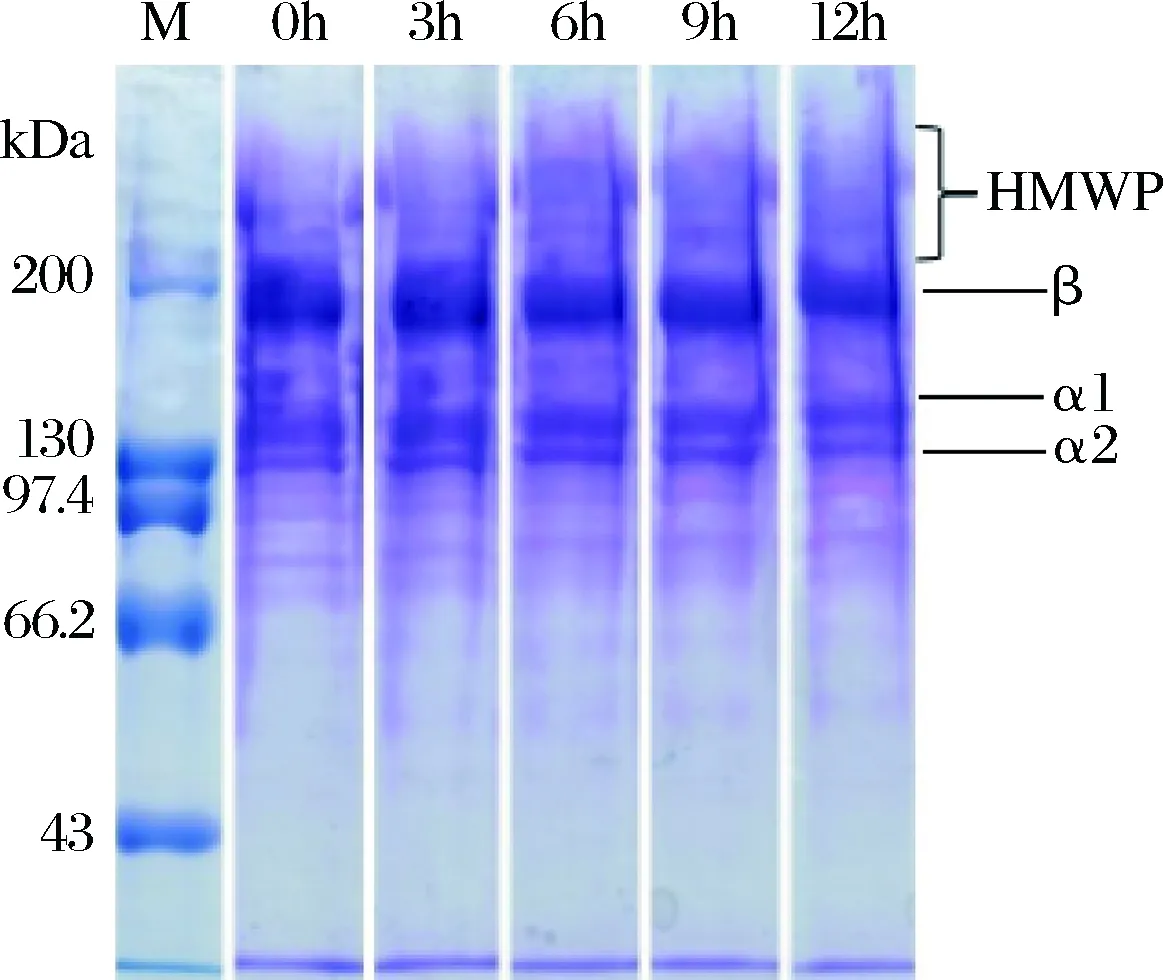
圖1 糖基化反應后魚鱗明膠的SDS-PAGE圖Fig.1 SDS-PAGE profile of fish gelatin treated byglycation reaction
2.3 游離氨基含量的變化
在美拉德反應初期階段,蛋白質中自由氨基基團(如賴氨酸和精氨酸的—NH2基團)與糖的羰基基團發生共價交聯反應,使蛋白質的自由氨基含量下降[27]。自由氨基含量的減少量在一定程度上反應了糖基化反應的程度[28]。
魚鱗明膠-葡萄糖體系在不同反應時間下的游離氨基變化情況如圖2所示。游離氨基含量隨著糖基化反應時間的增加而逐漸降低(p<0.05),說明糖基化反應程度逐步加大。這與李菁等[29]的研究結論一致,即隨著糖基化反應時間的延長,L-賴氨酸的游離氨基含量逐漸降低。
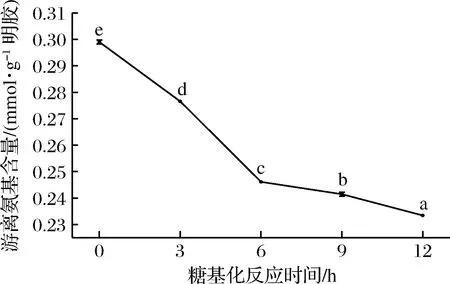
圖2 糖基化反應時間對魚鱗明膠游離氨基含量的影響Fig.2 The free amino group content of fish gelatintreated by glycation reaction
2.4 體外模擬的魚鱗明膠胃腸道消化性
糖基化反應對魚鱗明膠體外消化性的影響結果以游離氨基數目表征,游離氨基數目增多則表示魚鱗明膠消化性增強[22]。
圖3-A為糖基化反應對魚鱗明膠胃部消化性能的影響,糖基化反應誘導魚鱗明膠的天然結構發生一定改變,且過度的糖基化反應使得高級產物生成量增加,進而降低魚鱗明膠-葡萄糖體系的溶解性,同時糖基化反應掩蓋了部分消化位點,因此,在模擬人體胃部消化過程中,糖基化反應能夠顯著地降低魚鱗明膠-葡萄糖美拉德反應產物的消化性(p<0.05)。糖基化對魚鱗明膠模擬人體整個胃腸道消化性的影響如圖3-B所示。在模擬人體整個胃腸道消化過程中,魚鱗明膠-葡萄糖美拉德反應產物的消化性均比未糖基化的魚鱗明膠低。可能是因為胰蛋白酶能特異性水解賴氨酸和精氨酸殘基的羧基端肽鍵,然而糖基化反應使得魚鱗明膠的賴氨酸和精氨酸殘基被修飾而無法被胰蛋白酶識別,因此降低其在胃腸道的消化性。

A-胃消化后游離氨基含量;B-整個胃腸道消化后游離氨基含量圖3 糖基化反應后魚鱗明膠的體外模擬消化Fig.3 In vitro digestibility of fish gelatin treated byglycation reaction
2.5 胃腸道消化過程中的抗氧化特性
2.5.1DPPH·清除活性
由圖4可知,在糖基化反應9 h之前,魚鱗明膠-葡萄糖美拉德反應產物在胃部模擬消化和人體整個胃腸道模擬消化過程中,對DPPH·的清除能力均呈現先增強后下降的趨勢(p<0.05)。在糖基化反應9 h時,DPPH·的清除能力達到最大,即在糖基化反應的前9 h內,具有抗氧化活性的物質大量合成,9 h后逐漸下降(p>0.05)。隨著糖基化反應時間的延長,糖基化產物中的疏水性基團暴露,消化液的疏水性增強,使其易于與脂溶性的DPPH·反應[30],從而DPPH·清除率得以提高,在糖基化反應9 h時達到最大。糖基化反應9 h后,DPPH·清除率降低可能是因為糖基化反應產物的結構變得緊湊[31],一些疏水基團被包埋,減少了與脂溶性的DPPH·的反應。總體表明,糖基化修飾的魚鱗明膠模擬消化后得到的多肽呈現出較好的DPPH·清除能力。
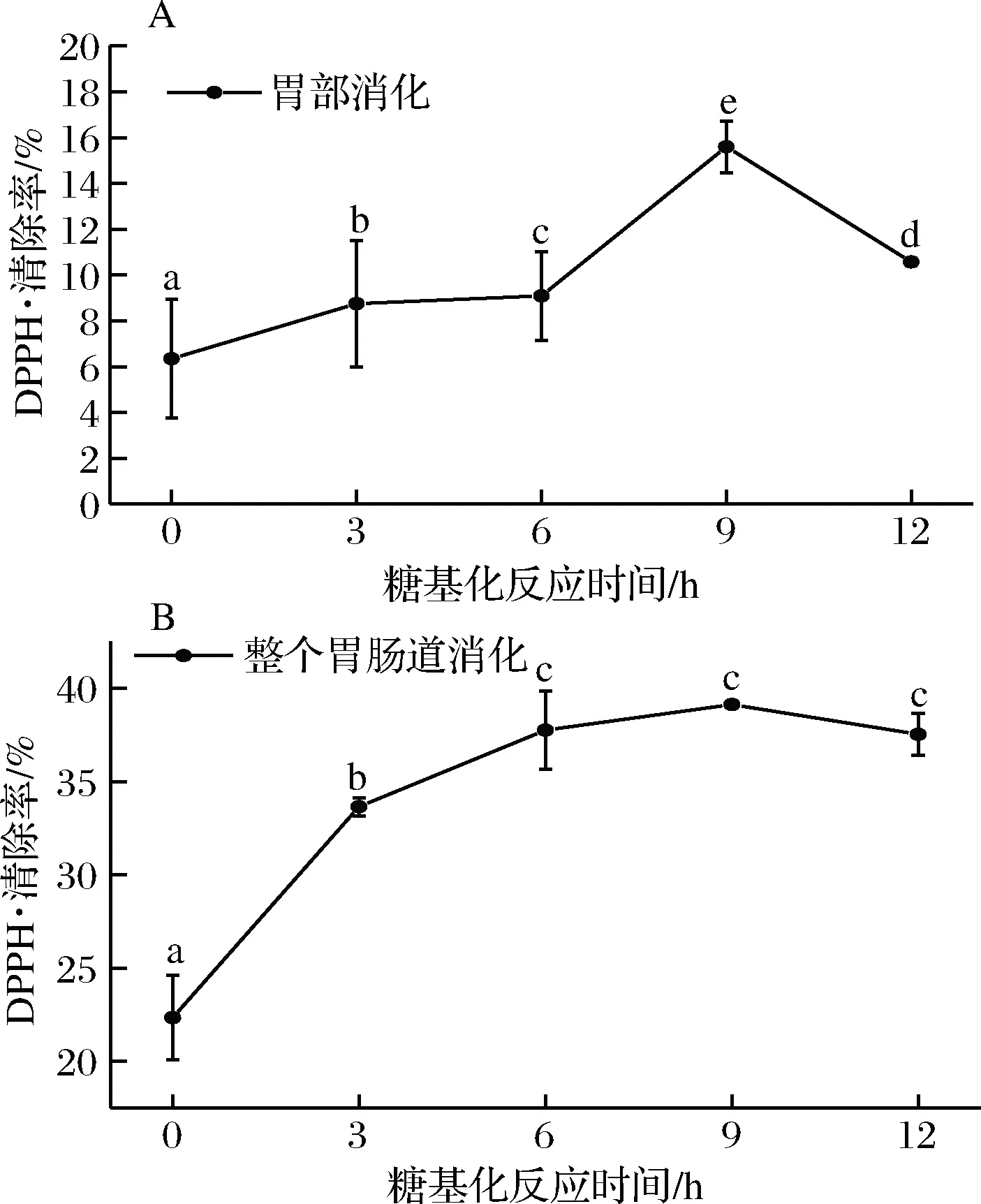
A-胃消化后DPPH·清除能力;B-整個胃腸道消化后DPPH·清除能力圖4 魚鱗明膠經體外模擬消化后的DPPH·清除能力Fig.4 DPPH radical clearance rate of fish gelatin treatedin vitro digestibility
2.5.2·OH清除率的測定
由圖5可知,在魚鱗明膠糖基化反應后模擬胃部消化過程中,糖基化反應9 h前,清除·OH的能力逐漸上升(p<0.05),糖基化反應9 h之后,清除·OH的能力開始下降(p<0.05)。可能是因為隨著糖基化反應時間的延長,作為氫供體的糖基化反應產物不斷增多[32],使得·OH清除能力增大。糖基化反應產物的·OH清除率降低可能是因為在糖基化反應后期階段生成的終產物中可作為氫供體的反應產物含量降低。在模擬人體整個胃腸道消化過程中,糖基化反應3 h前,清除·OH的能力下降幅度較快(p<0.05),糖基化反應3~6 h這一時間段內,清除·OH的能力逐漸上升(p<0.05),在糖基化反應6~9 h內,清除·OH的能力上升緩慢(p>0.05),在糖基化反應9 h之后,清除·OH的能力又開始下降(p<0.05),可能是因為糖基化反應使得魚鱗明膠的賴氨酸和精氨酸殘基被修飾而無法被胰蛋白酶識別,使得氫供體含量減少,·OH清除能力降低。總的來說,糖基化反應能提高魚鱗明膠在胃部的·OH的清除能力,但在模擬人體整個胃腸道消化過程中,糖基化反應會降低魚鱗明膠·OH的清除能力。
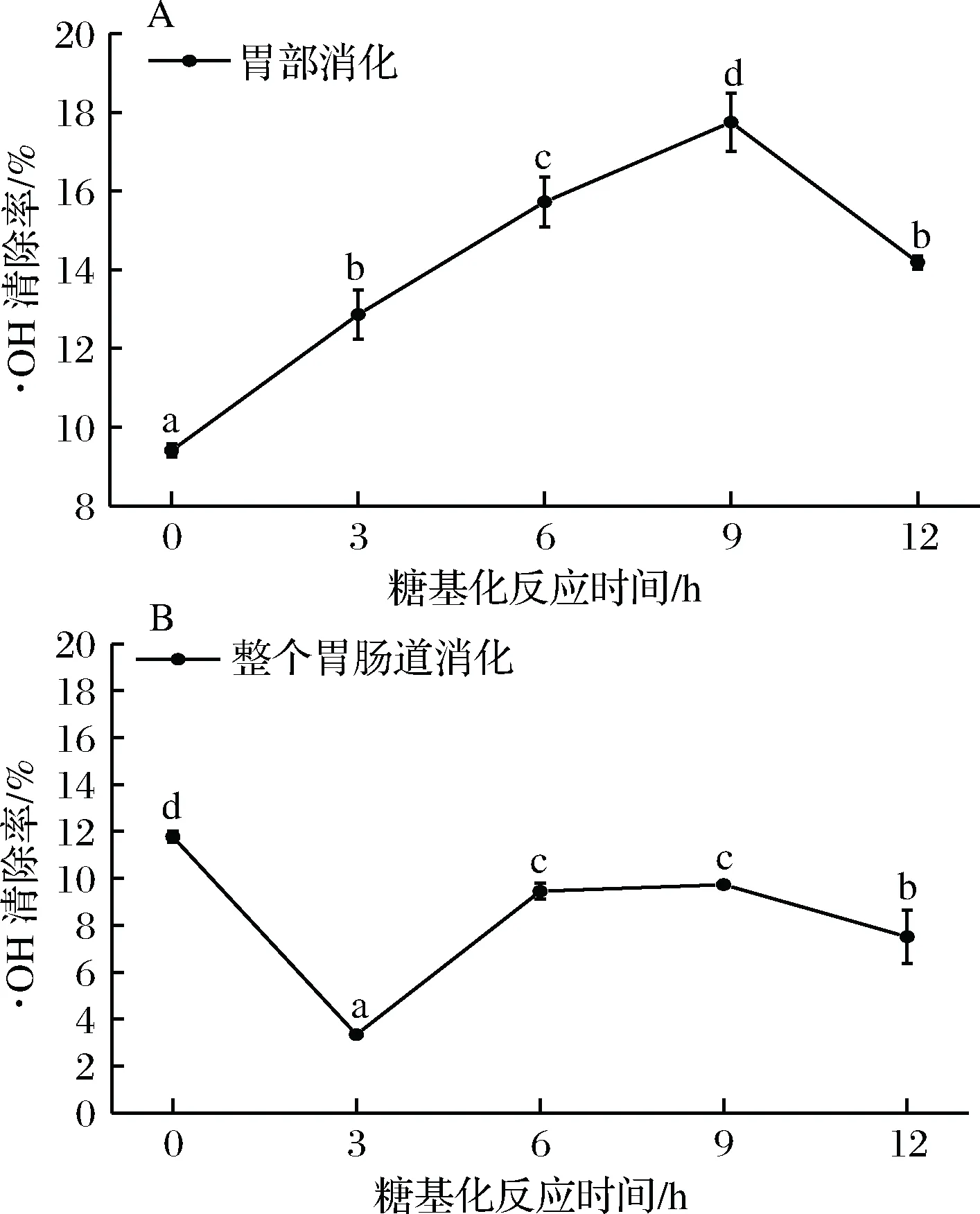
A-胃消化后·OH清除能力;B-整個胃腸道消化后·OH清除能力圖5 魚鱗明膠的體外模擬消化對·OH的清除能力Fig.5 ·OH clearance rate of fish gelatin treate in vitro digestibility
2.5.3Fe2+螯合能力的測定
由圖6可知,在模擬胃部消化過程中,魚鱗明膠糖基化反應3 h前,螯合Fe2+的能力變化不顯著(p>0.05),在糖基化反應3 h至9 h這一時間段內,螯合Fe2+的能力下降幅度增大(p<0.05),糖基化反應9 h時,螯合Fe2+的能力最小,糖基化反應9 h之后迅速上升(p<0.05),但糖基化9 h后的Fe2+螯合能力仍低于未糖基化的魚鱗明膠。這一結果說明在胃部,糖基化反應能降低Fe2+螯合能力。可能是因為隨著糖基化反應時間的延長,魚鱗明膠-葡萄糖美拉德反應產物的消化率降低,導致消化水解生成的水溶性物質減少所致[33]。在模擬人體整個胃腸道消化過程中,螯合Fe2+的能力不隨糖基化反應時間的推移而發生明顯變化(p>0.05),但與胃部消化相比,胰蛋白酶酶解后Fe2+螯合能力得到顯著提高(p<0.05)。胰蛋白酶酶解有助于提高酶解產物的Fe2+螯合能力,其螯合率達到76%左右(p<0.05)。在糖基化反應6、9、12 h時,胃蛋白酶酶解過程中酶解產物對Fe2+的螯合能力下降,但是經胰蛋白酶酶解又迅速回升。胰蛋白酶酶解產物螯合能力的提高可能是因為胰蛋白酶將魚鱗明膠酶解成活性肽或者肽段,同時親核性的離子結合基團完全暴露[21]。

A-胃消化后Fe2+螯合能力;B-整個胃腸道消化后Fe2+螯合能力圖6 魚鱗明膠的體外模擬消化后螯合Fe2+的能力Fig.6 Fe2+-chelating capacity offish gelatin treatedin vitro digestibility
3 結論
本文通過體外模擬消化實驗,明確糖基化反應對魚鱗明膠在胃腸道抗氧化活性的影響。隨著糖基化反應時間的延長,魚鱗明膠-葡萄糖體系的顏色由白色逐漸變成金黃色,且游離氨基含量也逐漸減少,在糖基化反應12 h時,魚鱗明膠分子量增大,表明糖基化反應程度逐漸增加。在胃部模擬消化過程中,隨著糖基化反應時間的延長,DPPH·、·OH的清除能力先增強后降低,而Fe2+螯合能力先降低后增加。在胃腸道消化過程中,DPPH·清除能力不斷增大至穩定,糖基化產物的·OH清除能力均小于未糖基化的魚鱗明膠,而Fe2+螯合能力未發生發生明顯變化。總體而言,糖基化反應會降低魚鱗明膠在胃腸道的消化特性,并影響其消化產物的抗氧化性。
作為一種常用的蛋白質改性方法,糖基化反應會改變魚鱗明膠在胃腸道消化過程中的抗氧化活性,但影響效果因抗氧化性評價方式不同而有所不同。然而,糖基化反應后魚明膠抗氧化活性與其結構(包括糖基化位點情況)的關系還有待深入研究,以揭示魚明膠抗氧化活性變化的內在原因。
[1]WANG Ling-zhao, YANG Bao, WANG Rui, et al. Extraction of pepsin-soluble collagen from grass carp (Ctenopharyngodonidella) skin using an artificial neural network[J]. Food Chemistry, 2008,111(3):683-686.
[2]農業部漁業局編制. 中國漁業統計年鑒. 2016[M]. 北京:中國農業出版社, 2016.
[3]MATMAROH K, BENJAKUL S, PRODPRAN T, et al. Characteristics of acid soluble collagen and pepsin soluble collagen from scale of spotted golden goatfish (Parupeneusheptacanthus)[J]. Food Chemistry, 2011,129(3):1 179-1 186.
[4]ZHANG Feng-xiang, XU Shi-ying, WANG Zhang. Pre-treatment optimization and properties of gelatin from freshwater fish scales[J]. Foodand Bioproducts Processing, 2011,89(3):185-193.
[5]WANGTUEAI S, NOOMHORM A. Processing optimization and characterization of gelatin from lizardfish (Sauridaspp.) scales[J]. LWT-Food Scienceand Technology, 2009,42(4):825-834.
[6]TU Zong-cai, HUANG T, WANG H, et al. Physico-chemical properties of gelatin from bighead carp (Hypophthalmichthysnobilis) scales by ultrasound-assisted extraction[J]. Journal of Food Scienceand Technology-Mysore, 2015,52(4):2 166-2 174.
[7]SHA Xiao-mei, TU Zong-cai, LIU Wei, et al. Effect of ammonium sulfate fractional precipitation on gel strength and characteristics of gelatin from bighead carp (Hypophthalmichthysnobilis) scale[J]. Food Hydrocolloids, 2014,36:173-180.
[8]KARIM A A, BHAT R. Gelatin alternatives for the food industry: recent developments, challenges and prospects[J]. Trendsin Food Science& Technology, 2008,19(12):644-656.
[9]KARIM A A, BHAT R. Fish gelatin: properties, challenges, and prospects as an alternative to mammalian gelatins[J]. Food Hydrocolloids, 2009,23(3):563-576.
[10]MOHTAR N F, PERERA C O, QUEK S, et al. Optimization of gelatine gel preparation from New Zealand hoki (Macruronusnovaezelandiae) skins and the effect of transglutaminase enzyme on the gel properties[J]. Food Hydrocolloids, 2013,31(2):204-209.
[11]LIN L H, CHEN Keng-Ming, LIU H J, et al. Preparation and surface activities of modified gelatin-glucose conjugates[J]. Colloidsand Surfaces A: Physicochemicaland Engineering Aspects, 2012,408:97-103.
[12]BHAT R, KARIM A A. Ultraviolet irradiation improves gel strength of fish gelatin[J]. Food Chemistry, 2009,113(4):1 160-1 164.
[13]LIU Jian-hua, RU Qiao-mei, DING Yu-ting. Glycation a promising method for food protein modification: Physicochemical properties and structure, a review[J]. Food Research International, 2012,49(1):170-183.
[14]SAMIRA S, THUANCHEW TAN T C, AZHAR M E. Effect of ribose-induced Maillard reaction on physical and mechanical properties of bovine gelatin films prepared by oven drying.[J]. International Food Research Journal, 2014, 21(1): 269-276.
[15]ETXABIDE A, URANGA J, GUERRERO P, et al. Improvement of barrier properties of fish gelatin films promoted by gelatin glycation with lactose at high temperatures[J]. LWT-Food Scienceand Technology, 2015,63(1):315-321.
[16]SPANNEBERG R, SCHYMANSKI D, STECHMANN H, et al. Glyoxal modification of gelatin leads to change in properties of solutions and resulting films[J]. Soft Matter, 2012,8(7):2 222-2 229.
[17]那治國,馬永強,韓春然,等. 米糠谷蛋白干法糖基化改性的研究[J]. 食品科學,2013, 34(2):52-57.
[18]MARTINEZ-ALVARENGA M S, MARTINEZ-RODRIGUEZ E Y, GARCIA-AMEZQUITA L E, et al. Effect of Maillard reaction conditions on the degree of glycation and functional properties of whey protein isolate-Maltodextrin conjugates[J]. Food Hydrocolloids, 2014,38:110-118.
[19]BALTI R, JRIDI M, SILA A, et al. Extraction and functional properties of gelatin from the skin of cuttlefish (Sepia officinalis) using smooth hound crude acid protease-aided process[J]. Food Hydrocolloids, 2011,25(5):943-950.
[20]HIMAYA S W A, NGO D, RYU B, et al. An active peptide purified from gastrointestinal enzyme hydrolysate of Pacific cod skin gelatin attenuates angiotensin-1 converting enzyme (ACE) activity and cellular oxidative stress[J]. Food Chemistry, 2012,132(4):1 872-1 882.
[21]YOU Li-jun, ZHAO Mou-ming, REGENSTEIN J M, et al. Changes in the antioxidant activity of loach (Misgurnus anguillicaudatus) protein hydrolysates during a simulated gastrointestinal digestion[J]. Food Chemistry, 2010,120(3):810-816.
[22]KAYASHITA J, SHIMAOKA I, NAKAJOH M, et al. Consumption of buckwheat protein lowers plasma cholesterol and raises fecal neutral sterols in cholesterol-Fed rats because of its low digestibility.[J]. The Journal of nutrition, 1997,127(7):1 395-1 400.
[23]ZHENG Lin, REN Jiao-yan, SU Guo-wan, et al. Comparison of in vitro digestion characteristics and antioxidant activity of hot-and cold-pressed peanut meals[J]. Food Chemistry, 2013,141(4):4 246-4 252.
[24]ZUO Li-li, WANG Zhen-yu, FAN Zi-luan, et al. Evaluation of antioxidant and antiproliferative properties of three actinidia (Actinidiakolomikta,Actinidiaarguta,Actinidiachinensis) extractsinvitro[J]. International Journalof Molecular Sciences, 2012,13(5):5 506-5 518.
[25]KITTIPHATTANABAWON P, BENJAKUL S, VISESSANGUAN W, et al. Effect of extraction temperature on functional properties and antioxidative activities of gelatin from shark skin[J]. Foodand Bioprocess Technology, 2012,5(7):2 646-2 654.
[26]畢偉偉. 微波對酪蛋白的糖基化反應及產物功能性質的研究[D]. 哈爾濱:東北農業大學, 2015.
[27]JING H, KITTS D D. Chemical and biochemical properties of casein-sugar Maillard reaction products[J].Food and Chemical Toxicology,2002, 40(7): 1 007-1 015.
[28]TSUBOKURA Y, FUKUZAKI S, NOMA S, et al. Glycation of ovalbumin in solid-state by conductive and microwave heating[J]. Food Scienceand Technology Research, 2009,15(4):377-380.
[29]李菁, 劉騫, 孔保華, 等.L-賴氨酸與3種還原糖美拉德反應產物的理化特性及抗氧化活性[J]. 食品科學, 2013,34(3):80-85.
[30]ZHU Li-juan, CHEN Jie, TANG Xue-yan, et al. Reducing, radical scavenging, and chelation properties ofinvitrodigests of alcalase-treated zein hydrolysates[J]. Journal of Agricultural & Food Chemistry, 2008, 56(8):2 714-2 721.
[31]黃小琴. 基于質譜技術的蛋白質組學方法對食品蛋白質糖基化的研究[D]. 南昌: 南昌大學, 2013.
[32]楊健, 李芳菲, 武淑影,等. 大豆蛋白美拉德反應產物的抗氧化特性及其機理[J]. 中國食品學報, 2017, 17(2):44-51.
[33]涂宗財, 李瑞平, 王輝,等. 微波預處理對草魚魚肉蛋白消化及其產物抗氧化活性的影響[J]. 食品科學, 2015, 36(7):56-60.

