柴油加氫脫硫三集總動力學
孫國權, 姚春雷, 全 輝
(中國石化 撫順石油化工研究院, 遼寧 撫順 113001)
隨著我國對柴油質量要求的不斷升級,大多數石化企業將降低柴油中硫含量、提高柴油質量、降低脫硫成本視為柴油生產的核心任務。開發新型加氫脫硫(HDS)催化劑是實現柴油低硫化的關鍵,而HDS動力學則是研究各種硫化物在催化劑上加氫機理的重要手段,對指導新HDS催化劑的研究開發具有重要的指導意義,也是設計反應器、預測不同操作條件下硫含量及優化工藝條件的基礎。
柴油餾分中硫化物的種類復雜,建立HDS動力學模型時,產品硫含量的計算值與實際值誤差較大。由于不同研究人員采用的催化劑、加氫反應器、操作條件以及分析測試水平的不同,實驗結果會有一定的差異,所開發的動力學模型也不相同,不能全面地解釋其動力學特性[1]。大量HDS的動力學分析數據表明[2-4],對每一類型硫化物,柴油餾分中硫化物的HDS均符合一級反應動力學方程,若將油品中的硫化物按其加氫反應活性的不同劃分為不同的集總來分別研究,則所建的柴油HDS動力學模型比較合理[5-8]。因此,筆者重點研究能夠預測在深度脫硫(硫質量分數小于50 μg/g和小于10 μg/g)條件下的HDS動力學模型,并對相應的動力學參數進行計算。
1 實驗部分
1.1 實驗原料及催化劑
柴油為中國石化鎮海煉化分公司Ⅰ套常減壓裝置的常二線、常三線和常二線常三線混合柴油,3種柴油原料的主要性質如表1所示。新氫為電解氫,純度大于99.7%(體積分數),大連港生產;催化劑為中國石化撫順石油化工研究院自主開發的加氫精制催化劑FH-UDS,具有孔體積大、比表面積大、HDS及加氫脫氮活性高、穩定性好、對原料適應性強等特點。
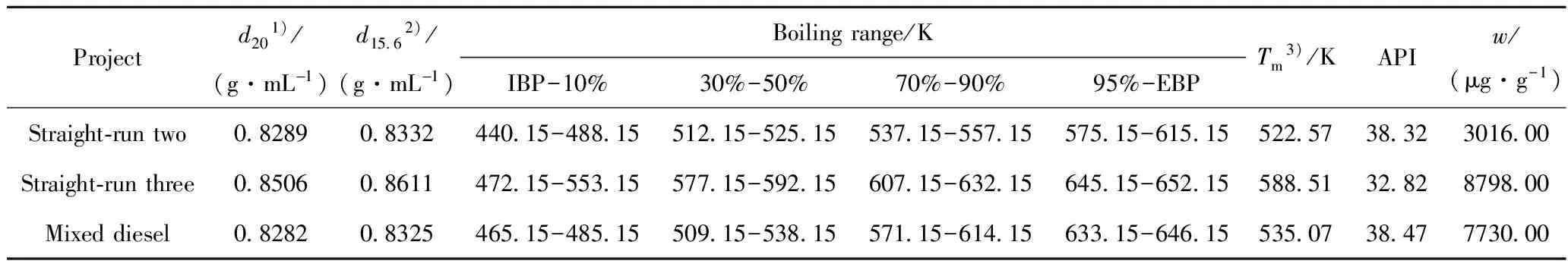
表1 柴油原料的主要性質Table 1 Main properties of diesel feedstock
1) Density of 293.15 K; 2) Density of 288.75 K; 3) Average boiling point
1.2 工藝流程
柴油加氫實驗裝置主要有進料泵,加熱爐,反應器,空氣壓縮機,濕式空氣流量計和溫控指示等設備。原料罐用氮氣氣封,柴油經原料油泵升壓輸入加氫反應器中,與循環氫壓縮機輸入的氫氣充分混合并反應,氣體質量流量計獲取氫氣的流量,反應生成油經高壓分離器完成氣、液分離,液體產品經低壓分離器后出裝置。采用Antek公司ANTEK-9000型X射線檢測儀,按照石油及石油產品硫含量測定法SH/T0689(石油化工行業標準)測定原料及產品中硫含量。
1.3 建模思路
在小型裝置上進行動力學數據分析,氫/油體積比400/1(V(H2)/V(Oil)=400),建立包含3個主要工藝條件(氫分壓、反應溫度和體積空速)影響的三集總動力學模型,擬合出各種原料油的動力學參數(如反應速率常數、活化能和指前因子等),實沸點蒸餾窄餾分的反應速率常數均與其中平均沸點的4次方成反比[9],在此基礎上建立三集總一級反應關聯式。在柴油原料硫質量分數差異很大時預測產品硫質量分數是否符合規定的指標,通過實沸點蒸餾實驗得到的每個窄餾分不必做實驗,只需將得出的每個窄餾分劃分成3個集總,計算各種柴油原料及各個窄餾分的中平均沸點,依據三集總一級動力學模型,由各個窄餾分的中平均沸點可求得其相應的反應速率常數及指前因子,減少了實驗時間,可獲得較精確的實驗數據。
1.4 動力學實驗數據
在不同HDS工藝條件下,生成油的硫質量分數如表2所示,氫/油體積比均為400。
2 動力學模型
2.1 集總組分劃分
將柴油中的硫化物根據加氫反應的難易,按照苯并噻吩類(Ⅰ),二苯并噻吩類(Ⅱ)和4,6-二甲基二苯并噻吩類(Ⅲ)簡單的分為3類。常二線常三線混合柴油實沸點蒸餾的切割方案及3類硫化物的分析數據如表3所示。由表3可知,混合柴油中硫化物類型的分布與餾程有密切聯系,在切割的<483.15 K、483.15~513.1 5K、513.15~543.15 K和543.15~573.15 K的4個窄餾分中,硫化物只有苯并噻吩類(Ⅰ)。剩余的窄餾分中均含有3類硫化物,但苯并噻吩類(Ⅰ)硫化物隨著餾程的增大而逐漸減少,二苯并噻吩類(Ⅱ)和4,6-二甲基二苯并噻吩類(Ⅲ)硫化物隨著餾程的增大而逐漸增多,通過餾程切割可以將硫化物簡單的分離,3類硫化物的分布明顯,其結果有利于集總的劃分。
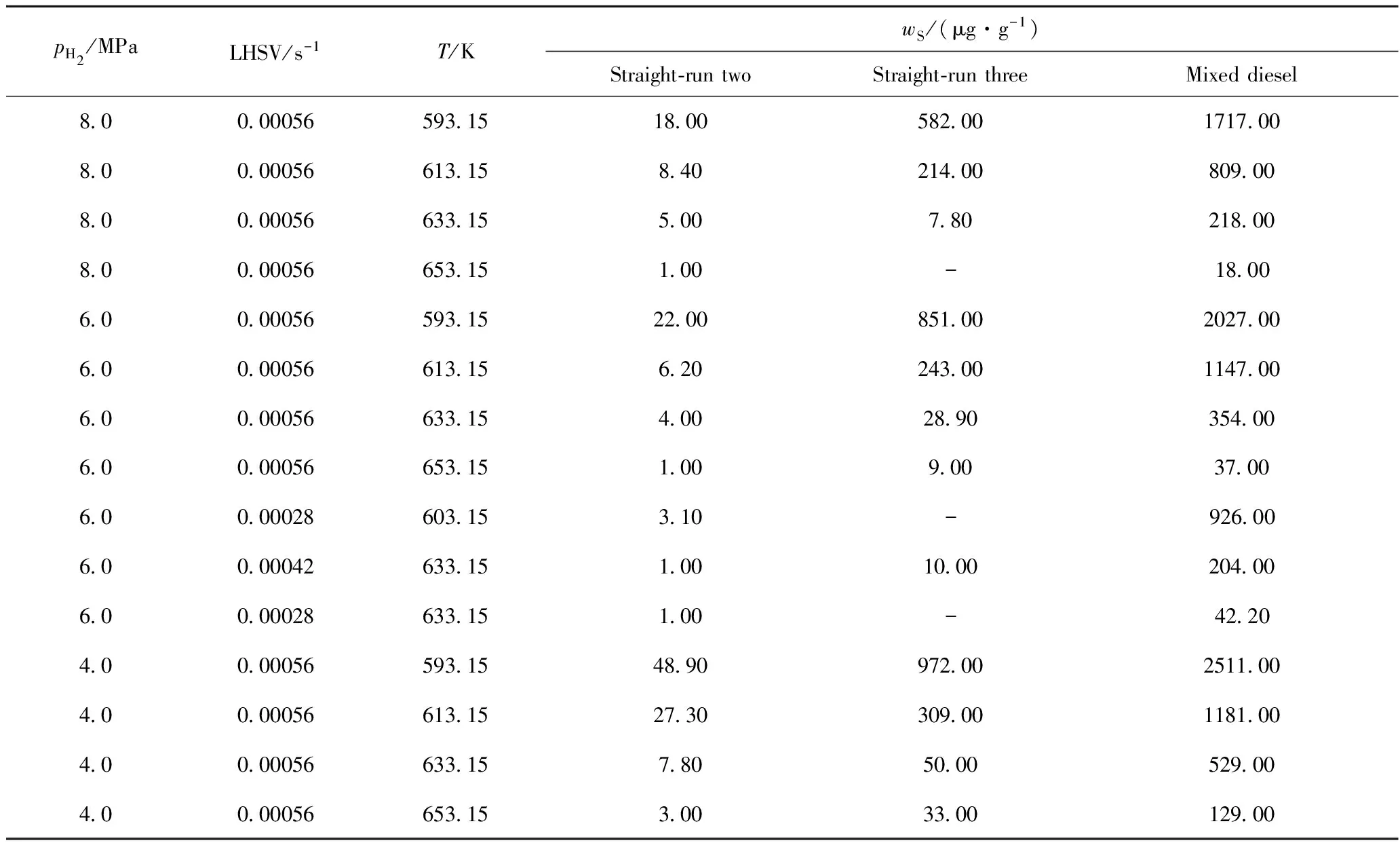
表2柴油的動力學實驗數據Table 2 Experimental kinetic data of diesel
V(H2)/V(Oil)=400
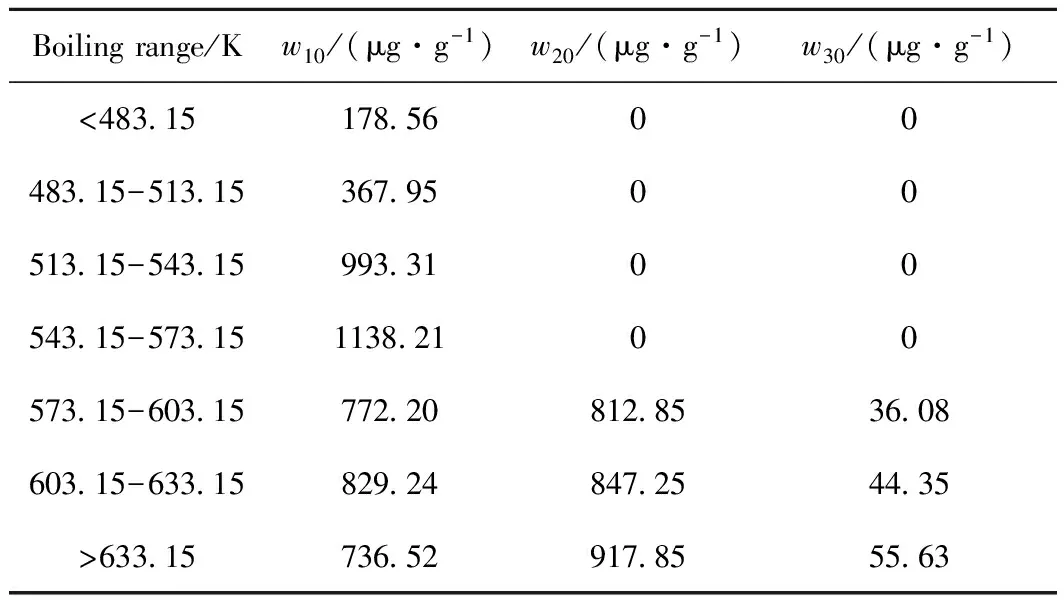
表3 混合柴油實沸點蒸餾切割方案及分析數據Table 3 Analysis data and cutting scheme of thetrue boiling point distillation for mixed diesel
2.2 模型的建立
根據集總劃分原則[9],忽略內外擴散影響,綜合各方面因素,主要以一級反應進行集總模型的建立。按苯并噻吩類,二苯并噻吩類和4,6-二甲基二苯并噻吩類3類不同的硫化物構成三集總HDS模型,3類硫化物均按一級反應動力學計算。動力學方程為:
(1)
將式(1)積分得HDS后產品的硫質量分數分別為:
(2)
由式(2)可推導出產品中硫質量分數ws隨反應時間和反應溫度變化的反應動力學模型為:
ws=w10exp(-k1t)+w20exp(-k2t)+
w30exp(-k3t)
(3)
以反應壓力6.0 MPa為基準,式中各反應的速率常數由反應壓力修正后為:
(4)
將式(3)和式(4)與實沸點蒸餾的窄餾分數據結合,通過式(3)和式(4)各參數的求解來建立三集總一級反應動力學模型:
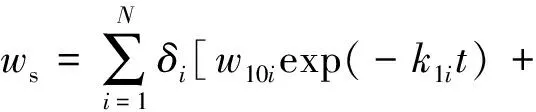
(5)
(6)
綜上,三集總一級反應動力學模型已建立,密度因同源性可不考慮,該模型由式(5)和式(6)共同組成,基本囊括了在本實驗中出現的各種影響脫硫的因素和反應條件。
2.3 模型參數求解
選擇Levenberg-Marquardt(簡稱L-M)算法,對實驗數據擬合。線性回歸參數獲得初值后,采用L-M非線性最小二乘法對式(3)和式(4)進行回歸,并對表2中混合柴油在不同實驗操作條件下的數據進行關聯,以柴油脫硫后硫質量分數實驗值和計算值的殘差平方和為最優目標函數Z:
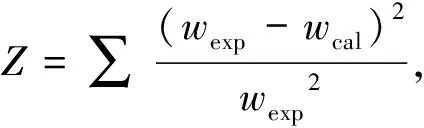
2.3.1反應速率常數
不同操作條件下,由于所需求的參數多,因此采用分步求解的方法。將表1中混合柴油初始硫質量分數w分為3類硫化物的硫質量分數w10、w20和w30,分別為5015.99 μg/g、2577.95 μg/g和136.06 μg/g,柴油硫質量分數與中平均沸點和密度相關聯,以柴油3類硫化物的實測值和計算值的殘差平方和為最優目標函數,經擬合得出3類硫化物的分配公式:
(7)
混合柴油在變化體積空速的條件下,以混合柴油脫硫后硫質量分數實驗值和計算值的殘差平方和為最優目標函數,對目標函數進行最小化,擬合出式(3)和式(4)中3個集總的硫質量分數及反應速率常數,結果如表4和表5所示。由表5可知,3類硫化物的反應速率常數揭示 了Ⅰ類硫化物在催化劑表面接近時發生反應最快,Ⅱ類硫化物次之,Ⅲ類硫化物反應最慢。
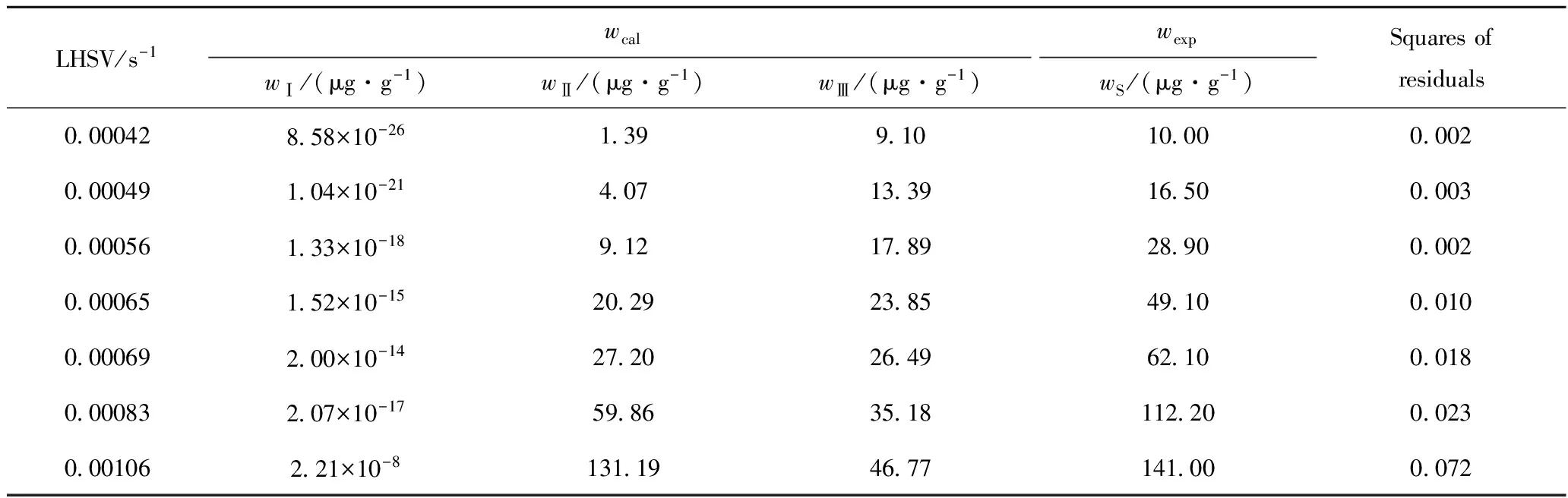
表4 不同空速下混合油HDS反應的計算Table 4 The parameters simulation of mixed diesel hydrodesulrization process at different LHSV
T=633.15 K;pH2=6.0 MPa;V(H2)/V(Oil)=400

表5 混合柴油HDS反應速率常數的擬合結果 Table 5 Reaction rate constants estimated by thekinetic model for mixed diesel hydrodesulrization process
T=633.15 K;pH2=6.0 MPa;V(H2)/V(Oil)=400
2.3.2指前因子和活化能
混合柴油在反應溫度變化時,擬合出3個集總的指前因子和活化能,結果如表6和表7所示。
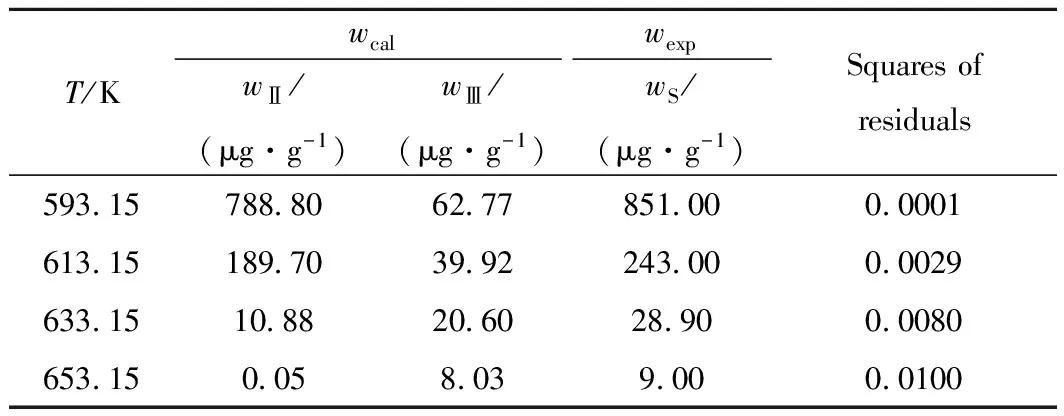
表6 不同溫度下混合柴油HDS反應的計算Table 6 The parameters simulation of mixed dieselhydrodesulrization process at different temperatures
LHSV=0.00056 s-1;pH2=6.0 MPa;V(H2)/V(Oil)=400
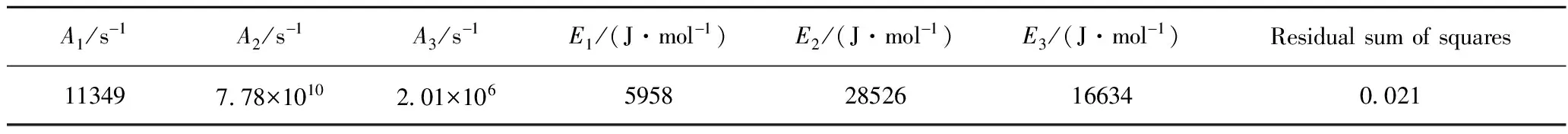
表7 混合柴油HDS反應擬合得到的動力學參數 Table 7 Kinetics model parameters estimated by the kinetic model for mixed diesel hydrodesulrization process
LHSV=0.00056 s-1;pH2=6.0 MPa;V(H2)/V(Oil)=400
由表7可知,混合柴油中難脫除硫化物的HDS活化能比易脫除硫化物的高,因而其反應速率隨溫度升高而加快的幅度也就更大,Ⅱ類硫化物HDS反應的活化能明顯大于其他兩類,說明Ⅱ類硫化物對溫度的敏感性最強。由回歸分析得到的動力學參數可知,Ⅰ類硫化物HDS反應的活化能為5958 J/mol,該反應活化能非常小,印證了這一反應很容易進行。
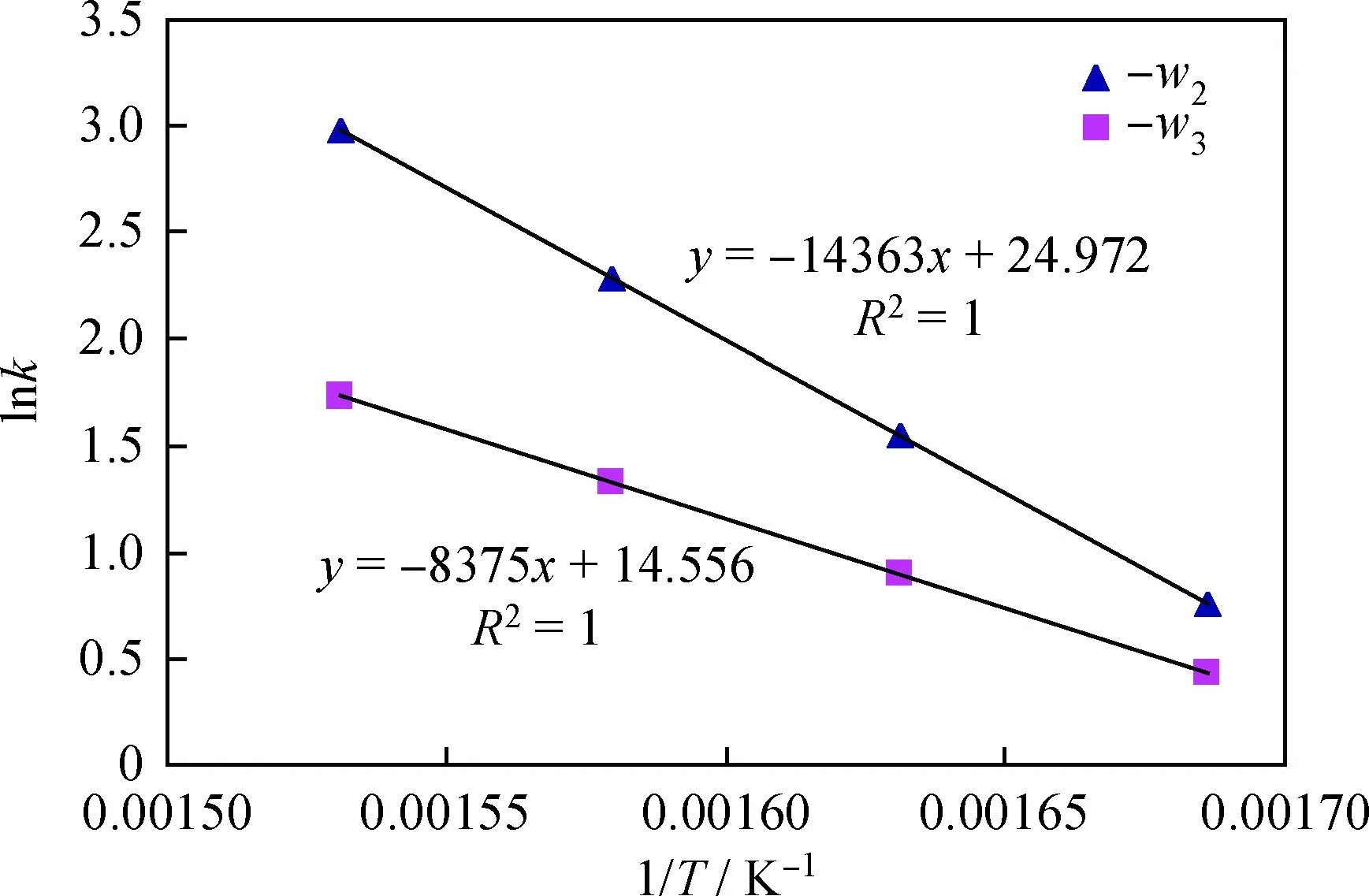
圖1 lnk與1/T的關系曲線Fig.1 Relation curve of lnk and 1/T
為檢驗以上擬合數據的合理性,計算得到混合柴油在4個反應溫度下的反應速率常數與反應溫度的關聯曲線,如圖1所示。由圖1可見,溫度對加氫脫硫反應速度影響符合阿累尼烏斯關系,曲線擬合很好,擬合得到的參數合理。
2.3.3氫分壓的修正參數
氫分壓對反應的影響也較明顯,因此對氫分壓進行一定的修正,擬合結果如表8和表9所示。表9 中α、β、γ分別表示3類硫化物的壓力指數項。由表9可見,Ⅰ類硫化物的壓力指數較小,表明氫分壓對Ⅰ類硫化物的HDS反應影響不大,敏感度不高;Ⅲ類硫化物的HDS反應對氫分壓的敏感性最強。驗證結果表明,用L-M算法對實驗數據擬合良好,各參數較好地描述了各類硫化物的HDS反應的過程。
2.3.4反應速率常數的修正參數
不同的油品,其餾程、密度等物理性質不盡相同,因而影響模型預測的精確度,這里僅對反應速率常數k進行修正,中平均沸點值由表1獲得,修正公式如下:
n=0.118×(API驗證柴油-API模型建立柴油)
修正后的反應速率常數k方程變為:
(8)
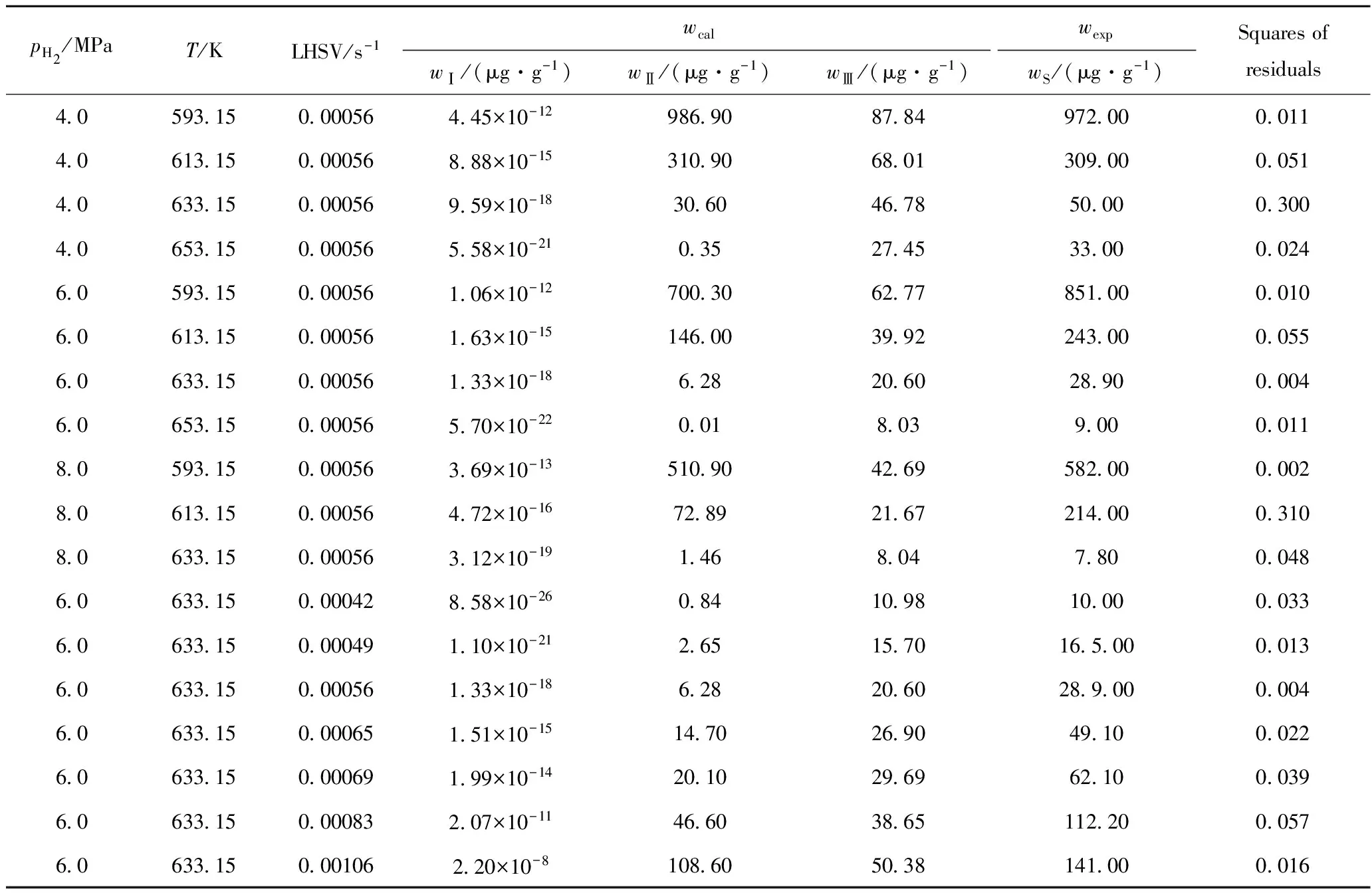
表8 不同操作條件(溫度、氫分壓、體積空速)下混合柴油HDS反應的計算結果Table 8 The parameters simulation of mixed diesel hydrodesulrization process atdifferent temperatures and hydrogen partial pressures and space velocities
V(H2)/V(Oil)=400

表9 混合柴油HDS反應擬合得到的動力學參數 Table 9 Kinetics model parameters estimated by thekinetic model for mixed diesel hydrodesulrization process
V(H2)/V(Oil)=400
將表2中常二線和常三線柴油的動力學數據代入式(3)、式(4)和式(7)驗證,計算值與實驗值的相關系數的平方(R2)均大于0.9550,表明分配公式符合硫化物分布,如表10所示。為了進一步考察該模型及參數的合理性,由表8中混合柴油加氫脫硫的實驗值與模型計算值作圖2可見,回歸分析的相關系數的平方為0.9721,實驗值與模型計算值的偏差較小,且均勻分布在對角線附近,回歸模型和實驗數據具有高度的相關性。表8數據實驗值和計算值的平均偏差為1.92%,說明模型參數的計算值和實驗值一致性較好。

表10 反應速率常數的修正參數和相關系數的平方Table 10 The correction parameters of reaction rateconstant and the correlation coefficient
1) Correlation coefficient
2.4 指前因子與中平均沸點的關系
由表1及以上數據可推導出其它2種柴油的指前因子A2和A3,如表11所示,Ⅰ類硫化物極容易脫除,在本實驗考慮中可忽略,因而只描述Ⅱ類硫化物和Ⅲ類硫化物的指前因子。為進一步提高式(3)和式(4)模型的精確度,將擬合出的各參數與實沸點蒸餾的窄餾分數據結合,建立更精準的式(5)和式(6)模型,同時用柴油的中平均沸點與3類硫化物的指前因子相關聯,可以得到關于每一類硫化物的關聯式,在關聯式上可以獲得不同柴油及各個窄餾分的指前因子,減少實驗時間。
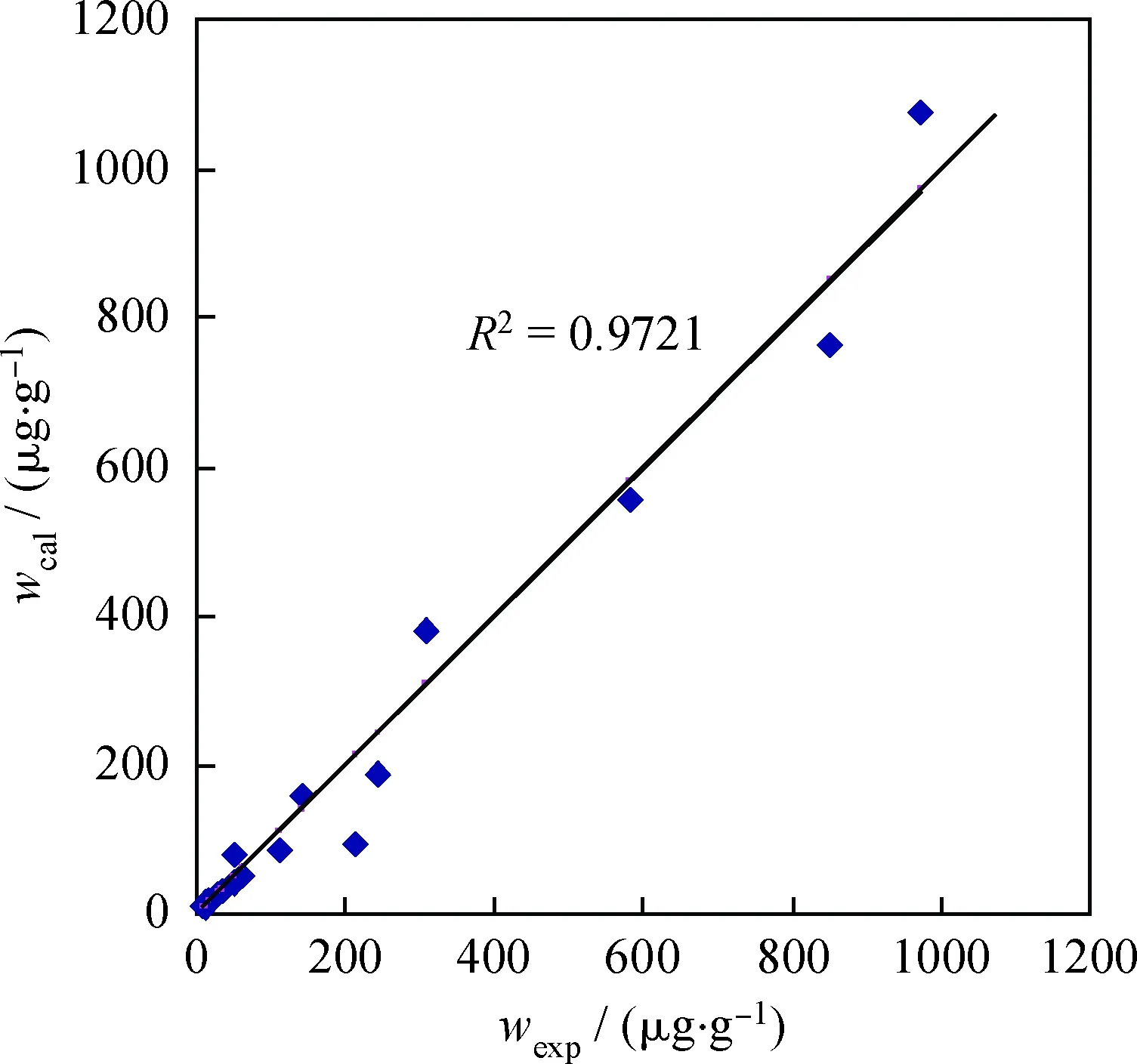
圖2 混合柴油產品硫質量分數實驗值與計算值Fig.2 Experimental and calculated ofmixed diesel sulfur mass fraction
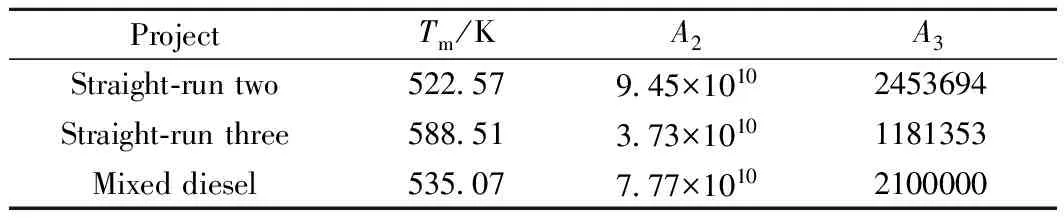
表11 柴油HDS反應的動力學參數Table 11 Kinetics model parameters estimated bydiesel hydrodesulrization process
三集總一級反應動力學模型以三集總為基礎,中平均沸點與反應速率常數的關聯公式即中平均沸點與指前因子的關聯公式為集總表現形式。Ⅱ類和Ⅲ類硫化物的指前因子隨中平均沸點變化的關聯式(9)如下:
(9)
3 模型驗證
表12為柴油實沸點蒸餾切割方案及3類硫化物的硫質量分數分析數據。以表12中常二和常三柴油的實沸點蒸餾切割數據對式(5)和式(8)三集總模型進行驗證,中平均沸點與反應速率常數的關聯公式在窄餾分中仍成立。常二和常三柴油在不同操作條件下的殘差平方和為1.08和0.69,常二線計算值偏差比常三線稍高的原因可能是其餾程輕,硫質量分數相對更低,3種硫化物的硫質量分數與常三線柴油差距較大所致。由圖3可知,擬合數據的相關系數平方為0.9635和0.9830,均優于式(3)和式(4)三集總模型時獲得的相關系數,說明集總模型中引入窄餾分是合理的,同時也能較好地用于預測柴油HDS的油品硫含量。
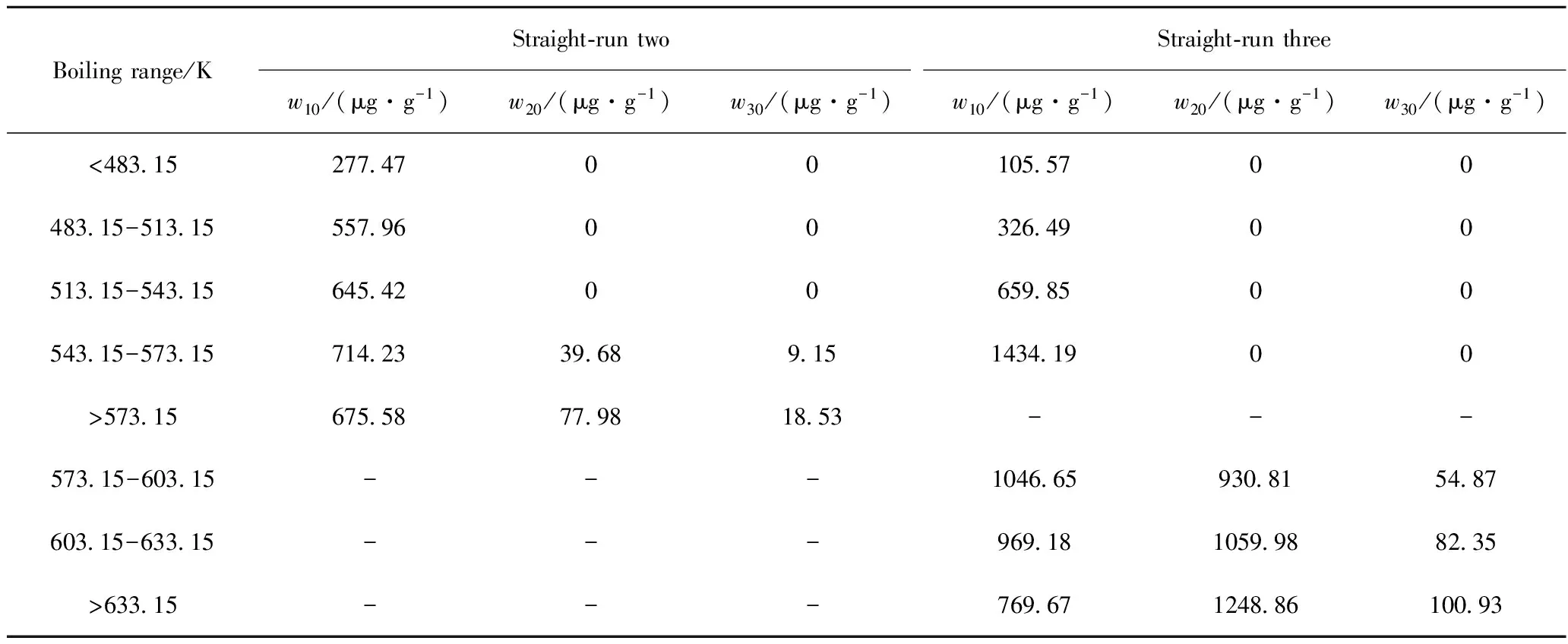
表12 柴油實沸點蒸餾切割方案及分析數據Table 12 Analysis data and cutting scheme of the true boiling point distillation for diesel
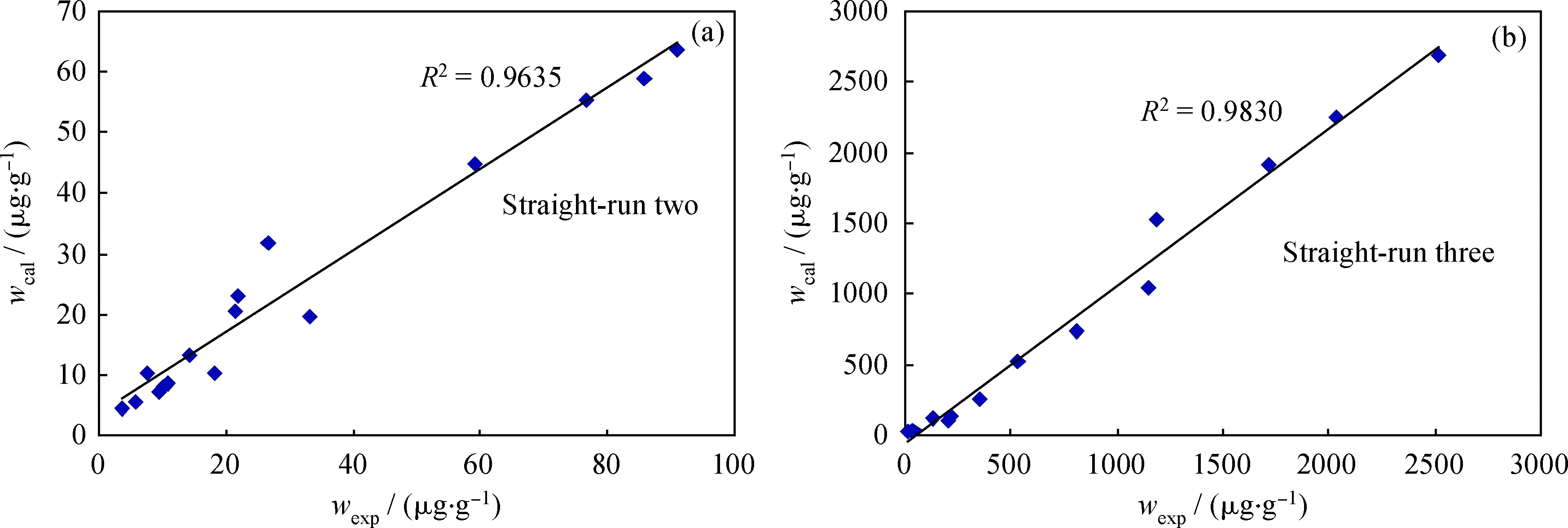
圖3 柴油產品硫質量分數實驗值與計算值Fig.3 Experimental and calculated of diesel sulfur mass fraction(a) Straight-run two; (b) Straight-run three
4 結 論
(1)在三集總模型基礎上將柴油實沸點蒸餾的窄餾分應用到建模當中,建立了三集總一級反應動力學模型,模型較高精度地預測深度和超深度脫硫操作條件下的產品硫含量,表明將柴油切割為窄餾分應用到建模當中是基本可行的。
(2)模型以中平均沸點與反應速率常數的關聯公式為依據,且反應速率常數均與其中平均沸點的4次方成反比,呈現了良好的規律性。通過柴油窄餾分的應用及硫化物分布擬合優化,調節參數,模型可以為柴油加氫精制工藝優化提供重要參考。
符號說明:
A1——Ⅰ集總HDS反應的指前因子,一級反應,s-1;
A2——Ⅱ集總HDS反應的指前因子,一級反應,s-1;
A3——Ⅲ集總HDS反應的指前因子,一級反應,s-1;
E1——Ⅰ集總HDS反應的活化能,J/mol;
E2——Ⅱ集總HDS反應的活化能,J/mol;
E3——Ⅲ集總HDS反應的活化能,J/mol;
k1——Ⅰ集總HDS反應速率常數,s-1;
k2——Ⅱ集總HDS反應速率常數,s-1;
k3——Ⅲ類集總HDS反應速率常數,s-1;
k1i——Ⅰ集總HDS反應速率常數,i為窄餾分,(i為1~N)數字由小至大表示餾分由輕到重,s-1;
k2i——Ⅱ集總HDS反應速率常數,i為窄餾分,(i為1~N)數字由小至大表示餾分由輕到重,s-1;
k3i——Ⅲ集總HDS反應速率常數,i為窄餾分,(i為1~N)數字由小至大表示餾分由輕到重,s-1;
LHSV——體積空速,s-1;
m——原料餾程對反應速率常數的修正參數;
mi——原料窄餾分餾程對反應速率常數的修正參數,i為窄餾分,(i為1~N)數字由小至大表示餾分由輕到重;
n——原料密度對反應速率常數的修正參數;
N——實沸點蒸餾切割的窄餾分份數;
pH2——氫分壓,MPa;
R——普適因子,8.314 J/(mol·K);
T——反應溫度,K;
Tm——油品的中平均沸點,K;
w——原料硫質量分數,μg/g;
w1——Ⅰ類硫化物HDS反應后剩余的硫質量分數,μg/g;
w2——Ⅱ類硫化物HDS反應后剩余的硫質量分數,μg/g;
w3——Ⅲ類硫化物HDS反應后剩余的硫質量分數,μg/g;
w10——Ⅰ類硫化物硫質量分數,μg/g;
w20——Ⅱ類硫化物硫質量分數,μg/g;
w30——Ⅲ類硫化物硫質量分數,μg/g;
w10i——Ⅰ類硫化物中窄餾分的初始硫質量分數,i為窄餾分編號,(i為1~N)數字由小至大表示餾分由輕到重,μg/g;
w20i——Ⅱ類硫化物中窄餾分的初始硫質量分數,i為窄餾分編號,(i為1~N)數字由小至大表示餾分由輕到重,μg/g;
w30i——Ⅲ類硫化物中窄餾分的初始硫質量分數,i為窄餾分編號,(i為1~N)數字由小至大表示餾分由輕到重,μg/g;
wⅠ——模型計算Ⅰ類硫化物硫質量分數,μg/g;
wⅡ——模型計算Ⅱ類硫化物硫質量分數,μg/g;
wⅢ——模型計算Ⅲ類硫化物硫質量分數,μg/g;
wexp——硫質量分數實驗值,μg/g;
wcal——硫質量分數計算值,μg/g;
ws——產品硫質量分數,μg/g;
α——Ⅰ類硫化物壓力的指數項;
β——Ⅱ類硫化物壓力的指數項;
γ——Ⅲ類硫化物壓力的指數項;
δi——實沸點蒸餾各窄餾分收率,i為窄餾分,(i為1~N)數字由小至大表示餾分由輕到重,%。
[1] 余夕志, 董振國, 任曉乾, 等. 柴油餾分加氫脫硫動力學及反應器研究進展[J].燃料化學學報, 2005, 33(3): 372-377.(YU Xizhi, DONG Zhenguo, REN Xiaoqian, et al. Recent progress in kinetics and reactor of hydrodesulfurization for diesel oil[J].Journal of Fuel Chemistry and Technology, 2005, 33(3): 372-377.)
[2] NAG N K, SPARE A V, BRODERICK DH, et al. Hydrodesulfurization of polycyclic aromatics catalyzed by sulfided:The relative reactivities[J].Journal of Catalysis, 1979, 57(3): 509-512.
[3] DALYF P.Hydrodesulfurization of benzothiopheneover CoO-MoO3-AL2O3catalyst[J].Journal of Catalysis, 1978, 51(2): 221-228.
[4] 王瑤, 孫仲超, 王安杰, 等. Co-Mo/MCM-41上二苯并噻吩加氫脫硫反應動力學研究[J].大連理工大學學報, 2004, 44(2): 207-211.(WANG Yao, SUN Zhongchao, WANG Anjie, et al. Kinetic study of hydrodesulfurization of dibenzothiophene over Co-Mo/MCM-41[J].Journal of Dalian University of Technology, 2004, 44(2): 207-211.)
[5] 方星, 方向晨, 程振民, 等. 柴油加氫脫硫反應動力學的研究[J].當代化工, 2005, 34(3): 145-153.(FANG Xing, FANG Xiangchen, CHENG Zhenmin, et al. Reaction kinetics of diesel deep hydrodesulfurization[J].Contemporary Chemical Industry, 2005, 34(3):145-153.)
[6] 馬成國, 翁惠新. 渣油加氫脫硫反應集總動力學模型的事前模擬[J].石油學報(石油加工), 2008, 24(6): 709-713. (MA Chengguo, WENG Huixin. Prior simulation of lumping kinetic models for residual oil HDS reaction[J].Acta Petrolei Sinica (Petroleum Processing Section), 2008, 24(6): 709-713.)
[7] 于航, 李術元, 靳廣洲, 等. 撫順頁巖油柴油餾分加氫脫硫動力學[J].石油學報(石油加工), 2011, 27(6): 924-928. (YU Hang, LI Shuyuan, JIN Guangzhou, et al. Kinetics of hydrodesulfurization diesel distillate from Fushun shale oil[J].Acta Petrolei Sinica (Petroleum Processing Section), 2011, 27(6): 924-928.)
[8] 李士才, 丁賀, 牛世坤, 等. 柴油深度加氫脫硫反應動力學研究[J].煉油技術與工程, 2015, 45(2): 39-42. (LI Shicai, DING He, NIU Shikun, et al. Study on kinetics of diesel deep hydrodesulfurization reaction[J].Petroleum Refinery Engineering, 2015, 45(2): 39-42.)
[9] 方向晨. 加氫裂化工藝與工程[M].北京:中國石化出版社, 2016.

