國產個性化3D打印全顳下頜關節生物力學分析
陳旭卓 周知航 王燁欣 鄭吉駟 張善勇 楊馳
顳下頜關節 (Temporomandibular joint,TMJ)是口腔頜面部唯一的左右雙側聯動關節,兼具滑動和轉動的功能,是人體最復雜的關節[1]。顳下頜關節病是一種常見且多發的疾病,表現為關節區疼痛、張口受限、咬牙合錯亂、頜骨嚴重功能障礙等一系列癥狀和體征[2]。終末期骨關節病、嚴重的髁突自溶性吸收、復發性關節強直、粉碎性髁突骨折和需要廣泛切除的關節區腫瘤等,需要應用自體骨移植或人工關節假體來重建功能和形態[3-4]。相對于自體骨移植技術,人工關節置換可有效避免供區的二次傷害,縮短手術時間,增加術區的適應性[3,5-6]。在國際上(尤其是發達國家),全TMJ假體是重建顳下頜關節的首選。在美國,每年進行1 000側以上的全TMJ假體置換手術[7]。根據人口比例,中國每年有4 000側以上TMJ需要進行假體置換[5,8]。國際上現有兩款主流全TMJ假體:Biomet/Lorenz標準型假體和TMJConcepts個性化假體。Biomet假體是根據歐美人的頜骨特征設計,所以在術中需要磨除大量骨組織[9]。而TMJConcepts缺乏國內注冊證,且價格昂貴 (每側15萬元),生產周期長。上述因素嚴重限制了兩種TMJ假體系統在中國的臨床應用[5,10]。
為了開發適合國人顱頜面解剖特征的全TMJ假體,我們測量了400名中國成年人的顱下頜解剖數據[11]。同時,我們遵循國際上提出的設計理念和原則,設計了羊的全TMJ假體,并植入羊體內,通過隨訪證實其效果良好[12-13]。基于以上基礎,我們設計并研發了國產的個性化的全TMJ假體。與TMJ Concepts類似,該假體關節窩部分使用3D打印鈦合金底座,通過先進的摩擦焊接技術與超高分子聚乙烯(UHMWPE)相連[14];下頜假體則是由鈷鉻鉬合金髁突頭和3D打印鈦合金下頜固位柄通過錐度連接。然而,這種假體的設計僅是基于臨床醫生的經驗,其生物力學性能是否符合臨床要求還有待研究。
本研究利用三維有限元方法,模擬在最大咀嚼力的條件下,關節假體各部分的應力分布和下頜骨的位移分布,借助模擬分析的結果,對假體的優化設計提供參考,同時為臨床應用提供一定的依據。
1 材料與方法
1.1 研究對象選擇及三維重建
選擇1例右側TMJ骨關節病晚期患者,在維持穩定的磨牙咬牙合基礎上,進行術前顱頜面CT檢查(GE Healthcare,Buckinghamshire,England), 掃描層厚為0.625 mm。隨后將數據存儲并導入到Mimics軟件(Version 18.0,Medical,Leuven,Belgium)用于顱頜面三維重建。對右側髁突病變部位進行模擬截骨后,使用 3-Matic Medical(Version9.0,Medical,Leuven,Belgium)設計個性化全顳下頜關節假體,然后導入三維重建模型(圖1)。
1.2 三維有限元模型的建立
以Hypermesh有限元網格生成模塊軟件(HyperWorks,美國)對模型預處理。以通用有限元分析軟件LS-DYNA(LSTC,美國)作為求解器和處理器。
考慮模型的對稱性及減少計算量,分析模型只考慮右側關節,并于對稱面施加對稱約束。由于分析結構較復雜,有限元模型以一階四面體網格為主,共19.5萬個單元,4.8萬個節點。考慮到一階四面體網格易使結構偏剛,分析采用帶節點轉動的選擇性縮減積分形式,可較好地減少一階四面體單元偏剛問題。同時,為了確保接觸面正常傳力,對接觸面網格進行了加密處理(圖2)。
1.3 材料參數
有限元分析所用材料的參數,參照部分材料供應商及相關文獻數據(表1)[16-18]。為確保TMJ假體的穩定性,假體各部分的應力應小于材料的屈服強度。根據文獻提供的肌肉力最大值和方向[19](表2、圖3),對關節假體施加最大肌力。由于部分骨組織已被切除,翼外肌作用力沒有附著點,在分析中未予考慮。
1.4 邊界條件和負載
在顴骨與關節窩假體之間,以及下頜骨與下頜升支假體之間,設置接觸關系。假體髁突頭與關節窩之間建立鉸鏈關系。對關節窩假體和和下頜骨前牙區設置固定約束,并在前牙區設定負載以在最大咀嚼力下模擬咬牙合運動。
2 結果
2.1 假體和下頜骨的位移分布
在閉口肌群肌力達到最大的情況下,模擬前牙的咬牙合運動。得出UHMWPE表面最大接觸力為495.7 N,前牙最大咬牙合力為 201.12 N(圖 3)。
下頜假體的最大位移分布于髁突頭與升支假體的連接部位,達0.4152 mm。隨著與髁突頭距離增加,假體各部位的位移量逐漸減小。就下頜骨而言,下頜骨后緣和冠突處的位移量最大(0.3691 mm)(圖4)。
2.2 假體各部位的應力分布情況
假體不同部位的Von Mises應力分布顯示,超高分子聚乙烯表面的最大應力達到20.66 MPa,略高于超高分子聚乙烯的屈服強度(19.00 MPa),也表明過大的咀嚼力可能導致關節窩假體部件的疲勞甚至斷裂。黏合層上的應力分布較均勻,最大應力為25.00 MPa(圖 5)。
下頜假體的最大應力值遠小于鈦合金的屈服強度。下頜假體的最大應力集中于髁突頭與下頜支的連接處的內側后緣,達122.1 MPa。
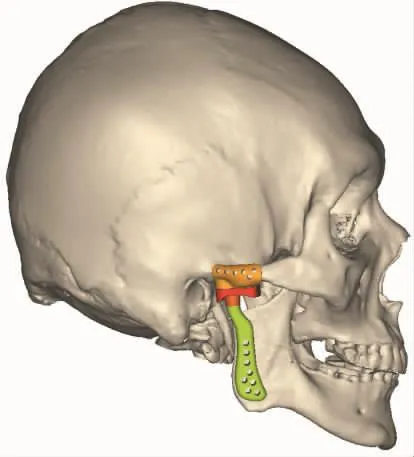
圖1 顱骨和個性化TMJ假體的三維模型重建Fig.1 Modeling of the skull and the custom-made TMJ prosthesis
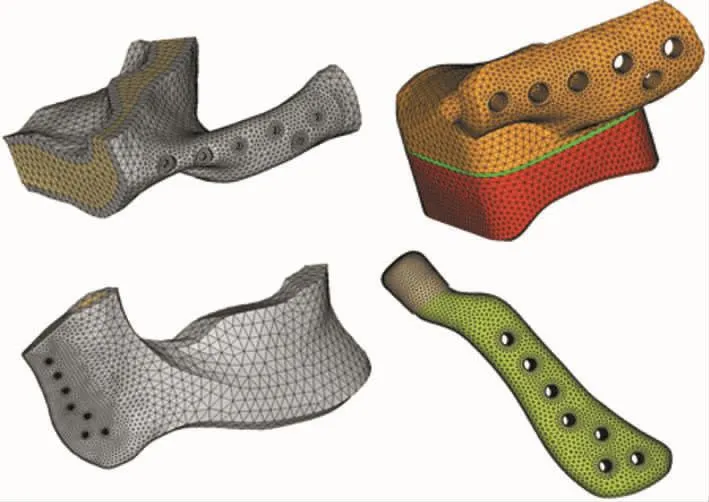
圖2 個性化全顳下頜關節假體的CAE有限元模型Fig.2 CAE finite element model of the custom-made TMJ prosthesis

表1 關節假體及骨材料參數Table 1 Mechanical parameters of the materials used in the modeling

表2 顳下頜關節肌肉作用力與方向Table 2 Parameters of jaw-elevator muscle forces

圖3 閉頜肌群在模型上的分布Fig 3 Jaw-closing muscles in the three-dimensional model
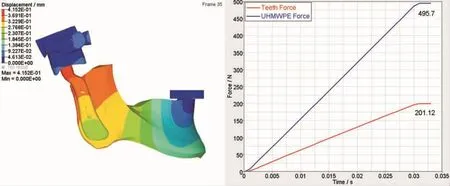
圖4 假體和骨的位移分布及最大關節窩最大壓力情況Fig 4 Displacement distribution of the TMJ prosthesis and the bone and the UHMWPE force

圖5 TMJ假體不同部位的應力分布Fig 5 Stress distribution on different parts of TMJ prosthesis
3 討論
國際上對顳下頜關節假體的設計研究已超過50年。半關節置換髁突或關節窩的方法曾盛行一時,但是由于骨與假體之間的摩擦可引起關節窩穿孔或髁突吸收,半關節置換的觀念已逐漸被淘汰[20]。到1965年,Christensen提出了全關節置換的概念,臨床上通過假體進行全顳下頜關節重建的技術逐漸成熟,出現了多種材料設計和概念[21],主要包括兩大類,即金屬對金屬接觸和金屬對塑料接觸。與骨科大關節假體發展一致,金屬關節窩對金屬關節頭的設計因磨損嚴重且產生金屬離子存在致癌風險而被淘汰[22]。基于骨科材料的成功經驗,鈷鉻鉬合金在髁突組件和UHMWPE在關節窩組件中的設計顯著提高了假體的成功率和使用壽命[23]。
TMJ假體材料的設計和選擇應符合以下原則[20]:①假體應由關節窩和下頜部組成。前者分為關節窩基部假體和窩部假體,后者分為下頜升支固位假體和髁突頭假體。②通過聚類分析,對關節窩窩部假體和下頜骨髁突頭假體進行標準化。關節窩基部假體和下頜升支固位假體應根據個人解剖特點進行個性化設計。③由于關節窩基部假體需要貼合顱底,因此在進行個性化設計時,必須考慮到顱底-關節窩的重建要求。④關節窩窩部應采用超高分子量聚乙烯制作,而髁突頭應采用鉻鈷鉬合金。
根據上述原則,我們運用3D打印技術成功設計了適合國人的個性化全TMJ假體。與其他全TMJ假體相比,該假體設計具有更深的關節窩和更窄的顴弓等解剖特征[24]。為了適合每個患者的解剖結構,關節窩基部和下頜升支固位部是個性化定制,避免了術中大量修整骨組織。這種改進不僅有效地節省手術時間,而且減少了頜骨的繼發性創傷。此外,3D打印技術首次被應用于顳下頜關節假體的加工制造。然而,這種創新性的假體需要生物力學分析來驗證其安全性、有效性和精確性。
均勻的應力分布和穩定的固位,是假體成功應用于臨床的前提條件。假體特定部位的應力集中可能引起災難性后果,如應力疲勞最終可導致假體折裂。這就要求仔細評估假體應力分布情況,防止機械缺陷引起的各類不良結果。此前有許多針對顳下頜關節假體應力分布的研究,但大部分研究僅局限于下頜假體的應力分布,很少有涉及關節窩假體應力分布的相關研究。Kashi等[25]研究發現,下頜假體最大應力位于距離髁突頭最近的螺釘孔內。若在此螺孔同一水平處另增加一螺釘固位,則可減小應力集中的程度。Abel等[26]對一種髁突支持式假體進行有限元分析研究,該假體優點在于可將假體上大部分應力轉移至下頜骨,減少了假體和螺釘周圍骨的局部應力。Bekcioglu等[19]認為,在對單側關節進行假體置換的模型中,假體側髁突頭局部的應力顯著增加,同時對側天然關節應力也增加,這意味著單側TMJ假體可能同時增加患側和健側關節的應力。雖然這些研究評估了下頜假體的應力分布,并對不同假體的改進方案提出了相應的建議,但缺乏對關節窩假體應力分布情況的有效分析。
本研究對全TMJ假體的應力分布進行了詳細研究,尤其針對關節窩假體。與Kashi等[25]的研究結果相一致,本研究發現下頜假體的應力主要集中在髁突后緣內側面,也是髁突假體與下頜固位假體的交界處。盡管該區域的最大應力為122.1MPa,遠低于鈦合金的屈服強度,但該交界區域存在局部進行性應力疲勞的風險。該結果表明,在下頜假體,除了髁突頭與下頜升支交界區域,其應力遠小于材料的屈服應力,材料安全系數比較高,可酌情進行材料削減。同時,我們發現UHMWPE表面的最大應力達到了20.66 MPa,略高于UHMWPE材料的屈服強度。說明咀嚼力過大時會對關節窩產生破壞,因此患者應盡量避免咀嚼硬物,同時應考慮采用強度更高的關節窩假體材料進行替換,或對現有關節窩假體材料進行材料復合及改性,以滿足理想的力學需求。
另一個不容忽視的結果是下頜假體的位移分布在髁突頭處最大,約為0.415 mm,假體各部分的位移量隨著與髁突間的距離增加而減少。此結果表明,髁突與下頜固位柄之間存在一定程度的相對位移。主要由于本有限元模型通過模擬機體最大咀嚼力分析假體的位移情況,是一種較為極端的情況;同時,該假體不同于Biomet標準型假體的單一鈷鉻鉬合金下頜假體,在髁突假體和下頜固位柄之間應用錐度連接。因此,為了提高髁突假體與下頜固位柄之間連接的穩定性,兩者之間的連接還有待進一步改進。目前在中國使用熔融焊接工藝連接髁突和下頜升支固位柄仍存在技術瓶頸,希望今后先進的焊接和黏合技術可以解決個性化假體下頜部件的連接問題。
本研究利用有限元分析工具進行生物力學研究,不可避免地存在一些缺陷。首先,本研究沒有模擬不同咬牙合狀態下的假體應力分布情況;其次,本研究通過假設假體與骨之間的黏合關系來評估應力分布,未建立固位螺釘模型。螺釘模型缺乏可能對最終結果產生一定的影響。今后的相關研究將建立固位螺釘模型,以分析不同配置和排列下的螺釘對骨和假體應力分布的影響;另外,本研究未對個體的咀嚼肌進行個性化肌力定制研究。因此,在后續研究中,我們會根據個體不同咀嚼肌的形態參數進行個性化肌力定制下的有限元分析。
綜上所述,本有限元分析結果表明,國產個性化3D打印全顳下頜關節假體應力分布較為均勻,穩定性良好。但是,該假體無論在設計和材料上都具有很大的改進空間,還需要進一步的機械力學測試和動物實驗以驗證其穩定性、安全性和精準性。
[1]Sidebottom AJ,UK TMJreplacement surgeons,British Association of Oral and Maxillofacial Surgeons.Guidelines for the replacement of temporomandibular joints in the United Kingdom[J].Br JOral Maxillofac Surg,2008,46(2):146-147.
[2]Franco R,Basili M,Venditti A,et al.Statistical analysis of the frequency distribution of signs and symptoms of patients with temporomandibular disorders[J].Oral Implantol(Rome),2016,9(4):190-201.
[3]Katsnelson A,Markiewicz MR,Keith DA,et al.Operative management of temporomandibular joint ankylosis:a systematic review and meta-analysis[J].J Oral Maxillofac Surg,2012,70(3):531-536.
[4]Kurtoglu C,Kurkcu M,Sertdemir Y,et al.Temporomandibular disorders in patients with rheumatoid arthritis:A clinical study[J].Niger JClin Pract,2016,19(6):715-720.
[5]Zhang SY,Liu H,Yang C,et al.Modified surgical techniques for total alloplastictemporomandibular joint replacement:One institution's experience[J].J Craniomaxillofac Surg,2015,43(6):934-939.
[6]Qiu YT,Yang C,Chen MJ.Endoscopically assisted reconstruction of the mandibular condyle with a costochondral graft through a modified preauricular approach[J].Br J Oral Maxillofac Surg,2010,48(6):443-447.
[7]Onoriobe U,Miloro M,Sukotjo C,et al.How many temporo mandibular joint total joint alloplastic implants will be placed in the United States in 2030[J]?JOral Maxillofac Surg,2016,74(8):1531-1538.
[8]Bai G,He D,Yang C,et al.Application of digital templates to guide total alloplastic joint replacement surgery with Biomet standard replacement system[J].J Oral Maxillofac Surg,2014,72(12):2440-2452.
[9]Giannakopoulos HE,Sinn DP,Quinn PD.Biomet microfixation temporomandibular joint replacement system:a 3-year follow-up study of patients treated during 1995 to 2005[J].JOral Maxillofac Surg,2012,70(4):787-794.
[10]Wolford LM,Mercuri LG,Schneiderman ED,et al.Twenty-year follow-up study on a patient-fitted temporomandibular joint prosthesis:the Techmedica/TMJ Concepts device[J].J Oral Maxillofac Surg,2015,73(5):952-960.
[11]焦子先,鄭吉駟,劉歡,等.成人顱下頜骨解剖測量分析[J].中國口腔頜面外科雜志,2015,13(2):151-154.
[12]Shen P,Zhang SY,Yang C,et al.Stability study of total TMJ replacement on sheep[J].J Craniomaxillofac Surg,2014,42(7):1265-1270.
[13]Shen P,Zhang SY,Yang C,et al.The mandibular symmetry evaluationof total temporomandibular joint replacement on developingsheep[J].JCraniomaxillofac Surg,2014,42(3):201-205.
[14]Chen K,Chen BX,Zhang SY,et al.Friction spot welding between porous TC4 titanium alloy and ultra-high molecular weight polyethylene[J].Mater Design,2017,132(15):178-187.
[15]Toniollo MB,Macedo AP,Pupim D,et al.Finite element analysis of bone stress in the posterior mandible using regular and short implants,in the same context,with splinted and nonsplinted prostheses[J].Int JOral Maxillofac Implants,2017,32(4):e199-e206.
[16]Ke Z,Li C,Zhu Z,et al.Measurement of the dynamic Young's modulus of porous titanium and Ti6Al4V[J].JMater Sci,2007,42(17):7348-7353.
[17]Suhendra N,Stachowiak GW.Computational model of asperity contact for the prediction of UHMWPE mechanical and wear behaviour in total hip joint replacements[J].Tribol Lett,2007,25(1):9-22.
[18]Geetha M,Singh AK,Asokamani R,et al.Ti based biomaterials,the ultimate choice for orthopaedic implants-A review[J].Prog Mater Sci,2009,54(3):397-425.
[19]Bekcioglu B,Bulut E,Bas B.The effects of unilateral alloplastic temporomand?bular joint replacement on the opposite side natural joint:A finite element analysis[J].J Oral Maxillofac Surg,2017,75(11):2316-2322.
[20]Driemel O,Ach T,Müller-Richter UD,et al.Historical development of alloplastic temporomandibular joint replacement before 1945[J].Int JOral Maxillofac Surg,2009,38(4):301-307.
[21]Guarda-Nardini L,Manfredini D,Ferronato G.Temporomandibular joint total replacement prosthesis:current knowledge and considerations for the future[J].Int J Oral Maxillofac Surg,2008,37(2):103-110.
[22]Speculand B,Hensher R,Powell D.Total prosthetic replacement of the TMJ:experience with two systems 1988-1997[J].Br JOral Maxillofac Surg,2000,38(4):360-369.
[23]Johnson NR,Roberts MJ,Doi SA,et al.Total temporomandibular joint replacement prostheses:a systematic review and biasadjusted meta-analysis[J].Int JOral Maxillofac Surg,2017,46(1):86-92.
[24]Zhang LZ,Meng SS,He DM,et al.Three-dimensional measurement and cluster analysis for determining the size ranges of Chinese temporomandibular joint replacement prosthesis[J].Medicine(Baltimore),2016,95(8):e2897.
[25]Kashi A,Chowdhury AR,Saha S.Finite element analysis of a TMJimplant[J].JDent Res,2010,89(3):241-245.
[26]Abel EW,Hilgers A,Mcloughlin PM.Finite element analysis of a condylar support prosthesis to replace the temporomandibular joint[J].Br JOral Maxillofac Surg,2015,53(4):352-357.

