術后持續靜脈鎮痛對肺癌患者細胞免疫功能的影響
段偉琴
目前臨床治療肺癌治療仍以手術治療為主。肺癌手術創傷大,術后疼痛劇烈,并通過神經內分泌系統對免疫系統造成一定影響,淋巴組織中的淋巴細胞增多,且淋巴細胞的反應降低,從而抑制患者免疫功能,增加術后感染率及術中脫落的腫瘤細胞微栓存活率,不利于患者的術后康復[1]。右美托咪定是1種α2腎上腺素受體激動劑,具有抑制交感活性,減輕應激反應等藥理特性,同時可減少術中阿片類藥物的用量,減輕對全身器官的影響,目前已作為麻醉輔助藥應用于臨床[2]。本研究在肺癌患者術后使用右美托咪定復合舒芬太尼用于靜脈自控鎮痛,分析其對細胞免疫功能的影響,為臨床合理用藥提供依據。
1 資料與方法
1.1 臨床資料
選擇2014年1月至2016年9月于本院行肺癌開胸根治術的80例患者作為研究對象。年齡25~53歲,ASAⅠ~Ⅱ級。排除標準:①小細胞肺癌患者;②伴有免疫系統疾病或其他嚴重臟器器質性疾病者;③阿片類藥物過敏者;④硬膜外阻滯有禁忌或近期應用擬腎上腺類藥物患者。將所有患者隨機分為對照組與觀察組各40例。觀察組在麻醉前給予右美托咪定預處理,其他同對照組。兩組擇期行肺癌開胸根治術的患者在年齡、體重、性別等方面基本一致(P>0.05)。
1.2 方法
觀察組在麻醉前泵注右美托咪定(0.5 μg/kg,溶于氯化鈉注射液 20 mL, 10 min 泵注完畢),對照組予以等量氯化鈉注射液。兩組麻醉誘導相同:0.5 μg/kg舒芬太尼、0.1 mg/kg咪達唑侖、0.15 mg/kg順式阿曲庫銨、1.5 mg/kg丙泊酚快速誘導。完成氣管插管后行機械通氣。麻醉維持:靜脈泵注5~8 mg/kg·h丙泊酚、4~5 μg/kg·h瑞芬太尼。術畢行自控靜脈鎮痛(PCIA)。泵內藥物配方:舒芬太尼3 μg/kg,用氯化鈉注射液稀釋至150 mL,背景輸注速率2 mL/h,自控劑量0.5 mL/次,鎖定時間15 min。
1.3 觀察指標及評定方法
①于術后24 h、48 h采用視覺模擬疼痛評分(VAS)法對患者進行疼痛分級評分;鎮靜程度采用Ramsay法評定。②于術前、術后1天及7天應用FACSCalibur 流式細胞儀測定患者外周靜脈血中NK細胞、T淋巴細胞亞群水平。③記錄兩組PCIA期間的不良反應發生情況。
1.4 統計學分析
2 結果
2.1 患者鎮痛鎮靜評分情況分析
于術后24 h、48 h時,觀察組較對照組VAS評分顯著下降(P<0.05),并且其Ramsay評分較對照組患者顯著升高(P<0.05),見表1。
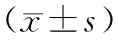
表1 患者鎮痛鎮靜評分
2.2 2組T細胞亞群及NK細胞水平比較
術前兩組各T細胞亞群及NK細胞水平對比無顯著性差異(P>0.05);術后1天觀察組CD3+細胞、CD4+細胞、CD8+細胞、CD4+/CD8+比值及NK細胞水平顯著高于對照組(P<0.05),見表2。
2.3 患者不良反應發生情況
對照組15例(32.5%)出現不良反應,觀察組4例(10.0%),觀察組較對照組不良反應發生率顯著下降(P<0.05),見表3。
3 討論
腫瘤的發生、發展及轉移與機體免疫功能的低下相關,同時免疫系統也在發揮著抗腫瘤作用[3]。機體對于腫瘤的免疫應答相當復雜,主要由細胞免疫、體液免疫以及細胞因子的分泌三方面組成,三者之者相互影響與調節,共同發揮抗腫瘤作用。其中細胞免疫的作用是機體抗腫瘤免疫的重要機制[4]。
作為人體重要的免疫效應細胞,T細胞亞群可直接反映人體的細胞免疫功能。代表細胞免疫總體水平的CD3+細胞,包括外周所有成熟T細胞;而作為輔助T細胞的CD4+細胞,可釋放多種細胞因子如白細胞介素-2、γ干擾素、白細胞介素-4等促進B淋巴細胞活化,生成抗體,發揮體液免疫效應,激活巨噬細胞與NK細胞,發揮細胞免疫效應[5];CD8+細胞是免疫抑制細胞,發揮負調節作用,抑制機體的免疫應答。CD4+/CD8+比值過高或過低均表示細胞免疫調節功能紊亂,CD4+/CD8+降低通常代表病人病情較嚴重及預后不良,可作為判定體內免疫系統狀態的重要指標[6]。正常情況下T細胞各亞群間保持動態平衡,共同發揮機體的免疫機制作用。NK細胞(自然殺傷細胞)T、B淋巴細胞之外的第三類淋巴細胞,是非特異性細胞免疫的重要組成部分,近年來發現在抗腫瘤方面具有重要意義,其數量的減少可直接造成機體的免疫功能下降[7]。

表2 患者NK細胞及T細胞亞群水平比較

表3 患者不良反應發生情況/例
本研究結果顯示,兩組在術前各T細胞亞群及NK細胞水平對比無顯著性差異(P>0.05);術后1天觀察組CD3+細胞、CD4+細胞、CD8+細胞、CD4+/CD8+比值及NK細胞水平顯著高于對照組(P<0.05)。研究表明,舒芬太尼和芬太尼等藥物對體內的免疫反應具有抑制作用,可使腫瘤轉移復發率顯著增高。本組病例中觀察組患者較對照組患者的細胞免疫水平顯著要高(P<0.05),其機制可能右美托咪定能作用于巨噬細胞表面的α2受體,從而激活巨噬細胞,使其介導的細胞免疫反應增強,進而在很大程度上使細胞免疫功能提高。此外右美托咪定的應用可使舒芬太尼的用量減少,從而使細胞免疫功能有效提高。
研究證明當右美托咪定用以輔助鎮靜時,能產生1種“可喚醒”鎮靜狀態,可術中可隨時被喚醒,且鎮靜效果較佳,術中患者呼吸循環穩定[8]。本研究結果顯示,在術后24 h、48 h時,觀察組患者較對照組患者的VAS評分顯著要低(P<0.05),并且其Ramsay評分也較對照組患者顯著要高(P<0.05)。提示采用右美托咪定進行預處理可獲得更好的鎮痛、鎮靜效果。此外,兩組不良反應發生率對比,觀察組共4例(10.0%),明顯低于對照組的13例(32.5%)(P<0.05)。表明右美托咪定具有較高的安全性。
綜上所述,在肺癌患者術后持續靜脈鎮痛中采用右美托咪定進行預處理,可提高鎮痛效果,且不會較大程度地抑制患者的細胞免疫功能,不良反應發生率低,有利于提高患者預后。
[1] 馮 芳.兩種不同術后鎮痛方式對肺癌根治術病人術后免疫功能的影響〔D〕.安徽醫科大學,2015.
[2] 周明明,袁建國,周艷紅,等.肺癌患者術后在ICU應用右美托咪定對免疫功能的影響〔J〕.中國藥房,2014,25(18):1685-1687.
[3] 陸海波,陳 默,司 波,等.多模式鎮痛對肺癌根治術患者術后疼痛和免疫功能的影響〔J〕.中國臨床研究,2015,28(11):1493-1495.
[4] 亓憲銀,劉民杰.復方苦參注射液對肺癌術后化療患者免疫功能的影響〔J〕.現代腫瘤醫學,2014,22(1):84-86.
[5] 屈 強,王 敏,李 新.肺癌患者術后不同鎮痛模式對免疫功能的影響〔J〕.重慶醫學,2010,39(23):3182-3184.
[6] 李亞林.兩種術后鎮痛方法對肺癌患者應激反應和細胞免疫的影響〔D〕.昆明醫學院,2007.
[7] 石世堅,張奕文,邢祖民.術后靜脈鎮痛對肺癌手術患者圍術期免疫反應及兒茶酚胺的影響〔J〕.中國實用醫藥,2010,5(3):24-26.
[8] 王建波,牛義凱,丁玉峰.右美托咪定對肺癌根治術患者圍術期免疫功能及術后蘇醒質量的影響〔J〕.實用臨床醫藥雜志,2015,19(7):125-126.

