碳酸鈣/鐵酸鈣復合催化劑制備及其催化性能
亓 峰
(徐州市教育局,江蘇徐州221000)
人類步入工業革命帶來的飛速發展的黃金時期,享受著各種如交通等帶來的便捷服務,但同時也面臨著嚴重的空氣污染。作為便捷服務的交通行業,驅動汽車等奔馳的源動力還主要以汽油為主,而汽油的主要成分是大量的硫化物,當其燃燒后會產生大量的硫氧化物,對空氣造成污染。目前,人類已經發明了很多方法來降低硫氧化物對空氣的污染,包括轉化抽提法、吸附法等[1-2]。然而,汽油中的噻吩類化合物具有較高的穩定性和空間位阻效應,采用上述傳統的方法很難進行脫硫去除[3-7]。因此,需要開發一種新型的催化劑進行氧化脫硫降解汽油。
目前,國內外研究較多的是單一催化劑對汽油的降解脫硫,對復合催化劑脫硫反應的研究相對較少。CaCO3/CaFe2O4是一種復合催化劑,可能具有較高的催化活性。然而,目前制備復合催化劑的方法主要是負載法和浸漬法,多采用工業級的現成產品進行負載或浸漬,很少采用相應的方法合成單一的催化劑后再進行負載或浸漬[8-10]。CaFe2O4載體合成方法較多,主要包括固相反應法、溶膠-凝膠法和燃燒法等[11-13],但對于以CaFe2O4為載體的復合催化劑,目前僅通過研磨-焙燒的方法[14]和自蔓延燃燒溶膠-凝膠法[15]分別合成了 CaFe2O4/Bi2WO6和CaFe2O4/α-Fe2O3催化劑,尚未見有合成CaCO3/CaFe2O4復合催化劑的報道。筆者采用兩步法合成CaCO3/CaFe2O4復合催化劑,先用水熱法合成CaFe2O4催化劑載體,再用超聲浸漬法合成CaCO3/CaFe2O4復合催化劑。用X射線衍射儀和磁性分析儀對催化劑的物相和磁性進行分析。用噻吩正辛烷模擬汽油,研究了CaCO3/CaFe2O4隨著反應時間、催化劑添加量和反應溫度的變化對模擬汽油脫硫率的影響,考察CaCO3/CaFe2O4的催化活性。
1 實驗部分
1.1 CaCO3/CaFe2O4復合催化劑制備
1.1.1 水熱法制備CaFe2O4
以 Ca(NO3)2·4H2O 和 Fe(NO3)3·9H2O 為原料,采用水熱法制備CaFe2O4催化劑。按CaFe2O4化學計量 比 稱 取 Ca(NO3)2·4H2O 和 Fe(NO3)3·9H2O 使n(Ca)∶n(Fe)=1∶2,將其分別配制成適當濃度的溶液,標記為A溶液和B溶液。將A溶液緩慢倒入B溶液中,獲得 Ca(NO3)2·4H2O 和 Fe(NO3)3·9H2O 的混合溶液。待溶液澄清后去除不溶物,得到一個相對穩定的溶液。為獲得一定酸度的溶液,用KOH對溶液的酸度進行調節。取65 mL混合溶液,轉移至反應釜中,密封反應釜。將反應釜放入真空干燥箱中,以5℃/min的升溫速率升溫至250℃并保溫32 h。待反應釜冷卻至室溫后,取出反應產物,靜置24 h,用吸管吸出上層清液,用相應的試劑沖洗沉淀數次,試劑為乙酸和乙酸銨。將獲得的初級產物用純度為98%的無水乙醇沖洗5次,放入真空干燥箱中在135℃干燥24 h,獲得CaFe2O4催化劑。
1.1.2 負載法制備CaCO3/CaFe2O4
稱取一定量CaFe2O4催化劑,加入到質量濃度為5 g/L的CaCO3溶液中,置于超聲波清洗器中在室溫進行超聲浸漬。超聲功率為200 W,超聲時間為1 h,超聲頻率為30 kHz。過濾,在真空干燥箱中在135℃干燥24 h,獲得CaCO3/CaFe2O4復合催化劑。
1.2 CaCO3/CaFe2O4復合催化劑表征
1.2.1 物相和磁性分析
用DX 2700型X射線衍射儀(XRD)對CaCO3/CaFe2O4的物相進行分析。用7304型振動樣品磁強計(VSM)對CaCO3/CaFe2O4的磁性進行測量。
1.2.2 催化活性評價
采用CaCO3/CaFe2O4復合催化劑,以模擬汽油為考察對象考察其脫硫反應,評價CaCO3/CaFe2O4的催化活性。在環境溫度下配制一定濃度的噻吩正辛烷來模擬汽油,取100 mL模擬汽油,加入適量CaCO3/CaFe2O4、H2O2,放入 50 mL 石英試管中,在光化學反應儀上進行光催化反應。光源為可見光光源,為400 W金鹵燈,試管與可見光光源的距離為6cm,垂直放置。反應一段時間后,用萃取劑乙腈溶劑萃取硫的生成產物。用微庫侖分析儀測定脫硫前后硫含量的變化,并繪制相應曲線。
2 結果與討論
2.1 XRD分析
圖1為CaCO3/CaFe2O4復合催化劑XRD譜圖。從圖1看出,CaCO3衍射峰主要集中在2θ為21.045、29.567、31.828、33.789、39.876、43.472、50.387 °處 ,對應的晶面指數分別為(020)(220)(221)(212)(302)(023)(313),JCPDS 標準卡號為 17-0763;CaFe2O4對應的JCPDS標準卡號為32-0168,衍射峰對應的晶面指數為(040)(320)(140)(201)(410)(131)(420)(311)(141)(331)(241)(051)(421)(260)(360)(351)(161)(170)。從圖1看出,采用超聲浸漬法將CaCO3浸漬到CaFe2O4上制成CaCO3/CaFe2O4,并未改變CaFe2O4的晶相結構,表明復合催化劑較為穩定。
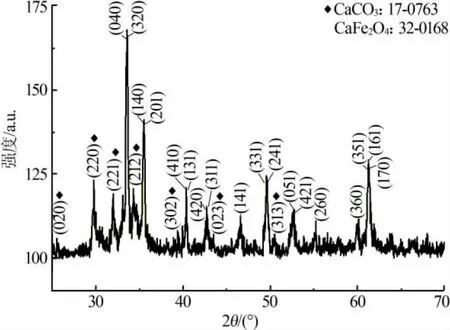
圖1 CaCO3/CaFe2O4復合催化劑XRD譜圖
2.2 磁性分析
磁性材料作為催化劑時,由于其具有良好的磁學性質,可以很好地回收甚至重復利用。CaCO3/CaFe2O4可能是一種磁性物質,將CaCO3/CaFe2O4在室溫下進行VSM檢測,測量范圍為(-3.98~3.98)×105A/m,結果見圖2。 從圖2看出,CaCO3/CaFe2O4在室溫下表現出鐵磁行為,由于CaFe2O4通常表現出順磁行為,表明采用該方法增強了CaFe2O4的磁性[12]。 其飽和磁化強度為 3.2 A·m2/kg、矯頑力為40 834.8 A/m。一般地,磁性材料具有大的磁矩比,可將其用于磁記錄介質、生物傳感器和信息存儲器等[16-17]。 磁矩比被定義為剩余磁化強度(Mr)和飽和磁化強度(Ms)的比值。根據計算可知,CaCO3/CaFe2O4的磁矩比約為0.83,表明該復合光催化劑可用作磁記錄介質、生物傳感器和信息存儲器等的候選材料。由于該復合催化劑具有較強的磁性,可方便回收再利用,在工業領域將具有潛在的應用。
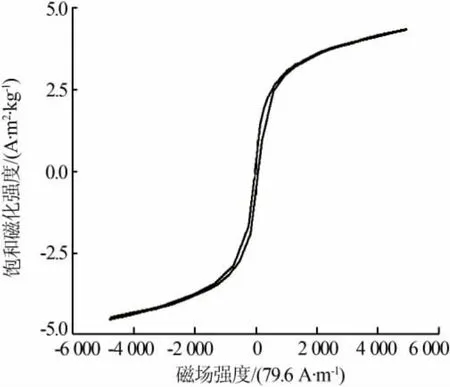
圖2 CaCO3/CaFe2O4復合催化劑VSM曲線
2.3 光催化活性評價
2.3.1 不同催化劑對脫硫率的影響
為考察CaCO3/CaFe2O4的催化活性,在3份同樣濃度的模擬汽油中分別加入1.2 mg/L的CaFe2O4、CaCO3/CaFe2O4和不加催化劑,光照時間為3 h,每隔20 min取一次樣進行測量,脫硫率隨時間的變化見圖3。從圖3看出,3個樣品的脫硫率均隨反應時間的增加而增加,達到一定時間后趨于穩定。脫硫反應幾乎均在140 min左右完成,之后變化不大。由圖3可知,不加入催化劑時,光照3 h脫硫率僅為29%。雖然這一比例很小,但也表明光照對模擬汽油有一定的降解作用,其主要原因可能是在模擬汽油中加入了H2O2,光照會激發H2O2產生羥基自由基,而羥基自由基本身是一種很強的氧化劑,可將部分模擬汽油氧化分解。當加入CaFe2O4時,3 h的脫硫率達到62%,表明光照射到CaFe2O4后,產生了大量的電子-空穴對,生成的光生空穴會向催化劑顆粒的表面移動,一部分直接與吸附的模擬汽油發生氧化反應,一部分則與H2O2發生反應生成羥基自由基,進而氧化模擬汽油;而生成的光生電子容易被模擬汽油中的溶解氧捕獲,經過一系列反應生成羥基自由基參與反應。加入CaFe2O4與不加入催化劑的作用機制一起,二者相互作用,增強了整個體系的脫硫率。當加入CaCO3/CaFe2O4后,3 h的脫硫率達到96%,表明CaCO3/CaFe2O4具有很好的催化活性。其脫硫率高的主要原因可能有2個:一是CaCO3的負載增加了復合催化劑的表面積,從而提高了模擬汽油的吸附量,最終導致模擬汽油降解的幾率提高;二是復合催化劑較大的比表面積增加了光催化反應的活性位,而這些活性位正是光催化氧化降解的必要因素,它會較大程度地吸附光子和模擬汽油分子,進而導致脫硫率提高。
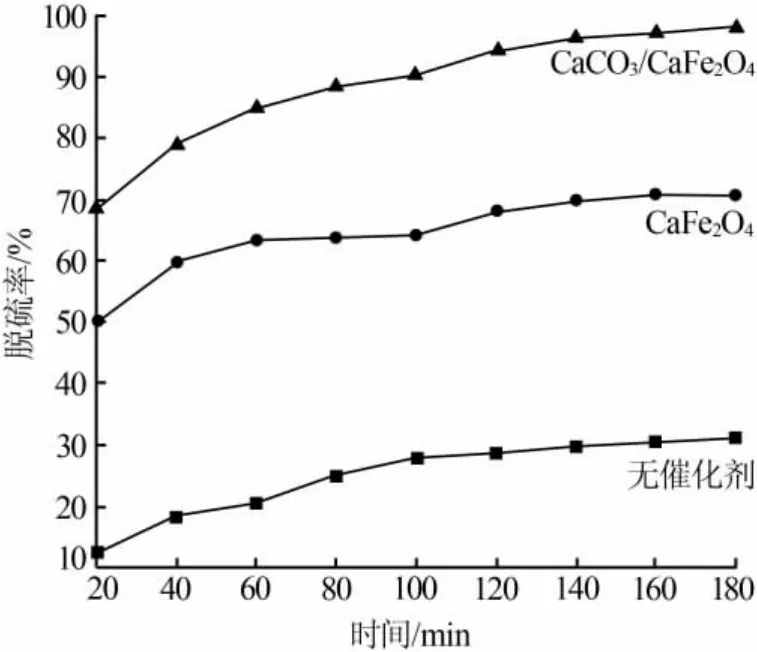
圖3 不同催化劑的脫硫率
2.3.2 催化劑添加量對脫硫率的影響
一般地,催化劑的催化反應主要在光催化劑的表面發生,它的催化活性的高低首先取決于電子-空穴對的產生量及電子-空穴對的復合速率,其次取決于光催化劑顆粒表面所能吸收的光子數和光催化降解目標的吸附率[18]。圖4為CaCO3/CaFe2O4不同添加量對模擬汽油脫硫率的影響。從圖4看出,模擬汽油的脫硫率隨著CaCO3/CaFe2O4添加量的增加先增大后減小。當CaCO3/CaFe2O4添加量由0.6mg/L增加到1.2mg/L時,模擬汽油的脫硫率不斷升高。這主要是由于反應溶液中催化劑含量少,產生的活性位溶液與模擬汽油發生氧化反應,且光子的利用率高,導致催化活性不斷升高。當CaCO3/CaFe2O4添加量為1.2 mg/L時,模擬汽油的脫硫率達到最大,表明最適合的催化劑添加量為1.2 mg/L,此時的光子利用率最高。然而,當CaCO3/CaFe2O4添加量超過1.2 mg/L以后,由于催化劑濃度的增大增強了光的散射作用,降低了光子的利用率,從而降低了復合催化劑的催化活性。從圖4也可以看出,無論催化劑的添加量是多少,模擬汽油的脫硫率均隨著反應時間的增加而不斷增加,當反應時間達到140 min后趨于穩定,與圖3的結果一致。

圖4 催化劑添加量對脫硫率的影響
2.3.3 反應溫度對脫硫率的影響
在光催化反應中,除了反應時間、催化劑添加量對脫硫率產生影響外,反應溫度也會對脫硫率產生影響。圖5給出了CaCO3/CaFe2O4在不同反應溫度下對模擬汽油的脫硫率。從圖5看出,在不同反應溫度下,CaCO3/CaFe2O4對模擬汽油的脫硫率均隨反應時間的增加而增大,且反應時間達到140 min時趨于穩定。從圖5也可以看出,隨著反應溫度的不斷升高脫硫率逐漸增加,當反應溫度達到45℃時脫硫率達到最高。然而,實驗中發現,隨著反應溫度的不斷升高,模擬汽油的揮發速率不斷增加,進而影響了整個光催化反應的進行。當反應時間稍長時,低反應溫度下的脫硫率也能達到高反應溫度時的脫硫率水平。根據圖5可知,CaCO3/CaFe2O4降解模擬汽油的反應溫度控制在室溫即可。
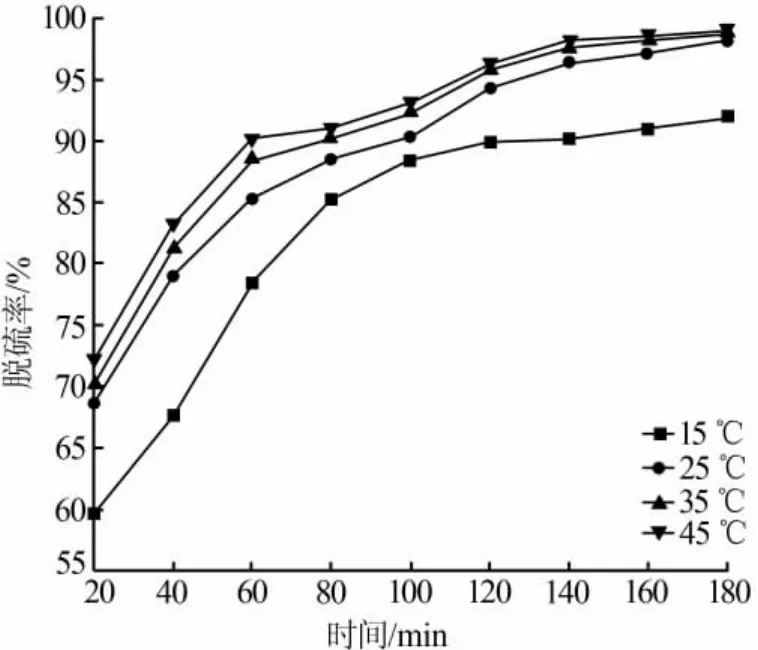
圖5 反應溫度對脫硫率的影響
3 結論
采用兩步法即水熱法和超聲浸漬法制備了CaCO3/CaFe2O4復合催化劑。XRD分析表明,CaCO3/CaFe2O4衍射峰僅包括CaCO3和CaFe2O4衍射峰,不含其他雜質峰。磁性測量表明,CaCO3/CaFe2O4表現出較強的鐵磁性,飽和磁化強度為3.2 A·m2/kg、矯頑力為40 834.8 A/m、磁矩比為0.83。模擬汽油催化脫硫實驗表明,CaCO3/CaFe2O4是一種較好的催化脫硫催化劑。通過研究不同反應時間、催化劑添加量以及反應溫度對催化劑脫硫反應的影響,表明最佳反應時間為140 min、催化劑添加量為1.2 mg/L、反應溫度為室溫。通過磁性分析和催化活性測試表明,CaCO3/CaFe2O4是一種可回收的具有較好催化活性的催化劑,是工業領域催化脫硫應用的候選材料。
[1]Li H M.Deep oxidative desulfurization of fuel oils catalyzed by decatungstates in the ionic liquid of[Bmim]PF6[J].Industrial &EngineeringChemistryResearch,2009,48(19):9034-9039.
[2]李晉昆.氯化鋇生產中氯氣脫硫提高產品質量[J].無機鹽工業,1980(4):36-37.
[3]陳蘭菊,郭紹輝,趙地順.催化裂化汽油中特征硫化物噻吩的催化氧化脫硫[J].化工學報,2007,58(3):652-655.
[4]Wang B,Zhu J,Ma H.Desulfurization from thiophene by SO42-/ZrO2catalyticoxidationatroomtemperatureandatmosphericpressure[J].Journal of Hazardous Materials,2009,164(1):256-264.
[5]趙地順,劉翠微,馬四國.FCC汽油模型化合物光催化氧化脫硫的研究[J].高等學校化學學報,2006,27(4):692-696.
[6]付輝,李會鵬,趙華,等.WO3-ZSM-5/MCM-41催化劑的合成及其催化氧化脫硫研究[J].無機鹽工業,2014,46(7):75-78.
[7]RobertsonJ.Removalofdibenzothiophenefromtetradecaneusingcatalytic photoxidation on TiO2/hectorite thin films layered catalyst[J].Journal of Colloid and Interface Science,2006,299(1):125-135.
[8]趙公大.磷鎢雜多酸鹽/SiO2可逆負載催化劑催化氯丙烯環氧化制環氧氯丙烷[J].催化學報,2008,29(6):509-512.
[9]黨丹.氧化鋁負載催化劑作用下以甲醇為烷基化試劑的苯酚氣相轉化制備苯甲醚[J].催化學報,2016,37(5):720-726.
[10]曹小華.AlH3P2W18O62·nH2O/皂土的制備、表征及其催化合成環己烯性能的研究[J].石油化工,2015,44(9):1083-1088.
[11]Zouari S,Ranno L,Cheikh-Rouhou A,et al.Structural and magnetic properties of the CaFe2-xMnxO4solid solution[J].Journal of Materials Chemistry,2003,13(4):951-956.
[12]Samariya A.Size dependent structural and magnetic behaviour of CaFe2O4[J].Current Applied Physics,2013,13(5):830-835.
[13]娜仁圖雅.燃燒法納米ZnFe2O4和CaFe2O4的制備及表征[J].內蒙古民族大學學報:自然科學蒙古文版,2009(1):9-12.
[14]張乾平,宿玲弟,王文慧,等.CaFe2O4/Bi2WO6光催化亞甲基藍降解性能的研究[J].廣州化工,2015,43(9):121-123.
[15]蘇天江,車如心,包躍宇.納米復合粉體CaFe2O4/α-Fe2O3的制備[J].大連交通大學學報,2008,29(4):72-75.
[16]Cao J,Kako T,Li P,et al.Fabrication of p-type CaFe2O4nanofilms for photoelectrochemical hydrogen generation[J].Electrochemistry Communications,2011,13(3):275-278.
[17]Kolev N.Temperature-dependent polarized Raman spectra of CaFe2O4[J].SolidStateCommunications,2003,128(4):153-155.
[18]高曉明,宜沛沛,付峰,等.活性白土-Bi2WO6的制備及其光催化氧化脫硫的研究[J].精細石油化工,2015,32(1):4-9.

