西妥昔單抗聯合化療治療轉移性結直腸癌的臨床觀察
王 玲
轉移性結直腸癌(metastatic colorectal cancer,MCRC)是危險系數較高的消化道類惡性腫瘤。手術治療是當前根治結直腸癌的唯一手段,但單一的手術治療對中晚期的患者效果不佳,需要結合一些藥物和放射的治療。伴隨著生長因子的受體單克隆的抗體藥物西妥昔的面世,結直腸癌的治療由此進入分子的靶向時代[1-2]。西妥昔單抗與腫瘤細胞的表皮生長的因子受體聯合,可以封閉其內源性的配體部位,避免分子過分地激活,控制細胞的生長,減少了血管內生長因子和金屬蛋白酶的產生;還可以調節身體的免疫系統,起到發揮抵抗腫瘤的作用[3]。因此,我們對采用西妥昔單抗聯合化療治療MCRC的臨床效果進行觀察,現將結果報告如下。
1 資料與方法
1.1 一般資料
選擇2015年10月至2016年10月在我院接受治療的結腸癌患者200例。所有患者都經過病理組織學的檢查并確診,其中男性112例,女性88例;年齡33~77歲,平均57.8歲;病理分類:高分化腺癌有67例,中分化腺癌有94例,低分化腺癌有23例,黏液腺癌有16例。患者均有可用CT測評療效的病灶。患者均沒有重要的器官功能損壞,肝腎功能、血尿常規檢查、心電圖等都正常,沒有化療的禁忌證。預判的生存期都大于3個月。
1.2 患者分組及治療方法
使用隨機對照性研究,把所有患者分為2組:治療組(92例)和對照組(108例)。2組患者的基本資料和病例史都沒有明顯的差異,有可比性。治療組采用西妥昔單抗結合Folffox4的化療方案對患者進行治療,對照組只用Folffox4的化療方案進行治療。對2組患者進行療效和不良反應的統計分析。治療組療法[4]:先使用西妥昔單抗,間隔1 h以后再使用化療藥物。在使用西妥昔單抗前的35 min,對患者進行苯海拉明的18 mg肌肉注射、地塞米松的8 mg靜脈推射和0.3 g的西米替丁靜脈滴注。患者第1次靜脈滴注西妥昔單抗時為410 mg/m2,持續120 min,以后每周500 mg/m2,連續靜脈滴注60 min。對照組療法:單一Folffox4化療。2組的治療均為14天1個周期。
1.3 治療效果的測評和不良反應
2組的患者都要完成4個周期以上的治療,如果患者在治療周期內病情嚴重,且證實是PD的患者則不再進行治療。患者每周進行一次心電圖、血常規和肝腎功能的檢查,每4周進行一次盆腔B超、腹部B超和胸片的檢查,需要進行CT和全身骨骼的掃描。
治療效果的評判標準:按照Recist的抗腫瘤標準[5],分為完全緩解(CR)、部分緩解(PR)、病情穩定(SD)和進展(PD)。
不良反應:按WHO的判定標準[6],分為0~Ⅳ級。神經毒性為Levis的感覺神經毒性的分級準則,分為4個等級。查看患者的血壓、胃腸道的反應、心率、體溫及肝腎功能、血常規的指標。重點記錄患者在治療過程中出現的白細胞減少、皮疹、腹瀉、過敏、嘔吐和骨髓抑制等反應。
1.4 統計學方法
采用SPSS20.0統計軟件進行數據分析,計量資料用均數±標準差來表示。組內數據用t檢驗,組間對比應用one-way anova分析,若方差不符合比較要求則用組組對比。計數資料采用χ2檢驗。P>0.05為差異無統計學意義。
2 結果
2.1 2組患者治療的效果情況比較
2組患者都完成了4個周期以上的治療,都可評判其治療效果。治療組的治療有效率(CR和PR)為54.3%(50/98),對照組的治療有效率為37.0%(40/108),2組的有效率有統計學差異(χ2=3.104,P=0.009),見表1。
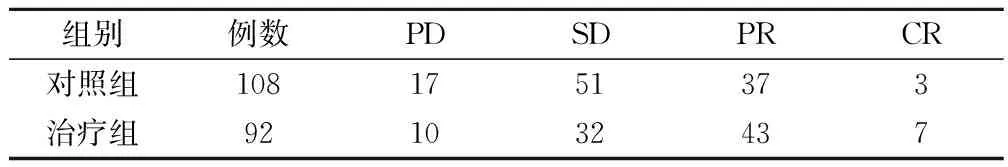
表1 治療組和對照組患者療效比較/例
2.2 2組患者出現的不良反應情況比較
2組患者出現的不良反應主要包含肝腎功能的損壞、骨髓的抑制、嘔吐、腹瀉、過敏、神經毒性和過敏等,但多數都是輕微型,不影響繼續治療。治療組患者大范圍地出現痤瘡樣的皮疹,這個是用西妥昔治療后出現的典型反應,一般發生在用藥的前3周,主要在面部、胸背部和四肢。治療組皮疹的發生率比對照組高,但經皮疹治療后不影響后續治療,見表2。
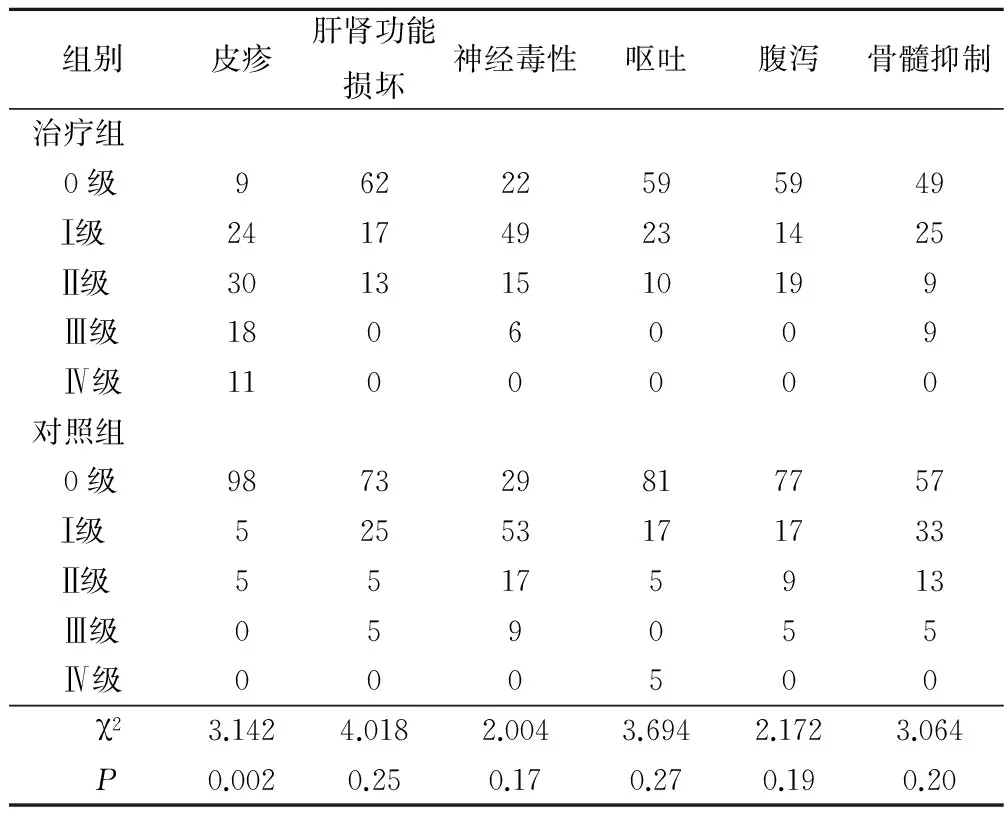
表2 對照組和治療組患者的不良反應情況對比/例
3 討論
晚期結直腸癌的治療措施主要就是化療。臨床常用化療藥物主要包含拓撲異構酶、5-FU和第三代的鉑類等[7-11],但這些藥物的毒副作用較嚴重,限制了其在臨床上的應用。當前,腫瘤分子的靶向治療日漸成熟,且治療藥物的效率高、靶向性較好、毒性低,在緩解患者病情、控制腫瘤的發展和改善患者生活質量方面有更廣闊的發展前景[12-15]。
本文使用隨機對照研究的方法,對200例患者分組進行調查,觀察患者在治療后的療效和不良反應,并對調查的結果進行統計學分析。結果顯示,治療組(西妥昔單抗結合化療)的總有效率達54.3%,病情好轉或痊愈的過半數,而對照組(單一化療)的總有效率只有37.0%,2組對比有明顯的差別。在毒副作用方面,2組患者出現的不良反應主要有神經毒性、肝腎功能的損壞、嘔吐、腹瀉和骨髓抑制等,但多數都是輕微型的,對癥治療或不治療即可自己痊愈;但治療組出現了大面積的皮疹反應,比對照組高,這是使用西妥昔單抗的正常反應,經過對癥治療后不影響后續的治療,其安全性也是可靠的。
綜上所述,西妥昔單抗是當前腫瘤分子靶向方面治療的研究成果之一,對于結直腸癌患者個體的治療有重大的意義。本研究也證實,西妥昔單抗結合化療可以有效地提高MERC患者的療效且安全。
[1] Ellis AG,Reginster JY,Luo X,et al.Bazedoxifene versus oral bisphosphonates for the prevention of nonvertebral fractures in postmenopausal women with osteoporosis at higher risk of fracture: a network meta-analysis〔J〕.Value Health,2014,17(4):424-432.
[2] Hamrick I,Schrager S,Nye AM.Treatment of osteoporosis:current state of the art〔J〕.Wien Med Wochenschr,2014,65(8):54-64.
[3] Wan L,Chen W,Yang L.The efficacy of parathyroid hormone analogues in combination with bisphosphonates for the treatment of osteoporosis:a meta-analysis of randomized controlled trials〔J〕.Medicine,2015,94(9):223-231.
[4] Zhang T,Su D,Li J,et al.Clinical efficacy observation of cetuximab combined with chemotherapy in the treatment of metastatic colorectal carcinoma〔J〕.Zhonghua wei chang wai ke za zhi,2015,18(6):584-588.
[5] Bai M,Deng T,Han R,et al.Gemcitabine plus S-1 versus cetuximab as a third-line therapy in metastatic colorectal cancer: an observational trial〔J〕.Int J Clin Exp Med,2016,8(11):2159-2165.
[6] Graham CN,Maglinte GA,Schwartzberg LS,et al.Economic analysis of panitumumab compared with cetuximab in patients with wild-type KRAS metastatic colorectal cancer that progressed after standard chemotherapy〔J〕.Clin Ther,2016,38(6):1376-1391.
[7] Lin L,Chen L,Wang Y,et al.Efficacy of cetuximab-based chemotherapy in metastatic colorectal cancer according to RAS and BRAF mutation subgroups: A meta-analysis〔J〕.Mol Clin Oncol,2016,4(6):78-80.
[8] Semrad TJ,Fahrni AR,Gong IY,et al.Integrating chemotherapy into the management of oligometastatic colorectal cancer:evidence-based approach using clinical trial findings〔J〕.Ann Surg Oncol,2015,22(Suppl 3):S855-862.
[9] Do K,Liang C,Kang Z,et al.A phase Ⅱ study of sorafenib combined with cetuximab in EGFR-expressing,KRAS-mutated metastatic colorectal cancer〔J〕.Clin Colorectal Cancer,2015,14(3):154-161.
[10] Pietrantonio F,Mazzaferro V,Miceli R,et al.Pathological response after neoadjuvant bevacizumab-or cetuximab-based chemotherapy in resected colorectal cancer liver metastases〔J〕.Med Oncol,2015,32(7):1-10.
[11] Inoue M,Takahashi S,Soeda H,et al.Gene-expression profiles correlate with the efficacy of anti-EGFR therapy and chemotherapy for colorectal cancer〔J〕.Int J Clin Oncol,2015,20(6):1147-1155.
[12] Taniguchi H,Yamazaki K,Yoshino T,et al.Japanese society of medical oncology clinical guidelines:RAS,(KRAS/NRAS) mutation testing in colorectal cancer patients〔J〕.Cancer Sci,2015,16(3):324-327.
[13] Boeckx N,Peeters M,Camp GV,et al.Prognostic and predictive value of RAS,gene mutations in colorectal cancer:moving beyond KRAS,Exon 2〔J〕.Drugs,2015,75(10):1739-1756.
[14] Chiadini E,Scarpi E,Passardi A,et al.EGFR methylation and outcome of patients with advanced colorectal cancer treated with cetuximab〔J〕.Oncol Lett,2015,9(3):1432-1438.
[15] Huiskens J,Gulik TMV,Lienden KPV,et al.Treatment strategies in colorectal cancer patients with initially unresectable liver-only metastases,a study protocol of the randomised phase 3 CAIRO5 study of the Dutch Colorectal Cancer Group (DCCG)〔J〕.Bmc Cancer,2015,15(1):1-7.

