非小細胞癌術后輔助順鉑和紫杉醇治療的臨床效果及對患者免疫功能和預后的影響
巫志華
手術是治療非小細胞肺癌(NSCLC)的重要手段之一,但非小細胞肺癌完全切除術后5年生存率并不理想。多數患者2年內出現復發和(或)轉移。對于術后是否需要輔助化療以及其效果如何仍存在較大爭議[1]。化療藥順鉑和紫杉醇等用于晚期不可切除NSCLC的臨床化療取得了令人矚目的療效[2],這無疑給NSCLC術后輔助化療增加了不少希望,但其用于非小細胞肺癌術后化療的效果如何,文獻報道較少。我院自2010年至2012年采用順鉑聯合紫杉醇對NSCLC術后患者進行輔助化療,現對其中90例臨床資料完整的Ⅱ~Ⅳ期的病例進行回顧性分析,報告如下。
1 資料與方法
1.1 一般資料
本組90例患者中男性55例,女性35例;年齡27~79歲,中位年齡56歲。術前臨床分期為Ⅱ~Ⅳ期,16例合并高血壓,8例合并2型糖尿病,20例乙型肝炎表面抗原陽性;心功能Ⅰ~Ⅱ級;肝、腎功能基本正常。術后臨床結合病理分期診斷為ⅢA期47例,ⅢB期36例,Ⅳ期7例。手術方式為單肺葉切除+肺門淋巴結清掃術46例,雙葉切除+肺門淋巴結清掃術14例,單側全肺切除術12例,楔形切除+肺門淋巴結清掃術9例,姑息性切除術9例。組織學診斷腺癌32例,鱗癌26例,肺泡細胞癌12例,乳頭狀腺癌11例,大細胞癌4例,黏液表皮樣癌4例,腺鱗癌1例。
1.2 治療方案
化療組45例患者于術后第4周開始接受順鉑聯合紫杉醇方案的輔助化療。給藥方法為前1~3 d應用25 mg/m2順鉑加入500 ml 生理鹽水進行靜脈滴定。同時于第1天、第8天和第15天,應用35 mg/m2多西紫杉醇靜脈滴注,每天滴注1 h。化療前常規使用格拉司瓊3 ml靜脈緩推預防嘔吐。白細胞低于3.5×109/L時給予粒細胞集落刺激因子支持。治療21 d為1周期,治療4個周期。對照組術后無任何治療,僅隨訪觀察。出現其它不良反應予對癥治療。
1.3 觀察指標
(1)療效判定標準:參考《實體瘤療效評價標準(RECIST)指南1.1版》[3]中相關標準評估將療效標準分為完全緩解、部分緩解、無變化及進展。總有效率(%)=(完全緩解例數+部分緩解例數)/總例數×100%。隨訪1年,觀察并比較2組患者近期治療效果;(2)不良反應參考《抗癌藥物急性及亞急性毒性反應分度標準《世界衛生組織(WHO)》[1]中相關內容評估。隨訪5年,觀察并比較2組患者不良反應發生情況;(3)免疫功能評價:化療療程結束后采用流式細胞儀檢測化療組和對照組患者外周靜脈血中T細胞亞群,如CD4+、CD8+、CD4+/CD8+的比例;ELISA法檢測上述患者血清中白細胞介素和干擾素的含量。
1.4 統計學方法
數據應用SPSS 19.0統計軟件進行分析,計數資料以百分率表示,組間比較采用χ2檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 臨床觀察
至2016年隨訪終止時,治療組患者總有效率、1年生存率、3年生存率與對照組比較,差異均有統計學意義(P均<0.05);但5年生存率2組差異無統計學意義。見表1。
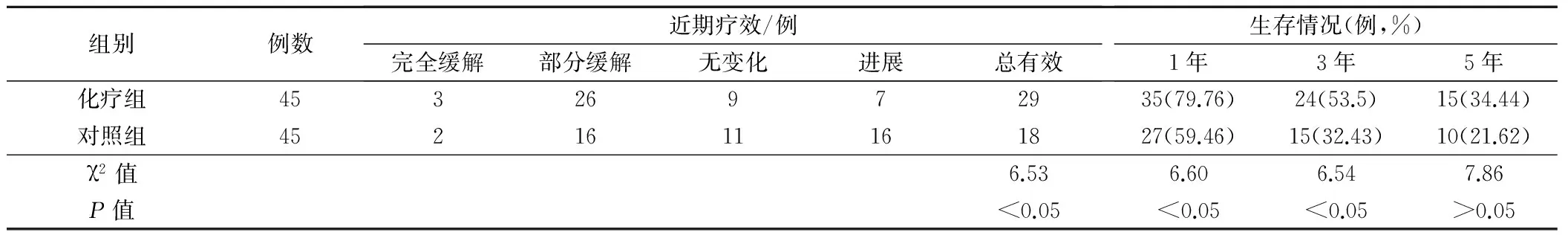
表1 2組患者臨床療效比較
2.2 免疫指標的比較
化療組外周血IFN-γ、IL-10、CD4+、CD8+、CD4+/CD8+均高于對照組(P<0.05),見表2。
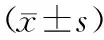
表2 化療組和對照組免疫指標的比較
2.3 預后不良反應
化療組化療不良反應以造血系統毒性和胃腸道毒性為主,主要表現為白細胞下降、血小板減少、惡心嘔吐,其中化療組45例患者中13例(28.8%)出現白細胞下降,其中Ⅲ度4例(8.8%)、Ⅳ度5例(11.1%);3例(6.6%)出現血小板減少現象;其中9例(20.0%)出現惡心嘔吐現象。
3 討論
NSCLC是發病率和病死率均較高的惡性腫瘤之一,且其發病率有逐年增高趨勢。由于肺癌患者發病年齡較大,常合并多器官系統疾病,且肺葉或全肺切除術后對化療耐受性差,再加之早期關于術后輔助化療臨床研究成功的報道不多。 因而對非小細胞肺癌的術后輔助化療一直存在爭議[1]。術后輔助化療的早期研究顯示,術后聯合化療如以植物堿類為主的方案可增加死亡危險性(HR 1.2)[4],而以順鉑為主的聯合化療能改善患者的生存質量,降低死亡危險性13%(HR 0.87),5年生存率提高,與該研究的結果相當。IATL的研究[5]: 對1867 例患者分別給予單純手術或手術和以順鉑為主的兩藥聯合方案,包括順鉑/足葉乙甙(56%)、順鉑/長春瑞賓(27%)順鉑/長春地辛(6%)、順鉑/ 長春花堿(7%),70%患者完成了預計治療,結果顯示:化療組TTP明顯延長(HR 0.83,P=0.003),生存質量明顯改善(HR 0.86,P=0.03),5年生存率提高4.1%,化療不良反應死亡率為0.8%。順鉑為主的聯合化療可改善Ⅰb~Ⅲa期術后NSCLC患者的生存質量,但改善幅度小且不恒定。美國的CALGB9633(美國腫瘤和血液病研究組)報告指出NSCLC患者術后行順鉑聯合紫杉醇輔助化療與單純手術治療對比生存率明顯提高。該項研究的對象是Ⅰb期的344例患者,結果術后輔助化療組生存率為71%,而對照組僅為51%;死亡率化療組為15%,對照組為26%;加拿大的JBR10也證實了術后輔助化療的有效性,該研究是對Ⅰb~Ⅱ期患者行長春瑞賓/順鉑輔助化療,化療組5年生存率為61%,對照組僅為48%(P=0.012)。
早期研究顯示術后化療患者依從性低,不能提高生存率和延長生存期[6]。 Rosell等[7]認為Ⅰb期NSCLC患者有50%以上發展成遠處轉移,其原因就在于術前即可能已存在微轉移,因此有必要進行術后輔助化療。趙玲等[8]報道用MVP(絲裂霉素+長春花堿酰胺+順鉑)方案對ⅢB期NSCLC患者進行化療,1年、3年、5年生存率分別為53.4%、19.5%、8.5%。 Melo等[9]進行的Ⅲ~Ⅳ期大樣本研究也顯示中位生存期僅有6.9~10.6個月。梁亦賢等[10]報道順鉑聯合紫杉醇方案治療晚期NSCLC 1年依從性好的患者占28.4%。我科自2010年開始用順鉑聯合紫杉醇方案對NSCLC術后患者進行化療,并進行跟蹤隨訪,至2016年止,1年生存率79.76%,明顯高于文獻報道的MVP聯合化療方案,不良反應發生率與文獻報道無明顯差異,總體毒副作用較輕,耐受性好,無1例因不良反應而中斷化療。本研究表明順鉑聯合紫杉醇化療方案應用于NSCLC術后化療療效確切,5年生存率較單純手術或非手術綜合治療明顯提高。
[1] 周際昌主編.實用腫瘤內科學〔M〕.北京:人民衛生出版社,2003:543-552.
[2] 譚紅霞,張 科,譚 詠.紫杉醇與順鉑治療晚期老年非小細胞肺癌臨床療效觀察〔J〕.河北醫學,2014,20(3):442-444.
[3] 劉秋華,林榕波.實體瘤療效評價標準(RECIST)指南1.1版〔C〕.第十二屆全國臨床腫瘤大會暨2009 年CSCO學術年會論文集,2009:451.
[4] Non-Small Cell Lung Cancer Collabortive Group.Chemotherapy in non-small cell lung cancer:A meta-analysis using updated data on individial patients from 52 randomized clinical trials〔J〕.BMJ,1995,311(1):899-909.
[5] 錢正子,王華慶.Ⅰb-Ⅲa期非小細胞肺癌術后輔助化療的進展〔J〕.中國腫瘤臨床,2004,31(24):1428-1430.
[6] Bunn PA,Mault J,Kelly K,et al.Adjuvant and Neoadjuvant Chemother-apy for non-small cell lung cancer:a time for reassessment〔J〕.Chest,2000,117(4 suppl1):119s-122s.
[7] Rosell R,Felip E,Maestre J,et al.The role of chemotherapy in early non-small-cell lung cancer management〔J〕.Lung Cancer,2001,34(Suppl3):63-74.
[8] 趙 玲,張燦珍.ⅢB期非小細胞肺癌非手術治療遠期療效分析〔J〕.昆明醫學院學報,2001,22(1):95-96.
[9] Melo MJ,Barradas P,Costa A,et al.Results of a randomized phaseⅢtrial comparing4cisplatin(p)-based regimens in the treatment of lo-cally advanced and metastatic non-small cell lung cancer(NSCLC):(MVP)is no longer a therapeutic opertion〔J〕.American Society of Clinical Oncology,2002,21:302a.
[10] 梁亦賢,茅乃權,左傳田,等.Ⅱ~Ⅲ期NSCLC患者術后輔助化療依從性分析〔J〕.醫學研究雜志,2015,44(11):118-121.

