CT引導下精準微波消融在肝癌治療中的應用
何勇,周林,鐘鼎文,謝元才
(贛州市人民醫院普外一科,江西 贛州 341000)
肝癌是臨床常見的腫瘤類型,屬于死亡率較高的惡性腫瘤,該病發病率較高,對患者的健康造成了嚴重的危害[1]。患者發病初期無明顯的癥狀,且該病具有一定的隱匿性,較難發現,待確診時一般已經進入肝癌晚期,對患者的生命安全造成了嚴重的威脅,不利于其生存質量的提高,臨床也對該病的治療引起了高度的重視[2]。目前,臨床治療肝癌仍以手術為首選方法,但多數患者存在合并肝硬化以及多發病灶現象,所以術后極易復發[3]。CT引導下精準微波消融術具有安全、微創以及操作簡便的優勢,在臨床應用較為廣泛,對患者的創傷較小,具有顯著的治療效果,在臨床得到了一定的認可[4]。為進一步證明CT引導下精準微波消融在肝癌治療中的應用價值,本次研究選取2014年12月~2017年6月在本院接受治療的90例肝癌患者進行研究,現報道如下。
1 資料與方法
1.1 臨床資料 實驗時間為2014年12月~2017年6月,實驗對象為在本院接受治療的90例肝癌患者,將所選患者隨機分為觀察組(n=45)以及對照組(n=45),其中觀察組男27例,女18例;年齡41~76歲,平均年齡(58.5±17.5)歲;病灶數量:25例單個病灶患者,20例2~3個病灶患者;病灶直徑:病灶直徑在3 cm以下的患者23例,病灶直徑在3 cm以上的患者22例。對照組男21例,女24例;年齡42~77歲,平均年齡(59.5±17.5)歲;病灶數量:27例單個病灶患者,18例2~3個病灶患者;病灶直徑:病灶直徑在3 cm以下的患者26例,病灶直徑在3 cm以上的患者19例。兩組患者臨床資料比較差異無統計學意義,表明研究資料一致性較好。排除標準:①肝外轉移患者;②肝內彌漫性轉移患者;③血管侵范患者;④肝功能Child C級的患者;⑤具有嚴重高血壓手術禁忌證患者;⑥具有嚴重心臟病手術禁忌證患者;⑦治療依從性較低的患者;⑧治療中途轉入他院的患者。
1.2 方法
1.2.1 對照組給予經肝動脈化學栓塞術(TACE)治療具體方法如下 確診之后在患者的右股動脈處采用Seldinger技術進行常規的肝動脈造影,之后根據患者的血液供應情況以及腫瘤的大小進行常規的灌注,首先使用5-Fu 0.5~2.0 g的碘化油乳劑緩慢栓塞,若使用量超過25~30 ml時患者的血液仍然較快,可食用明膠海綿顆粒栓塞阻止血液的流速,直到血液明顯減慢為止。針對巨大型的肝癌要分次進行栓塞,其中每次之間需要間隔4~6周左右。對于動靜脈瘺病灶在栓塞處理的過程中應選用無水乙醇進行。叮囑患者手術之后2~4周內進行復查,并根據患者的檢查結果選擇下一步的介入治療方法,針對甲胎蛋白為陰性的患者需要定期復查CT以及MR,并結合動脈造影術決定是否繼續隨訪;針對甲彈蛋白為陽性的患者若轉陰則繼續隨訪,若仍然高于正常水平就需要對其病灶的情況進行明確,評估手術的處理結果,并將對患者的損傷降至最低,行經肝動脈化學栓塞術治療[5]。
1.2.2 觀察組給予CT引導下精準微波消融治療 給予患者CT引導下精準微波消融術治療,治療所選用的儀器以及設備為微波治療刀、微波治療儀以及16層的螺旋CT儀。手術之前對患者進行常規的止血、止咳以及鎮靜治療,以此來改善患者的咳嗽癥狀以及心肺功能狀況,之后對患者進行血糖、血常規以及肝腎功育瞼等常規的檢查。完成之后使用掃描儀對患者進行掃描,然后根據掃描的具體結果對穿刺的角度以及進針的具體深度進行明確,同時還要根據患者腫瘤的大小形態以及具體的位置確定穿刺點,之后取利多卡因對病灶周圍進行局部麻醉,然后根據進針的角度以及深度進針,同時使用CT掃描儀重復掃描,保證進針的準確性。另外,在進針的過程中應該沿著腫瘤的長軸進入,直到腫瘤遠端的外側為穿刺完成。對針尖的具體位置進行確定之后將其與濃度為0.9%的氯化鈉注射液相連接,同時建立水流循環系統并設置相關的參數,將功率設置為40~80 w左右,治療時間在12~20 min左右。治療結束后拔針時要叮囑患者屏住呼吸,在治療的同時進行拔針操作,然后使用CT掃描儀對患者的病灶部位進行掃描,掃描的同時檢查是否存在血胸以及氣胸等較為嚴重的并發癥,還應該叮囑患者注意休息,同時對患者進行止血以及止咳鎮痛等相關的治療,密切監測患者的生命體征[6]。
1.3 療效評價指標 對兩組患者的臨床療效以及不良反應發生率進行比較分析。臨床療效評價標準:完全緩解,患者經過治療之后其病灶部位完全消失,AFP降至正常狀態,且1月之后無復發現象;部分緩解,患者經過治療之后其病灶范圍明顯縮小一半以上,AFP與之前相比降低50%以上,且1月之后無復發現象;穩定,患者經過治療之后病灶范圍所小幅度較小,甚至無變化,AFP降低25%左右,且1月之后無復發現象;進展,患者經過治療之后病灶不但未消失,甚至出現新的病灶,AFP無降低或繼續升高。
1.4 統計學方法 采用SPSS 17.0統計學軟件進行統計分析,所有數據均錄入計算機進行分析,臨床療效以及不良反應發生率均以[n(%)]表示,組間比較采用χ2檢驗,組內比較采用配對χ2檢驗,統計值有統計學差異的判定標準為P<0.05。
2 結果
2.1 臨床療效比較 觀察組患者的總發生率為(97.8%),低于對照組(84.4%),差異有統計學意義(χ2=4.939,P<0.05),見表1。
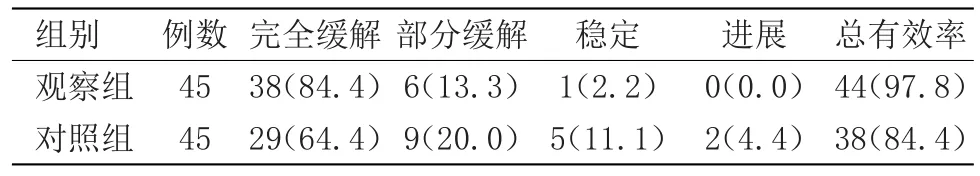
表1 臨床療效比較[n(%)]Table 1 Comparison of clinical efficacy[n(%)]
2.2 不良反應發生率比較 觀察組患者的總發生率為(6.7%),低于對照組(24.4%),差異有統計學意義(P<0.05),見表2。
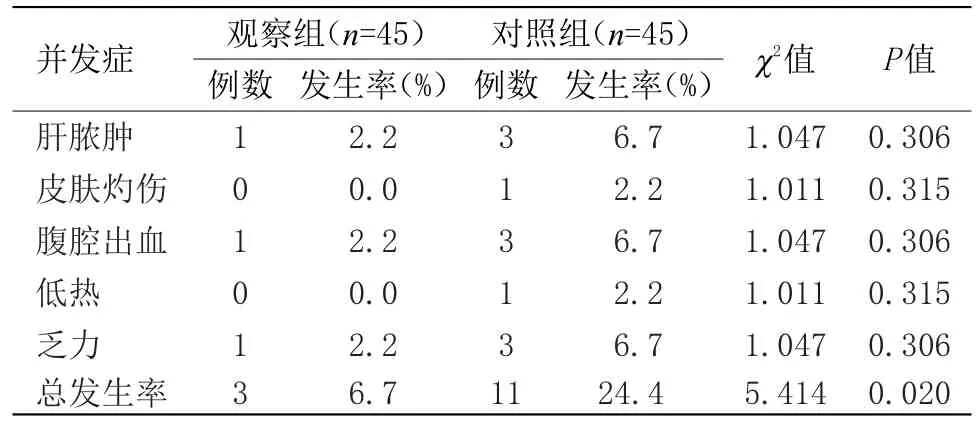
表2 不良反應發生率比較Table 2 Comparison of incidence of adverse reactions
3 討論
隨著人們生活水平的不斷提高,肝癌的發病率呈現出不斷上升的趨勢,患有肝癌的患者也越來越多,對患者的健康以及生活質量的提高造成了嚴重的影響,甚至威脅到患者的生命安全,具有較高的死亡率[7]。臨床一般選用外科手術治療該病,但是當前我國肝癌患者的確診率較低,患者在確診之后已進入肝癌晚期,患者病情較為嚴重,延誤了最佳治療時機,加大了治療難度[8]。加之老年患者自身具有較多的基礎性疾病,在治療的過程中耐受程度較低,不利于手術順利進行,嚴重影響到手術效果[9]。
本次研究中,觀察組患者的總有效率為97.8%,不良反應發生率為6.7%與對照組差異具有統計學意義(P<0.05)。原因分析為:①在醫療技術不斷發展進步的同時,精準微波消融術應運而生,并在癌癥領域的治療中取得了顯著的療效,還可有效的延長患者的生存期,對患者的生活質量也有一定的改善作用,在臨床應用范圍較廣[10]。②微波屬于非電離輻射的高頻電磁波,對患者的創傷較小,治療精度較高,通過CT引導對惡性腫瘤的治療受到廣泛的關注。CT引導下精準微波消融術屬于微創手術,治療肝癌的安全性較高,其中的高溫不但可有效的殺傷腫瘤組織,還可導致腫瘤細胞破裂、細胞核固縮以及溶解,消除壞死的病灶,進而不斷增強患者自身的免疫力[11]。③CT引導下精準微波消融屬于臨床治療肝癌的新技術,主要是通過微波熱凝固達到治療目的,其安全性較高,對患者創傷較小,術后并發癥較少,近期療效較為確切,患者接受治療后可明顯延長生存期,提高患者生存質量。④經肝動脈化學栓塞術對肝癌治療雖有一定效果,但其對患者創傷較大,安全性不能得到有效保障,術后并發癥較多,不利于患者快速康復,而CT引導下精準微波消融在臨床得到了廣泛認可[12]。
綜上所述,相對于經肝動脈化學栓塞術來說,CT引導下精準微波消融治療肝癌患者療效顯著,安全性較高,可有效的減少不良反應,具有較高的臨床應用價值,值得臨床推廣應用。
[1] 李麗珍,鐘秋紅,黃昌輝,等.超聲引導下經皮微波消融與CT超聲引導下腫瘤射頻消融治療原發性肝癌的臨床比較[J].中國CT和MRI雜志,2017,15(1):76-78,82.
[2] 高峰,黃祥忠,任冬青,等.導管鞘輔助穿刺技術在CT引導微波消融治療原發性肝癌中的應用[J].介入放射學雜志,2016,25(12):1074-1077.
[3] 張春淼,何晶,張艷霞,等.CT引導經皮穿刺微波消融治療原發性肝癌的護理[J].介入放射學雜志,2015,24(3):265-267.
[4] 王穎,張春淼,王璇,等.CT引導下原發性肝癌微波消融治療并發癥的護理研究[J].全科護理,2015,12(12):1448-1450.
[5] 房達,崔石昌,李京華,等.CT引導微波消融治療肝癌中CT劑量的優化控制[J].醫學影像學雜志,2016,26(10):1837-1840.
[6] 彭壽洲.CT引導微波消融術在肺癌治療中的應用[J].深圳中西醫結合雜志,2016,26(14):121-122.
[7] An Zhongjun,Gu Youliang,Li Dongfeng,et al.Application of CT guided water-cooled cycle microwave ablation in the treatment of lung cancer[J].Journal of Regional Oncology,2010,19(1):38.
[8] Tu Fuping,Huang Li,Wang Xiangcai,et al.Application of central venous catheters in CT-guided subcranial hepatocellular carcinoma with microwave ablation[J].Journal of Gannan Medical College,2015,35(1):66-69.
[9] Shen Li-jie,Yan Peng,Zhang Juan-na,et al.Comparison of therapeutic effect of argon helium cryoablation,radiofrequency ablation and microwave ablation in the treatment of hepatocellular carcinoma[J].Journal of Medical Imaging,2015,25(10):1836-1839.
[10]Ni JY,Sun HL,Chen YT,et al.Prognostic factors forsurvival after transarterialchemoembolization combined with microwave ablation for hepatocellular carcinoma[J].World J Gastroenterol,2014,20:17483-17490.
[11]Gao Bin,Gao Xiao-ying,Cai Jun,et al.Clinical applicationofCT-guidedradiofrequencyablationin the treatment of liver cancer[J].Journal of Practical Medical Imaging,2012,13(6):354-355.
[12]Chen Wen-hui,Jiang Xu,Yang Ji-jing,et al.Study on Effective Radiation Dose of Patients in CT-guided Intervention Operation[J].Journal of Interventional Radiology,2012,21(7):570-573.

