分散支撐液膜法處理含Tb(Ⅲ) 和Dy(Ⅲ)稀土廢水
趙 楠 裴 亮
(齊齊哈爾大學 化學與化學工程學院,黑龍江 齊齊哈爾 161006; *中國科學院 地理科學與資源研究所 陸地水循環及地表過程重點實驗室,北京 100101)
水是地球上最寶貴的資源。雖然地球表面的71%為水域,然而其中僅不足3%為淡水,而在淡水資源中只有不足1%可供人類直接使用。稀土礦石冶煉后排出的廢水中含有的鋱、鏑等稀土離子,對人類健康危害很大[1],對稀土金屬廢水傳統的處理方法已不能滿足既回收金屬又將水回用的要求[2]。膜技術作為一種新興的分離技術,在工業金屬廢水處理過程中越來越受到人們的重視。通常,溶液中金屬離子不能直接用膜除去,但采用溶劑萃取和膜技術結合的方法,可以實現溶液中單一或混合金屬離子的分離,其中萃取劑的選取起著非常重要的作用。
在過去的近40年里,由于液膜傳質速率高、選擇性好等特點,使其成為分離與濃縮的有效手段,支撐液膜(SLM)體系的操作簡單,不需引入昂貴的表面活性劑,但由于膜溶液(有機溶劑,萃取劑及改性劑)溶于水相而引起的膜穩定性下降和高傳輸通量的矛盾至今仍未很好解決[3]。
針對SLM存在的問題,近年來國內外有人轉而探索新的液膜構型,希望在保持液膜分離特點的同時,克服支撐液膜不穩定等缺點,因而提出了“組合液膜”[4,5]和“組合技術”的概念,它將固體膜或各種化學過程和液膜組合在一起,能有效地克服支撐液膜的載體從膜相泄漏的缺陷,延長膜的壽命。本文將文獻提出的“反萃分散技術”[6]和支撐液膜組合,用分散支撐液膜來處理模擬稀土廢水,以2-乙基己基磷酸-單-2-乙基己基酯(PC-88A)為萃取劑,對鋱與鏑離子水溶液進行液膜分離實驗,并考察了分離鋱、鏑混合離子的可能性。
1實驗部分
1.1 試劑和儀器
2-乙基己基膦酸-單-2-乙基己基酯(PC-88A);日本大八化學工業公司提供,經銅鹽純化,純度達98%;Tb(CH3COO)3·4H2O(西安化學試劑廠);Dy(CH3COO)3·4H2O(西安化學試劑廠);HCl(西安市長安區化學試劑廠);硫酸H2SO4(西安三浦精細化工廠);以上試劑均為分析純試劑。商用煤油(西安誠信試劑廠);實驗用水全部為去離子水。
DSLM遷移池(自制)由料液池、解析池和支撐體組成。料液池和解析池的容量均為80 mL,并配有可調速電動攪拌器;支撐體為疏水性多孔聚偏氟乙烯膜(PVDF)(上海亞東核級樹脂有限公司),孔徑0.22 μm,膜厚65 μm,孔隙率75%,曲折因子1.67,有效面積為12 cm2。實驗裝置見圖1。
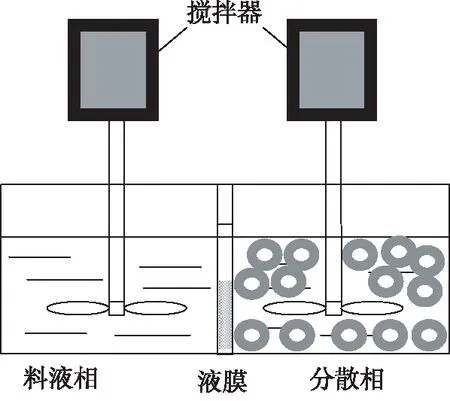
圖1 分散支撐液膜裝置示意圖Fig 1 Schematic description of dispersionsupported liquid membrane apparatus
1.2 實驗方法
模擬稀土廢水采用蒸餾水加入兩種稀土離子的方式配制,使 Tb(Ⅲ) 和Dy(Ⅲ)濃度分別為1×10-4mol/L。
先將PVDF置于PC-88A體積分數為5%的膜溶液中浸取吸附一定的時間,然后用濾紙吸干膜表面的液體,固定在DSLM遷移池中。其次分別將事先配好的試樣料液和膜溶液加到料液池和分散池中,開動料液池和分散池中的攪拌器,再將HCl加到分散池中,同時開始計時,間隔一定時間取樣分析。Tb(Ⅲ) 和Dy(Ⅲ)濃度分別在350.917 nm和353.170 nm處用原子發射光譜法測定。
2實驗原理
圖2描述了Tb(Ⅲ) 和Dy(Ⅲ)在DSLM中的反應和遷移過程,以逆向耦合遷移為例,其遷移機理概述如下(以Dy(Ⅲ)為例):
遷移過程大致分為以下幾個步驟:
(1)Dy(Ⅲ)在料液相側邊界層內擴散。
設Dy(Ⅲ)在料液主體的濃度是均勻的,而在料液相側邊界層內濃度梯度是線性的,Dy(Ⅲ)沿垂直于膜平面的軸向擴散并遵守Fick 第一定律,則此過程通量Jf可表示為:
(1)

圖2 Re(Ⅲ)在DSLM內遷移過程示意圖Fig 2 Schematic description of Re(Ⅲ) transport in DSLM process
其中,下標f表示料液相組分、Df為Dy(Ⅲ)在料液相中擴散系數;df為料液相側擴散層厚度;cf為料液主體的Dy(Ⅲ)濃度;cfi為料液相與膜相界面處的Dy(Ⅲ)濃度。
(2)在水相-膜相界面,Dy(Ⅲ)與載體(HR)發生如下的配合反應[7]:
(2)
其中:右下標org—有機相;右下標f—料液相;Dy(Ⅲ)—三價金屬鏑離子;(HR)2—在非極性油中主要以二聚體形式存在的萃取劑。
Dy(Ⅲ)與載體在水油界面發生絡合反應,生成絡合物DyR3(HR)3。反應發生在水油兩相界面處,因此為反應萃取過程,定義表觀反應萃取平衡常數Kex為:
(3)

(3)絡合物DyR3(HR)3在膜內的擴散過程。
膜溶劑的介電常數要求足夠小,絡合物的離解度小至忽略不計。在這種條件下,只考慮膜內絡合物在膜內的擴散過程。設膜內濃度為線性變化,絡合物的擴散滿足 Fick 第一定律:
(4)
因為支撐液膜的支撐膜為多孔性聚偏氟乙烯膜,需對擴散面積及擴散距離進行如下校正:
(5)

(4)當絡合物DyR3(HR)3擴散到解析相CD,與反萃取劑發生如下的解析反應[7]:
(6)
其中:右下標S-解析相。
由于此解離反應過程比在膜內反應要快的多[11],因此可以忽略此反應對整個傳質過程的影響。
(5) 載體返回料液相和膜相界面。由于這一擴散過程經充分攪拌比膜內擴散速率快得多,也可忽略其對整個傳質過程速率的影響。
若假設體系經過一段時間后處于穩態[8-15],過程為擴散控制,則:
J=Jf=Jm=JS
(7)
聯立(1)、(3)、(5)及(7)式可推導出:
(8)
根據滲透系數定義:
(9)
其中:Vf-料液相體積;A-膜的有效面積;cf-料液相中遷移物質的濃度;Pc-滲透系數
可得:
(10)
因此,式(10)可以簡化為:

(11)

同理, Tb(Ⅲ)的動力學方程也是式11的形式。
其次,Tb(Ⅲ)和Dy(Ⅲ)的傳質通量可通過測定料液相中Tb(Ⅲ)和Dy(Ⅲ)的濃度隨時間t的變化速率dc/dt而求得,
即對式(9)進行積分得:
(12)
其中:cf(t)和cf(0)分別為t時刻及起始料液相中Tb(Ⅲ)或Dy(Ⅲ)濃度。通過測定不同條件下Tb(Ⅲ)或Dy(Ⅲ)的濃度,以-ln(ct/c0)對t作圖,從直線斜率的大小分析各種因素對遷移速率的影響程度。
3結果與討論
3.1 膜溶液與HCl溶液的體積比對Tb(Ⅲ)和Dy(Ⅲ)去除的影響
由于分散相是將HCl均勻的分散在膜溶液中形成的,膜溶液與HCl的體積比直接影響Tb(Ⅲ)和 Dy(Ⅲ)的萃取和解析速率。HCl在分散相中占的比例越大,所形成的乳化液越不穩定,不利于稀土離子的遷移去除。比例越小,所提供的額外的反萃取面積也減小,降低了稀土離子的去除率。因此膜溶液與HCl體積比的大小是影響稀土離子去除率大小的重要因素之一。
選擇料液相pH值為4.0,分散相HCl濃度為4.0 mol/L,遷移時間是170 min。在膜溶液與HCl體積比不同的情況下Tb(Ⅲ)和 Dy(Ⅲ)的去除情況如表1所示。可見隨著膜溶液的比例增大,去除率增大,當體積比增大到50∶10和40∶20時,去除效果與30∶30時很接近。考慮經濟因素,適宜的膜溶液與HCl體積比應選擇在30∶30左右。

表1 膜溶液與HCl溶液體積比對去除率的影響Table 1 Effect of volume ratio of membranesolution and HCl solution on removal rate
3.2 料液相pH值對Tb(Ⅲ)和Dy(Ⅲ)去除的影響
由Tb(Ⅲ)和 Dy(Ⅲ)在DSLM中的傳質機理可知,H+在料液相與解析相中的濃度差是稀土離子在DSLM的傳質動力。因此,料液相酸度越低,越有利于Tb(Ⅲ)和Dy(Ⅲ)的去除。然而,由于解析相使用的反萃取劑為強酸,當料液相酸度較高時,兩相間高強度的H+濃度差,加快了H+透過膜相的滲透作用。不僅嚴重影響液膜的穩定性,而且也會影響稀土離子在分散液膜中的去除率。因此,料液相與解析相的酸度差是影響稀土離子去除率的重要因素之一。
選擇分散相中HCl濃度為4.0 mol/L,膜溶液與HCl溶液體積比為30∶30,遷移時間是170 min,不同酸度下Tb(Ⅲ)和 Dy(Ⅲ)的遷移情況如表2所示。
可見隨著料液相pH值的增大,去除率增大,當pH值增大到5.4時,Tb(Ⅲ)的去除效果反而變差,可能是由于部分水解造成的。而在pH值為5.1時Tb(Ⅲ)和 Dy(Ⅲ)的去除效果都很好,分別為93.8%和94.7%。考慮Tb(Ⅲ)和 Dy(Ⅲ)共同的去除效果,適宜的料液相pH值應選擇在5.1左右。
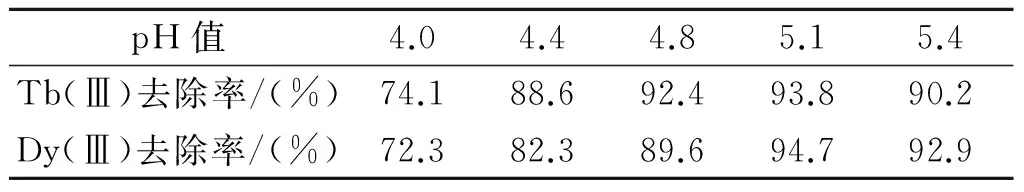
表2 料液相pH值對去除率的影響Table 2 Effect of pH value in thefeed phase on removal rate
3.3 分散相中HCl濃度對Tb(Ⅲ)和Dy(Ⅲ)去除的影響
為考察分散相中HCl的濃度對Tb(Ⅲ)和 Dy(Ⅲ)去除率的影響,實驗中確定了料液相pH值為5.1、分散相中膜溶液與HCl溶液體積比為30∶30,改變HCl濃度分別為2.0、3.0、4.0、5.0、6.0 mol/L。不同濃度下Tb(Ⅲ)和 Dy(Ⅲ)去除率情況如表3所示。
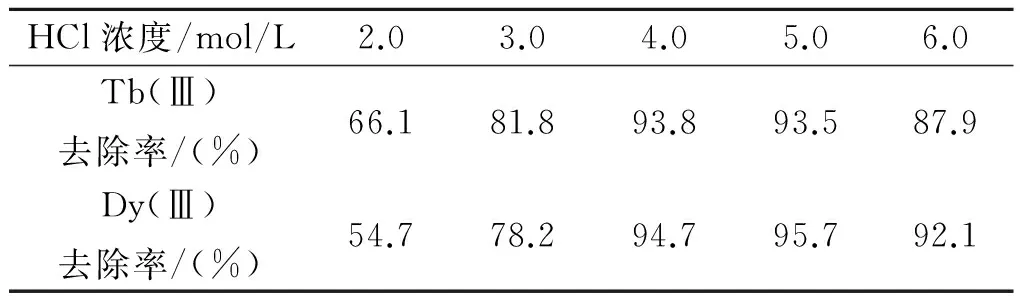
表3 分散相HCl的濃度對去除率的影響Table 3 Effect of HCl concentration in thedispersion phase on removal rate
可見隨著分散相酸度的增大,Tb(Ⅲ)和 Dy(Ⅲ)去除率增大,當酸度增大到6mol/L時,去除效果反而變差,可能是由于酸度過高,載體和稀土離子的絡合能力變差以及反萃效果不穩定。而在分散相酸度為4.0 mol/L時Tb(Ⅲ)和 Dy(Ⅲ)的去除效果都很好,分別為93.8%和94.7%。所以適宜的分散相酸度應選擇在4.0 mol/L左右。
4傳質動力學分析
由上述結論可知,在一定的載體濃度下,料液相的酸度是影響金屬離子傳輸的主要因素,本實驗進行了不同酸度下Tb(Ⅲ)和 Dy(Ⅲ)的去除實驗,為了進一步定量描述Tb(Ⅲ)和 Dy(Ⅲ)在DSLM中的去除過程,我們對去除過程進行動力學研究。按照式11和式12我們可以得到以下兩個動力學方程:
Tb(Ⅲ):Pc=1/(3.10 ×104+0.42×1017[H+]3)
Dy(Ⅲ):Pc=1/(3.20 ×104+0.48×1017[H+]3)
5結 論
(1)實驗表明,此DSLM體系對Tb(Ⅲ)和 Dy(Ⅲ)有顯著的去除效果。料液相酸度,分散相中HCl濃度、膜溶液與HCl溶液的體積比都會影響稀土離子的去除率。Tb(Ⅲ)和 Dy(Ⅲ)的最佳去除條件為膜溶液與HCl溶液體積比為30∶30;料液相pH值控制在5.1左右;分散相HCl濃度為4.0 mol/L。在最佳條件下,遷移170 min,Tb(Ⅲ)和 Dy(Ⅲ)的去除分別可以達到93.8%和94.7%。
(2)建立了Tb(Ⅲ)和 Dy(Ⅲ)在DSLM中反應和去除的模型,推導出了新的動力學方程:
Tb(Ⅲ):Pc=1/(3.10 ×104+0.42 ×1017[H+]4)
Dy(Ⅲ):Pc=1/(3.20 ×104+0.48×1017[H+]3)
(3)在以PC-88A為流動載體DSLM,由于在解析相中使用了適量的膜溶液,這樣解決了支撐液膜中載體的流失問題,提高了稀土離子的去除率,增加了膜的穩定性,延長了膜的使用壽命。
[1] 孟祥和, 胡國飛. 重金屬廢水處理[M]. 北京:化學工業出版社, 2000.
[2] El-Shafey E l, Cox M, Pichugin A., et al. Application of a carbon sorbent for the removal of cadmium and other heavy metal ions from aqueous solution [J]. J. Chem. Technol. Biotechnol., 2002, 77(4):429~436.
[3] He D S, Ma M, Wang H., et al. Effect of kinetic synergist on transport of copper (II) through a liquid membrane containing P507in kerosene[J]. Can J. Chem. 2001, 79(8): 1 213~1 219.
[4] Gu S X,Yu Y D, He D S., et al.Comparison of transport and separation of Cd(II) between strip dispersion hybrid liquid membrane (SDHLM) and supported liquid membrane (SLM) using tri-n-octylamine as carrier[J]. Sep. Purif. Technol., 2006, 51(3): 277~284.
[5] He D S, Gu S X, Ma M. Simultaneous removal and recovery of cadmium (II) and CN?from simulated electroplating rinse wastewater by a strip dispersion hybrid liquid membrane (SDHLM) containing double carrier[J]. J. Membr. Sci., 2007, 305(1-2): 36~47.
[6] Sonawane J V, Pabby A K, Sastre A M. Au(I) extraction by LIX-79/n-heptane using the pseudo-emulsion- based hollow-fiber strip dispersion (PEHFSD) technique[J]. J. Membr. Sci., 2007, 300(1-2): 147~155.
[7] Kubota F, Goto M, Nakashio F. Extraction of earth metals with 2-ethylhexyl phosphonic acid mono-2-ethylhexyl ester in the presence of diethylenetriaminepentaacetic acid in aqueous phase[J]. Solvent Extr. Ion Exch., 1993, 11(3): 437~453.
[8] Danesi P R. Separation of metal species by supported liquid membrane[J]. Sep. Sci and Tech., 1984-1985, 19(11-12): 857~894.
[9] Danesi P R, Horwitz E P, Vandegrift G F., et al.Mass transfer rate through liquid membrane:interfacial chemical reactions and diffusion as simultaneous permeability controlling factors[J]. Sep. Sci. Technol., 1981, 16: 202~214.
[10] He D S, Luo X J, Yang C M, et all. Study of transport and separation of Zn(Ⅱ) by a combined supported liquid Membrane/strip dispersion containing D2EHPA in kerosene as the carrier[J]. Desalination, 2006, 194:40~51.
[11] Danesi P R, Horwitz E P, Rickert P G.Transported of Eu2+through a bis(2-ethylhexyl)phosphoric acid,n-dodecanol solid supported liquid membrane[J]. Sep. Sci. Technol., 1982, 17: 1 183~1 192.
[12] Yaftian M R, Burgard M, Dieleman C B, et all. Rare-earth metal-ion separation using a supported liquid membrane mediated by a narrow rim phosphorylated calix(Ⅳ) arene[J]. J. Membr. Sci., 1998, 144(1-2): 57~64.
[13] Pei Liang, Yao Binghua, Zhang Chengjie. Transport of Tm(Ⅲ) through Dispersion supported liquid membrane Containing PC-88A in Kerosene as the Carrier[J]. Sep. Purif. Technol., 2009, 65(2): 220~227.
[14] Pei Liang, Yao Binghua, Wang Liming., et al. Transport of Tb3+in Dispersion Supported Liquid Membrane system with Carrier P507[J]. Chin. J. Chem., 2010, 28(5): 839~846.
[15] Pei Liang, Yao Binghua, Wang Liming., et al. Tb(III) transport in dispersion supported liquid membrane system with D2EHPA as carrier in kerosene[J]. Chem. Res. Chin. Univ., 2011, 27(1): 132~139.
[16] 劉又年, 舒萬艮, 黃可龍. 支撐液膜法提取稀土的動力學[J].中南礦冶學院學報,1994, 25(4): 535~539.

