A-Raf-S214C突變體的構建、表達及其對MAPK信號通路的影響
李安毅 楊洋 劉瑩 郭曉汐 郝倩 徐天瑞 安輸
(昆明理工大學生命科學與技術學院 云南省高校靶點藥物篩選與利用重點實驗室,昆明 650500)
A-Raf-S214C突變體的構建、表達及其對MAPK信號通路的影響
李安毅 楊洋 劉瑩 郭曉汐 郝倩 徐天瑞 安輸
(昆明理工大學生命科學與技術學院 云南省高校靶點藥物篩選與利用重點實驗室,昆明 650500)
為了觀察A-Raf的突變體A-Raf-S214C對MAPK(mitogen-activated protein kinase,絲裂原活化蛋白激酶)信號通路的影響,并探討其誘發肺癌和朗格漢斯增生癥的可能分子機制。通過定點突變構建pcDNA5-FRT-TO-A-Raf-S214C突變質粒,并利用該質粒構建穩定表達A-Raf-S214C突變體的HEK293細胞系,之后通過檢測下游ERK磷酸化程度,確定該突變體對MAPK信號通路的影響。結果顯示,通過實驗成功構建了穩定表達A-Raf-S214C突變體的細胞系,在不同濃度的多西環素誘導下,其表達量有所不同。與野生型相比,A-Raf-S214C突變體可明顯增強MAPK信號通路中下游信號分子ERK的磷酸化。結果表明A-Raf-S214C突變體是A-Raf激酶的激活突變體,可以導致MAPK信號通路下游信號分子ERK磷酸化明顯增強。
A-Raf激酶;MAPK信號通路;信號傳導
Raf激 酶(Rapidly accelerated fibrosarcoma) 是逆轉錄病毒致癌基因v-Raf的同源蛋白,它調控細胞的生長、分化、轉化和凋亡等諸多生命過程,Raf-MEK-ERK通路是細胞信號傳導的一條主干通路,這條通路的調控失常是細胞癌變的主要原因之一[1-2]。
Raf激酶家族有3個成員A-Raf、B-Raf和C-Raf(Raf-1),它們均可被上游信號分子Ras激酶激活(Ras突變和異常活化與20%的人類癌癥相關[3]),從細胞質轉位到細胞膜,并通過磷酸化靶蛋白MEK來進一步激活ERK。但3個成員生物學功能卻各有所不同[4-5]。與 B-Raf和 C-Raf相比,A-Raf的激酶活性最低,僅為 C-Raf的 20%[6]。而且,A-Raf突變在癌癥中的發現相對較少,目前僅在肺癌細胞中發現了 A-Raf-S214C 突變體[7]。
A-Raf-S214C突變體是A-Raf的第214位氨基酸絲氨酸突變為半胱氨酸。通過基因組學篩查在肺癌細胞中發現該突變體,并且它能轉化支氣管表皮細胞,使其發生癌變[7]。在朗格漢氏增生癥中也發現該突變[8]。A-Raf(S214C)突變體對MAPK的激活能力幾乎與 B-Raf(V600E)相同[8]。
本研究通過點突變法構建了A-Raf-S214C位點突變真核表達質粒,并在Flp-In T-Rex HEK293細胞進行穩轉,構建該突變體的穩定表達細胞系,檢測其在Flp-In T-Rex HEK293細胞中的表達水平,以及其對MAPK信號通路的作用。
1 材料與方法
1.1 材料
1.1.1 細胞、菌株和質粒 A-Raf cDNA、Flp-In細胞、pcDNA5/FRET/TO載體由本實驗室保存,感受態大腸桿菌DH5α購自TaKaRa公司。引物合成和測序工作由生工生物工程(上海)有限公司完成。
1.1.2 主要試劑盒與抗體 TOYOBO點突變試劑盒購自東洋紡(上海)生物科技有限公司(該試劑盒含 有 KOD-Plus-、DpnI、T4 Polynucleotide Kinase、Ligation high等);膠回收試劑盒、質粒提取試劑盒等購自Tiangen公司;DMEM培養基、Blasticidin、Zeocin、Hygromycin、轉染試劑Lipo-fectamine2000均購自Invitrogen corporation;胎牛血清和Opti-MEM培養基購自北京Solarbio有限公司;Anti-VSV、Anti-GAPDH、Anti-ERK、Anti-p-ERK購 自 Santa Cruz Biotechnology;辣根過氧化物標記鼠、羊、兔IgG抗體購自Kirkegaarg & laboratories公司。
1.2 方法
1.2.1 pcDNA5/FRT/TO-VSV-A-Raf質粒的構建 首先根據載體特點及VSV標簽序列設計上下游引物(表1)。然后用PCR的方法將VSV標簽序列及限制性酶切位點引入A-Raf的cDNA,并用BamH I和Xho I酶對pcDNA5/FRET/TO載體和含有VSV標簽和酶切位點的A-Raf cDNA進行雙酶切,利用連接酶將擴增的VSV-A-Raf基因連接到pcDNA5/FRET/TO載體,從而得到pcDNA5/FRT/TO-VSV-A-Raf質粒(以下簡稱A-Raf質粒)。將質粒送生工生物工程(上海)有限公司測序。
1.2.2 設計點突變引物 以A-Raf質粒為模板,設計點突變引物(表1),并送生工生物工程(上海)有限公司合成。
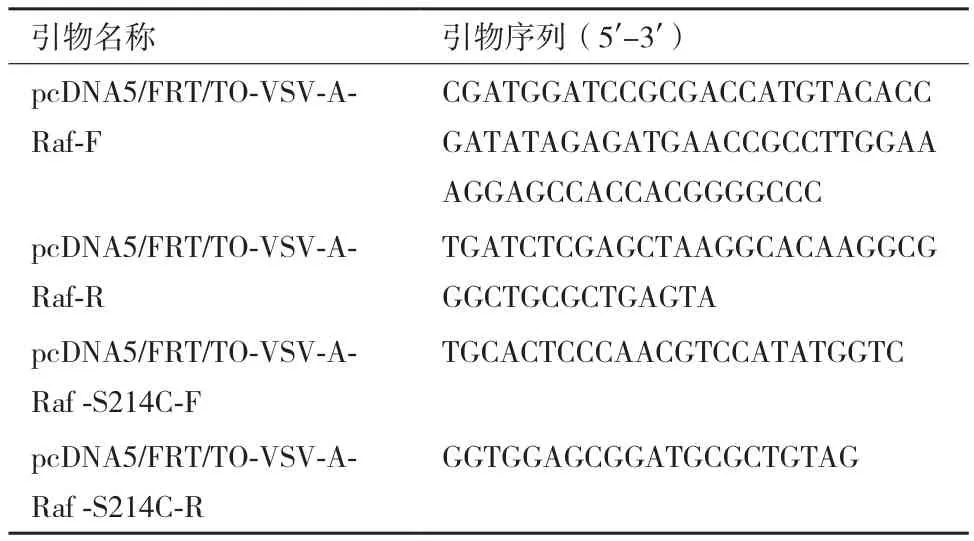
表1 引物列表
1.2.3 pcDNA5/FRT/TO-VSV-A-Raf-S214C突變體(以下簡稱A-Raf-S214C)的構建與鑒定 用TOYOBO點突變試劑盒構建突變體質粒。第一步,以A-Raf質粒為模板,用反向設計的兩條引物對質粒進行完整的PCR。第二步,用Dpn I對模板質粒進行消化,37℃反應1 h。第三步,PCR產物自身環化:將Dpn I處理后PCR產物、滅菌蒸餾水、Ligation high、T4 Polynucleotide Kinase 以2∶7∶5∶1的體積比進行混合,混合物在16℃條件下反應1 h,實現PCR產物的自身環化。第四步,轉化質粒:將自身環化后產物轉化至DH5α感受態細胞中,涂布于含有氨芐青霉素的LB固體培養基平板,37℃恒溫培養12 h后,挑取單克隆菌落進行PCR鑒定,篩選陽性克隆,用質粒提取試劑盒抽提質粒,用Xho I和BamH I酶進行雙酶切,并測序驗證定點突變是否成功。
1.2.4 細胞培養及轉染 Flp-In T-Rex HEK293細胞培養于含有10%胎牛血清、100 U/mL的青霉素、100 μg/mL的鏈霉素、3 μg/mL Blasticidin、100μg/mL 的Zeocin的DMEM維持培養基中,培養條件為37℃,5%CO2和80%濕度。待細胞生長至密度為70%-80%時(T25培養瓶培養),將構建成功的pcDNA5/FRT/TO-VSV-A-Raf-S214C質粒(以下簡稱A-Raf-S214C質粒)和pOG44質粒按1∶9的比例共轉染該細胞。具體步驟:將質粒DNA(0.3 μg)與 pOG44(2.7 μg)混合物溶入 500 μL Opti-MEM 培養基中,并將6 μL脂質體Lipo-fectamine2000也溶入500 μLOpti-MEM培養基中,將二者混合均勻,靜置15-20 min。在靜置期間,將T25培養瓶中的培養基吸出,用1 mL 1×PBS洗滌3次,并加入2.5 mL Opti-MEM培養基,并放回培養箱繼續培養。待靜置結束后,輕輕將質粒與轉染試劑混合物均勻混合,加入T25培養瓶中,混勻后放回37℃培養箱中繼續培養。6 h后,將Opti-MEM培養基更換為正常維持培養基5 mL,繼續培養。第2天,將轉染了質粒的Flp-In T-Rex HEK293細胞傳代至T125培養瓶中繼續培養。第3天,將T125培養瓶中的維持培養基更換成含200 μg/mL Hygromycin 的篩選培養基繼續培養。之后每3-5 d更換一次篩選培養基,直至有單克隆細胞出現。然后將單克隆細胞用胰酶消化,轉移至T25培養瓶,并更換為維持培養基繼續擴大培養,用于后續試驗。
1.2.5 免疫印記分析 將A-Raf 野生型和A-Raf-S214C穩定表達細胞系鋪6孔板,用濃度為0、1、5、10、100和1 000 ng/mL六個濃度梯度的Doxycycline(Dox)誘導VSV-A-Raf和VSV-A-Raf-S214C的表達,誘導24 h后裂解細胞,收集蛋白樣品,并進行BCA定量,進行SDS-PAGE電泳、PVDF膜轉膜、牛奶封閉、孵育一抗、1×TBST洗膜、孵育二抗、1×TBST洗膜、顯影,用凝膠成像系統軟件對結果進行分析。根據VSV的表達水平,可確定誘導劑的最佳濃度。再次將A-Raf野生型和A-Raf-S214C穩定細胞系鋪6孔板,用之前檢測得到的Dox最佳誘導濃度分別誘導細胞0、12、18和24 h后收集細胞,進行Western blot檢測,方法同前,可確定Dox最佳誘導時間。
1.2.6 A-Raf-S214C突變體活性檢測 將A-Raf野生型和A-Raf-S214C突變體穩定表達細胞系分別鋪6孔板,每種細胞分成3組。待細胞生長至密度為70%-80%時,用最佳Dox誘導濃度分別誘導A-Raf野生型和A-Raf-S214C突變體穩定表達細胞。誘導12 h后,第1組細胞不做任何處理,將第2組和第3組細胞更換為無血清培養基,并繼續用Dox誘導。再過12 h后,將第2組細胞用200 μL胎牛血清刺激5 min(加入血清后,培養基中血清終濃度為10%),其余兩組不作處理。然后進行細胞收樣,用Western blot檢測ERK的磷酸化水平,Western blot方法同前。1.2.7 統計學分析 本實驗數據處理應用SPASS21.0統計軟件,采用t檢驗進行統計分析,顯著性差異水平定位P<0.05。
2 結果
2.1 pcDNA5/FRT/TO-VSV-A-Raf質粒的鑒定
將構建的A-Raf質粒用瓊脂糖凝膠電泳分析,結果(圖1)顯示,pcDNA5/FRT/TO-VSV-A-Raf質粒在相應位置具有清晰的條帶,大小正確。質粒測序結果與NCBI數據庫中基因序列完全一致,說明構建的A-Raf質粒符合實驗要求。
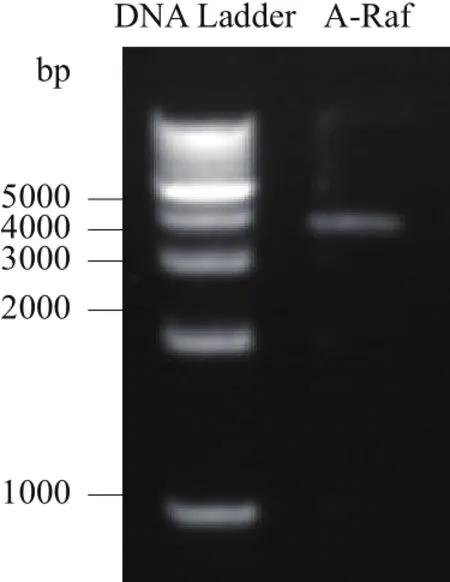
圖1 瓊脂糖凝膠電泳測定pcDNA5-FRT-TO-A-Raf質粒的大小
2.2 pcDNA5/FRT/TO-VSV-A-Raf-S214C突變體質粒構建
通過反向PCR法對A-Raf進行點突變PCR產物經Dpn I酶切及產物自身環化后,將環化產物轉染至DH5α感受態細胞中,挑取單克隆菌落進行菌液PCR鑒定,其中12個代表性單克隆菌落的菌落PCR電泳結果如圖2-A所示。通過菌液PCR篩選陽性克隆,用質粒提取試劑盒抽提質粒,將其中前8個菌落的質粒分別進行Xho I和BamH I雙酶切鑒定它們是否含有相應大小的插入片段,酶切的電泳結果如圖2-B所示。經序列比對,發現A-Raf序列第641位堿基C突變為G,即編碼214位氨基酸的絲氨酸(TCC)突變為半胱氨酸(TGC),即可確定點突變成功。測序結果如圖3所示。
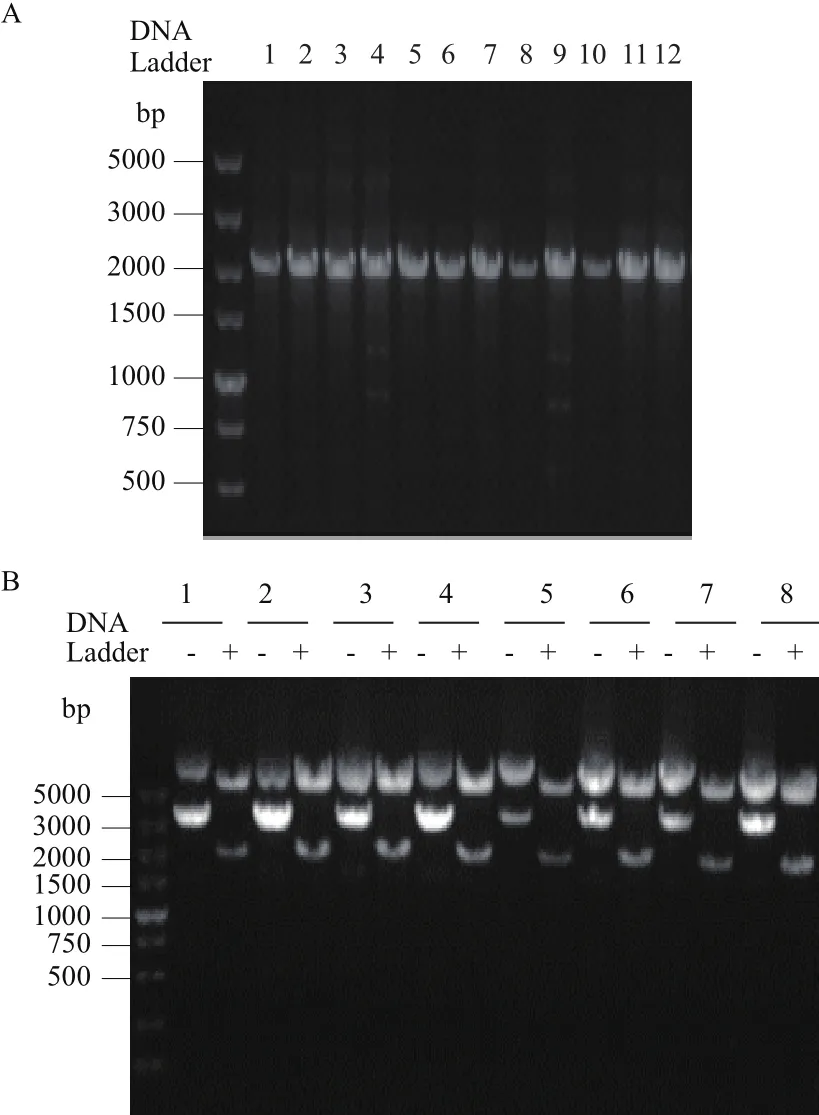
圖2 瓊脂糖凝膠驗證A-Raf-S214C菌落PCR產物(A)及pcDNA5-FRT-TO-A-Raf-S214C質粒的雙酶切驗證(B)
2.3 免疫印記檢測A-Raf-S214C突變體在Flp-In T-Rex HEK293細胞表達情況
用 濃 度 為 0、1、5、10、100和 1 000 ng/mL Doxycycline分別處理穩定表達A-Raf及其突變體A-Raf-S214C的兩個細胞系,處理24 h后,用抗VSV標簽蛋白抗體檢測A-Raf及其突變體A-Raf-S214C的表達情況,免疫印記結果(圖4-A)顯示,100 ng/mL Dox是A-Raf及其突變體A-Raf-S214C的最佳誘導濃度。用該最佳濃度,再次分別誘導兩個細胞系0、12、18和24 h,結果(圖4-B)顯示誘導24 h后,A-Raf和A-Raf-S214C的表達量可達最大。本實驗說明,用100 ng/mL Dox處理細胞24 h是誘導A-Raf和A-Raf-S214C表達的最佳條件。
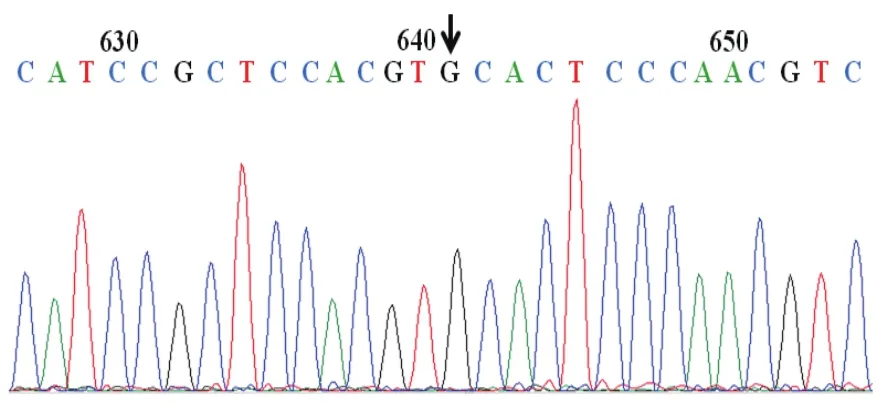
圖3 A-Raf-S214C突變體測序
2.4 A-Raf-S214C突變體對MAPK信號通路的影響
將A-Raf 野生型和A-Raf-S214C穩定表達細胞系分別分為正常培養誘導組、饑餓組和饑餓后加血清刺激組進行實驗,之后用Western blot檢測ERK的磷酸化水平,發現饑餓組中的A-Raf-S214C突變體細胞的ERK磷酸化水平明顯高于A-Raf野生型細胞(圖5-A)。重復3次該實驗,并進行統計學分析,饑餓處理組A-Raf野生型和A-Raf-S214C突變體的ERK磷酸化水平,差異顯著(**P<0.01),結果如圖5-B所示。該結果初步證明A-Raf-S214C突變體是A-Raf的激活突變體,與A-Raf相比,A-Raf-S214C對MAPK信號通路下游信號分子ERK的磷酸化能力更強。
3 討論
Ras-Raf-MEK-ERK通路是細胞信號傳導的一條主干通路,它調控著細胞的生長、分化、轉化和凋亡等諸多生命過程[9]。在這條通路中,Raf激酶作為關鍵組分之一發揮著重要作用[6]。
Raf激酶是逆轉錄病毒致癌基因v-Raf的同源蛋白,Raf激酶家族有3個成員A-Raf、B-Raf 和C-Raf(Raf-1),3個成員結構相似(由調節區和激酶活性區兩部分組成),大小接近(A-Raf:606個氨基酸;B-Raf:806個氨基酸;C-Raf:648個氨基酸),都可以被Raf激酶的結合蛋白Ras激活,之后從細胞質轉位到細胞膜,并通過磷酸化靶蛋白MEK進一步激活ERK。但3個成員生物學功能和調控機制卻各不相同[10]。其中對B-Raf和C-Raf的研究最為深入,它們是Ras-Raf-MEK-ERK信號通路上的主要致癌蛋白也是激活MEK的主要蛋白[10]。研究表明Ras-Raf-MEK-MAPK信號通路中的組分過表達或發生激活突變,與超過30%的人類腫瘤相關[11]。其中Raf激酶的突變是導致細胞癌變的主要原因之一,如B-Raf突變與57%的神經系統癌變、39%的皮膚癌和38%胸腺癌相關[12];C-Raf突變與超過90%的小細胞肺癌相關[13]。因此,調控Raf激酶也就成為了治療癌癥的最主要手段之一[13-14]。
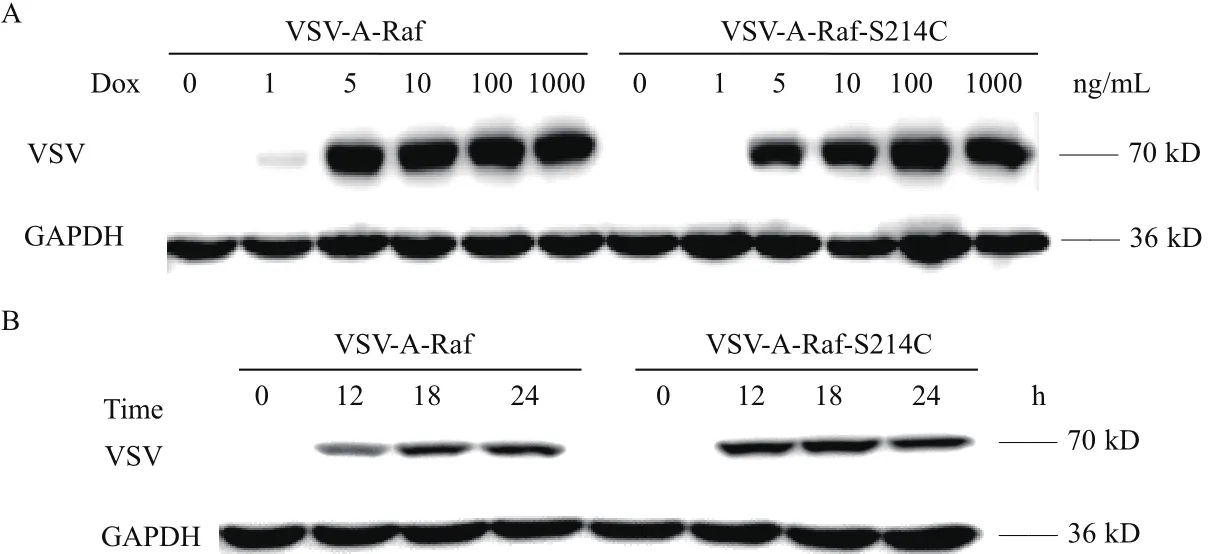
圖4 不同多西環素濃度(A);及在100 ng/mL多西環素誘導的條件下,不同誘導時間(B)對VSV-A-Raf野生型和VSV-A-Raf-S214C突變體表達的影響

圖5 免疫印跡檢測VSV-A-Raf野生型細胞和VSV-A-Raf-S214C突變體細胞的ERK磷酸化水平
與B-Raf和C-Raf相比,A-Raf具有較低的激酶活性,其最大活性僅為C-Raf的20%[15],而且當前在腫瘤中發現A-Raf發生基因突變的報道較少。因此,人們對A-Raf激酶的關注較少,作為Raf激酶家族中重要一員,對其生物學功能仍不是非常清楚。這同時也給我們一種啟示,為什么在進化過程中會形成一個較差的MEK激酶A-Raf,而與之同源的B-Raf和C-Raf會具有非常強的激酶活性?因此,這些問題驅使我們對A-Raf及其激活突變體進行研究。本研究發現,與野生型A-Raf相比,其突變體A-Raf-S214C可明顯增強下游信號分子ERK的磷酸化程度,該突變體是A-Raf激酶的構建性激活突變體,可引起MAPK信號通路下游信號分子ERK異常活化。而異常活化的ERK可通過轉錄因子調控細胞周期進展、細胞分化、蛋白質合成、代謝、細胞存活[16]、細胞遷移和入侵等使正常細胞獲得許多腫瘤細胞的特征[17]。也有報道稱,A-Raf激酶在細胞凋亡[18]、腫瘤形成[19]、拮抗 Raf激酶抑制劑[20]等過程中扮演重要角色。因此,進一步了解A-Raf-S214C突變體的具體激活機制有助于幫助我們了解A-Raf的致癌機制,為人們尋找治療癌癥的方法提供了新的思路。
4 結論
利用點突變的方法,成功構建了A-Raf-S214C突變體質粒。并且成功構建了在Flp-In T-Rex HEK293細胞中穩定表達的A-Raf野生型和A-Raf-S214C突變體細胞系。在不同濃度的多西環素誘導下,A-Raf野生型細胞與A-Raf-S214C突變體細胞的表達量有所不同,二者均在100 ng/mL的多西環素誘導24 h的條件下,表達水平達最大值。與野生型相比,A-Raf-S214C突變體可明顯增強MAPK信號通路中下游信號分子ERK的磷酸化水平,即A-Raf-S214C突變體是A-Raf激酶的激活突變體。
[1]Kolch W. Coordinating ERK/MAPK signalling through scaffolds and inhibitors[J]. Nat Rev Mol Cell Biol, 2005, 6(11):827-837.
[2]Matallanas D, Birtwistle M, Romano D, et al. Raf family kinases:old dogs have learned new tricks[J]. Genes Cancer, 2011, 2(3):232-260.
[3]Montagut C, Settleman J. Targeting the Raf-MEK-ERK pathway in cancer therapy[J]. Cancer Lett, 2009, 283(2):125-134.
[4]Leicht DT, Balan V, Kaplun A, et al. Raf kinases:function,regulation and role in human cancer[J]. Biochim Biophys Acta,2007, 1773(8):1196-1212.
[5]Osborne JK, Zaganjor E, Cobb MH. Signal control through Raf:in sickness and in health[J]. Cell Res, 2012, 22(1):14-22.
[6]An S, Yang Y, Ward R, et al. A-Raf:A new star of the family of raf kinases[J]. Crit Rev Biochem Mol Biol, 2015, 50(6):520-530.
[7]Imielinski M, Gredulich H, Kaplan B. Oncogenic and sorafenibsensitive A-Raf mutations in lung adenocarcinoma[J]. J Clin Invest, 2014, 124(4):1582-1586.
[8]Nelson DS, Quispel W, Badalian-Very G, et al. Somatic activating A-Raf mutations in Langerhans cell histiocytosis[J]. Blood, 2014,123(20):3152-3155.
[9]Olson JM, Hallahan AR. P38MAPK kinase:a convergence pointin cancer therapy[J]. Trends Mol Med, 2004, 10(3):125-129.
[10]Osbome JK, Zaganjor E, Cobb HM. Signal control through Raf:in sickness and in health[J]. Cell Res, 2012, 22(1):14-22.
[11]Fernandez-Medarde A, Santos E. Ras in cancer and developmental diseases[J]. Genes Cancer, 2011, 2(3):344-358.
[12]Santarpia L, Lippman SM, El-Naggar AK. Targeting the MAPKRAS-RAF signaling pathway in cancer therapy[J]. Expert Opin Ther Targets, 2012, 16(1):103-119.
[13]Beeram M, Patnaik A, Rowinsky EK. Raf:a strategic target for therapeutic development against cancer[J]. J Clin Oncol, 2005,23(27):6771-6779.
[14]Kim DH, Sim T. Novel small molecule Raf kinase inhibitors for targeted cancer therapeutics[J]. Arch Pharm Res, 2012, 35(4):605-615.
[15]Martin-Liberal J, Larkin J. New RAF kinase inhibitors in cancer therapy[J]. Expert Opin Pharmacother, 2014, 15(9):1235-1245.
[16]鄒平, 何濤, 陳顥, 等. 細胞衰老過程中JNK、p38和Akt的活性變化[J]. 中國生物化學與分子生物學報, 2006, 22(7):571-574.
[17]Scheid MP, Schubert KM, Duronio V. Regulation of bad phosphorylation and association with Bcl-x(L)by the MAPK/ERK kinase[J]. J Biol Chem, 1999, 274(43):31108-31113.
[18]Rauch J, Moran-Jones K, Albrecht V, et al. c-Myc regulates RNA splicing of the A-Raf kinase and its activation of the ERK pathway[J]. Cancer Res, 2011, 71(13):4664-4674.
[19]Imielinski M, Greulich H, Kaplan B, et al. Oncogenic and sorafenib-sensitive ARAF mutations in lung adenocarcinoma[J].J Clin Invest, 2014, 124(4):1582-1586.
[20]Mooz J, Oberoi-Khanuja TK, Harms GS, et al. Dimerization of the kinase ARAF promotes MAPK pathway activation and cell migration[J]. Sci Signal, 2014, 7(337):ra73.
Construction and Expression of Mutant A-Raf-S214C and Studies on Its Role in MAPK Signaling Pathway
LI An-yi YANG Yang LIU Ying GUO Xiao-xi HAO Qian XU Tian-rui AN Shu
(University Based Provincial Key Laboratory of Screening and Utilization of Targeted Drugs,Faculty of Life Science and Technology,Kunming University of Science and Technology,Kunming 650500)
This study is to observe the influence of A-Raf mutant A-Raf-S214C on MAPK(mitogen-activated protein kinase)signal pathway and to explore the molecular mechanism of lung cancer and Langerhans cell histiocytosis caused by A-Raf-S214C. The pcDNA5-FRT-TO-A-Raf-S214C plasmid was constructed through point mutation,and then it was used to establish HEK293 cell lines stably expressing A-Raf-S214C. Further,the influence of A-Raf-S214C on MAPK signaling pathway was determined by detecting the level of ERK phosphorylation. Results showed that HEK293 cell line with stable expression of A-Raf-S214C was successfully constructed,and A-Raf-S214C expression levels increased under induction with increasing concentrations of doxycycline. In comparison with wild type A-Raf,mutant A-Raf-S214C significantly enhanced the phosphorylation level of ERK . Conclusively,A-Raf-S214C mutant is an activating mutant of A-Raf kinase,resulting in significantly increased phosphorylation level of ERK,a downstream signaling molecule in MAPK pathway.
A-Raf kinase;MAPK signaling pathway;signal transduction
10.13560/j.cnki.biotech.bull.1985.2017-0445
2017-05-30
國家自然科學基金項目(81460253,U1302225),云南省人才培養項目(KK23201426014)
李安毅,女,碩士研究生,研究方向:細胞信號傳導;E-mail:82291898@qq.com
安輸,男,博士,副教授,研究方向:細胞信號傳導;E-mail:aslxj@mail.ustc.edu.cn徐天瑞,男,博士,教授,研究方向:細胞信號傳導;E-mail:xtrgfq@hotmail.com
(責任編輯 李楠)

