腦卒中高危人群血清尿酸水平與頸動脈狹窄的關系
趙慈余 余細平 夏 駿 徐 柯 胡慶豐 邱蓮女 周永列
(浙江中醫藥大學醫學技術學院,浙江 杭州 310053)
腦卒中高危人群血清尿酸水平與頸動脈狹窄的關系
趙慈余 余細平 夏 駿 徐 柯 胡慶豐 邱蓮女 周永列
(浙江中醫藥大學醫學技術學院,浙江 杭州 310053)
目的探討血清尿酸(UA)升高合并肥胖、高血壓、空腹血糖(FPG)、血脂異常等危險因素與頸動脈狹窄之間的相關性。方法從杭州市下城區朝暉街道篩查出腦卒中高危人群539例,用彩色多普勒超聲診斷儀檢查頸動脈狹窄程度,同時采用生化自動分析儀檢測血清UA、甘油三酯(TG)、總膽固醇(TC)、低密度脂蛋白膽固醇(LDL-C)、高密度脂蛋白膽固醇(HDL-C)、FPG、同型半胱氨酸(HCY)和游離脂肪酸(FFA)水平。結果根據UA水平分為第一分位數組181例,第二分位數組178例,第三分位數組180例,3組年齡、體重指數(BMI)、收縮壓(SBP)、HDL-C及HCY差異顯著(均P<0.05)。與第一分位數組比較,第三分位數組LDL-C、FFA、TG、舒張壓(DBP)及動脈狹窄發生率顯著升高(均P<0.05)。UA是腦卒中患者頸動脈狹窄病變的獨立危險因素,頸動脈狹窄程度與UA水平有關(OR=1.011,P<0.01)。BMI異常組合中,第二和第三分位數組頸動脈狹窄發生率分別是參照組(項目正常+第一分位數組)的1.565、1.686倍(均P<0.05)。血壓異常組合的頸動脈狹窄發生率分別是參照組的1.488、1.691、1.774倍(均P<0.05)。血糖異常組合中,第二和第三分位數組頸動脈狹窄的發生率分別是參照組的1.493、1.574倍(P<0.05)。TG異常組合的頸動脈狹窄發生率分別是參照組的1.456、1.639、1.714倍(均P<0.05)。FFA異常組合的頸動脈狹窄發生率分別是參照組的1.365、1.580、1.671倍(均P<0.05)。HDL-C異常組合的頸動脈狹窄發生率分別是參照組的1.344、1.593、1.699倍(均P<0.05)。結論腦卒中高危人群血清UA水平與頸動脈狹窄密切相關,高UA合并肥胖、高血壓、血糖和血脂異常等危險因素對頸動脈狹窄的發生具有促進作用。
腦卒中;尿酸;頸動脈狹窄
腦卒中是急性腦循環障礙迅速導致局限性或彌漫性腦功能缺損的臨床事件,已成為當今世界威脅人類健康的第二位致死原因〔1〕。缺血性腦卒中具有高發病率、高死亡率、高復發率、高致殘率等特點,占全部腦卒中的70%〔2〕。缺血性腦卒中是由于局部腦組織區域出現血液供應障礙,以動脈粥樣硬化為主要原因的心血管疾病,嚴重威脅人類健康和生命。患者的年齡、肥胖、吸煙、高血壓、糖尿病、房顫或瓣膜性心臟病、血脂異常及腦卒中家族史等遺傳因素均是缺血性腦卒中危險因素。目前我國對腦卒中的主要采取一級預防措施,高度重視腦卒中高危人群篩查并進行早期干預。本研究探討血清尿酸(UA)升高合并多個腦卒中危險因素人群發生頸動脈狹窄的風險性。
1 對象與方法
1.1研究對象 依托浙江省人民醫院國家衛計委腦卒中篩查與防控基地,在杭州市下城區朝暉街道進行腦卒中高危人群篩查,該項篩查得到我院倫理審查委員會的批準,所有篩查人員簽署知情同意書。根據2012年我國衛生部腦防辦頒發的《腦卒中高危人群篩查和干預試點項目技術方案》作為篩查腦卒中高危人群標準,從1 500名居民信息中篩查腦卒中高危患者,排除標準:①惡性腫瘤、腎功能不全者、血液病或者其他可能會影響血清UA水平的慢性疾病;②發病前3 個月使用B族維生素、葉酸(FA)、甲氨蝶呤及其他藥物影響血清學指標判斷者;③有心源性腦栓塞及其他周圍血管栓塞疾病;④所獲資料不全影響結果判斷者。以上一種或多種表現均需排除,最后539例腦卒中高危人群納入本研究,男215例,平均年齡(71.48±7.62)歲;女324例,平均年齡(70.41±7.43)歲。根據血清UA水平的三分位數將人群分為:①第一分位數組:181例(33.58%),UA<300 mmol/L;②第二分位數組:178例(33.02%),UA 300~390 mmol/L;③第三分位數組:180例(33.39%),UA>390 mmol/L。
1.2資料采集 通過調查問卷收集入組者一般資料,測量身高、體質量、腹圍、血壓。體質量指數(BMI)≥28 kg/m2,收縮壓≥140 mmHg或舒張壓≥90 mmHg為異常。調查問卷人員由固定的研究調查員和體檢醫師組成,均經過統一的培訓。
1.3血生化的檢測 入組者禁食12 h,于清晨空腹抽取靜脈血4 ml,離心分離血清。采用Beckman AU5400生化分析儀。測定患者UA、同型半胱氨酸(HCY)、游離脂肪酸(FFA)、空腹血糖(FPG)、甘油三酯(TG)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、總膽固醇(TC)。采用酶定量分析法測定UA,試劑盒由美國Beckman公司提供,嚴格按規程和試劑盒說明進行操作與判斷結果,每日用雙水平質控血清按Westgard質控規則進行嚴格室內質控,試劑均在有效期內使用。
1.4頸部血管超聲檢查 于篩查結束后對腦卒中高危人群采用西門子S2000 彩色多普勒超聲診斷儀,探頭9L4,頻率4.0~9.0 MHz,對入組者進行頸部血管超聲檢查。所有圖像由專人閱讀、測量。常規采用寬頻或變頻線陣探頭,患者取仰臥位,充分暴露頸部,檢查時頭偏向對側,左側從無名動脈、右側從頸總動脈起始部做橫切面及縱切面檢測,依次檢查雙側頸總動脈、頸內外動脈分叉處、頸內動脈顱外段全程、頸外動脈主干及分支。患者血管動脈狹窄程度依照北美癥狀性頸動脈內膜切除術〔3〕分級法劃分,狹窄程度<50%為輕度狹窄,50%~69%為中度狹窄,狹窄程度大于70%為重度狹窄,但發生重度狹窄的人群不多,因此將中、重度高危人群合并為一組。
1.5統計學方法 采用SPSS17.0軟件進行t檢驗或方差分析、χ2檢驗。以頸動脈狹窄有無賦值為因變量建立Logistic回歸模型,可能的危險因素進入該回歸模型。同時將危險因素的正常值和異常值分別與按照血清UA水平分的3個組進行組合,將頸動脈狹窄有無作為因變量引入Logistic回歸模型,評定合并相關危險因素后與頸動脈狹窄形成的相關性。
2 結 果
2.1各組臨床資料比較 見表1。3組年齡、BMI、收縮壓、HDL-C及HCY差異顯著(均P<0.05)。與第一分位數組比較,第三分位數組LDL-C、FFA、TG、舒張壓及動脈狹窄發生率顯著升高(均P<0.05)。第三分位數組動脈狹窄發生率是第一分數位組的1.542倍(OR=1.542,P<0.05)。
2.2UA水平與頸動脈狹窄程度相關性的單因素分析 頸動脈狹窄程度與UA水平有關(OR=1.011,P<0.01)。與無狹窄組比較,隨著血管狹窄程度的增加FPG,LDL-C,FFA,HCY,UA及收縮壓均顯著升高(P<0.05)。見表2。
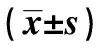
表1 根據尿酸三分位法分組各組間臨床資料比較
與第一分位數組比較:1)P<0.05;與第二分位數組比較:2)P<0.05
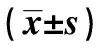
表2 頸動脈狹窄程度臨床資料比較
與無狹窄組比較:1)P<0.05;與輕度狹窄組比較:2)P<0.05
2.3不同UA水平合并其他代謝異常與頸動脈狹窄形成的關系 見表3。將各危險因素正常且合并第一分位數組作為參照組,分析不同水平UA與相關危險因素異常組合的頸動脈狹窄發生的情況。BMI異常組合中,第二和第三分位數組頸動脈狹窄發生率分別是參照組的1.565、1.686倍(均P<0.05)。血壓異常組合的頸動脈狹窄發生率分別是參照組的1.488、1.691、1.774倍(均P<0.05)。血糖異常組合中,第二和第三分位數組的頸動脈狹窄的發生率分別是參照組的1.493、1.574倍(P<0.05)。TG異常組合的頸動脈狹窄發生率分別是參照組的1.456、1.639、1.714倍(均P<0.05)。FFA異常組合的頸動脈狹窄發生率分別是參照組的1.365、1.580、1.671倍(均P<0.05)。HDL-C異常組合的頸動脈狹窄發生率分別是參照組的1.344、1.593、1.699倍(均P<0.05)。

表3 不同UA水平合并其他代謝異常與頸動脈狹窄形成的關系
3 討 論
高UA血癥是動脈粥樣硬化的獨立危險因素,與冠心病、心肌梗死、原發性高血壓、腦卒中、心血管事件發生率、死亡率呈正相關〔4〕。Li等〔5〕對1 026例患者血UA與頸動脈內膜中層厚度(IMT)的研究發現,血UA增高與頸動脈IMT厚度具有顯著的相關性。腦卒中高發病率、高死亡率、高復發率、高致殘率的“四高”特點,重在一級預防。腦卒中的危險因素包括年齡、肥胖、吸煙、高血壓、糖尿病、房顫或瓣膜性心臟病、血脂異常及腦卒中家族史等,其中肥胖、吸煙、高血壓、糖尿病、血脂異常等可通過相關措施進行干預。本研究顯示,血清UA水平與頸動脈狹窄發生率和狹窄程度有關,且血清UA水平升高者可能伴有更多的腦卒中危險因素,如高血壓,高HCY血癥,血糖、血脂異常和肥胖等,而這些危險因素本身又是血UA升高的可能原因,因而推測UA合并這些危險因素對頸動脈粥樣硬化的發生和進展起到協同作用,促進頸動脈狹窄的形成。
UA可能通過下列機制參與頸動脈狹窄的形成:①UA濃度增加促進LDL-C氧化和脂質過氧化,加速巨噬細胞吞噬脂質形成泡沫細胞導致平滑肌細胞死亡且生成脂質核心和脂質堆積,在推進頸動脈粥樣硬化的早期階段起著關鍵的作用〔6〕。②UA對血管平滑肌細胞可能有直接的促進炎癥效應,激活炎癥通路〔7〕。③高濃度UA能誘導內皮細胞內皮型一氧化氮合酶蛋白表達下降,一氧化氮(NO)分泌減少,進而導致內皮細胞功能障礙〔8〕。④UA鹽結晶誘發富含血小板血漿中的5-羥色胺釋放,會增加血小板重量,從而可能誘導體內血小板激活,促進血栓形成〔9〕。而高FPG、高TG、高FFA、高HCY、高BMI和低HDL-C是動脈粥樣硬化的危險因素,當這些危險因素合并高UA時,尤其是高血壓合并高UA時,頸動脈狹窄的發生率更顯著升高。
本研究以血UA>390 mmol/L為界定標準,也并非高UA血癥的標準。因此,所得結果可能有一定的局限性,尚需進一步研究,以明確血UA水平與頸動脈狹窄形成的關系。但我們所獲患者資料均是連續隨機,且樣本量較大,頸動脈狹窄的分類嚴格按照國際標準劃分,從單一因素考慮,本研究結論可信。
1王維治.神經病學〔M〕.第5版.北京:人民衛生出版社,2005:9-11.
2Yang G,Wang Y,Zeng Y,etal.Rapid health transition in China,1990-2010:findings from the Global Burden of Disease Study 2010〔J〕.Lancet,2013;381(9882):1987-2015.
3Fox AJ,Eliasziw M,Rothwell PM,etal.Identification,prognosis,and management of patients with carotid aftery near occlusion〔J〕.AJNR,2005;26(8):2086-94.
4Qin L,Yang Z,Gu H,etal.Association between scrum uric acid levels and cardiovascular disease in middle-age elderly Chinese individuals〔J〕,BMC Cardiovasc Disord,2014;14(1):26.
5Li Q,Yang Z,Lu B,etal.Serum uric acid level and its association with metabolic syndrome and atherosclerosis in patients with type 2 diabetes〔J〕.Cardiovasc Diabetol,2011;10(1):72.
6Nishi K,Itabe H,Uno M,etal.Oxidized LDL in carotid plaques and plasma associates with plaque instability〔J〕.Arterioscler Thromb Vasc Biol,2002;22(10):1649-54.
7Kanellis J,Watanabe S,Li JH,etal.Uric acid stimulates monocyte chemoattractant protein-1 production in vascular smooth muscle cells via mitogen-activated protein kinase and cyclooxygenase-2〔J〕.Hypertension,2003;41(6):1287-93.
8張雪光,洪 權,侯 凱,等.高尿酸通過miR-155下調eNOS表達而導致內皮細胞功能障礙〔J〕.南方醫科大學學報,2013;33(8):1141-5.
9李 勍,趙錫海,趙性泉.尿酸與頸動脈粥樣硬化斑塊的關系研究進展〔J〕.中國卒中雜志,2014;9(11):975-9.
浙江省醫藥衛生平臺重點資助課題 (2013ZDA005)
趙慈余(1991-),女,碩士,主要從事生物化學與分子生物學檢驗研究。
R743
A
1005-9202(2017)20-5041-04;
10.3969/j.issn.1005-9202.2017.20.039
〔2016-11-16修回〕
(編輯 曹夢園)

