分散液液微萃取-氣相色譜法快速測定水中15種硝基苯類物質
杜小弟 李俊升 郭麗萍 雷家珩
(武漢理工大學化學化工與生命科學學院化學系, 武漢 430070)
分散液液微萃取-氣相色譜法快速測定水中15種硝基苯類物質
杜小弟 李俊升 郭麗萍 雷家珩*
(武漢理工大學化學化工與生命科學學院化學系, 武漢 430070)
建立了分散液液微萃取-氣相色譜電子捕獲檢測器測定水中15種硝基苯類物質的方法。篩選出了具有高密度且能夠適用于電子捕獲檢測器的萃取劑。優化了色譜條件,對萃取劑種類及用量、分散劑種類及用量、萃取時間、萃取溫度等條件進行了優化。DB-35毛細管柱對15種硝基苯類物質具有最好的分離效果。使用程序升溫,初始80℃保持2 min,以5℃/min速率升溫至180℃,可以在22 min內完成分離。以100 μL氯苯作為萃取劑、400 μL甲醇作為分散劑,對5.00 mL水樣在室溫下進行萃取,僅需30 s即可達到萃取平衡,15種目標物的萃取率均可達到90%以上,富集倍數達到45.0~48.8。離心分離,取下層沉積相進行氣相色譜測定,使用電子捕獲檢測器檢測,方法的定量限為0.03~0.15 μg/L,線性范圍為0.20~50.0 μg/L,相關系數不低于0.998。方法的相對標準偏差在3.3%~8.9%之間,加標回收率在86.0%~103.5%之間。
氣相色譜; 分散液液微萃取; 硝基苯類; 飲用水
2017-08-09收稿;2017-09-18接受
本文系國家自然科學基金項目(No. 21476177)資助
* E-mail: yhx2000@263.net
1 引 言
硝基苯類物質是環保部門重點監控的污染物之一。水中硝基苯類物質一般是通過固相萃取[1~6]或液液萃取[4~6]等方法進行分離富集之后,再采用氣相色譜法[1~6]或液相色譜法[7,8]進行測定。其中氣相色譜法是現行的標準方法[4~6]。液液萃取法較為簡便,但溶劑消耗量大,而且萃取之后常還需要進一步蒸發濃縮。固相萃取法的富集效果較好,但仍然存在試樣和溶劑用量大的問題,而且耗時很長。固相微萃取法(Solid-phase microextraction, SPME)[9]、單滴萃取法(Single drop microextraction, SDME)[10]、頂空溶劑微萃取法(Headspace solvent microextraction, HSME)[11]也應用于水中硝基苯類物質的分離富集,效果較好但耗時很長。分散液液微萃取法(DLLME)是近年來出現的一種新型萃取方法[12,13],且已被廣泛應用[14,15]。通過DLLME法萃取水中硝基苯類物質已有報道[16~21],但一般采用氣相色譜的火焰離子化檢測器(GC-FID)[16,17,21]或者質譜檢測器(GC-MS)[18~20]進行測定,而靈敏度更高的電子捕獲檢測器(GC-ECD)卻很少使用[22]。這是由于DLLME方法需選擇高密度萃取劑(通常為鹵代烴),以便于離心收集。但多數鹵代烴萃取劑的電負性強,不適用于GC-ECD。為了適應GC-ECD,文獻[22,23]提出采用十二醇、甲苯等萃取硝基苯類物質。但這些萃取劑的密度都小于水,不能離心收集,需要在低溫下進行懸浮固化(Solidification of floating organic-droplets, SFO)[22],或者需要使用特制的萃取容器[23]。這使DLLME方法的簡便性大打折扣。
為了同時發揮DLLME法簡便快速和GC-ECD法靈敏度高的優點,需要篩選出密度大于水且能夠適用于ECD檢測器的萃取劑。文獻報道中符合上述兩個條件的萃取劑僅有二硫化碳[24]和氯苯[25,26],其中用氯苯萃取硝基苯類物質已經有文獻進行了嘗試[17,19],但涉及到的硝基苯類物質種類較少,且未使用GC-ECD檢測。本研究將文獻報道的氯苯和二硫化碳,以及本課題組通過實驗篩選出的1,4-二氯丁烷、二氯甲烷、1,2-二氯乙烷共5萃取劑進行了比較,建立了簡便、快速、靈敏度高的檢測水中硝基苯類物質的方法。
2 實驗部分
2.1儀器與試劑
GC2010氣相色譜儀(日本島津公司),配有不分流直接進樣口(WBI-2010)和電子捕獲檢測器(ECD-2010); DB-35彈性石英毛細管色譜柱(30 m×0.32 mm×0.25 μm,美國安捷倫公司); 微量注射器(美國SGE公司)。萃取容器為10 mL尖底玻璃離心管(帶磨口塞)。
15種硝基苯類標樣物質見表1,其中TNT標液(濃度1.01 g/L,甲醇溶劑),購于中國計量科學研究院,其余純度均不低于99%,購于上海阿拉丁試劑公司; 氯苯、二硫化碳、1,4-二氯丁烷、二氯甲烷、1,2-二氯乙烷(分析純,上海阿拉丁試劑公司),重蒸3次后使用; 甲醇、乙腈、丙酮(色譜純,美國Fisher公司)。實驗用水為蒸餾水。
待測試樣為武漢市內不同居民區采集的自來水,以及分別采自湯遜湖、東湖的湖水。
表1 本方法測定的15種硝基苯類物質
Table 1 15 kinds of nitroaromatic compounds determined by this method
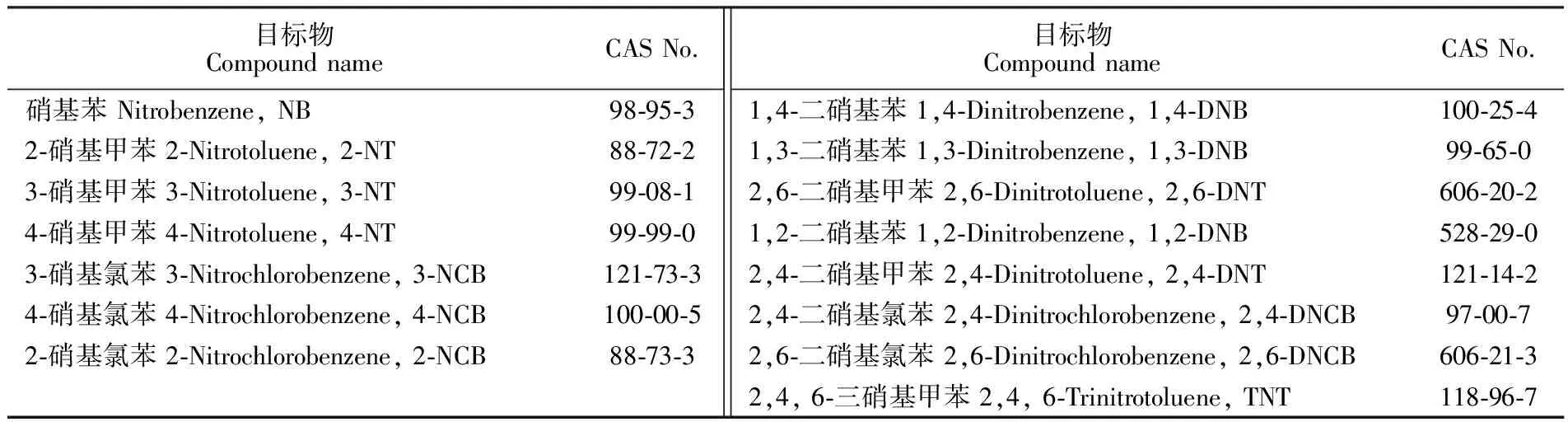
目標物CompoundnameCASNo.硝基苯Nitrobenzene,NB98?95?32?硝基甲苯2?Nitrotoluene,2?NT88?72?23?硝基甲苯3?Nitrotoluene,3?NT99?08?14?硝基甲苯4?Nitrotoluene,4?NT99?99?03?硝基氯苯3?Nitrochlorobenzene,3?NCB121?73?34?硝基氯苯4?Nitrochlorobenzene,4?NCB100?00?52?硝基氯苯2?Nitrochlorobenzene,2?NCB88?73?3目標物CompoundnameCASNo.1,4?二硝基苯1,4?Dinitrobenzene,1,4?DNB100?25?41,3?二硝基苯1,3?Dinitrobenzene,1,3?DNB99?65?02,6?二硝基甲苯2,6?Dinitrotoluene,2,6?DNT606?20?21,2?二硝基苯1,2?Dinitrobenzene,1,2?DNB528?29?02,4?二硝基甲苯2,4?Dinitrotoluene,2,4?DNT121?14?22,4?二硝基氯苯2,4?Dinitrochlorobenzene,2,4?DNCB97?00?72,6?二硝基氯苯2,6?Dinitrochlorobenzene,2,6?DNCB606?21?32,4,6?三硝基甲苯2,4,6?Trinitrotoluene,TNT118?96?7
2.2實驗方法
標準溶液配制:除TNT外,其它標樣分別用甲醇配制成1.00 g/L的單標儲備液。使用時稀釋成所需濃度的混合工作標液。
水樣的預處理:水樣經0.45 μm尼龍濾膜過濾,移取5.00 mL于尖底玻璃離心管中,用微量注射器將100 μL氯苯(萃取劑)與400 μL甲醇(分散劑)的混合液迅速注入到水樣中,加塞輕搖約30 s,得到均勻乳狀液。以6000 r/min離心2 min破乳。棄去上層水相,吸取下層沉積相進行色譜分析。
色譜條件:使用DB-35色譜柱,高純氫氣(99.999%)為載氣,恒線速度控制(65 cm/s)。程序升溫,初始80℃保持2 min,以5℃/min速率升溫至180℃,保持5 min。ECD檢測器溫度220℃,尾吹氣為高純氮氣(99.999%),流速40 mL/min。WBI不分流直接進樣口,溫度200℃,進樣1.00 μL。
萃取率(Extraction recovery, ER)和富集倍率(Enrichment factor, EF)按下列公式計算:

其中,C0為水相中目標物的濃度,模擬樣中C0為已知;Csed為沉積相中目標物的濃度,通過氣相色譜外標法測得;Vaq為水樣體積;Vsed為沉積相體積,由于1 mL水中僅能溶解0.4 μL氯苯,因此近似認為沉積相體積與加入的萃取劑體積相等。
2.3分析方法全程質量控制
以純水代替實際水樣進行空白實驗,所測得空白值小于方法檢出限,因此測定中未進行空白扣除。將標準儲備液用甲醇稀釋成混合標樣,并添加到水樣中進行加標回收實驗,測定萃取過程的萃取率和方法的加標回收率。以現行國標方法[5]作為對照方法,采用固相萃取-氣相色譜法(SPE-GC-ECD)對相同的水樣和加標水樣進行測定。
3 結果與討論
3.1色譜條件優化
3.1.1色譜柱的選擇由于目標物均為芳烴衍生物,根據相似相容原則,選擇含苯基的聚硅氧烷固定相進行分離。實驗結果表明, DB-5和DB-35毛細管柱均可有效分離15種硝基苯類物質,但DB-35的選擇性更好,能夠獲得更高的分離度。因此本研究選擇DB-35毛細管柱,15種硝基苯類物質標樣的色譜圖見圖1。
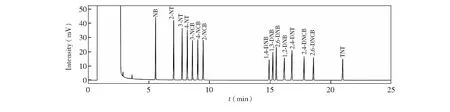
圖1 DB-35毛細管色譜柱分離15種硝基苯類物質的色譜圖,色譜條件如2.2節所述Fig.1 Chromatograms of 15 nitroaromatic compounds using capillary columns with DB-35 stationary phase, Chromatographic conditions are as described in Section 2.2
3.1.2柱溫的優化為了提高靈敏度,本方法采用不分流進樣。為了避免進樣產生的峰展寬,必須使用較低的初始柱溫,使溶劑和目標物在柱頭冷凝。分別以60℃、80℃、100℃、120℃為初始柱溫進行程序升溫,結果表明,初溫80℃時可以獲得尖銳的峰型,且溶劑峰完全不拖尾,分離時間也較短。
3.1.3檢測器溫度的優化由于ECD的響應信號具有溫度敏感性,本研究考察了檢測器溫度在220℃~280℃范圍內變化時各目標物響應信號的變化。結果表明,各目標物的峰高隨檢測器溫度變化不明顯,但溶劑峰的強度隨檢測器溫度的降低而減弱。因此選擇220℃作為ECD檢測器的溫度對減弱溶劑峰的干擾比較有利。
3.2萃取條件的優化
3.2.1萃取劑的種類和用量實驗比較了二硫化碳、氯苯和1,4-二氯丁烷、二氯甲烷, 2-二氯乙烷共5種萃取劑。結果表明,二氯甲烷由于在水中溶解度很大而無法形成沉積相,1,2-二氯乙烷也存在類似問題,能夠收集到的沉積相太少,難以進行后續實驗。二硫化碳、氯苯和1,4-二氯丁烷3種萃取劑可以順利進行萃取,這3種萃取劑對15種硝基苯類物質的萃取率見圖2。二硫化碳對所有目標物的萃取率都較低,1,4-二氯丁烷和氯苯的萃取效果較好。氯苯由于具有與目標物類似的苯環結構,因此具有較好的相容性,從而對大部分目標物都有較高的萃取率。1,4-二氯丁烷對NB、4-NCB、2,4-DNCB這3個目標物的萃取率略高于氯苯,但對其它12種目標物的萃取率明顯低于氯苯。綜合考慮,選擇氯苯作為萃取劑效果較好。
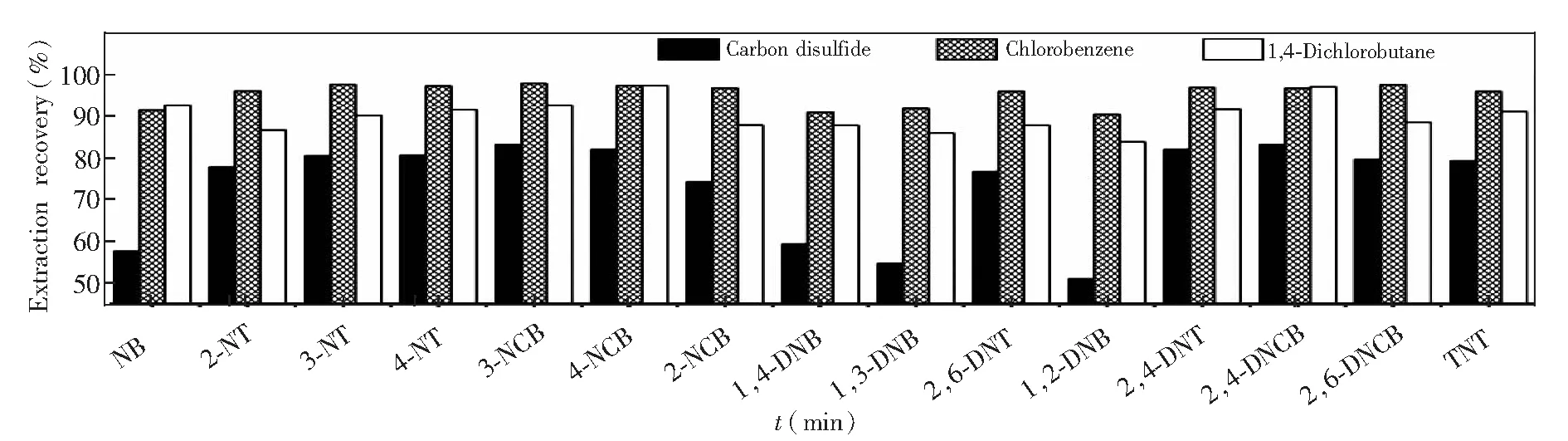
圖2 不同萃取劑對15種硝基苯類物質的萃取率的影響,萃取條件如2.2節所述Fig.2 Effect of different extraction solvents on extraction recovery of 15 nitroaromatic compoundsExtraction conditions are as described in Section 2.2
進一步考察了萃取劑用量對萃取效果的影響, 分別使用50、100、150和200 μL氯苯進行萃取(圖3),結果表明,使用50 μL氯苯不能完全萃取目標物,特別是NB、1,4-DNB、1,3-DNB、1,2-DNB這4種目標物的萃取率較低,僅約為80%。使用100 μL氯苯萃取時,各目標物的萃取率明顯提高,均達到90%以上。進一步提高氯苯用量,萃取率仍可提高。但考慮到富集倍數與萃取劑用量成反比,萃取劑用量過多會導致富集倍數顯著降低,為了兼顧富集倍率和萃取率,萃取劑氯苯的最佳用量選擇100 μL。
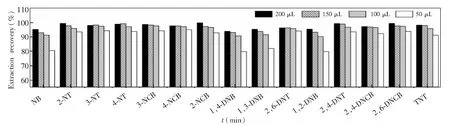
圖3 萃取劑(氯苯)用量對15種硝基苯類物質的萃取率的影響,萃取條件如2.2節所述Fig.3 Influence of extraction solvent (chlorobenzene) volume on extraction recovery of 15 kinds of nitroaromatic compoundsExtraction conditions are as described in Section 2.2
3.2.2分散劑的種類和用量DLLME方法中的分散劑需與水和萃取劑都能完全混溶。本研究選擇常用的甲醇、乙腈、丙酮3種分散劑進行了對比。3種分散劑在用量相同時對各目標物萃取率的影響見圖4。使用丙酮作分散劑時,所有目標物的萃取率都較低。對于硝基甲苯類物質和硝基氯苯類物質,使用甲醇或乙腈作分散劑都能獲得較高的萃取率,無明顯差異。但對于硝基苯和3種二硝基苯異構體,使用乙腈為分散劑時萃取率明顯較低。這可能是由于硝基苯和二硝基苯極性較強且在乙腈溶液中溶解度更大。綜合考慮,選擇甲醇作為分散劑對目標物進行萃取。

圖4 不同分散劑對15種硝基苯類物質的萃取率的影響,萃取條件如2.2節所述Fig.4 Influence of different disperser solvents on extraction recovery of 15 kinds of nitroaromatic compoundsExtraction conditions are described in Section 2.2.
由于DLLME方法中分散劑的用量一般在0.2~1.0 mL左右[15],本研究分別以200、400和600 L甲醇作為分散劑進行萃取。結果表明,200 μL甲醇不能形成穩定的乳狀分散體系,必須靠手動振蕩進行萃取。使用400和600 μL甲醇作為分散劑時效果較好,都能形成均一、穩定的乳狀液,各目標物的萃取率無顯著差異。考慮到甲醇用量增加會使硝基苯類物質在水相中溶解度增大,因此本方法選擇分散劑的用量為400 μL。
3.2.3萃取的時間和溫度根據文獻報道,使用DLLME方法可以在很短時間內達到萃取平衡[12,13]。分別在萃取時間為0.5、5和10 min的條件下進行實驗,結果表明,各目標物的萃取率基本一致。因此本方法選擇萃取時間為0.5 min。
溫度變化會改變目標物在兩相中的分配系數,對萃取效果會產生一定影響。但一般室內環境溫度變化不會太大。分別在15℃、25℃、30℃的水浴條件下進行萃取,發現各目標物的萃取率無顯著變化。因此萃取在室溫條件下進行。
3.2.4水相的鹽濃度和酸度一般認為,通過鹽析作用可以提高有機物的萃取率。考察了水樣中添加NaCl(0.20~1.00 mol/L)對各種目標物萃取率的影響,結果表明,鹽濃度增加時萃取率變化小于3%。這可能是因為硝基苯類物質極性較強,受鹽析作用不明顯。因此本方法在萃取時不添加無機鹽。
實際水樣的pH值一般變化范圍不大,通常在弱酸性到弱堿性范圍,部分水樣在采集時為了方便保存而添加HCl酸化。實驗采用HCl和NaOH將水樣分別調至pH=2.0、4.0、7.0、10.0進行萃取,結果表明,pH值變化對萃取率的影響很小。因此采集的水樣可直接進行萃取,不需調節pH值。
3.2.5沉積相的分離由于萃取劑氯苯的密度大于水,以6000 r/min離心2 min可使有機相完全沉積到離心管底部,水相澄清透明。由于萃取過程已經達到平衡,有機相濃度是均一的,在分離不完全的情況下也可以獲得一致的測定結果。由于水在氯苯中的溶解度很低,有機相含水很少,無需干燥,可直接進行色譜測定[17,19,25,26]。
3.3方法的分析性能
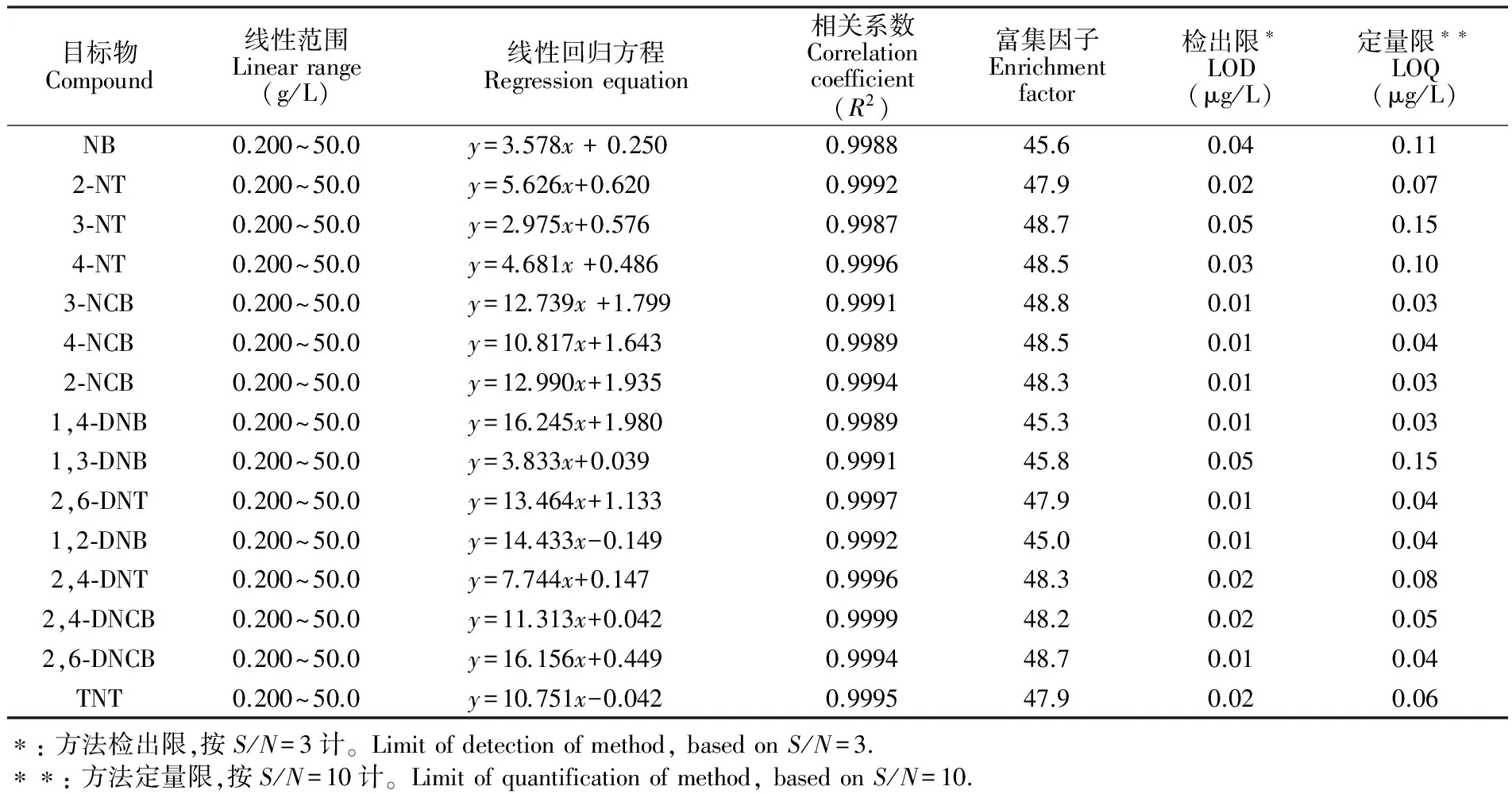
將混合標液用純水稀釋成不同濃度范圍的模擬樣品,按2.2節所述條件進行萃取和測定,以各目標物的峰面積對其濃度進行線性回歸(表2)。各目標物在0.200~50.0 μg/L范圍內均有很好的線性響應,相關系數大于0.998。根據最低濃度標樣計算信噪比(S/N),以S/N=3、S/N=10求得方法的檢出限和定量限(表2)。由于本方法通過萃取獲得了接近50倍的富集因子,因此靈敏度較高,定量限為0.03~0.15 μg/L,完全可以滿足地表水中硝基苯類物質檢測的要求。
表2 15種硝基苯類物質的線性范圍、檢出限、定量限和富集因子
Table 2 Linear range, limit of detection (LOD), limit of quantification (LOQ), and enrichment factor of 15 kinds of nitroaromatic compounds
目標物Compound線性范圍Linearrange(g/L)線性回歸方程Regressionequation相關系數Correlationcoefficient(R2)富集因子Enrichmentfactor檢出限?LOD(μg/L)定量限??LOQ(μg/L)NB0.200~50.0y=3.578x+0.2500.998845.60.040.112?NT0.200~50.0y=5.626x+0.6200.999247.90.020.073?NT0.200~50.0y=2.975x+0.5760.998748.70.050.154?NT0.200~50.0y=4.681x+0.4860.999648.50.030.103?NCB0.200~50.0y=12.739x+1.7990.999148.80.010.034?NCB0.200~50.0y=10.817x+1.6430.998948.50.010.042?NCB0.200~50.0y=12.990x+1.9350.999448.30.010.031,4?DNB0.200~50.0y=16.245x+1.9800.998945.30.010.031,3?DNB0.200~50.0y=3.833x+0.0390.999145.80.050.152,6?DNT0.200~50.0y=13.464x+1.1330.999747.90.010.041,2?DNB0.200~50.0y=14.433x-0.1490.999245.00.010.042,4?DNT0.200~50.0y=7.744x+0.1470.999648.30.020.082,4?DNCB0.200~50.0y=11.313x+0.0420.999948.20.020.052,6?DNCB0.200~50.0y=16.156x+0.4490.999448.70.010.04TNT0.200~50.0y=10.751x-0.0420.999547.90.020.06?:方法檢出限,按S/N=3計。Limitofdetectionofmethod,basedonS/N=3.??:方法定量限,按S/N=10計。Limitofquantificationofmethod,basedonS/N=10.
3.4實際樣品分析
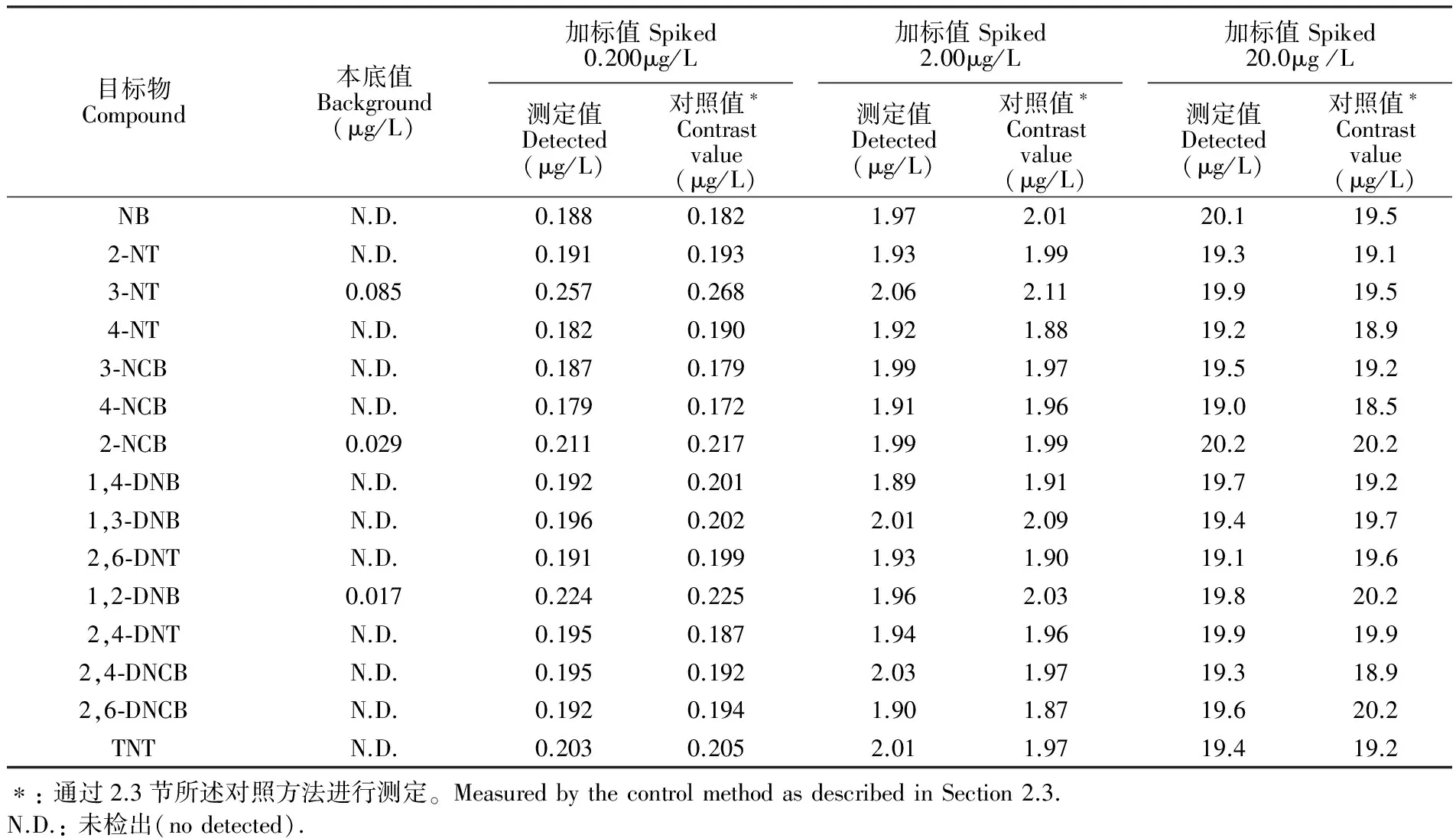
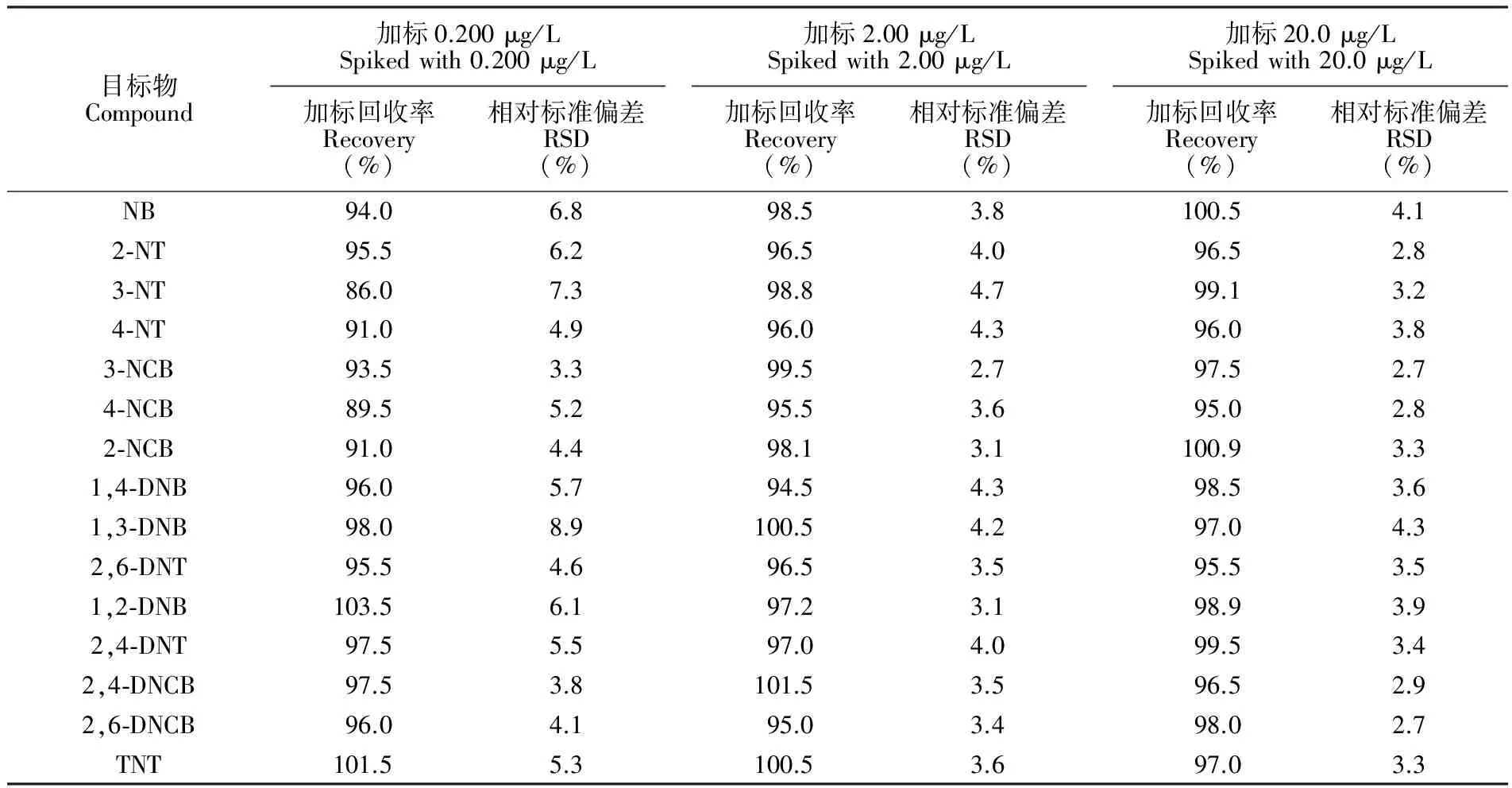
測定了3個飲用水試樣和兩個湖水試樣,僅有一個湖水試樣檢出3種硝基苯化合物。有檢出試樣的色譜圖見圖5A,經過萃取處理后,試樣基體凈化效果較好,干擾峰較少且能夠有效分離。以該試樣為基體,進行了0.200、2.00和20.0 μg/L共3個水平的加標實驗,其中加標0.200 μg/L試樣的色譜圖見圖5B。加標試樣的測定結果見表3,以現行國標方法作為對照方法的測定結果也列于表3,可以看出,兩種方法的結果具有較好的一致性。本方法的相對標準偏差(RSD)和加標回收率見表4。在接近方法的定量限的加標水平(0.200 μg/L)下,方法的相對標準偏差在3.3%~8.9%之間,加標回收率為86.0%~103.5%,可滿足痕量分析的要求。在中、高濃度水平(2.00和20.0 μg/L)下,方法的相對標準偏差均不超過5%,加標回收率在94.5%~101.5%之間。
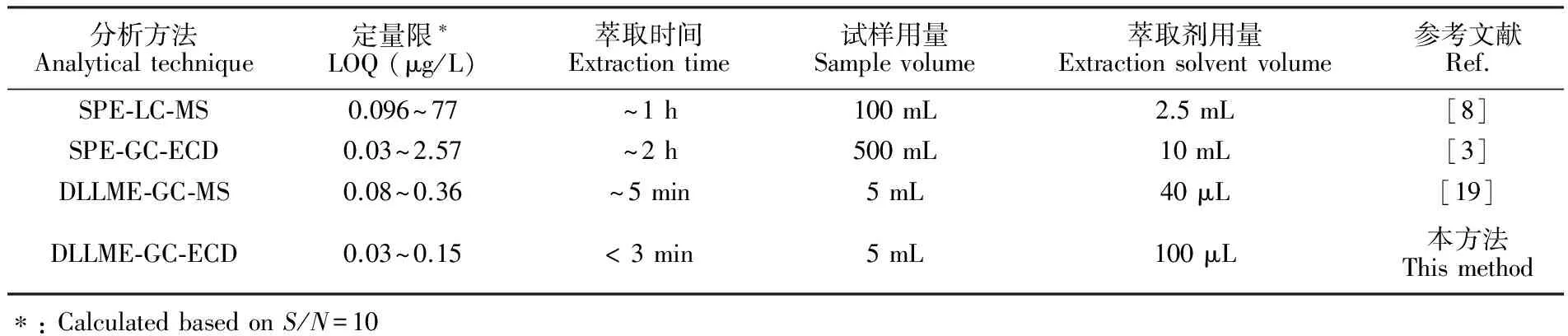
進一步將本方法與文獻報道的測定水中硝基苯類物質的方法進行對比(表5)可知,本方法靈敏度高、簡便、快速。與現行國標方法相比,樣品處理時間由2 h縮短至約3 min,處理效率顯著提高。另外,本方法的試樣和萃取劑用量少,僅為國標方法的1%,節約了試劑,減少了污染。
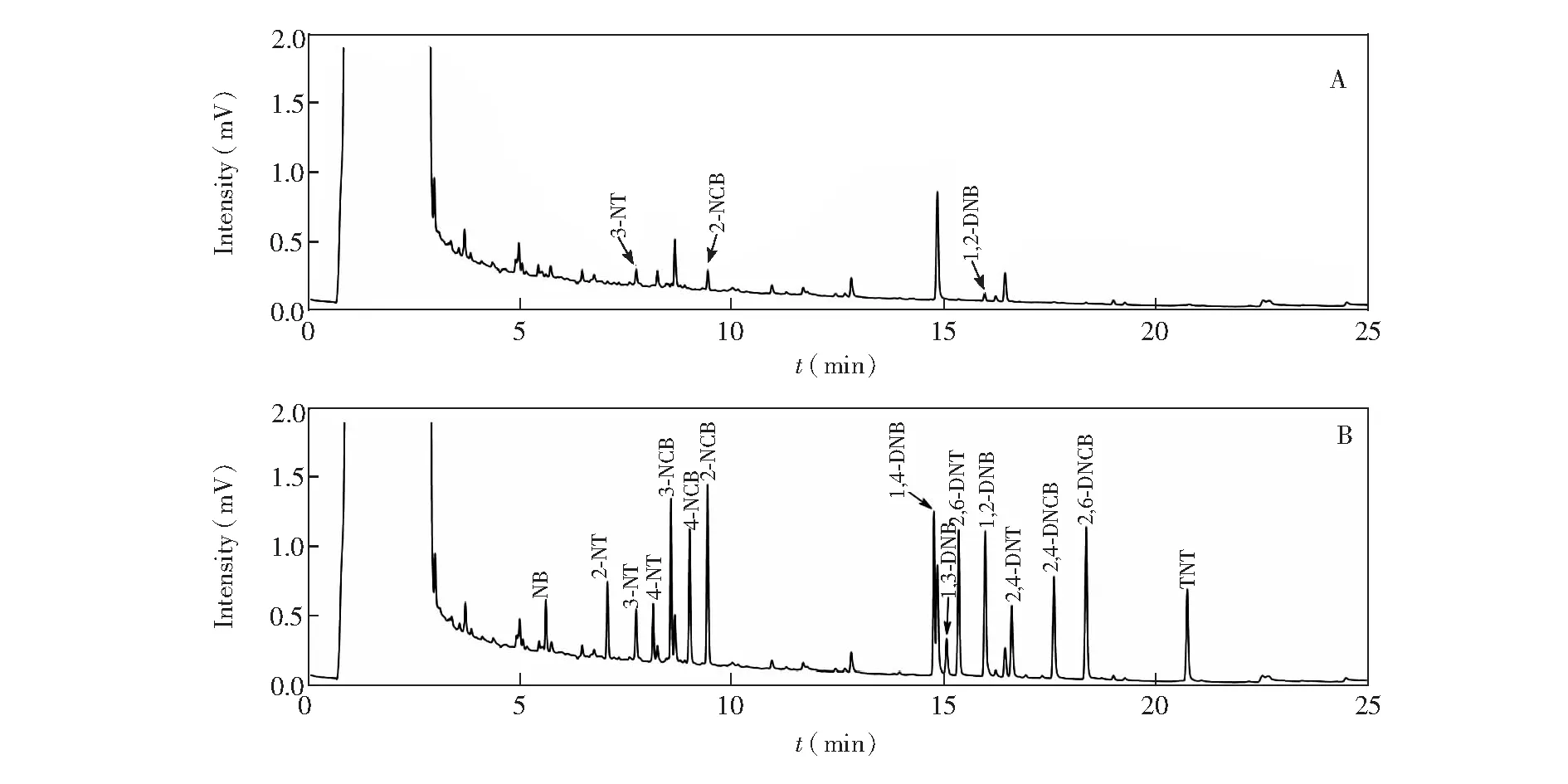
圖5 實際水樣與加標水樣的色譜圖Fig.5 Chromatograms of real water sample and spiked water sample obtained by DLLME-GC-ECD methdA:實際水樣; B:加標水樣,每種目標物的加標水平為0.200 μg/L。色譜條件見2.2節所述A: Real water sample; B: spiked water samples at the concentration level of 0.200 μg/L for each nitroaromatic compound. Chromatographic conditions are as described in Section 2.2
表3 本方法與國標方法測定結果的比較(n=7)
Table 3 Comparison of the results by the proposed method and national standard method (n=7)
目標物Compound本底值Background(μg/L)加標值Spiked0.200μg/L測定值Detected(μg/L)對照值?Contrastvalue(μg/L)加標值Spiked2.00μg/L測定值Detected(μg/L)對照值?Contrastvalue(μg/L)加標值Spiked20.0μg/L測定值Detected(μg/L)對照值?Contrastvalue(μg/L)NBN.D.0.1880.1821.972.0120.119.52?NTN.D.0.1910.1931.931.9919.319.13?NT0.0850.2570.2682.062.1119.919.54?NTN.D.0.1820.1901.921.8819.218.93?NCBN.D.0.1870.1791.991.9719.519.24?NCBN.D.0.1790.1721.911.9619.018.52?NCB0.0290.2110.2171.991.9920.220.21,4?DNBN.D.0.1920.2011.891.9119.719.21,3?DNBN.D.0.1960.2022.012.0919.419.72,6?DNTN.D.0.1910.1991.931.9019.119.61,2?DNB0.0170.2240.2251.962.0319.820.22,4?DNTN.D.0.1950.1871.941.9619.919.92,4?DNCBN.D.0.1950.1922.031.9719.318.92,6?DNCBN.D.0.1920.1941.901.8719.620.2TNTN.D.0.2030.2052.011.9719.419.2?:通過2.3節所述對照方法進行測定。MeasuredbythecontrolmethodasdescribedinSection2.3.N.D.:未檢出(nodetected).
4 結 論
通過DLLME法分離富集水中的15種硝基苯類物質, 氯苯和1,4-二氯丁烷均可作為萃取劑,但氯苯的萃取效果更好,萃取率不低于90%,富集因子接近50。萃取液經DB-35毛細管柱分離,用ECD定量檢測,定量限達到0.03~0.15 μg/L。本方法在處理速度上顯著優于文獻方法,樣品和試劑的用量也更少。
表4 方法的精密度及加標回收率(n=7)
Table 4 Precision and recovery results of this method (n=7)
目標物Compound加標0.200μg/LSpikedwith0.200μg/L加標回收率Recovery(%)相對標準偏差RSD(%)加標2.00μg/LSpikedwith2.00μg/L加標回收率Recovery(%)相對標準偏差RSD(%)加標20.0μg/LSpikedwith20.0μg/L加標回收率Recovery(%)相對標準偏差RSD(%)NB94.06.898.53.8100.54.12?NT95.56.296.54.096.52.83?NT86.07.398.84.799.13.24?NT91.04.996.04.396.03.83?NCB93.53.399.52.797.52.74?NCB89.55.295.53.695.02.82?NCB91.04.498.13.1100.93.31,4?DNB96.05.794.54.398.53.61,3?DNB98.08.9100.54.297.04.32,6?DNT95.54.696.53.595.53.51,2?DNB103.56.197.23.198.93.92,4?DNT97.55.597.04.099.53.42,4?DNCB97.53.8101.53.596.52.92,6?DNCB96.04.195.03.498.02.7TNT101.55.3100.53.697.03.3
表5 不同分析方法用于測定水中硝基苯類物質的比較
Table 5 Comparison of different analytical methods for determination of nitroaromatics in aqueous samples
分析方法Analyticaltechnique定量限?LOQ(μg/L)萃取時間Extractiontime試樣用量Samplevolume萃取劑用量Extractionsolventvolume參考文獻Ref.SPE?LC?MS0.096~77~1h100mL2.5mL[8]SPE?GC?ECD0.03~2.57~2h500mL10mL[3]DLLME?GC?MS0.08~0.36~5min5mL40μL[19]DLLME?GC?ECD0.03~0.15<3min5mL100μL本方法Thismethod?:CalculatedbasedonS/N=10
1 Peng X T, Zhao X, Feng Y Q.J.Chromatogr.A,2011, 1218(52): 9314-9320
2 Zhang G J, Zhou X, Zang X H, Li Z, Wang C, Wang Z.ChineseChem.Lett.,2014, 25 (11): 1449-1454
3 ZOU Hai-Min, ZHOU Chen, YU Hui-Ju, ZHANG Qian, ZENG Hong-Yan, LI Yong-Xin.ChineseJ.Anal.Chem.,2016, 44(2): 297-304
鄒海民, 周 琛, 余輝菊, 張 潛, 曾紅燕, 李永新. 分析化學,2016, 44(2): 297-304
4 EPA 8091,NitroaromaticsandCyclicKetonesbyGasChromatography. US Environmental Protection Agency Standards
5 HJ 648-2013,WaterQuality:DeterminationofNitroaromaticsbyGasChromatography. National Environmental Protection Standards of the People's Republic of China
水質: 硝基苯類化合物的測定 液液萃取/固相萃取-氣相色譜法. 中華人民共和國國家環境保護標準, HJ 648-2013
6 HJ 716-2014,WaterQuality:DeterminationofNitroaromaticsbyGasChromatographyMassSpectrometry. National Environmental Protection Standards of the People's Republic of China
水質: 硝基苯類化合物的測定 氣相色譜-質譜法. 中華人民共和國國家環境保護標準, HJ 716-2014
7 Gaurav Kaur V, Kumar A, Kumar Malik A, Rai P K.J.Hazard.Mater.,2007, 147(3): 691-697
8 Rapp-Wright H, McEneff G, Murphy B, Gamble S, Morgan R, Beardah M, Barron L.J.Hazard.Mater.,2017, 329(1): 11-21
9 Reyes-Gallardo E M, Lasarte-Aragonés G, Lucena R, Cárdenas S, Valcárcel M.J.Chromatogr.A,2013, 1271(1): 50-55
10 Psillakis E, Kalogerakis N.J.Chromatogr.A,2001, 907(1): 211-219
11 Ebrahimzadeh H, Yamini Y, Kamarei F, Khalili-Zanjani M.Talanta,2007, 72(1): 193-198
12 Rezaee M, Assadi Y, Milani Hosseini M R, Aghaee E, Ahmadi F, Berijani S.J.Chromatogr.A,2006, 1116(1-2): 1-9
13 Berijani S, Assadi Y, Anbia M, Milani Hosseini M R, Aghaee E.J.Chromatogr.A,2006, 1123(1): 1-9
14 Yan H Y, Wang H.J.Chromatogr.A,2013, 1295(5): 1-15
15 Campillo N, Vias P,andrejovJ, Andruch V.Appl.Spectrosc.Rev.,2017, 52(4): 267-415
16 Ebrahimzadeh H, Yamini Y, Kamarei F.Talanta,2009, 79(5): 1472-1477
17 Sobhi H R, Kashtiaray A, Farahani H, Javaheri M, Ganjali M R.J.Hazard.Mater.,2010, 175(1): 279-283
18 Zhang D, Zeng X, Yu Z, Sheng G, Fu J.Anal.Methods,2011, 3(10): 2254-2260
19 Cortada C, Vidal L, Canals A.Talanta,2011, 85(5): 2546-2552
20 XIONG Jun, XIE Si-Long, LAI Yi-Dong.ChineseJournalofChromatography,2011, 29(2): 115-119
熊 珺, 謝思龍, 賴毅東. 色譜,2011, 29(2): 115-119
21 Jowkarderis M, Raofie F.Talanta,2012, 88(1): 50-53
22 Wu Y, Dai L, Cheng J, Guo F, Li J.Chromatographia,2010, 72(7-8): 695-699
23 Bahmaei M, Mashayekhi H A, Khalilian F.J.Braz.Chem.Soc.,2015, 26(7): 1475-1481
24 Ahmad U K, Mechor W H, Mohamed M.Anal.Lett.,2012, 45(15): 2198-2209
25 Fattahi N, Assadi Y, Hosseini M R M, Jahromi E Z.J.Chromatogr.A,2007, 1157(1): 23-29
26 Kozani R R, Assadi Y, Shemirani F, Hosseini M R M, Jamali M R.Talanta,2007, 72(2): 387-393
This work was supported by the National Natural Science Foundation of China (No. 21476177).
Determinationof15KindsofNitroaromaticsinAqueousSamples
UsingDispersiveLiquid-LiquidMicroextractionand
GasChromatographywithElectronCaptureDetection
DU Xiao-Di, LI Jun-Sheng, GUO Li-Ping, LEI Jia-Heng*
(DepartmentofChemistry,SchoolofChemistry,ChemicalEngineeringandLifeSciences,
WuhanUniversityofTechnology,Wuhan430070,China)
A method for the determination of 15 kinds of nitroaromatics in aqueous samples was developed by dispersive liquid-liquid microextraction and gas chromatography with electron capture detection. A high-density extractant applied in electron capture detector was screened out. The chromatographic conditions, types and dosages of extractants, types and dosages of dispersants, extraction time and the extraction temperature were optimized. The results showed that DB-35 capillary column had the best separation performance for the 15 kinds of nitroaromatics. The nitroaromatics could be separated within 22 min using programmed temperature control as follows: holding at an initial temperature of 80℃ and then heating to 180℃ at a ramping rate of 5℃/min. For the extraction of 15 kinds of nitroaromatics from 5 mL of aqueous sample, the extraction equilibrium could be reached within 30 s with a high extraction recovery of over 90% when using 100 μL of chlorobenzene as extracting solvent and 400 μL of methanol as disperser solvent. In addition, the enrichment factor could approach a high value of 45.0-48.8. The sediment collected by centrifugation was injected and analyzed by gas chromatography with electron capture detector. The limits of quantification of the developed method were 0.03-0.15 μg/L (S/N=10). The linear range was from 0.20 μg/L to 50.0 μg/L, while the correlation coefficients (R2) were more than 0.998. At the spiked level of 0.200 μg/L, the relative standard deviations of this method were 3.3%-8.9%, the relative recoveries ranged from 86.0% to 103.5%. At higher spiked level, the relative standard deviations were less than 5%, and the relative recoveries ranged from 94.5% to 101.5%.
Gas chromatography; Dispersive liquid-liquid microextraction; Nitroaromatics; Drinking water
9 August 2017; accepted 18 September 2017)
10.11895/j.issn.0253-3820.171160

