不同階段老年糖尿病患者血管內(nèi)皮功能差異及大血管保護(hù)機(jī)制
盧廣民
(臨沂市第三人民醫(yī)院,山東 臨沂 276023)
不同階段老年糖尿病患者血管內(nèi)皮功能差異及大血管保護(hù)機(jī)制
盧廣民
(臨沂市第三人民醫(yī)院,山東 臨沂 276023)
目的比較不同階段老年2型糖尿病(T2DM)患者血管內(nèi)皮功能差異并探討大血管保護(hù)機(jī)制。方法選取糖耐量受損患者97例,T2DM患者290例,選取同期在該院體檢的正常糖耐量老年人106例。進(jìn)一步將T2DM患者分為新診斷的T2DM組(N1組)86例;T2DM達(dá)標(biāo)組(N2組)101例;T2DM未達(dá)標(biāo)組(N3組)103例。超聲測(cè)定各組內(nèi)皮依賴的血管擴(kuò)張率(FMD)、非內(nèi)皮依賴的血管擴(kuò)張率(GTN)、頸動(dòng)脈內(nèi)膜中層厚度。硝酸還原酶法、酶聯(lián)免疫吸附(ELISA)法測(cè)定一氧化氮(NO)、內(nèi)皮素(ET)-1含量。分離外周血單個(gè)核細(xì)胞,熒光定量PCR檢測(cè)胃蛋白酶原C(PGC)-1α mRNA、白細(xì)胞介素(IL)-1 mRNA轉(zhuǎn)錄水平;Western印跡檢測(cè)P-Akt(Ser473)蛋白表達(dá)。結(jié)果T2DM組FMD值明顯低于正常糖耐量組和糖耐量受損組(P<0.05);N2組和N3組GTN值和頸動(dòng)脈內(nèi)膜中層厚度均明顯低于N1組、正常糖耐量組、糖耐量受損組(P<0.05)。N1組基礎(chǔ)NO、ET-1水平明顯高于其余各組(P<0.05)。T2DM組PGC-1α mRNA、IL-1 mRNA表達(dá)量均明顯高于非T2DM組(P<0.05)。T2DM組P-Akt(Ser473)蛋白表達(dá)量明顯低于正常糖耐量組與糖耐量受損組(P<0.05);N1組明顯高于N3組(P<0.05)。PGC-1α mRNA水平是FMD的獨(dú)立影響因素;低密度脂蛋白膽固醇(LDL-C)、舒張壓是GTN的獨(dú)立影響因素;收縮壓是頸動(dòng)脈內(nèi)膜中層厚度的獨(dú)立影響因素。結(jié)論FMD可敏感預(yù)測(cè)早期老年T2DM大血管病變,GTN、頸動(dòng)脈內(nèi)膜中層厚度偏重于病變進(jìn)展;PGC-1α基因可經(jīng)內(nèi)皮依賴和非依賴兩種機(jī)制保護(hù)糖尿病大血管。
2型糖尿病;血管內(nèi)皮功能;大血管保護(hù)
2型糖尿病(T2DM)存在Pi3k-Akt信號(hào)通路傳導(dǎo)障礙,而該通路又參與胰島素刺激的血管內(nèi)皮一氧化氮(NO)分泌的調(diào)控〔1〕,因此可推測(cè)新確診的T2DM患者可能存在NO水平下降導(dǎo)致的血管內(nèi)皮功能障礙。目前,關(guān)于不同血糖水平下內(nèi)皮依賴的血管擴(kuò)張率(FMD)、非內(nèi)皮依賴的血管擴(kuò)張率(GTN)、頸動(dòng)脈內(nèi)膜中層厚度對(duì)早期血管內(nèi)皮功能障礙的預(yù)測(cè)價(jià)值以及胃蛋白酶原C(PGC)-1α基因?qū)μ悄虿?DM)大血管保護(hù)機(jī)制尚無系統(tǒng)研究報(bào)道。本研究旨在探討不同階段老年T2DM患者血管內(nèi)皮功能差異及PGC-1α基因?qū)Υ笱艿谋Wo(hù)作用。
1 資料與方法
1.1一般資料 經(jīng)倫理委員會(huì)批準(zhǔn)并簽署知情同意書后,根據(jù)中國(guó)糖尿病指南標(biāo)準(zhǔn)收集2015年6月至2016年6月臨沂市第三人民醫(yī)院就診的糖耐量受損患者97例,其中男46例,女51例,年齡60~78歲,平均(68.31±5.08)歲;T2DM患者290例,男138例,女152例,年齡60~81歲,平均(69.81±7.35)歲。選取同期在本院體檢的正常糖耐量老年人106例為對(duì)照,男48例,女58例,年齡60~76歲,平均(68.12±7.34)歲。按病程和糖化血紅蛋白(HbA1c)水平將T2DM患者分為:病程≤1年新診斷的T2DM組(N1組)86例;病程≥5年且HbA1c<7%的糖尿病達(dá)標(biāo)組(N2組)101例;病程≥5年且HbA1c≥7%的T2DM未達(dá)標(biāo)組(N3組)103例。
1.2方法
1.2.1血管擴(kuò)張率測(cè)定 FMD測(cè)定:研究對(duì)象清晨空腹且膀胱排空后,超聲獲取右肘肱動(dòng)脈縱切面,固定探頭。以靜息狀態(tài)下肱動(dòng)脈內(nèi)徑為基礎(chǔ)對(duì)照,充氣使壓力升至250 mmHg,完全阻斷血流5 min后放氣,在1 min時(shí)測(cè)定肱動(dòng)脈內(nèi)徑,計(jì)算血管擴(kuò)張率。GTN測(cè)定:研究對(duì)象舌下含服500 μg硝酸甘油時(shí)加壓和釋壓形成的肱動(dòng)脈內(nèi)徑擴(kuò)張情況,計(jì)算血管擴(kuò)張率。
1.2.2頸動(dòng)脈內(nèi)膜中層厚度檢測(cè) 研究對(duì)象頸動(dòng)脈內(nèi)膜中層厚度定義為頸動(dòng)脈壁內(nèi)膜和中膜厚度之和。選取左、右兩側(cè)頸動(dòng)脈近端、中端、遠(yuǎn)端各1 cm長(zhǎng)的血管腔為靶區(qū),超聲測(cè)定血液內(nèi)膜界面與血管壁中膜、外膜界面間的距離,取雙側(cè)均值為頸動(dòng)脈內(nèi)膜中層厚度。
1.2.3血管內(nèi)皮功能指標(biāo)檢測(cè) 酶聯(lián)免疫吸附(ELISA)試劑盒檢測(cè)內(nèi)皮素(ET)-1水平,試劑盒購(gòu)于上海廣銳生物科技有限公司;采用硝酸還原酶法測(cè)定NO水平,試劑盒購(gòu)于上海恒遠(yuǎn)生物科技有限公司。檢測(cè)過程均嚴(yán)格按試劑盒說明書進(jìn)行。
1.2.4外周血單個(gè)核細(xì)胞分離 取5 ml抗凝處理后的靜脈血用等量磷酸緩沖液稀釋,緩慢加于淋巴細(xì)胞分離液表面,室溫下3 000 r/min離心30 min,離心管內(nèi)液體從上到下分別為血漿磷酸緩沖液、外周血單個(gè)核細(xì)胞層、淋巴細(xì)胞分離液、粒細(xì)胞、紅細(xì)胞;吸取外周血單個(gè)核細(xì)胞轉(zhuǎn)入加含1640細(xì)胞培養(yǎng)基的離心管中備用。
1.2.5熒光定量PCR檢測(cè) Trizol試劑提取外周血單個(gè)核細(xì)胞中總RNA,逆轉(zhuǎn)錄制備cDNA。使用實(shí)時(shí)熒光定量PCR儀檢測(cè)PGC-1α mRNA、IL-1 mRNA轉(zhuǎn)錄水平。反應(yīng)體系40 μl,包括SYBR Green 15 μl、上游和下游引物各1 μl、cDNA 1 μl、蒸餾水23 μl。以GAPDH為內(nèi)標(biāo)基因,引物設(shè)計(jì)由上海滬宇生物科技有限公司完成。常規(guī)擴(kuò)增條件下進(jìn)行40個(gè)循環(huán),讀取Ct值。
1.2.6Western印跡檢測(cè)P-Akt(Ser473)蛋白表達(dá) 外周血單個(gè)核細(xì)胞與100 μl蛋白裂解液混勻,水浴反應(yīng)10 min,5 000 r/min離心15 min,BCA法測(cè)定總蛋白含量。取50 μg蛋白行SDS-PAGE電泳,濕法轉(zhuǎn)移到PVDF膜,滴加兔抗人P-Akt(Ser473)一抗(1∶100)和β-actin單克隆抗體(1∶500)孵育過夜,滴加HRP標(biāo)記的二抗,孵育2 h后洗膜,ECL試劑盒顯影,圖像掃描軟件測(cè)定膠片上條帶灰度值。
1.3統(tǒng)計(jì)學(xué)分析 使用SPSS18.0軟件進(jìn)行t檢驗(yàn)、Pearson檢驗(yàn)和Logistic回歸分析。
2 結(jié) 果
2.1各組臨床資料和血管內(nèi)皮超聲檢測(cè)結(jié)果 各組收縮壓、舒張壓、總膽固醇(TC)、甘油三酯(TG)、低密度脂蛋白膽固醇(LDL-C)差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。T2DM組FMD值明顯低于正常糖耐量組和糖耐量受損組(P<0.05);正常糖耐量組和糖耐量受損組之間差異無統(tǒng)計(jì)學(xué)意義(P>0.05);T2DM組中FMD值由高到低依次為:N1組>N2組>N3組,組間差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。N2組和N3組GTN值和頸動(dòng)脈內(nèi)膜中層厚度均明顯低于N1組、正常糖耐量組、糖耐量受損組(P<0.05)。見表1。
2.2各組NO、ET-1水平比較 N1組基礎(chǔ)NO、ET-1水平明顯高于N2組、N3組、正常糖耐量組、糖耐量受損組(P<0.05);正常糖耐量組與糖耐量受損組之間差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。見表2。
2.3各組PGC-1α mRNA、IL-1 mRNA表達(dá)水平比較 N1、N2、N3組間差異均有統(tǒng)計(jì)學(xué)意義(P<0.05);正常糖耐量組與糖耐量受損組之間差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。見表3。
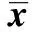
表1 各組臨床資料和血管內(nèi)皮超聲檢測(cè)結(jié)果比較(±s)
與正常糖耐量組比較:1)P<0.05;與糖耐量受損組比較:2)P<0.05;與N1組比較:3)P<0.05

表2 各組血管內(nèi)皮功能指標(biāo)比較(±s)
與N1組比較:1)P<0.05
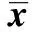
表3 各組PGC-1α mRNA、IL-1 mRNA表達(dá)水平比較(±s)
2.4各組P-Akt(Ser473)蛋白水平比較 N1組、N2組、N3組P-Akt(Ser473)蛋白表達(dá)量分別為(0.76±0.22)、(0.74±0.20)、(0.46±0.11),明顯低于正常糖耐量組與糖耐量受損組的(0.91±0.14)、(0.89±0.10),P<0.05;N1組與N2組差異無統(tǒng)計(jì)學(xué)意義(P>0.05);N1組明顯高于N3組(P<0.05)。見圖1。

圖1 Western印跡檢測(cè)各組P-Akt(Ser473)蛋白的表達(dá)
2.5相關(guān)性分析 收縮壓與FMD呈負(fù)相關(guān)(r=-0.318,P<0.05);收縮壓、舒張壓、LDL-C與GTN呈負(fù)相關(guān)(r=-0.206、-0.293、-0.164,P<0.05);收縮壓、TG與頸動(dòng)脈內(nèi)膜中層厚度呈正相關(guān)(r=0.327、0.235,P<0.05)。PGC-1α mRNA表達(dá)量與FMD、GTN呈正相關(guān)(r=0.260、0.227,P<0.05)。多因素Logistic回歸分析顯示,PGC-1α mRNA水平是FMD的獨(dú)立影響因素,LDL-C、舒張壓是GTN的獨(dú)立影響因素,收縮壓是頸動(dòng)脈內(nèi)膜中層厚度的獨(dú)立影響因素。
3 討 論
FMD通過檢測(cè)血內(nèi)容積瞬間最大改變從而間接反映出肱動(dòng)脈內(nèi)皮細(xì)胞瞬間NO釋放量,與血管內(nèi)皮功能密切相關(guān)〔2〕。GTN可直接刺激平滑肌細(xì)胞引發(fā)血管舒張,其機(jī)制與內(nèi)皮細(xì)胞分泌的NO無相關(guān)性,與血管平滑肌功能相關(guān)〔3〕。相關(guān)研究顯示,當(dāng)危險(xiǎn)因素存在時(shí)頸總動(dòng)脈因壓力較大,出現(xiàn)血管壁內(nèi)膜增厚的風(fēng)險(xiǎn)明顯高于其他部位,可作為大血管動(dòng)脈硬化早期預(yù)測(cè)因子〔4〕。本研究結(jié)果說明FMD早期預(yù)測(cè)敏感性較高GTN和頸動(dòng)脈內(nèi)膜中層厚度更側(cè)重于對(duì)動(dòng)脈硬化進(jìn)展的預(yù)測(cè)。
血管平滑肌重構(gòu)引發(fā)的動(dòng)脈粥樣硬化是DM大血管并發(fā)癥的主要病理基礎(chǔ),多為血管舒張機(jī)制受損〔5〕。相關(guān)研究顯示,血管內(nèi)皮細(xì)胞分泌的NO、ET-1可誘發(fā)血管舒張,內(nèi)皮功能受損會(huì)導(dǎo)致NO、ET-1合成降低,進(jìn)而促發(fā)動(dòng)脈粥樣硬化。因此,對(duì)血管內(nèi)皮合成的NO、ET-1進(jìn)行評(píng)估可有效預(yù)測(cè)大血管并發(fā)癥〔6〕。本研究結(jié)果提示P-Akt(Ser473)信號(hào)通路介導(dǎo)的血管內(nèi)皮NO、ET-1合成在DM早期已出現(xiàn)缺損,同時(shí)IL-1介導(dǎo)的NO、ET-1合成在N1組中對(duì)NO、ET-1貢獻(xiàn)較大。N2組NO、ET-1水平明顯低于N1組,但I(xiàn)L-1 mRNA水平無明顯變化,考慮因?yàn)镻GC-1α轉(zhuǎn)錄水平降低,其原因可能與線粒體功能減弱誘發(fā)eNOS合成量降低有關(guān)。
PGC-1α基因可促進(jìn)線粒體合成、脂肪酸氧化,減少細(xì)胞中ROS聚集,是調(diào)控血管內(nèi)皮細(xì)胞能量代謝和抑制凋亡的主要因子〔7〕。本研究結(jié)果說明PGC-1α基因可通過對(duì)血管內(nèi)皮細(xì)胞線粒體功能的調(diào)控,經(jīng)內(nèi)皮依賴和非依賴兩種途徑保護(hù)DM大血管。
1邢玲玲.P13K/Akt通路在糖尿病腎病足細(xì)胞損傷中的作用〔D〕.石家莊:河北醫(yī)科大學(xué),2012.
2de Jager J,Kooy A,Schalkwijk C,etal.Long-term effects of metformin on endothelial function in type 2 diabetes:a randomized controlled trial〔J〕.J Int Med,2014;275(1):59-70.
3Hopkins ND,Cuthbertson DJ,Kemp GJ,etal.Effects of 6 months glucagon-like peptide-1 receptor agonist treatment on endothelial function in type 2 diabetes mellitus patients〔J〕.Diabetes Obes Metab,2013;15(8):770-3.
4魏海峰,錢 軍,鮑丙波,等.微血管形成在腰椎間盤退變過程中的表現(xiàn)特征及影響因素〔J〕.北華大學(xué)學(xué)報(bào)(自然科學(xué)版),2016;17(5):632-5.
5龔 蕾.高糖致胰島微血管內(nèi)皮細(xì)胞凋亡的機(jī)制及年齡相關(guān)胰島β細(xì)胞再生的研究〔D〕.濟(jì)南:山東大學(xué),2013.
6Barone Gibbs B,Dobrosielski DA,Bonekamp S,etal.A randomized trial of exercise for blood pressure reduction in type 2 diabetes:effect on flow-mediated dilation and circulating biomarkers of endothelial function〔J〕.Atherosclerosis,2012;224(2):446-53.
7孫慧琳.GLP-1對(duì)AGEs誘導(dǎo)的血管內(nèi)皮細(xì)胞損傷的拮抗作用及機(jī)制研究〔D〕.廣州:南方醫(yī)科大學(xué),2015.
〔2016-12-12修回〕
(編輯 郭 菁)
盧廣民(1967-),男,副主任醫(yī)師,主要從事內(nèi)分泌-糖尿病方面的臨床研究。
R587.1
A
1005-9202(2017)16-3986-03;doi:10.3969/j.issn.1005-9202.2017.16.035

