碳量子點合成及其在食品檢測中的應用
魏 偉,石星波,3,*,鄧放明
(1.湖南農業大學食品科學技術學院,湖南 長沙 410128;2.湖南農業大學東方科技學院,湖南 長沙 410128;3.湖南大學 化學生物傳感與計量學國家重點實驗室,湖南 長沙 410082)
碳量子點合成及其在食品檢測中的應用
魏 偉1,2,石星波1,2,3,*,鄧放明1,2
(1.湖南農業大學食品科學技術學院,湖南 長沙 410128;2.湖南農業大學東方科技學院,湖南 長沙 410128;3.湖南大學 化學生物傳感與計量學國家重點實驗室,湖南 長沙 410082)
碳量子點(carbon dots,CDs)作為一類新型的熒光納米材料,具備很多優良的光學特性。相比于半導體量子點,其毒性低、生物相容性好、穩定性與抗光漂白性更高,這些優良的性質使其在檢測食品中重金屬、抗生素、病原菌、農藥殘留與違禁添加劑以及營養功能成分等方面有很好的發展前景。近年來,有關CDs的文獻綜述著重于總結其合成與光學性質,鮮有關于CDs在食品檢測中的應用。本文介紹CDs的光學性質與合成方法,重點綜述CDs在食品檢測中的應用,并提出未來CDs的發展趨勢。
碳量子點;光學性質;重金屬;抗生素;病原菌
2004年,Xu Xiaoyou等[1]通過電弧放電的方法合成了單壁碳納米管,在將其懸浮液進行分離純化時,發現了新型熒光納米材料碳量子點(carbon dots,CDs),進而引發一系列關于CDs熒光性質、合成方法和應用方面的研究。研究表明,CDs具有上轉換熒光特性、激發波長和發射波長的可調控性、較高的穩定性與抗光漂白性等優良性質[2-4]。相比于半導體量子點,CDs較低的毒性和較高的生物相容性,使其在生物成像和化學生物傳感等方面成為半導體量子點的有力競爭者,實際應用有望更為廣泛。近幾年,有關CDs的熒光性質與合成方法等方面的綜述較多[5],而鮮有關于CDs應用于食品檢測等方面的文獻總結。本文基于近年來關于CDs的最新研究,介紹了CDs的熒光性質與合成方法,重點綜述CDs在食品檢測中的應用。
1 光學性質
1.1 熒光產生機理
一般認為,納米顆粒的尺寸與其激子的波爾半徑相近時,電子-空穴對的運動被限制在小尺寸的勢阱中,進而分成準分立的類分子能級。而發光的過程則是電子-空穴對的復合過程,CDs的發光也就是這種電子-空穴對的復合發光。CDs尺寸越大,其發射波長越長[4],即量子尺寸效應。然而,最近Ding Hui等[6]合成了平均尺寸大小一致,但發射波長不同的CDs,他們認為這是CDs表面的氧化程度不一致導致的。研究表明,表面氧化產生的表面缺陷,可作為激子的俘獲中心,產生與表面缺陷態相關的熒光。氧化程度越大,π-電子系統的范圍越大,CDs表面態的能級降低就越多,故熒光發射峰的紅移程度越大[6-7],他們將這種發光機理表述為表面缺陷態熒光發射理論。這些機理可以各自解釋一部分熒光現象,而有些現象則需要幾種機理共同解釋[7-8]。更為準確地闡述,還需對CDs及其熒光性質做更為深入的研究。
1.2 上轉換熒光性質
上轉換熒光是一種熒光發射波長比激發波長短的反斯托克斯位移型的熒光發射現象[9]。通常,CDs與生物組織經紫外光照射均發藍色熒光,從而干擾了CDs在生物體內的熒光分析。而具有上轉換熒光特性的CDs能夠吸收近紅外區的可見光,發射出藍光。因不需要紫外光照射,降低了生物組織自發熒光的背景,提高了組織的穿透深度和信噪比,使得CDs在生物成像方面具備更多優勢[4]。相比摻有鑭系元素的稀土納米顆粒等傳統材料,CDs合成簡單,省略了復雜的修飾步驟,其上轉換性質應用將更為廣泛。
1.3 依賴于激發光的熒光性質
CDs普遍具有隨著激發波長不同而熒光最大發射波長變化的性質。Zheng Baozhan等[10]對以十六烷基氯化吡啶為底物合成的CDs的研究表明,當激發波長在400 nm以上時,熒光發射峰隨著激發波長增大而紅移。他們認為這種現象可能與CDs中芳香族的C=C鍵和來自于C—OH、C=O基團的表面缺陷有關。與此同時,利用檸檬酸銨和乙二胺合成的CDs也具有這種性質。實驗證明,其表面缺陷和較窄的大小分布可能與此現象相關[11]。這種熒光現象的發現,佐證了表面缺陷態有關的熒光產生機理。
1.4 依賴于pH值的熒光性質
研究表明,依賴于pH值的熒光性質與CDs表面功能基團的質子化與去質子化有關。CDs中存在石墨型和吡啶型氮原子,只有吡啶型氮才可接受質子。隨著pH值減小,CDs的吡啶型氮逐漸被質子化,電子可從質子化的氮轉移到與之相鄰的共軛結構的碳原子上,從而提高熒光強度[12]。Qian Zhaosheng等[12]研究表明,隨著pH值增大,熒光發射峰發生藍移,且熒光強度隨pH值而變化。當pH≤5 時,CDs熒光強度基本不變,他們認為可能是在pH 5時,CDs中氮位點的質子處于飽和狀態,導致多余的質子不能結合到氮原子上。進一步說明作為熒光發射活性位點的氮,對CDs的熒光有很大影響。同時,利用pH值與熒光強度間的關系,可以開發酸堿傳感器[13]。其中,Wang Chuanxi等[14]發現從pH 3~9的變化過程中,CDs的溶液顏色由淡黃色變為深黃色,且可以往復循環多次,熒光強度幾乎不變。
1.5 穩定性與抗光漂白性
較高的穩定性和抗光漂白性是CDs又一重要的光學特性。不管使用何種原材料還是采用不同方法合成的CDs,其熒光強度在6 個月[15]甚至1 年[16]內都能保持基本不變。同時,有關CDs的抗光漂白特性得到了多個課題組的驗證。如,Wang Chunfeng等[17]利用紫外光照射合成的CDs 3 h,其熒光強度保持不變;而有的課題組進一步延長照射時間至12 h,發現CDs的熒光強度為初始熒光強度的70%[18];甚至用紫外光照射CDs 24 h,其熒光強度還能保持基本不變[19]。
2 CDs的合成
CDs的合成方法可以歸為兩類:自上而下法和自下而上法,其中自上而下法是利用物理、化學方法將較大的碳結構破碎為納米尺寸的碳結構而產生CDs,如弧放電法、激光銷蝕法、電化學氧化法等。相比自上而下法,通過加熱、微波處理等方式,利用一些富含碳的分子前體合成CDs的自下而上法,步驟較簡單、成本較低、應用更為廣泛。基于此,下面將重點介紹自下而上合成法,其中包括水熱法、溶劑熱法、微波消解法和超聲振蕩法。
2.1 水熱法
水熱法是目前CDs合成與研究較為熱門的一種方法,它是直接加熱有機分子前體的水溶液而獲得CDs的方法。水熱法合成原材料來源廣泛且成本低廉,如氨基酸[15]、檸檬酸[9]、檸檬酸銨[4]、乙二胺[11]等化學物質都可作為合成CDs的前體物質。近年來,科研工作者更偏向于尋求自然可持續的有機生物原材料,如以黃瓜汁為原材料,加熱可合成含氮、硫、磷的CDs(圖1)[17]。另外,選用天然蠶絲[20]、土豆[21]、荔枝[22]、椰奶[23]、燕麥片[24]等原材料,也同樣獲得了高品質的CDs。然而,以上方法需要較高的溫度和較長的時間,量子產率一般在50%以下,故選取合適的原材料、低溫、短時間合成高量子產率CDs的方法將有更好的前景。如,Zheng Baozhan等[10]以氯化十六烷基吡啶和氫氧化鈉為原材料,在室溫條件下即可合成量子產率為16.7%的CDs。這些在室溫條件下的水熱法,再進一步優化量子產率后,有望廣泛應用于CDs的合成。
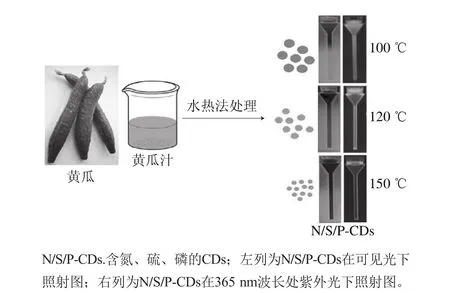
圖1 通過水熱法處理黃瓜汁合成N/S/P-CDs的示意圖[17]Fig. 1 Schematic illustration of the formation of N/S/P-CDs from hydrothermal treatment of cucumber juice[17]
2.2 溶劑熱法
溶劑熱法是在通過加熱含有機分子前體的有機溶劑而合成CDs的方法。如,Wu Hongyan等[25]以VC為碳源,乙二醇和蒸餾水為溶劑,加熱合成了發綠色熒光的CDs。Zhang Yanqing等[26]通過加熱CCl4和不同濃度的NaNH2,合成了可發射藍色、藍綠色、黃綠色和黃色熒光的CDs。同時,這種摻有氮且被氨基功能化的CDs的量子產率達到22%,高于被胺類化合物鈍化的CDs的量子產率。他們進一步研究表明,作為摻入到CDs中的雜原子,其含量的變化實質是改變了CDs表面缺陷發生的概率,這種現象符合表面缺陷效應的熒光產生機理。這種加熱有機溶劑來合成CDs的方法,操作相對簡單,由于有機溶劑的毒性,在應用方面不及水熱合成法。
2.3 微波消解法
微波消解法是利用微波消解含碳的前體分子而合成CDs的方法,因其操作簡單、合成時間短而受到科研工作者的青睞。比如以蔗糖為碳前體、磷酸為氧化劑,混合后于微波爐中100 W加熱3 min 40 s,可以合成發綠色熒光的CDs[27]。同樣也可在微波爐中750 W加熱丙三醇和磷酸鹽溶液14 min來合成CDs,且不需要額外的表面鈍化劑[28]。此外,Liu Changjun等[29]以4,7,10-三氧-1,13-十三烷二胺為鈍化劑,因在微波消解丙三醇的過程中完成了對CDs的表面鈍化,使CDs的量子產率從4.63%提高到了12.02% ,并證明了表面鈍化可改善CDs熒光性質。但這種方法的量子產率普遍不高,需要繼續優化合成原材料與合成條件。
2.4 超聲波振蕩法
超聲波振蕩法是通過提高溶液混合和反應的速率,促進原料聚合、碳化而形成CDs的一種方法。Ma Zheng等[30]于室溫條件下,超聲處理葡萄糖和氨水的混合液24 h,得到了摻有氮的CDs。這種方法合成的CDs,其發射光譜寬(從可見區擴展到近紅外區),同時還存在上轉換熒光現象。相比傳統的紫外-可見區的熒光性質,近紅外區的熒光有背景干擾少、在生物體組織中的穿透力更大等優勢,但該合成方法反應時間較長,量子產率較低。
總體而言,這些自下而上的合成方法各有優缺點。尋找綠色、廉價的原材料,使CDs表面容易鈍化、功能化,且易于摻入雜原子來改善CDs光學性質的快速、綠色合成方法一直為科研工作者們所熱衷。在諸多考慮因素中,尋找綠色的原材料和CDs表面易鈍化的特點尤為重要。因在合成過程中,綠色原材料的碳化可完成對CDs表面的鈍化,不僅可以提高CDs的量子產率,還能在其表面引入羧基、羥基等功能基團,從而提高其水溶性。同時原材料中存在的雜元素可在合成過程中摻入到CDs,進一步改善熒光性質,擴展其應用領域[22,31]。
3 食品檢測中的應用
獨特的光學、理化性質,使納米材料受到越來越多研究者的關注,其中基于納米材料的化學生物傳感器尤為簡單、靈敏、快速。近年來,半導體量子點以其高量子產率和優異的熒光發射性質,在光學傳感方面具有很強的競爭力[32-34]。但半導體量子點具有的生物毒性限制了其在多領域的應用。而CDs制備更簡單、成本更低,特別是較好的生物相容性、穩定性與抗光漂白性使其應用更廣泛。下面將簡述CDs在重金屬離子、抗生素、病原菌、農藥殘留與違禁添加劑、食品中營養與功能成分及其他生物分子等方面的檢測應用,旨在為科研工作者開展食品檢測的相關工作提拱思路。
3.1 重金屬離子檢測
傳統檢測重金屬離子的方法包括絡合滴定法、化學發光法、原子光譜法等,但這些方法靈敏度不高、操作復雜、成本較高。近年來,基于CDs開發的化學傳感器已廣泛應用于多種重金屬離子的高靈敏、快速檢測。
考查重金屬離子對CDs熒光強度的影響,進而制定利用CDs高靈敏檢測重金屬離子的策略,是檢測重金屬離子較為普遍的一種方法。目前,利用這種策略已實現了對Hg2+、Fe3+、Cu2+等離子的檢測。Zhou Li等[35]研究表明,Hg2+與羧酸鹽或羥基基團相互作用使得CDs之間相互靠近,通過電子轉移途徑促進激子的無輻射再結合,導致CDs熒光強度降低。而加入的生物巰基化合物與CDs表面的Hg2+的結合力更大,導致Hg2+與CDs分離,CDs熒光恢復(圖2)。基于Hg2+對CDs的熒光猝滅效應,他們對Hg2+實現了線性范圍為0.0~3.0 μmol/L、檢出限為4.2 nmol/L的高靈敏檢測,并根據熒光恢復的熒光強度與生物巰基化合物(半胱氨酸、同型半胱氨酸和谷胱甘肽)濃度間的線性關系,實現了對生物巰基化合物(半胱氨酸、同型半胱氨酸和谷胱甘肽)的檢測,其檢測限分別為4.9、6.1、8.5 nmol/L。目前諸多課題組已開展了與檢測Hg2+相關的工作,主要在降低檢測限與拓寬線性范圍兩方面[11,17,23]。
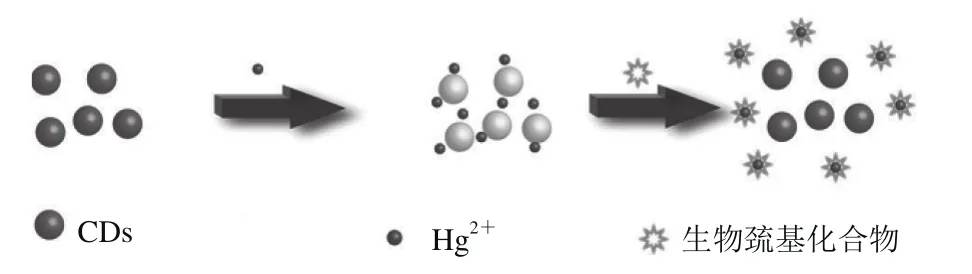
圖2 利用CDs檢測Hg2+與生物巰基化合物的原理示意圖[35]Fig. 2 Schematic illustration of the detection of Hg2+and biothiols using CDs[35]
Fe3+對CDs的猝滅作用體現在Fe3+與CDs可以形成穩定的化合物,即Fe3+與CDs表面的酚羥基相互作用,進而發生無輻射電子轉移或能量轉移[3,21,36]。根據此原理,Wen Xiangping等[37]通過不斷提高Fe3+的濃度,使混合液中CDs熒光強度逐漸下降,實現了高靈敏檢測Fe3+。其線性范圍為50 nmol/L~10 μmol/L、檢出限為27 nmol/L。而Qian Zhaosheng等[12]發現Fe2+對CDs的熒光強度影響不大,但在檢測體系中加入過氧化氫,將Fe2+轉化為Fe3+,則可使CDs熒光強度下降,進而開發出檢測過氧化氫的方法。值得注意的是,他們基于Ag+對氮原子有親和力,使CDs帶正電,且不同CDs之間的動態碰撞導致正電子數目減少,還首次發現了Ag+對熒光強度有增強作用,其檢測Ag+的線性范圍為1.00~100.00 μmol/L。
此外,由于Cu2+能與CDs的氮、氧原子結合,而使不同CDs相互靠近,通過電子或能量轉移導致CDs熒光猝滅,不同課題組均實現了靈敏檢測Cu2+[38-39]。其中Liu Sen等[40]對Cu2+實現了線性范圍為0~50 nmol/L、檢測限為1 nmol/L的高靈敏檢測,且在實際水樣中的檢出限均遠遠低于美國環境保護局的檢出限(20 μmol/L)。
綜合檢測不同重金屬離子的多種CDs,不難發現不同原材料合成的CDs對檢測的離子類型、檢測線性范圍與檢測限都有所不同,這可能是不同原材料合成的CDs的表面功能基團不同所致。對于不同CDs和不同重金屬離子的關聯性,以及如何影響熒光強度的原理,還需要系統深入地研究。同時不難發現,CDs對檢測一些重金屬離子的選擇性不高,共存離子對檢測的干擾較大,因此,未來仍需進一步改善其響應的特異性。
3.2 抗生素的檢測
近年來,抗生素在養殖行業的濫用,導致了其在動物源性食品中的高殘留,對人類的健康產生很大威脅。由于傳統的檢測方法不能滿足食品中抗生素分析的要求,許多科研工作者基于CDs的熒光性質對多種抗生素的高靈敏、快速檢測進行了廣泛地探索,研究較多的有四環素及其衍生物、氨芐青霉素、鹽酸土霉素。
Yang Xiaoming等[41]根據加入不同濃度的四環素對CDs熒光的不同猝滅效果,實現了高靈敏檢測四環素,相應的檢出限為7.5 nmol/L。同時對氧四環素、氯四環素和脫氧四環素也進行了定量分析,檢出限分別為6.9、4.2、4.8 nmol/L。隨后,類似的研究實現了對另一種四環素衍生物——多四環素的檢測,其線性檢測范圍為0.080~60.000 μmol/L、檢出限為20 nmol/L[39]。相比其他方法,這種熒光分析方法的線性檢測范圍更寬、檢出限更低和檢測更靈敏。
根據特殊的合成原材料,可實現對CDs合成原材料本身的靈敏檢測。Mishra等[42]利用葡萄糖和不同量的氨芐青霉素合成了熒光性質不同的CDs,發現CDs在340 nm波長處的吸收值與氨芐青霉素的含量(18.9~572.0 μmol/L)存在線性關系,其檢出限為16.5 μmol/L。同時,CDs的熒光強度也隨氨芐青霉素的含量(0.0~190.0 μmol/L)呈線性變化,因此,也可以用于檢測氨芐青霉素。
另外,利用Fe3+猝滅CDs熒光的機理及競爭絡合作用,根據加入鹽酸土霉素的量與CDs熒光恢復的關系,可實現高靈敏檢測鹽酸土霉素,其線性范圍為0.10~2.70 μmol/L、檢出限為22.8 nmol/L,且在牛乳樣品中的回收率為92.5%~103.0%[43]。
3.3 病原菌的檢測
由于沙門氏菌、金黃色葡萄球菌、大腸桿菌等病原菌易通過飲食途徑而感染人體,引發疾病,病原菌的檢測和定量技術在食品相關領域變得越來越重要。檢測病原菌的傳統方法由于耗時、步驟繁多等因素越來越不能滿足對快速靈敏的檢測要求。基于CDs的熒光分析法尤以靈敏度高、選擇性高、操作簡單、檢測快速等而成為諸多科研工作者研究的熱點。
Wang Renjie等[44]基于CDs的較高生物相容性與穩定性,通過設計的生物傳感器可實現快速靈敏檢測鼠傷寒沙門氏菌。他們以表面帶有羧基的CDs與連有氨基的適配體為熒光探針,通過適配體與細菌膜蛋白的特異性結合,使熒光探針與細菌相連。根據細菌上可識別位點,在優化熒光探針的最佳體積和最佳細菌培養時間后,可得到不同濃度CDs標記的鼠傷寒沙門氏菌與總體熒光強度之間的線性關系,進而開發出檢出限為50 CFU/mL的熒光分析法。
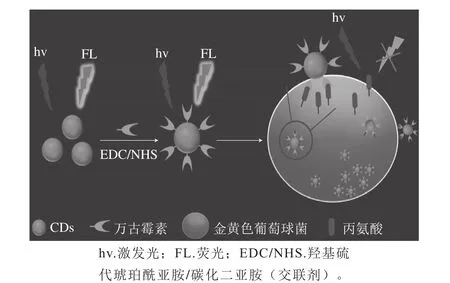
圖3 利用CDs檢測金黃色葡萄球菌的方法示意圖[45]Fig. 3 Schematic illustration of the detection of Staphylococcus aureus by using CDs[45]
針對牛乳、肉制品等在不清潔環境中易滋生金黃色葡萄球菌,Zhong Dan等[45]利用萬古霉素和細胞壁間存在配體-受體相互作用、萬古霉素修飾的CDs與革蘭氏陽性菌有較強親和力,通過萬古霉素修飾的CDs在細菌表面團聚,導致CDs熒光強度降低的方法提高了檢測金黃色葡萄球菌的靈敏度(圖3)。他們發現,隨著金黃色葡萄球菌濃度不斷增大,在3.18×105~1.59×108CFU/mL范圍內,CDs的熒光強度逐漸降低,其檢出限為9.40×104CFU/mL,并在橘汁中成功實踐。該方法也適用于枯草芽孢桿菌(檢出限為1.03×105CFU/mL)和單核細胞增多性李斯特氏菌(檢出限為9.84×104CFU/mL)等其他革蘭氏陽性菌的檢測。與此同時,Bhaisare等[46]成功合成出氨基修飾的磁性CDs(magnetic carbon dots,Mag-CDs),利用其熒光特性與磁性分離效應,并基于隨金黃色葡萄球菌數量增加,CDs熒光強度增大的現象,實現了對金黃色葡萄球菌的檢測,檢出限低至3×102CFU/mL。此外,他們利用Mag-CDs表面的氨基可吸附表面帶負電的大腸桿菌的特點,實現了對大腸桿菌的靈敏檢測,其檢出限為3.5×102CFU/mL。
值得注意的是,Lai等[47]借助甘露糖,將飲用水、蘋果汁、人體尿液等實際樣品的大腸桿菌檢出限降至1×102CFU/mL。他們利用甘露糖與大腸桿菌菌毛上的蛋白質的多價結合,可使被甘露糖修飾的CDs特異性標記大腸桿菌,在一定范圍內,大腸桿菌濃度和CDs熒光強度的呈線性變化,進而成功應用于樣品檢測。
3.4 農藥殘留及違禁添加物的檢測
當前,有機磷農藥廣泛應用于現代農業,殘留于食品中的有機磷農藥可對人體和環境造成潛在的危害。而傳統色譜分析方法對有機磷農藥的分析存在一定的局限性,不同課題組熱衷于開發以CDs為熒光探針檢測有機磷農藥的新型熒光分析法。
Hou Juying等[48]基于CDs熒光猝滅、恢復與再猝滅的特性,對有機磷農藥敵敵畏實現了靈敏檢測,其檢出限達到了3.8 nmol/L。實驗中,首先利用Cu2+猝滅CDs熒光,而乙酰膽堿酯酶(acetyl cholinesterase,AChE)催化氯代乙酰硫代膽堿(acetylthiocholine chloride,ATChCl)生成硫代膽堿(thiocholine,TCh),TCh可與Cu2+反應使CDs熒光恢復。加入敵敵畏可抑制乙酰膽堿酯酶的活性,從而再猝滅CDs熒光(圖4)。根據抑制速率與敵敵畏的濃度對數在6.0~60.0 nmol/L范圍內呈線性關系,該方法成功應用于白菜和果汁樣品的檢測。同時該方法也成功應用于馬拉硫磷(檢出限為3.4 nmol/L)和乙硫磷 (檢出限為4.2 nmol/L)的檢測。Hou Juying等[49]還利用AChE可催化硫代乙酰膽堿生成TCh,TCh與5,5-二硫雙(2-硝基苯甲酸)生成5-硫-2-氮苯甲酸(5-thio-2-nitrobenzoic acid,TNB);TNB(受體)可與CDs(供體)構成熒光共振能量轉移系統,使CDs熒光猝滅;加入有機磷化合物抑制AChE的活性,進而恢復CDs的熒光。依據抑制速率與敵敵畏的濃度對數呈線性關系,得到了線性范圍為0.050 0~100.000 0 nmol/L、檢出限為0.019 nmol/L的檢測效果。該方法同樣適用于馬拉硫磷和對氧磷的高靈敏檢測,其檢出限分別為0.048 nmol/L和0.003 5 nmol/L。該檢測系統具有抗干擾能力、高穩定性與高選擇性。
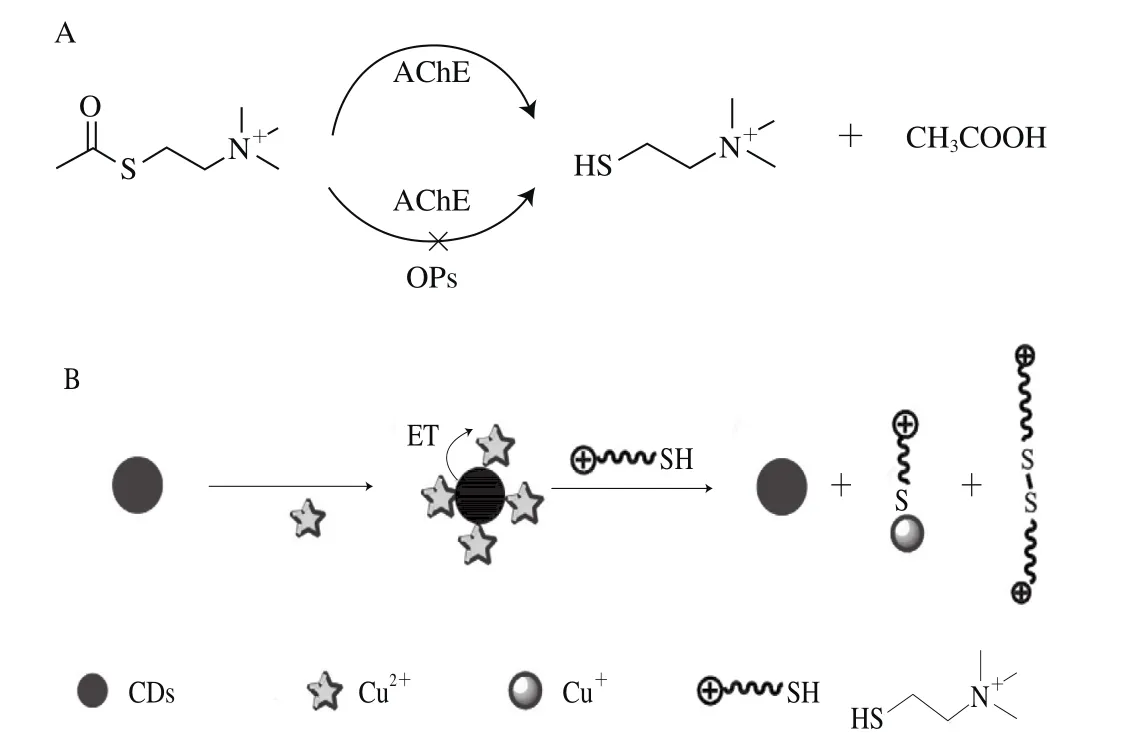
圖4 檢測有機磷農藥的傳感器示意圖[48]Fig. 4 Schematic illustration of the working principle of organophosphorus pesticides (Ops) sensor[48]
除敵敵畏之外,Hou Juying等[50]通過酪氨酸甲酯功能化的CDs對另外一種有機磷殺蟲劑——甲基對硫磷,進行了靈敏檢測。實驗利用酪氨酸酶催化CDs表面的酪氨酸甲酯產生的醌產物(一種電子的受體)可猝滅CDs熒光,再加入有機磷農藥,來抑制酪氨酸酶的活性和減輕熒光猝滅的方法,得到抑制率與甲基對硫磷的對數濃度(1.0×10-10~1.0×10-4mol/L)間的線性關系,樣品中的檢出限為4.8×10-11mol/L,也成功實踐于白菜、牛奶和果汁樣品。
除草劑也是一類重要的農藥殘留物。Tao Huilin等[51]以CDs為供體、碲化鎘量子點為受體構成的熒光共振能量轉移系統,實現了高靈敏檢測除草劑綠麥隆。由于能量從CDs轉移到CdTe,CdTe熒光強度增大。而后加入的綠麥隆與CdTe通過形成綠麥隆-CdTe基態物質,導致CdTe熒光猝滅,而CDs的熒光基本保持不變。他們以熒光猝滅的程度來衡量綠麥隆的殘留量,得出線性范圍為2.4×10-10~8.5×10-8mol/L,檢出限為7.8×10-11mol/L。相比高效液相色譜法等方法,該方法檢出限低、靈敏度高,且在灌溉用水的應用實驗中有較高的回收率(98.50%~102.50%)。
作為違禁添加到日常食品和動物飼料來提高含氮量的三聚氰胺,可造成腎結石等危害。Lei Cuihua等[52]基于CDs、三聚氰胺兩種物質與汞離子的競爭作用,實現了高靈敏檢測三聚氰胺。當汞離子猝滅CDs熒光后,加入的三聚氰胺可通過多氮雜環與汞離子結合,減弱汞離子與CDs間的作用,而使CDs熒光逐步恢復。該方法的檢出限(0.300 μmol/L)遠低于美國食品藥品管理局的標準(20.0 μmol/L)。此外,也可通過以CDs為供體,金納米顆粒(gold nanoparticle,AuNPs)為受體組成的能量轉移系統來檢測三聚氰胺[53]。當熒光被AuNPs猝滅后,加入的三聚氰胺憑借氨基鍵合到AuNPs表面,從而防止CDs與AuNPs作用,使熒光強度增大。根據熒光強度恢復程度與三聚氰胺濃度(50.0~500.0 nmol/L)間的線性關系,可將檢出限降至36.0 nmol/L。加之分析快速、成本低、靈敏度高、選擇性高,可廣泛應用于牛乳制品中三聚氰胺的超靈敏檢測[53]。
3.5 食品中營養與功能成分的檢測
3.5.1 葡萄糖的檢測
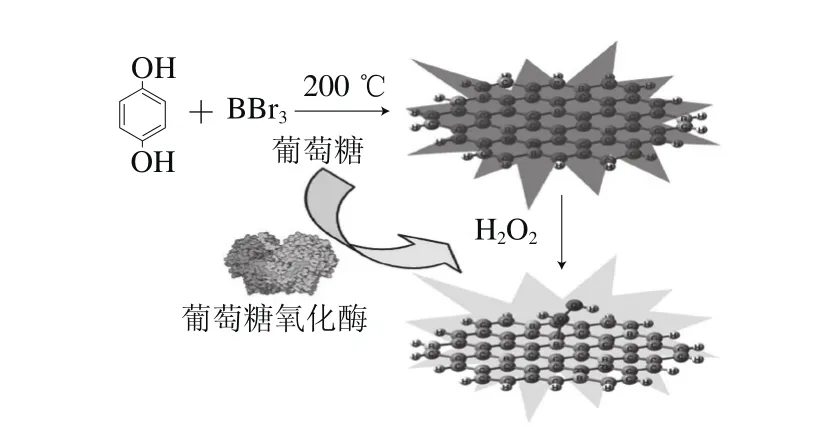
圖5 含硼的CDs合成示意圖和基于CDs、過氧化氫的葡萄糖檢測機理[54]Fig. 5 Schematic representation of the synthesis of B-doped CDs and the glucose-sensing mechanisms based on B-doped CDs and H2O2[54]
Shan Xiaoyue等[54]發現含硼CDs的熒光可被過氧化氫猝滅,為此,他們基于葡萄糖氧化酶可催化葡萄糖產生葡萄糖酸和過氧化氫,實現了快速高靈敏檢測葡萄糖。當葡萄糖氧化酶和葡萄糖同時存在時,CDs熒光的猝滅程度與葡萄糖濃度線性相關,其線性范圍為8.00~80.00 μmol/L、檢出限為8.00 μmol/L(圖5)。
3.5.2 檸檬黃的檢測
在研究食品中一些成分對CDs熒光的影響時,有科研工作者根據檸檬黃能猝滅CDs的熒光,實現了對檸檬黃高靈敏的檢測,其線性范圍為0.250~32.500 μmol/L、檢出限為73.0 nmol/L[55]。值得注意的是,該方法在饅頭、蜂蜜、冰糖3 種食品中有較好的回收率(24 h內為88.60%~103.40%、48 h內為87.30%~106.60%),表明該方法可廣泛應用于食品中檸檬黃的檢測。
3.5.3 VB12、VB2、VB9的檢測
基于VB12的紫外吸收光譜和CDs的熒光光譜存在明顯的光譜重疊,Wang Jilong等[56]設計了以CDs為供體,VB12為受體的熒光共振能量轉移體系,當向體系中加入VB12的質量濃度不斷增大時,CDs的熒光強度不斷降低。根據CDs熒光強度與VB12質量濃度間存在的線性關系,實現了VB12的高靈敏檢測。實驗中,相對于甘氨酸、酪氨酸、三聚氰胺,CDs對VB12有很好的選擇性,同時檢出限低至0.1μg/mL。此外,還可對VB2、VB9實現檢出限均為1.2 nmol/L的高靈敏檢測[57-58]。
3.5.4 植酸的檢測
植酸是植物組織(谷類食品、水果和蔬菜等)中磷的主要存在形式。為了給飲食攝入量和新陳代謝提供更有價值的信息,Gao Zhao等[59]利用Fe3+可猝滅CDs熒光,而植酸與Fe3+有更強親和力的原理,實現了高靈敏檢測植酸。具體而言,當CDs熒光被Fe3+猝滅后,加入的植酸可與Fe3+形成復合物,減輕Fe3+對CDs熒光的猝滅效應,使得熒光逐漸恢復。這種分析方法操作簡單、成本低、靈敏高(線性范圍為0.68~18.69 μmol/L、檢出限為0.36 μmol/L),同時在標樣和實際樣品中具有高選擇性、穩定性和回收比例。
3.6 其他生物分子的檢測
除了在重金屬離子、抗生素、病原菌、農藥殘留與違禁添加劑、食品中營養與功能成分的檢測中發揮了重要的作用外,CDs還可用于檢測透明質酸[60]、DNA[61]、凝血酶[62]與ATP[63]等其他生物分子。
Liu Siyu等[60]根據CDs的熒光發射光譜和透明質酸鹽-AuNPs的吸收光譜大部分重疊,使帶正電的氨基功能化的CDs和帶負電的透明質酸鹽-AuNPs形成了表面能量轉移系統,并以此來定量檢測在生理學過程中重要的透明質酸酶。當透明質酸鹽-AuNPs猝滅CDs熒光后,加入透明質酸酶,因其能降解透明質酸鹽成小分子,導致AuNPs團聚,并從表面能量轉移系統脫離,從而使CDs熒光恢復。其線性檢測范圍為0.1~80.0 U/mL、檢出限為0.068 U/mL。同樣利用熒光共振能量轉移、CDs熒光先猝滅后恢復的原理及DNA堿基互補配對的原理,可廣泛應用于食品安全、遺傳識別中的DNA檢測,該方法更加快速靈敏,線性范圍可增至0.04~400.00 nmol/L、檢出限可低至17.4 nmol/L[61]。
而尺寸較大的碳納米顆粒表現出很強的熒光猝滅作用,故可將其用于以能量轉移為基礎的生物傳感中。如Liu Jinhua等[62]利用碳納米顆粒吸附標有熒光素的凝血酶適配體,從而猝滅熒光素的熒光,當加入凝血酶后,適配體與凝血酶形成的混合物脫離碳納米顆粒表面,使熒光恢復。基于凝血酶的濃度與熒光恢復的程度,開發了檢測凝血酶的生物傳感方法。同時利用類似的方法也可靈敏快速檢測ATP[63]。
4 結 語
自2004年首次合成CDs以來,多個課題組就合成方法及其應用開展了大量探索工作。相對于自上而下法,利用自下而上法合成CDs的方法由于成本低廉、操作簡單、熒光性質多樣化,尤其能選用廉價綠色原材料而倍受青睞。未來的CDs的合成方法將朝著利用廉價綠色原材料,一步完成表面鈍化和功能化,快速合成的自下而上法方向發展,以期進一步提高CDs量子產率、抗光漂白性及生物相容性。
然而,目前通過不同方法、利用不同原材料合成CDs,致使CDs的組成、結構及表面鈍化程度不一致,進而導致其光學理化性質各異,對酸堿度、重金屬離子、生物分子等響應的敏感度也不盡相同。復雜的食品基質,進一步了增加CDs在食品檢測中的難度,這也正是現今利用CDs分析食品樣品的最大阻力。未來基于CDs開發食品中有毒有害物質及營養成分的分析方法時,將著重研究如何提高生物傳感方面的響應特異性。
[1] XU Xiaoyou, RAY R, GU Yunlong, et al. Electrophoretic analysis and purification of fluorescent single-walled carbon nanotude fragments[J]. Journal of the American Chemical Society, 2004, 126(40): 12736-12737. DOI:10.1021/ja040082h.
[2] SUN Dong, BAN Rui, ZHANG Penghui, et al. Hair fiber as a precursor for synthesizing of sulfur- and nitrogen-co-doped carbon dots with tunable luminescence properties[J]. Carbon, 2013, 64: 424-434. DOI:10.1016/j.carbon.2013.07.095 .
[3] ZHU Shoujun, MENG Qingnan, WANG Lei, et al. Highly photoluminescent carbon dots for multicolor patterning, sensors, and bioimaging[J]. Angewandte Chemie International Edition, 2013, 52(14): 3953-3957. DOI:10.1002/anie.201300519.
[4] CUI Yanyan, HU Zhongbo, ZHANG Chunfang, et al. Simultaneously enhancing up-conversion fluorescence and red-shifting downconversion luminescence of carbon dots by a simple hydrothermal process[J]. Journal of Materials Chemistry B, 2014, 2(40): 6947-6952. DOI:10.1039/c4tb01085j.
[5] LIM Shiying, SHEN Wei, GAO Zhiqiang. Carbon quantum dots and their applications[J]. Chemical Society Reviews, 2015, 44(1): 362-381. DOI:10.1039/c4cs00269e.
[6] DING Hui, YU Shangbo, WEI Jishi, et al. Full-color lightemitting carbon dots with a surface-state-controlled luminescence mechanism[J]. American Chemical Society Nano, 2016, 10(1): 484-491. DOI:10.1021/acsnano.5b05406.
[7] BAO Lei, LIU Cui, ZHANG Zhiling, et al. Photoluminescencetunable carbon nanodots: surface-state energy-gap tuning[J]. Advanced Materials, 2015, 27(10): 1663-1667. DOI:10.1002/adma.201405070.
[8] BAO Lei, ZHANG Zhiling, TIAN Zhiquan, et al. Electrochemical tuning of luminescent carbon nanodots: from preparation to luminescence mechanism[J]. Advanced Materials, 2011, 23(48): 5801-5806. DOI:10.1002/adma.201102866.
[9] ZHANG Yue, HE Junhui. Facile synthesis of S, N co-doped carbon dots and investigation of their photoluminescence properties[J]. Physical Chemistry Chemical Physics, 2015, 17(31): 20154-20159. DOI:10.1039/c5cp03498a.
[10] ZHENG Baozhan, LIU Tao, PAAU M C, et al. One pot selective synthesis of water and organic soluble carbon dots with green fl uorescent emission[J]. American Chemical Society Advances, 2015, 5(15): 11667-11675. DOI:10.1039/C4RA16529B.
[11] LI Zi, YU Huijun, BIAN Tong, et al. Highly luminescent nitrogendoped carbon quantum dots as effective fluorescent probes for mercuric and iodide ions[J]. Journal of Materials Chemistry C, 2015, 3(9): 1922-1928. DOI:10.1039/c4tc02756f.
[12] QIAN Zhaosheng, MA Juanjuan, SHAN Xiaoyue, et al. Highly luminescent N-doped carbon quantum dots as an effective multifunctional fluorescence sensing platform[J]. Chemistry, 2014, 20(8): 2254-2263. DOI:10.1002/chem.201304374.
[13] JIN Xiaozhe, SUN Xiaobo, CHEN Guo, et al. pH-sensitive carbon dots for the visualization of regulation of intracellular pH inside living pathogenic fungal cells[J]. Carbon, 2015, 81: 388-395. DOI:10.1016/ j.Carbon.2014.09.071.
[14] WANG Chuanxi, XU Zhenzhu, CHENG Hao, et al. A hydrothermal route to water-stable luminescent carbon dots as nanosensors for pH and temperature[J]. Carbon, 2015, 82: 87-95. DOI:10.1016/ j.carbon.2014.10.035.
[15] ZENG Yawen, MA Dekun, WANG Wei, et al. N,S co-doped carbon dots with orange luminescence synthesized through polymerization and carbonization reaction of amino acids[J]. Applied Surface Science, 2015, 342: 136-143. DOI:10.1016/j.apsusc.2015.03.029.
[16] PEI Supeng, ZHANG Jing, GAO Mengping, et al. A facile hydrothermal approach towards photoluminescent carbon dots from amino acids[J]. Journal of Colloid and Interface Science, 2015, 439: 129-133. DOI:10.1016/j.jcis.2014.10.030.
[17] WANG Chunfeng, SUN Dong, ZHUO Kelei, et al. Simple and green synthesis of nitrogen-, sulfur-, and phosphorus-co-doped carbon dots with tunable luminescence properties and sensing application[J]. RSC Advances, 2014, 4(96): 54060-54065. DOI:10.1039/c4ra10885j.
[18] WANG Baogang, TANG Weiwei, LU Hongsheng, et al. Hydrothermal synthesis of ionic liquid-capped carbon quantum dots with high thermal stability and anion responsiveness[J]. Journal of Materials Science, 2015, 50(16): 5411-5418. DOI:10.1007/s10853-015-9085-y.
[19] ZHUO Yan, MIAO Hong, ZHONG Dan, et al. One-step synthesis of high quantum-yield and excitation-independent emission carbon dots for cell imaging[J]. Materials Letters, 2015, 139: 197-200. DOI:10.1016/j.matlet.2014.10.048.
[20] WU Zhulian, ZHANG Pu, GAO Mingxuan, et al. One-pot hydrothermal synthesis of highly luminescent nitrogen-doped amphoteric carbon dots for bioimaging from Bombyx mori silk-natural proteins[J]. Journal of Materials Chemistry B, 2013, 1(22): 2868-2873. DOI:10.1039/c3tb20418a.
[21] XU Jingyi, ZHOU Ying, CHENG Guifang, et al. Carbon dots as a luminescence sensor for ultrasensitive detection of phosphate and their bioimaging properties[J]. Luminescence, 2015, 30(4): 411-415. DOI:10.1002/bio.2752.
[22] CHAUDHARY V, BHOWMICK A K. Green synthesis of fl uorescent carbon nanoparticles from lychee (Litchi chinensis) plant[J]. Korean Journal of Chemical Engineering, 2015, 32(8): 1707-1711. DOI:10.1007/s11814-014-0381-z.
[23] ROSHNI V, OTTOOR D. Synthesis of carbon nanoparticles using one step green approach and their application as mercuric ion sensor[J]. Journal of Luminescence, 2015, 161: 117-122. DOI:10.1016/ j.jlumin.2014.12.048.
[24] YU Caiyan, XUAN Tongtong, CHEN Yiwei, et al. A facile, green synthesis of highly fl uorescent carbon nanoparticles from oatmeal for cell imaging[J]. Journal of Materials Chemistry C, 2015, 3(37): 9514-9518. DOI:10.1039/c5tc02057c.
[25] WU Hongyan, MI Congcong, HUANG Huaiqing, et al. Solvothermal synthesis of green-fluorescent carbon nanoparticles and their application[J]. Journal of Luminescence, 2012, 132(6): 1603-1607. DOI:10.1016/j.jlumin.2011.12.077.
[26] ZHANG Yanqing, MA Dekun, ZHANG Yan, et al. One-pot synthesis of N-doped carbon dots with tunable luminescence properties[J]. Journal of Materials Chemistry, 2012, 22(33): 16714-16718. DOI:10.1039/c2jm32973e.
[27] CHANDRA S, DAS P, BAG S, et al. Synthesis, functionalization and bioimaging applications of highly fl uorescent carbon nanoparticles[J]. Nanoscale, 2011, 3(4): 1533-1540. DOI:10.1039/c0nr00735h.
[28] WANG Xiaohui, QU Konggang, XU Bailu, et al. Microwave assisted one-step green synthesis of cell-permeable multicolor photoluminescent carbon dots without surface passivation reagents[J]. Journal of Materials Chemistry, 2011, 21(8): 2445-2450. DOI:10.1039/ c0jm02963g.
[29] LIU Changjun, ZHANG Peng, TIAN Feng, et al. One-step synthesis of surface passivated carbon nanodots by microwave assisted pyrolysis for enhanced multicolor photoluminescence and bioimaging[J]. Journal of Materials Chemistry, 2011, 21(35): 13163-13167. DOI:10.1039/ c1jm12744f.
[30] MA Zheng, MING Hai, HUANG Hui, et al. One-step ultrasonic synthesis of fluorescent N-doped carbon dots from glucose and their visible-light sensitive photocatalytic ability[J]. New Journal of Chemistry, 2012, 36(4): 861-864. DOI:10.1039/c2nj20942j.
[31] FENG Ji, WANG Wenjing, HAI Xin, et al. Green preparation of nitrogen-doped carbon dots derived from silkworm chrysalis for cell imaging[J]. Journal of Materials Chemistry B, 2016, 4(3): 387-393. DOI:10.1039/C5TB01999K.
[32] 文學方, 楊安樹, 陳紅兵. 量子點標記技術在食品安全檢測中的應用[J]. 食品科學, 2009, 30(21): 399-402. DOI:1002-6630(2009)21-0399-04.
[33] 馬良, 賀亞萍, 張宇昊. 量子點熒光分析法在食品污染物分析中的應用[J].食品科學, 2013, 34(21): 389-393. DOI:10026630(2013)21-0389-05.
[34] 雷鵬, 何燦霞, 劉曉東, 等. 硒化鎘量子點的安全性及在食品領域的應用[J]. 食品科學, 2015, 36(11): 240-244. DOI:1002-6630(2015)11-0240-05.
[35] ZHOU Li, LIN Youhui, HUANG Zhenzhen, et al. Carbon nanodots as fl uorescence probes for rapid, sensitive, and label-free detection of Hg2+and biothiols in complex matrices[J]. Chemical Communications, 2012, 48(8): 1147-1149. DOI:10.1039/c2cc16791c.
[36] ZHOU Jin, WANG Chen, QIAN Zhaosheng, et al. Highly efficient fluorescent multi-walled carbon nanotubes functionalized with diamines and amides[J]. Journal of Materials Chemistry, 2012, 22(24): 11912-11914. DOI:10.1039/c2jm31192e.
[37] WEN Xiangping, SHI Lihong, WEN Guangming, et al. Green synthesis of carbon nanodots from cotton for multicolor imaging, patterning, and sensing[J]. Sensors and Actuators B: Chemical, 2015, 221: 769-776. DOI:10.1016/j.snb.2015.07.019.
[38] SHI Lihong, LI Yanyan, LI Xiaofeng, et al. Controllable synthesis of green and blue fl uorescent carbon nanodots for pH and Cu(2+) sensing in living cells[J]. Biosensors and Bioelectronics, 2016, 77: 598-602. DOI:10.1016/j.bios.2015.10.031.
[39] WANG Yue, WU Wenting, WU Mingbo, et al. Yellow-visual fluorescent carbon quantum dots from petroleum coke for the efficient detection of Cu2+ions[J]. New Carbon Materials, 2015, 30(6): 550-559. DOI:10.1016/s1872-5805(15)60204-9.
[40] LIU Sen, TIAN Jingqi, WANG Lei, et al. Hydrothermal treatment of grass: a low-cost, green route to nitrogen-doped, carbon-rich, photoluminescent polymer nanodots as an effective fl uorescent sensing platform for label-free detection of Cu(II) ions[J]. Advanced Materials, 2012, 24(15): 2037-2041. DOI:10.1002/adma.201200164.
[41] YANG Xiaoming, LUO Yawen, ZHU Shanshan, et al. One-pot synthesis of high fluorescent carbon nanoparticles and their applications as probes for detection of tetracyclines[J]. Biosensors and Bioelectronics, 2014, 56: 6-11. DOI:10.1016/j.bios.2013.12.064.
[42] MISHRA R K, PULIDINDI I N, KABHA E, et al. In situ formation of carbon dots aids ampicillin sensing[J]. Analytical Methods, 2016, 8(11): 2441-2447. DOI:10.1039/c6ay00413j.
[43] AN Xuting, ZHUO Shujuan, ZHANG Ping, et al. Carbon dots based turn-on fluorescent probes for oxytetracycline hydrochloride sensing[J]. RSC Advances, 2015, 5(26): 19853-19858. DOI:10.1039/ c4ra16456c.
[44] WANG Renjie, XU Yi, ZHANG,Tao, et al. Rapid and sensitive detection of Salmonella typhimurium using aptamer conjugated carbon dots as fluorescence probe[J]. Analytical Methods, 2015, 7(5): 1701-1706. DOI:10.1039/C4AY02880E.
[45] ZHONG Dan, ZHUO Yan, FENG Yuanjiao, et al. Employing carbon dots modif i ed with vancomycin for assaying Gram-positive bacteria like Staphylococcus aureus[J]. Biosensors and Bioelectronics, 2015, 74: 546-553. DOI:10.1016/j.bios.2015.07.015.
[46] BHAISARE M L, GEDDA G, KHAN M S. Fluorimetric detection of pathogenic bacteria using magnetic carbon dots[J]. Analytica Chimica Acta, 2016, 920: 63-71. DOI:10.1016/j.aca.2016.02.025.
[47] LAI I P J, HARROUN S G, CHEN S Y, et al. Solid-state synthesis of self-functional carbon quantum dots for detection of bacteria and tumor cells[J]. Sensors and Actuators B: Chemical, 2016, 228: 465-470. DOI:10.1016/j.snb.2016.01.062.
[48] HOU Juying, DONG Guangjuan, TIAN Zhengbin, et al. A sensitive fluorescent for selective determination of dichlorvos based on the recovered fluorescence of carbon dots-Cu(II) system[J]. Food Chemistry, 2016, 202: 81-87. DOI:10.1016/ j.foodchem.2015.11.134.
[49] HOU Juying, TIAN Zhengbin, XIE Huizhi, et al. A fluorescence resonance energy transfer sensor based on quaternized carbon dots and Ellman’s test for ultrasensitive detection of dichlorvos[J]. Sensors and Actuators B: Chemical, 2016, 232: 477-483. DOI:10.1016/ j.snb.2016.03.092.
[50] HOU Juying, DONG Jing, ZHU Haishuang, et al. A simple and sensitive fl uorescent sensor for methyl parathion based on L-tyrosine methyl ester functionalized carbon dots[J]. Biosensors and Biolectronics, 2015, 68: 20-26. DOI:10.1016/j.bios.2014.12.037.
[51] TAO Huilin, LIAO Xiufen, SUN Chao, et al. A carbon dots-CdTE quantum dots fluorescence resonance energy transfer system for the analysis of ultra-trace chlotoluron in water[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2015, 136: 1328-1334. DOI:10.1016/j.saa.2014.10.020.
[52] LEI Cuihua, ZHAO Xianen, JIAO Shulin, et al. A turn-on fl uorescent sensor for the detection of melamine based on the anti-quenching ability of Hg2+to carbon nanodots[J]. Analytical Methods, 2016, 8(22): 4438-4444. DOI:10.1039/c6ay01063f.
[53] DAIA H C, SHI Yan, WANG Yilin, et al. A carbon dot based biosensor for melamine detection by fl uorescence resonance energy transfer[J]. Sensors and Actuators B: Chemical, 2014, 202: 201-208. DOI:10.1016/ j.snb.2014.05.058.
[54] SHAN Xiaoyue, CHAI Lujing, MA Juanjuan, et al. B-doped carbon quantum dots as a sensitive fl uorescence probe for hydrogen peroxide and glucose detection[J]. Analyst, 2014, 139(10): 2322-2325. DOI:10.1039/c3an02222f.
[55] XU Hua, YANG Xiupei, LI Gu, et al. Green synthesis of fl uorescent carbon dots for selective detection of tartrazine in food samples[J]. Journal of Agricultural and Food Chemistry, 2015, 63(30): 6707-6014. DOI:10.1021/acs.jafc.5b02319.
[56] WANG Jilong, WEI Junhua, SU Siheng, et al. Novel fluorescence resonance energy transfer optical sensors for vitamin B12detection using thermally reduced carbon dots[J]. New Journal of Chemistry, 2015, 39(1): 501-507. DOI:10.1039/c4nj00538d.
[57] KUNDU A, NANDI S, DAS P, et al. Facile and green approach to prepare fluorescent carbon dots: emergent nanomaterial for cell imaging and detection of vitamin B2[J]. Journal of Colloid and Interface Science, 2016, 468: 276-283. DOI:10.1016/ j.jcis.2016.01.070.
[58] CHEN Zhangbao, WANG Jing, MIAO Hong, et al. Fluorescent carbon dots derived from lactose for assaying folic acid[J]. Science China Chemistry, 2015, 59(4): 487-492. DOI:10.1007/s11426-015-5536-1.
[59] GAO Zhao, WANG Libing, SU Rongxin, et al. A carbon dot-based“off-on” fl uorescent probe for highly selective and sensitive detection of phytic acid[J]. Biosensors and Bioelectronics, 2015, 70: 232-238. DOI:10.1016/j.bios.2015.03.043.
[60] LIU Siyu, ZHAO Ning, CHENG Zhen, et al. Amino-functionalized green fl uorescent carbon dots as surface energy transfer biosensors for hyaluronidase[J]. Nanoscale, 2015, 7(15): 6836-6842. DOI:10.1039/ c5nr00070j.
[61] LOO A H, SFOER Z, BOUSA D, et al. Carboxylic carbon quantum dots as a fluorescent sensing platform for DNA detection[J]. American Chemical Society Applied Materials and Interfaces, 2016, 8(3): 1951-1957. DOI:10.1021/acsami.5b10160.
[62] LIU Jinhua, LI Jishan, JIANG Ying, et al. Combination of π-π stacking and electrostatic repulsion between carboxylic carbon nanoparticles and fl uorescent oligonucleotides for rapid and sensitive detection of thrombin[J]. Chemical Communications, 2011, 47(40): 11321-11323. DOI:10.1039/c1cc14445f.
[63] LIU Jinhua, YU Jing, CHEN Jianrong, et al. Noncovalent assembly of carbon nanoparticles and aptamer for sensitive detection of ATP[J]. RSC Advances, 2014, 4(72): 38199-38205. DOI:10.1039/c4ra05631k.
Synthesis of Carbon Dots and Its Applications in Food Detection
WEI Wei1,2, SHI Xingbo1,2,3,*, DENG Fangming1,2
(1. College of Food Science and Technology, Hunan Agricultural University, Changsha 410128, China; 2. Orient Science & Technology College, Hunan Agricultural University, Changsha 410128, China; 3. State Key Laboratory of Chemo/Biosensing and Chemometrics, Hunan University, Changsha 410082, China)
As a new type of fl uorescent nanomaterial, carbon dots (CDs) possess a number of unique optical properties. Compared with semiconductor quantum dots, some advantages of CDs, including lower toxicity, higher biocompatibility, higher photostability and stronger anti-photobleaching effect, are attractive in various fields. Interestingly, increasing attention is attracted to the detection of heavy metals, antibiotics, pathogenic bacteria, pesticide residues and banned additives, and nutritional and functional components in foods by using CDs nowadays. Recently, the synthesis and optical properties of CDs have been reviewed by many researchers, but there are few reviews that focus on the application of CDs in food detection. This article brief l y reviews the optical properties and synthesis of CDs, with emphasis on its applications in food detection. Meanwhile, the future trend of carbon dots is also discussed.
carbon dots; optical properties; heavy metals; antibiotics; pathogenic bacteria
10.7506/spkx1002-6630-201715041
TS207.3
A
1002-6630(2017)15-0256-09
魏偉, 石星波, 鄧放明. 碳量子點合成及其在食品檢測中的應用[J]. 食品科學, 2017, 38(15): 256-264. DOI:10.7506/ spkx1002-6630-201715041. http://www.spkx.net.cn
WEI Wei, SHI Xingbo, DENG Fangming. Synthesis of carbon dots and its applications in food detection[J]. Food Science, 2017, 38(15): 256-264. (in Chinese with English abstract)
10.7506/spkx1002-6630-201715041. http://www.spkx.net.cn
2016-07-04
國家自然科學基金青年科學基金項目(31301484);湖南省自然科學基金青年基金項目(2015JJ3082);湖南農業大學青年項目(14QN11;14QNZ14);化學生物傳感與計量學國家重點實驗室(湖南大學)開放項目(Z2015025);湖南省高校青年骨干教師培養對象資助項目
魏偉(1994—),男,本科,研究方向為碳量子點的合成與應用和食品質量與安全分析。E-mail:1213691488@qq.com
*通信作者:石星波(1984—),男,副教授,博士,研究方向為食品化學與分析、納米生物傳感和單分子成像。
E-mail:shixingbo123@aliyun.com

