重組AthrobacterramosusS34MTSase和MTHase的酶學(xué)性質(zhì)及其制備海藻糖的應(yīng)用條件優(yōu)化
王魁, 宿玲恰, 吳敬, 陳晟*
1(江南大學(xué), 食品科學(xué)與技術(shù)國家重點實驗室,江蘇 無錫,214122) 2(江南大學(xué),生物工程學(xué)院工業(yè)生物技術(shù)教育部重點實驗室,江蘇 無錫,214122)
研究報告
重組AthrobacterramosusS34MTSase和MTHase的酶學(xué)性質(zhì)及其制備海藻糖的應(yīng)用條件優(yōu)化
王魁1,2, 宿玲恰1,2, 吳敬1,2, 陳晟1,2*
1(江南大學(xué), 食品科學(xué)與技術(shù)國家重點實驗室,江蘇 無錫,214122) 2(江南大學(xué),生物工程學(xué)院工業(yè)生物技術(shù)教育部重點實驗室,江蘇 無錫,214122)
以淀粉為底物,通過麥芽寡糖基海藻糖合成酶(maltosyltrehalose synthase, MTSase)和麥芽寡糖基海藻糖水解酶(maltosyltrehalose hydrolase,MTHase)的共同作用生產(chǎn)海藻糖是一種經(jīng)濟高效的方法。對ArthrobacterramosusS34來源并分別在E.coliBL21(DE3)中表達的MTSase和MTHase的酶學(xué)性質(zhì)進行研究,發(fā)現(xiàn)MTSase的最適溫度為45 ℃,最適pH為7.0,MTHase的最適溫度為55 ℃,最適pH為6.0。隨后用2種酶共同作用生產(chǎn)海藻糖,優(yōu)化反應(yīng)條件,考查反應(yīng)溫度、初始pH、底物DE值、加酶量以及底物濃度等因素對酶轉(zhuǎn)化過程中海藻糖產(chǎn)率的影響。最佳酶轉(zhuǎn)化條件為反應(yīng)溫度45 ℃、初始pH5.5,底物DE值8.5,加酶量分別為MTSase最小加量15.75 U/g淀粉,MTHase最小加量7.5 U/g淀粉。
海藻糖;麥芽寡糖基海藻糖合成酶(maltosyltrehalose synthase, MTSase);麥芽寡糖基海藻糖水解酶(maltosyltrehalose hydrolase, MTHase);酶學(xué)性質(zhì);酶轉(zhuǎn)化
海藻糖是一種在自然界中普遍存在的非還原性二糖,以穩(wěn)定的α-1,1-糖苷鍵連接,不能被α-葡萄糖苷酶分解[1]。海藻糖無毒,作為糖類能夠為生物體提供能量和碳源。另有研究表明,當(dāng)海藻糖與蛋白質(zhì)、脂質(zhì)、組織、器官等共存時,能夠幫助它們抵抗環(huán)境壓力,因此海藻糖還可用于生物物質(zhì)的保存[2-3]。
不同的酶系統(tǒng)可以有效地以麥芽糖、蔗糖和淀粉作為底物分別產(chǎn)生海藻糖[4-6]。1994年,有研究所發(fā)現(xiàn),2種不同的酶,麥芽寡糖基海藻糖合成酶(maltosyltrehalose synthase, MTSase)和麥芽寡糖基海藻糖水解酶(maltosyltrehalose hydrolase, MTHase)在以淀粉作為反應(yīng)起始底物時,在產(chǎn)生海藻糖的過程中起重要作用[7]。之后,又有研究人員報道了以蔗糖為底物通過3種不同的酶(海藻糖磷酸化酶,蔗糖磷酸化酶和葡萄糖異構(gòu)酶)進行海藻糖代謝的合成[4]。1998年,經(jīng)研究發(fā)現(xiàn),通過海藻糖合酶可以使以α-1,4-糖苷鍵連接的麥芽糖重組轉(zhuǎn)變?yōu)橐驭?1,1-糖苷鍵連接的海藻糖,實現(xiàn)以麥芽糖為底物合成海藻糖[8-9]。
考慮工業(yè)應(yīng)用中的成本因素,雙酶法所用的底物是比蔗糖和麥芽糖更便宜的淀粉,因此以MTSase和MTHase生產(chǎn)海藻糖是最具成本效益的方法。在雙酶法生成海藻糖的過程中,淀粉液化后,位于糊精末端的2個葡萄糖分子間的α-1,4-糖苷鍵可在MTSase的催化下轉(zhuǎn)化為α-1,1-糖苷鍵,使其變成帶有1分子海藻糖的糊精。此后,經(jīng)MTHase的水解作用將其水解成2部分,一部分為目標(biāo)產(chǎn)物海藻糖分子,另一部分為減少2個葡萄糖分子的糊精,而第二部分的糊精則作為底物參與下一輪反應(yīng),繼續(xù)生產(chǎn)海藻糖[7]。
國內(nèi)外研究人員已經(jīng)對根瘤菌[10]、谷氨酸棒狀桿菌[11]、微黃短桿菌[6]、節(jié)桿菌[12]、分支節(jié)桿菌[7]、芝田硫化葉菌[13]以及嗜熱硫礦硫化葉菌[14]來源的MTSase和MTHase兩種酶基因進行了克隆表達,并對2種酶的酶學(xué)性質(zhì)及在生產(chǎn)海藻糖過程中的應(yīng)用條件進行了研究。
MTSase和MTHase兩種酶分別由基因treY和treZ控制表達,本實驗室于前期構(gòu)建了分別含有treY和treZ的基因工程菌E.coliBL21(DE3)/pET-24a-treY和E.coliBL21(DE3)/pET-24a-treZ,經(jīng)過發(fā)酵優(yōu)化,發(fā)現(xiàn)目的基因源自于ArthrobacterramosusS34的2株基因工程菌的發(fā)酵酶活明顯高于已報道的該來源2種酶的發(fā)酵酶活,具有較高的應(yīng)用價值。此來源的2種酶在E.coliBL21(DE3)中的重組表達之前未見報道。本研究對這2種重組酶的酶學(xué)性質(zhì)以及在制備海藻糖過程中的條件優(yōu)化進行了研究。
1 材料與方法
1.1材料與試劑
海藻糖、麥芽四糖、麥芽六糖,美國Sigma公司。
1.2儀器與設(shè)備
安捷倫1200高效液相色譜系統(tǒng),美國Agilent公司。
1.3方法
1.3.1 MTSase和MTHase酶活力的測定
MTSase酶活測定:10 μL稀釋一定倍數(shù)的 MTSase酶液(空白加高溫滅活的MTSase),加到190 μL的10 g/L的麥芽六糖溶液中(20 mmol/L pH 6.0的磷酸鹽緩沖液配制),45 ℃反應(yīng)10 min,100 ℃沸水中煮10 min終止反應(yīng)。取100 μL反應(yīng)液于10 mL具塞試管中,注入900 μL水和1 mL DNS溶液,沸水中煮7 min,加水補至10 mL,最后在540 nm波長下測定吸光度值。MTSase的酶活單位定義為:在45 ℃時,其他條件恒定,單位時間內(nèi)每消耗1 μmol麥芽六糖所需的酶量。酶活計算公式:
MTSase的酶活=

MTHase酶活測定:10 μL MTSase濃縮酶液加到490 μL 10 g/L的麥芽六糖溶液中(20 mmol/L pH 6.0的磷酸鹽緩沖液配制),45 ℃反應(yīng)2 h,100 ℃沸水中煮10 min終止反應(yīng)。待溶液冷卻后,加入10 μL 稀釋一定倍數(shù)的MTHase酶液(空白加高溫滅活的MTHase)到190 μL的處理過的底物中,55 ℃反應(yīng)10 min,100℃沸水中煮10 min終止反應(yīng),取100 μL反應(yīng)液,加入900 μL水和1 mL DNS溶液,沸水中煮7 min,加水補至10 mL,最后在540 nm波長下測定吸光度值。MTHase的酶活單位定義為:在55 ℃時,其他條件恒定,單位時間內(nèi)轉(zhuǎn)化生成1 μmol麥芽四糖所需的酶量。酶活計算公式:
MTHase的酶活=

1.3.2 重組蛋白酶學(xué)性質(zhì)的研究
1.3.2.1 重組MTSase和MTHase的最適溫度
分別將底物置于35、40、45、50、55、60、65 ℃水浴中預(yù)熱3 min,按照1.3.1所述方法測定酶活,算出百分比。定義最高酶活為100%。
1.3.2.2 重組MTSase和MTHase的溫度穩(wěn)定性
將酶液置于45℃中保溫,定期取樣按照1.3.1操作步驟測定殘余酶活,算出百分比(設(shè)定0 h酶活為100%)。
1.3.2.3 重組MTSase和MTHase的最適pH
將酶液分別置于20 mmol/L pH為 4.0~8.0(梯度為0.5)的緩沖液中,在相應(yīng)溫度下預(yù)熱3 min,按照1.3.1所述方法測定相應(yīng)pH條件下的酶活,算出百分比,定義最高酶活為100%。
1.3.2.4 重組MTSase和MTHase的pH穩(wěn)定性
將酶分別置于20 mmol/L pH 4.0~8.0(梯度為0.5)緩沖液中,于4 ℃靜置24 h,按照1.3.1操作步驟測定剩余酶活,算出百分比(設(shè)定0 h酶活為100%)。
1.3.3 MTSase和MTHase制備海藻糖的工藝條件優(yōu)化
1.3.3.1 反應(yīng)溫度的優(yōu)化
200 g/L的玉米淀粉液化至DE值10,初始pH為6.0,加入5 U/g淀粉的普魯蘭酶,30 U/g 底物的 MTSase和MTHase在150 r/min的水浴搖床中進行反應(yīng)。溫度分別設(shè)置為35、40、45、50、55 ℃,反應(yīng)36 h后終止反應(yīng)并煮沸處理。產(chǎn)物稀釋沉淀后用液相測定其中海藻糖含量,算出產(chǎn)率。
1.3.3.2 底物DE值的優(yōu)化
200 g/L的玉米淀粉液化至DE值分別達到3.5、6.5、8.5和10.5,初始pH為6.0,加入5 U/g淀粉的普魯蘭酶,30 U/g的 MTSase和MTHase在45 ℃,150 r/min水浴搖床中反應(yīng)36 h后終止反應(yīng)并煮沸處理。液相測定其中海藻糖含量,算出產(chǎn)率。
1.3.3.3 初始pH的優(yōu)化
200 g/L的玉米淀粉液化至DE值8.5,加入5 U/g淀粉的普魯蘭酶,30 U/g的 MTSase和MTHase,分別調(diào)節(jié)初始pH為4.5、5.0、5.5、6.0、6.5、7.0在45 ℃,150 r/min水浴搖床中反應(yīng)36 h后終止反應(yīng)并煮沸處理。測定其中海藻糖含量,算出產(chǎn)率。
1.3.3.4 加酶量的優(yōu)化
200 g/L的玉米淀粉液化至DE值8.5,初始pH為5.5,加入5 U/g淀粉的普魯蘭酶,再分別加入終濃度為114、75.5、38、19、7.5、3.75、1.875 U/g 底物的 MTHase和終濃度為31.5 U/g底物的MTSase。另外分別加入終濃度為31.5、15.75、7.875、3.15、1.575 U/g 的MTSase和終濃度為114 U/g底物的 MTHase在45 ℃,150 r/min水浴搖床中反應(yīng)36 h后終止反應(yīng)并煮沸處理。液相測定其中海藻糖含量,算出產(chǎn)率。
1.3.3.5 底物含量的優(yōu)化
分別配置170、240、270、320 g/L的玉米淀粉作為底物,液化至DE值8.5,初始pH為5.5,加入5 U/g淀粉的普魯蘭酶,30 U/g 底物的 MTSase和MTHase在45 ℃,150 r/min的水浴搖床中反應(yīng)36 h后終止反應(yīng)并煮沸處理。測定其中海藻糖含量,算出產(chǎn)率。
1.3.4 底物轉(zhuǎn)化率的測定
產(chǎn)物中的海藻糖含量采用高效液相色譜檢測,NH2柱,體積分數(shù)80%的乙腈溶液,流速為0.8 mL/min,柱溫為40 ℃。
1.3.5 底物轉(zhuǎn)化率的計算
1.3.6 優(yōu)化條件下反應(yīng)過程中海藻糖產(chǎn)量的測定
170 g/L的玉米淀粉液化至DE值8.5,初始pH為5.5,加入5 U/g淀粉的普魯蘭酶,15.75 U/g底物的MTSase和7.5 U/g底物的 MTHase在45 ℃,150 r/min的水浴搖床中反應(yīng)。反應(yīng)過程中每隔6 h取樣并煮沸處理,36 h后終止反應(yīng)。測定其中海藻糖含量,算出產(chǎn)率。
2 結(jié)果與討論
2.1重組MTSase和MTHase的酶學(xué)性質(zhì)
2.1.1 重組蛋白最適溫度及溫度穩(wěn)定性
蛋白酶的催化反應(yīng)速率與反應(yīng)溫度密切相關(guān)。如圖1示,MTSase的最適溫度為45 ℃,MTHase的最適溫度為55 ℃。在一定溫度范圍內(nèi),重組MTSase和MTHase的酶活性隨著溫度的升高也呈現(xiàn)逐漸升高的趨勢,由于過高的溫度會使蛋白質(zhì)性質(zhì)發(fā)生不可逆的改變,當(dāng)溫度高于45 ℃時,MTSase的活性隨著溫度的升高開始降低;當(dāng)溫度高于55 ℃時,MTHase的活性開始降低。MTSase和MTHase在45 ℃、50 ℃下的穩(wěn)定性結(jié)果顯示在圖2中。MTSase和MTHase在45 ℃的半衰期分別為96 h和6 h,在50 ℃的半衰期分別為50 h和3 h。可以看出,MTSase在45 ℃和50 ℃時具有較高的穩(wěn)定性,MTHase在2種溫度下的穩(wěn)定性都比較差。
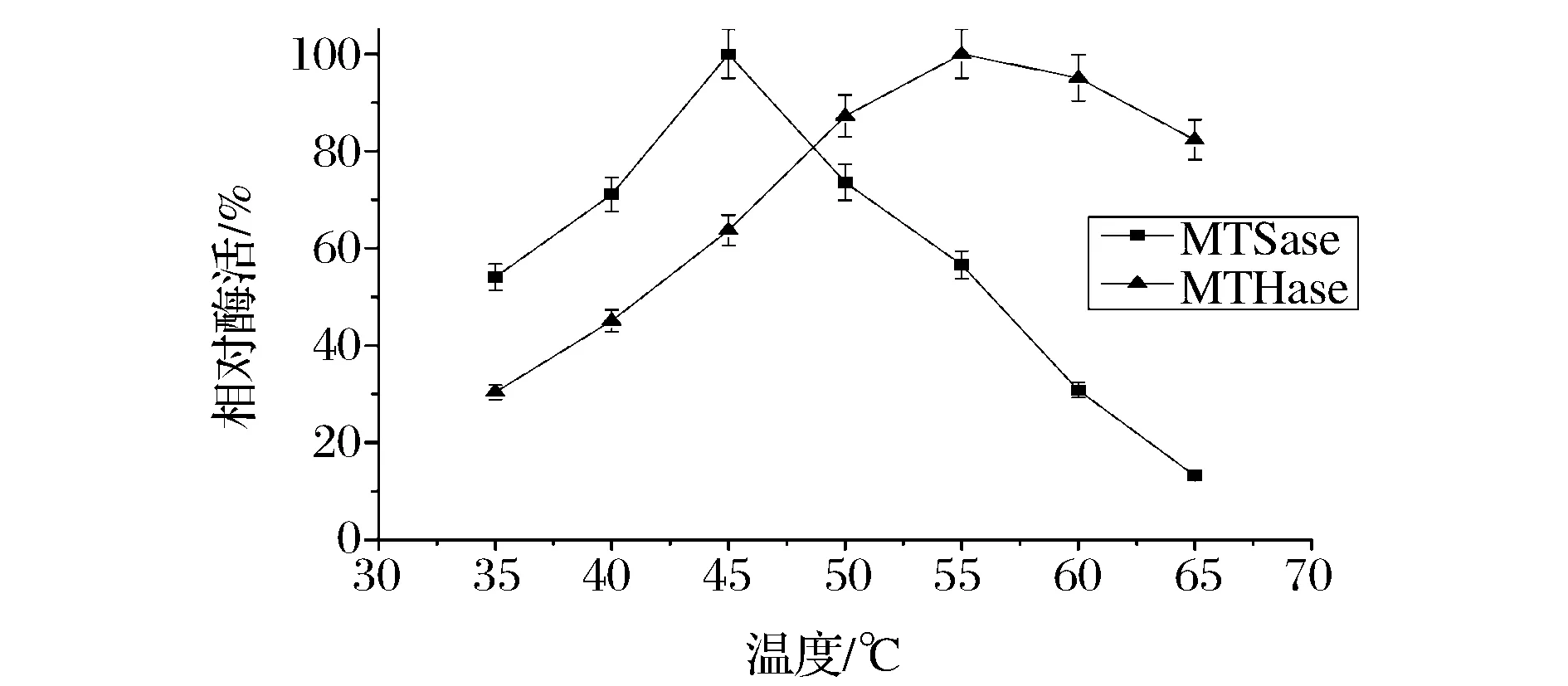
圖1 MTSase和MTHase的最適溫度Fig.1 Optimum temperature of MTSase and MTHase

a-MTSase在45 ℃和50 ℃的穩(wěn)定性;b-MTHase在45 ℃和50 ℃的穩(wěn)定性圖2 MTSase和MTHase的溫度穩(wěn)定性Fig.2 Temperature stability of MTSase and MTHase
2.1.2 重組蛋白最適pH及pH穩(wěn)定性
酶反應(yīng)的反應(yīng)速率會受到環(huán)境pH的影響。如圖3所示,MTSase在pH值5.5~8.0的范圍內(nèi)均有70%以上的酶活,并在pH7.0的環(huán)境下,測得的酶活最高,大于或小于7.0的pH環(huán)境都會使酶活逐漸降低。MTHase的最適pH為6.0,在大于6.0的pH環(huán)境下,MTHase的活性急速降低,如當(dāng)pH為6.5時,酶活相對值迅速降低至57.9%;而在小于6.0大于5.0的pH時,MTHase的酶活能夠穩(wěn)定在一定的范圍,達到酶活相對值85%以上;在更低的pH(<5.0)時,MTHase的酶活相對值則急速降低到42%以下。綜上,重組MTHase適合的pH范圍應(yīng)為5.0~6.0。另外,pH穩(wěn)定性結(jié)果(圖4)表明,在4 ℃時,MTSase和MTHase在pH 4.0~8.0均能保證較好的穩(wěn)定性。
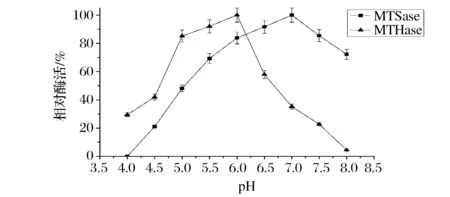
圖3 MTSase和MTHase的最適 pHFig.3 Optimum pH of MTSase and MTHase

圖4 MTSase和MTHase的pH穩(wěn)定性Fig.4 pH stability of MTSase and MTHase
2.2重組MTSase和重組MTHase制備海藻糖的工藝條件
2.2.1 反應(yīng)溫度與底物轉(zhuǎn)化率的關(guān)系
如圖5所示,在反應(yīng)溫度逐漸升高時,海藻糖的轉(zhuǎn)化率也隨著提高,并在45 ℃時到達最高值,為54.2%。但在45℃之后,海藻糖的轉(zhuǎn)化率隨著溫度的升高快速下降,這可能是高溫使得MTHase快速失活而導(dǎo)致的。綜合以上因素,最終選擇45℃作為轉(zhuǎn)化產(chǎn)海藻糖的反應(yīng)溫度。

圖5 溫度與底物轉(zhuǎn)化率的關(guān)系Fig.5 The relationship between temperature and trehalose conversion
2.2.2 底物液化DE值與底物轉(zhuǎn)化率的關(guān)系
底物玉米淀粉液化結(jié)束時的DE值會對與海藻糖的轉(zhuǎn)化率之間也有著密切的聯(lián)系。如圖6所示,海藻糖的轉(zhuǎn)化率隨著DE值的升高而增加,并在DE值為8.5時達到最大值56.8%。這可能是因為在DE值過低時,糊化過的淀粉底物在溫度自然下降的過程中更易發(fā)生老化,使得淀粉內(nèi)部已被破壞的分子氫鍵再次結(jié)合,隨著部分分子的有序排列,即造成結(jié)晶沉淀,從而使得底物利用率大大降低[15]。而當(dāng)?shù)孜顳E值達到8.5時,更高的DE值代表著更低的聚合度,由于MTSase和MTHase在反應(yīng)過程中只會對聚合度3的糖鏈起作用[7],因此在一定范圍內(nèi),底物轉(zhuǎn)化成海藻糖的轉(zhuǎn)化率會隨著淀粉底物聚合度的降低而減少,因此,在DE值為8.5時,最適合進行底物制備海藻糖的反應(yīng)。
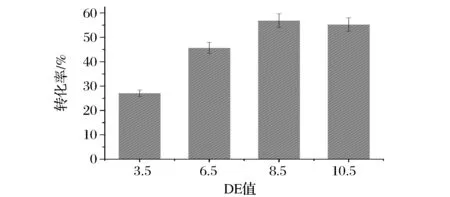
圖6 DE值與底物轉(zhuǎn)化率的關(guān)系Fig.6 The relationship between DE value and trehalose conversion
2.2.3 初始pH與底物轉(zhuǎn)化率的關(guān)系
由圖7可以看出,重組MTSase和重組MTHase轉(zhuǎn)化底物生成海藻糖的最適初始pH為5.5。
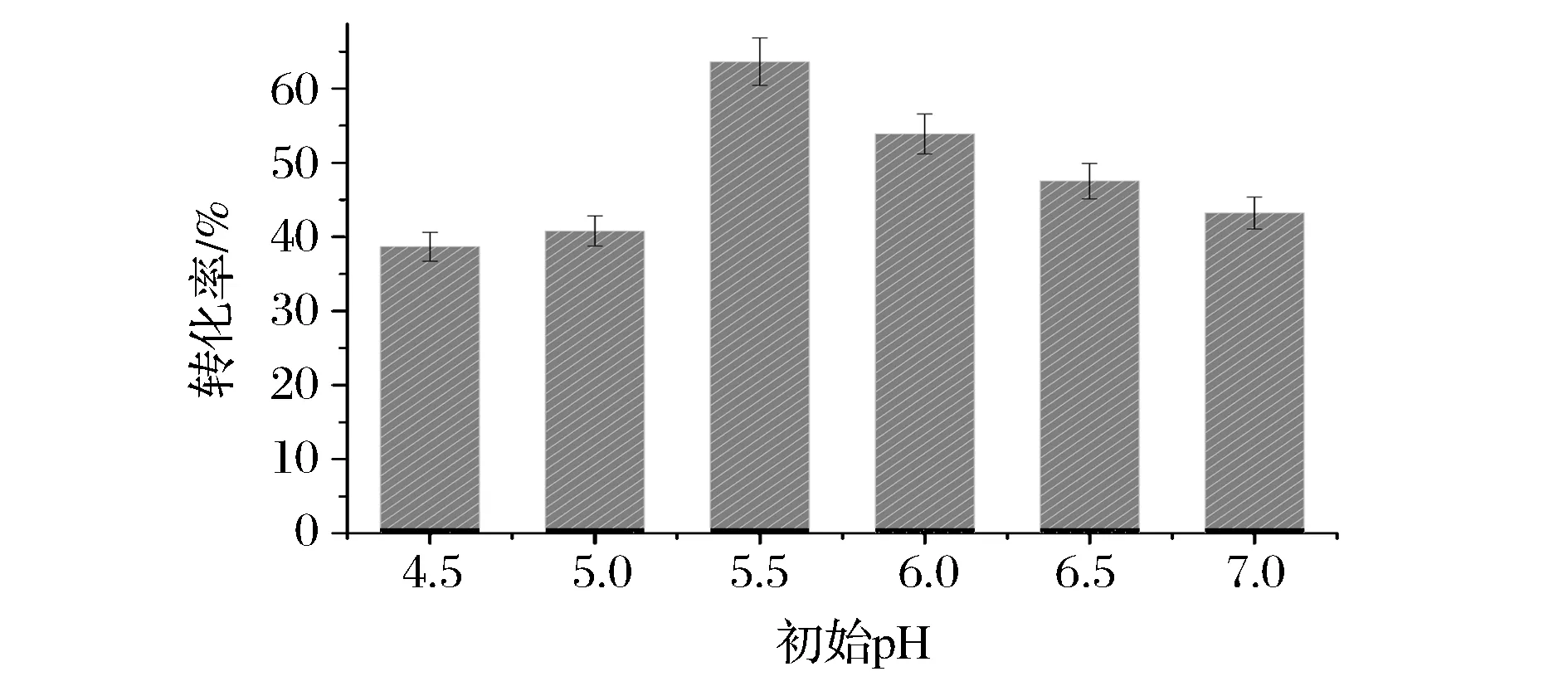
圖7 初始pH與底物轉(zhuǎn)化率的關(guān)系Fig.7 The relationship between initial pH and trehalose conversion
初始pH低于5.5或過高時,底物轉(zhuǎn)化率顯著降低,很可能是一方面過高或過低的pH使得酶活性中心的構(gòu)象發(fā)生改變,甚至改變了酶分子的整體結(jié)構(gòu)使其變形失活,導(dǎo)致酶分子的穩(wěn)定性大大降低;另一方面可能是不同pH會對酶活性中心附近相關(guān)基團的解離狀態(tài)產(chǎn)生一定的影響,造成活性部位與底物結(jié)合難易度的區(qū)別[16]。當(dāng)初始pH處于5.5~6.5之間時,底物轉(zhuǎn)化率也逐漸減少,可能是因為在該pH范圍內(nèi),不同pH導(dǎo)致酶穩(wěn)定性的變化,而這種變化對海藻糖產(chǎn)率的影響高于酶最適pH對其的影響。綜上考慮,選擇5.5作為反應(yīng)的初始pH。
2.2.4 加酶量與底物轉(zhuǎn)化率的關(guān)系
由于海藻糖的轉(zhuǎn)化需要MTSase和MTHase的共同作用,因此對2種酶的加量進行了研究。如圖8所示,在加酶量充足的情況下,2種酶的加量比例對海藻糖的轉(zhuǎn)化率沒有明顯的影響。在轉(zhuǎn)化過程中,如要保證一定的底物轉(zhuǎn)化率,2種酶都有對應(yīng)的最少加量。如圖8(a),加入足量恒定的MTHase時,控制MTSase的加量,當(dāng)其降低到15.75 U/g時,依然能夠保持65%以上的轉(zhuǎn)化率,而當(dāng)MTSase的加量降低到7.875 U/g時,底物轉(zhuǎn)化率則直接降低到55%。如圖8(b),加入足量恒定的MTSase時,控制MTHase的加量,在其加量7.5 U/g時,底物轉(zhuǎn)化率可始終穩(wěn)定在63%以上。因此,在酶轉(zhuǎn)化產(chǎn)海藻糖過程中,MTSase和MTHase的最少加量分別為15.75 U/g和7.5 U/g。
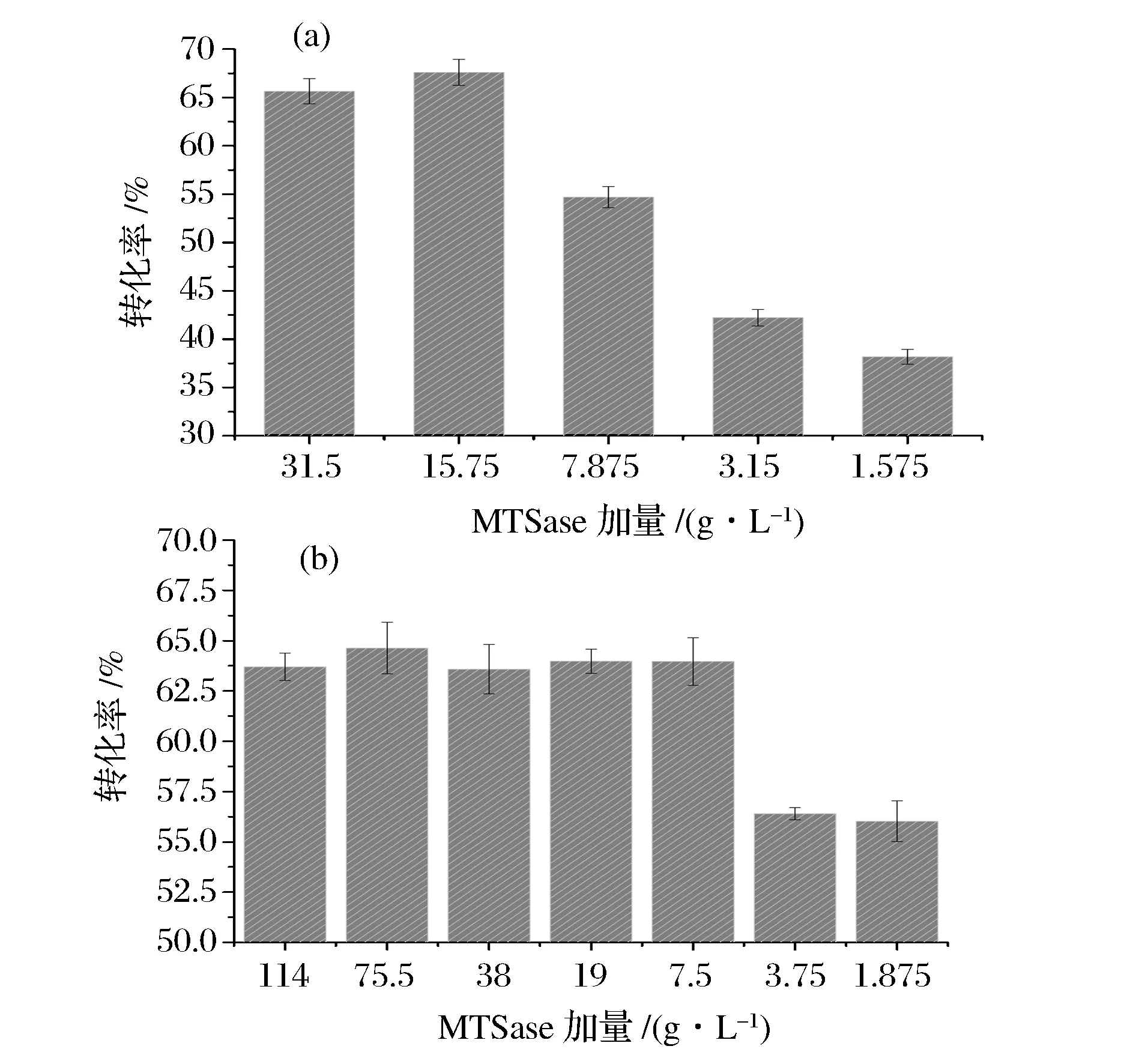
a-不同MTSase加量;b-不同MTHase加量圖8 加酶量與底物轉(zhuǎn)化率的關(guān)系Fig.8 The relationship between enzyme dosage and trehalose conversion
2.2.5 底物濃度與海藻糖轉(zhuǎn)化率的關(guān)系
為了提高工業(yè)生產(chǎn)中制備底物的效率,研究了底物濃度對2種酶共同作用生成海藻糖的轉(zhuǎn)化率的影響,分別在17%、24%、27%、32%四個不同的底物濃度下對其進行研究。結(jié)果(圖9)顯示,更高的底物濃度會伴隨有更低的底物轉(zhuǎn)化率,其轉(zhuǎn)化率最高點在底物濃度為17%時達到,為67.7%。雖然底物轉(zhuǎn)化率隨著底物濃度的升高而逐漸降低,但考慮到工業(yè)生產(chǎn)中進行一批生產(chǎn)所需的人力物力是一定的,因此在具體生產(chǎn)過程中,應(yīng)對總體成本進行核算,以選取最佳底物濃度。

圖9 底物濃度與底物轉(zhuǎn)化率的關(guān)系Fig.9 The relationship between substrate concentration and trehalose conversion
2.2.6 優(yōu)化條件下海藻糖產(chǎn)量的過程研究
經(jīng)條件優(yōu)化后得知,MTHase和MTSase協(xié)同作用產(chǎn)海藻糖在45 ℃時能達到最高的產(chǎn)率。考慮到MTHase在45 ℃時的半衰期為6 h,因此在45 ℃下對海藻糖轉(zhuǎn)化進行過程研究。同時,作為對照,在反應(yīng)進行到12 h時,向反應(yīng)體系中補加終濃度為7.5 U/g底物的 MTHase,繼續(xù)反應(yīng)至36 h。結(jié)果(圖10)表明,補加MTHase對海藻糖最終的轉(zhuǎn)化率沒有明顯提高。主要的轉(zhuǎn)化過程在前24 h完成,在24~30 h,海藻糖含量的增速降低,但依然在增加,直到轉(zhuǎn)化進行到30~36 h之間時,海藻糖含量開始穩(wěn)定。這表明在整個反應(yīng)過程中,MTHase均有著合適的酶活性來保證反應(yīng)的進行,分析原因可能是當(dāng)酶液與底物共同存在時,底物對MTHase具有保護作用。
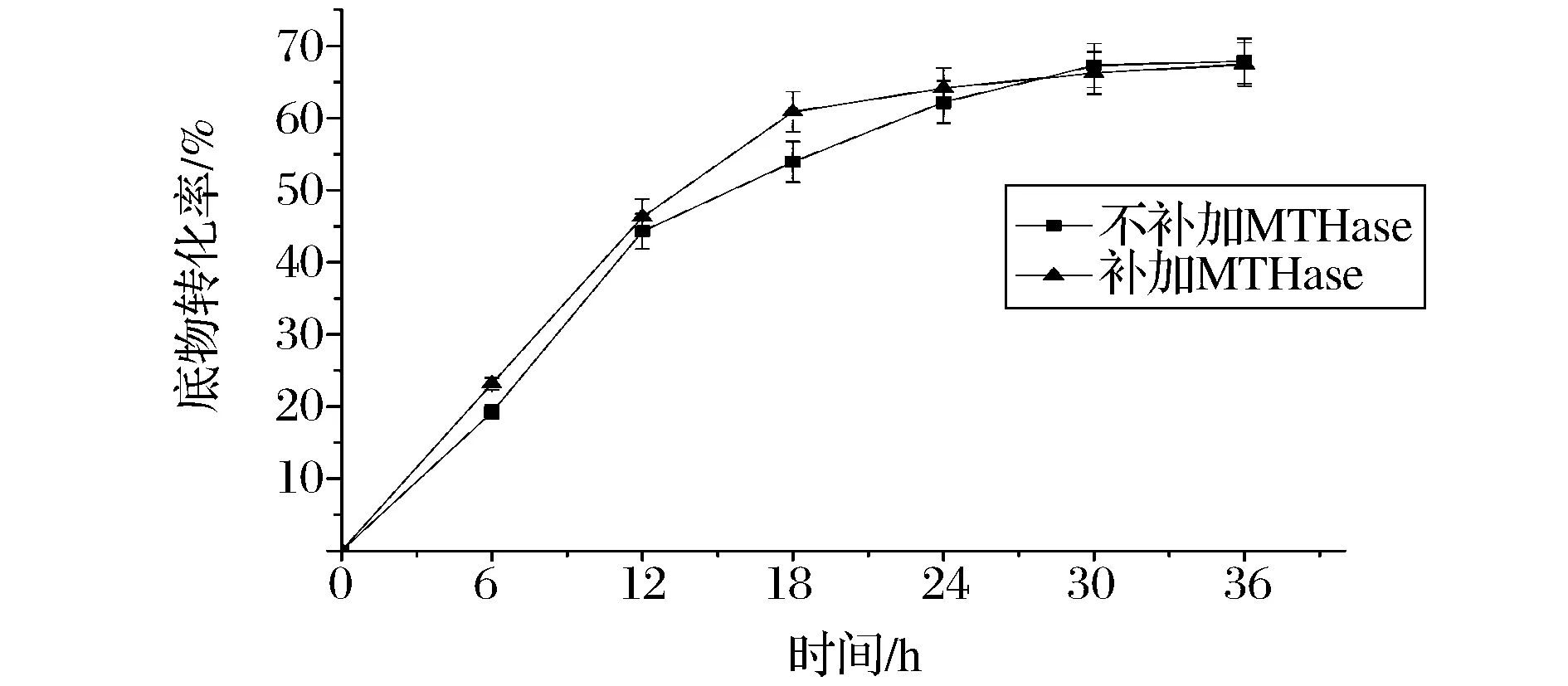
圖10 優(yōu)化條件下底物轉(zhuǎn)化率產(chǎn)量隨時間的變化Fig.10 Changes of trehalose yield over time under optimized conditions
3 結(jié)論
本研究中重組菌E.coliBL21(DE3)/pET-24a-treY和E.coliBL21(DE3)/pET-24a-treZ能夠分別高效表達MTHase和MTSase,MTSase的最適溫度為45℃,最適pH為7.0,MTHase的最適溫度為55℃,最適pH為6.0。在2種酶的產(chǎn)海藻糖應(yīng)用研究中發(fā)現(xiàn)其最適轉(zhuǎn)化溫度和pH為45℃、初始pH5.5,這與其酶學(xué)性質(zhì)研究結(jié)果相對應(yīng)。另外,其最適底物DE值為8.5,過高和過低的DE值對其轉(zhuǎn)化率的影響都較大,因此后期在實際工廠生產(chǎn)中應(yīng)嚴(yán)格控制底物淀粉的液化時間,以使其DE值達到8.5左右,保證底物轉(zhuǎn)化率。在反應(yīng)過程中,MTSase和MTHase最小加量分別為15.75 U/g淀粉和7.5 U/g淀粉,并且過量的2種酶對海藻糖的轉(zhuǎn)化率都沒有明顯的影響。因此,在生產(chǎn)過程中,可以適當(dāng)?shù)卦黾覯TSase和MTHase兩種酶的加量,保證反應(yīng)的正常進行。最后,底物濃度對反應(yīng)的進行也有著較大的影響,在其他條件恒定時,轉(zhuǎn)化率在一定范圍內(nèi)隨著底物濃度的升高而降低。同時考慮到生產(chǎn)過程中的成本問題,應(yīng)當(dāng)結(jié)合具體情況,全面考慮以選擇最優(yōu)的底物濃度。
[1] RICHARDSAB.Trehalose:a review of properties,history of use and human tolerance,and results of multiple safety studies[J].Food and Chemical Toxicology,2002,40(7):871-898.
[2] ELEUTHERIO EC,ARAUJO PS,PANEK AD.Protective role of trehalose during heat stress inSaccharomycescerevisiae[J].Cryobiology,1993,30(6):591-596.
[3] OHTAKE S,WANG YJ.Trehalose:current use and future applications[J].J Pharm Sci,2011,100(6):2 020-2 053.
[4] SCHICK I,HALTRICH D,KULBE KD.Trehalose phosphorylase from Pichia fermentans and its role in the metabolism of trehalose[J].Applied Microbiology and Biotechnology,1995,43(6):1 088-1 095.
[5] SAITO K, KASE T, TAKAHASHI E, et al. Purification and characterization of a trehalose synthase from the basidiomyceteGrifolafrondosa[J].Applied and Environmental Microbiology,1998,64(11):4 340-4 345.
[6] KIM Y H, KWON T K, PARK S, et al. Trehalose synthesis by sequential reactions of recombinant maltooligosyltrehalose synthase and maltooligosyltrehalosetrehalohydrolase fromBrevibacteriumhelvolum[J].Appl Environ Microbiol,2000,66(11):4 620-4 624.
[7] YAMAMOTOT T, MARUTA K, WATABABE H, et al.Trehalose-producing operontreYZfromArthrobacterramosusS34[J].BiosciBiotechnol Biochem,2001,65(6):1 419-1 423.
[8] SUKHOON Koh, HYUNJAE Shin, JOONGSU, Kim, et al. Trehalose synthesis from maltose by a thermostable trehalose synthase fromThermuscaldophilus[J].Biotechnology Letters,1998,20(8):757-761.
[9] CHO Y J,PARK O J,SHIN HJ.Immobilization of thermostable trehalose synthase for the production of trehalose[J].Enzyme and Microbial Technology,2006,39(1):108-113.
[10] MARUTA K,HATTORI K,NAKADAT,et al.Cloning and sequencing of trehalose biosynthesis genes fromRhizobiumsp.M-ll[J].Bioscience, Biotechnology,and Biochemistry,1996,60(4):717-720.
[11] CARPINELLI J,KRAMER R,AGOSINE.Metabolic engineering ofCorynebacteriumglutamicumfor trehaloseoverproduction:role of theTreYZtrehalose biosynthetic pathway[J].Applied and Environmental Microbiology,2006,72(3):1 949-1 955.
[12] MARUTA K,HATTORI K,NAKADAT,etal.Cloning and sequencing of trehalose biosynthesis genes fromArthrobactersp.Q36[J].Biochimica et BiophysicaActa (BBA)-General Subjects,1996,1 289(1):10-13.
[13] Di LERNIA I,MORANA A,OTTOMBRINOA,etal.Enzymes fromSulfolobusshibataefor the production of trehalose and glucose from starch[J].Extremophiles,1998,2(4):409-416.
[14] FANG TY,TSENG WC,GUO MS,etal.Expression,purification, and characterization of the maltooligosyltrehalose trehalohydrolase from the thermophilic archaeonsulfolobussolfataricusATCC 35092[J].Journal of Agricultural and Food Chemistry,2006,54(19):7 105-7 112.
[15] 唐聯(lián)坤.淀粉糊化、老化特性與食品加工[J].西部糧油科技,1996,21(3):26-29.
[16] 王寧,吳丹,陳晟,等.利用來源于Paenibacillusmacerans的α-CGTase突變體Y89D制備α-環(huán)糊精[J].食品科學(xué),2011,32(3):165-170.
EnzymaticpropertiesofrecombinantAthrobacterramosusS34MTSaseandMTHaseandoptimizationofapplicationconditionsforproductionoftrehalose
WANG Kui1,2, SU Ling-qia1,2, WU Jing1,2, CHEN Sheng1,2*
1(State Key Laboratory of Food Science and Technology, Jiangnan University,Wuxi 214122, China) 2(School of Biotechnology and Key Laboratory of Industrial Biotechnology Ministry of Education, Jiangnan University, Wuxi 214122, China)
The production of trehalose from starch is an effective method under the combined action of maltosyltrehalose synthase (MTSase) and maltosyltrehalose hydrolase (MTHase). The optimum temperature of MTSase was 45℃, the optimal pH was 7.0, and the optimal temperature of MTHase was 55℃, the optimum pH was 6.0. Then trehalose was produced by the two enzymes together, and the reaction conditions were optimized. The effects of reaction temperature, initial pH, substrate DE value, enzymes amounts and substrate concentration on trehalose yield were investigated. The optimal conditions were as follows: the reaction temperature was 45℃, the initial pH was 8.5, the substrate DE value was 8.5 and the amount of MTSase and MTHase was 15.75 U/g and 7.5 U/g, respectively.
trehalose; maltosyltrehalosesynthase(MTSase); maltosyltrehalose hydrolase(MTHase); enzymatic properties; enzyme transformation
10.13995/j.cnki.11-1802/ts.013741
碩士研究生(陳晟副教授為通訊作者,E-mail:chensheng@jiangnan.edu.cn)。
國家杰出青年基金(31425020);江蘇高校優(yōu)秀科技創(chuàng)新團隊項目(吳敬)
2017-01-03,改回日期:2017-03-09

