夫西地酸對新生兒和小嬰兒血清膽紅素水平的影響
于寶東
夫西地酸對新生兒和小嬰兒血清膽紅素水平的影響
于寶東
目的 探討新生兒和小嬰兒應用夫西地酸后血清膽紅素的變化。方法 對 2012-2014 年青島市婦女兒童醫院應用夫西地酸的半歲以下患兒用藥前后的血清膽紅素等指標進行回顧性分析,比較用藥前后的血清膽紅素變化情況。結果 所有138例應用夫西地酸治療的患兒,治療后均未出現新發黃疸或原有黃疸加重的情況;其中64例用藥前后檢測了血生化指標,治療前后白蛋白、丙氨酸轉氨酶、天冬氨酸轉氨酶等均無顯著差異,治療后的間接膽紅素與總膽紅素比值(Ibil/Tbil)比用藥前下降了約8%。結論 該系列應用夫西地酸的患兒中未見該藥對血清膽紅素水平的明顯影響。
夫西地酸 ; 膽紅素 ; 不良反應 ; 黃疸
夫西地酸(fusidic acid)屬梭鏈孢酸類抗生素,1962 年首次在梭鏈孢酸脂球菌發酵液中發現并提取獲得[1]。在結構上與頭孢菌素 P1 相似,臨床上主要用于治療革蘭陽性菌感染,尤其是耐藥金黃色葡萄球菌感染,凝固酶陰性葡萄球菌對該藥的敏感率在 70%~85%[2-3]。其療效可靠、不良反應相對較少[4]、價格比萬古霉素和利奈唑胺便宜等優點,在兒科臨床中也有一定應用。
體外研究表明,夫西地酸與血清白蛋白具有高度親和力,可以競爭性替換出血清中與蛋白結合的膽紅素,使血液中的游離間接膽紅素水平升高[5]。臨床治療劑量的夫西地酸分子數量足以替換出大部分的結合型膽紅素,因此說明書中將早產兒、黃疸、嚴重病體弱等新生兒的使用列入注意事項。本文回顧分析了我院 2012-2014 年應用夫西地酸治療的新生兒和小嬰兒血清膽紅素測定結果及臨床癥狀,探討夫西地酸對新生兒和小嬰兒肝功能的影響。
1 材料與方法
1.1 臨床資料
共納入半歲以下患兒 138 例,日齡 1~156 d,平均 67.24 d,均為新生兒肺炎、支氣管肺炎和肺炎病例,抗感染治療均僅使用夫西地酸,全部患兒均獲得臨床治愈。其中 64例患兒治療前后測定了總膽紅素(Tbil)、直接膽紅素(Dbil)、間接膽紅素(Ibil)、白蛋白(ALB)、丙氨酸轉氨酶(ALT)、天冬氨酸轉氨酶(AST)等指標,這些患兒按治療前的總膽紅素水平 35 μmol/L 為界分為高、低兩組[6],比 較其 間接 膽 紅 素 比 值 變 化 的 差 異 ;其 余74例患兒僅治療前測定了這些指標,治療后對黃疸的臨床表現進行了觀察。
1.2 安全性評價標準
安全性評價項目包括心電圖、血常規、尿常規、肝腎功能等指標,以及生命體征檢測與體格檢查等。不良事件與藥品的關聯性采用我國通用的6級評價標準,即:肯定、很可能、可能、可能無關、待評價和無法評價。評價為肯定、很可能、可能的不良事件判定為藥物不良反應。
1.3 治療用藥
注射用夫西地酸鈉粉針,0.125 g/支,成都天臺山制藥有限公司。患兒夫西地酸實際用藥量平均 為(18.95±1.05)mg ·kg-1·d-1, 平 均 用 藥 天 數為(8.92±3.18)d。
1.4 統計學方法
使用 SPSS19.0 版統計軟件分析。計量資料以均數±標準差表示,組間比較采用 t檢驗;計數資料采用卡方檢驗。
2 結果
2.1 用藥前后生化指標
應用夫西地酸治療后,Tbil值、Ibil值及Ibil/ Tbil比值均顯著下降(P<0.01)。64例患兒中,1例用藥前ALT、AST分別為75和196 U/L,用藥后下降為18和24 U/L;1例用藥前ALT、AST分別為73和38 U/L,用藥后升高至100和168 U/L,尚不確定與藥物或病毒感染有關;其他62例用藥前后的ALB、ALT、AST等指標均在正常范圍內。用藥前后的血液指標比較見表1。
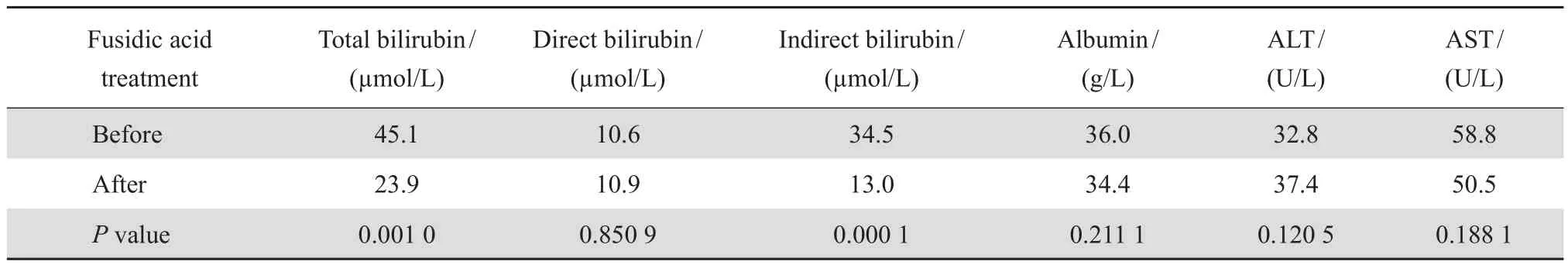
表1 64 例患兒用藥前后的血液指標比較Table 1 Change of serum biochemical markers after fusidic acid treatment (n=64)
2.2 不同水平膽紅素治療前后的下降情況
所有患兒感染性疾病治愈,可排除感染性疾病導致的病理性黃疸的影響。所有患兒在治療中均未應用白蛋白、血漿,3例治療前膽紅素水平較高的患兒應用了藍光照射治療。64 例患兒中有 16例治療前 Tbil在正常范圍內,治療后 9 例略有升高但仍在正常范圍內 ;48 例治療前 Tbil高于正常范圍上限的患兒,治療后9例略有升高,但升高幅度小于5%。
治療后有60.9%(39/64)的患者出現間接膽紅素比值(Ibil/Tbil)下降。其中,高膽紅素組的間接膽紅素比值(Ibil/Tbil)治療后下降了約13%,低膽紅素組下降了約7%,但兩組的變化值差異無統計學意義。兩組Tbil和Ibil的下降例數和下降值比較差異具有統計學意義(P<0.05)。見表2。
2.3 不同年齡組治療前后的膽紅素變化情況
將 64 例患兒分為新生兒組(≤28 d)和小嬰兒 組(>28 d) 各 32 例, 治 療 后 兩 組 的 Tbil值和 Ibil值均有降低,但新生兒組下降的更多 ;兩組 Dbil值 的 下 降 幅 度 差 距 較 小。 兩 組 Ibil/Tbil比值下降人數和變化值差異有顯著統計學意義(P <0.01)。見表3。
2.4 用藥前后的黃疸情況
用 藥 前 Tbil 高 于 35 μmol/L 的 32 例 患 兒 中,17例應用夫西地酸前后皮膚、鞏膜均無黃疸表現;其他 15 例治療前有黃疸表現的患兒,用藥后 12例黃疸消失,3例還有輕度黃疸。
用 藥 前 Tbil 低 于 35 μmol/L 的 106 例 患 兒,103 例用藥前后均未觀察到黃疸表現 ;余 3 例用藥前有輕度黃疸,用藥后1例減輕、2例消失。
3 討論
兒童使用夫西地酸的安全性臨床資料鮮有報道,新生兒使用更不多見。本研究主要針對新生兒用藥后的膽紅素指標進行分析。
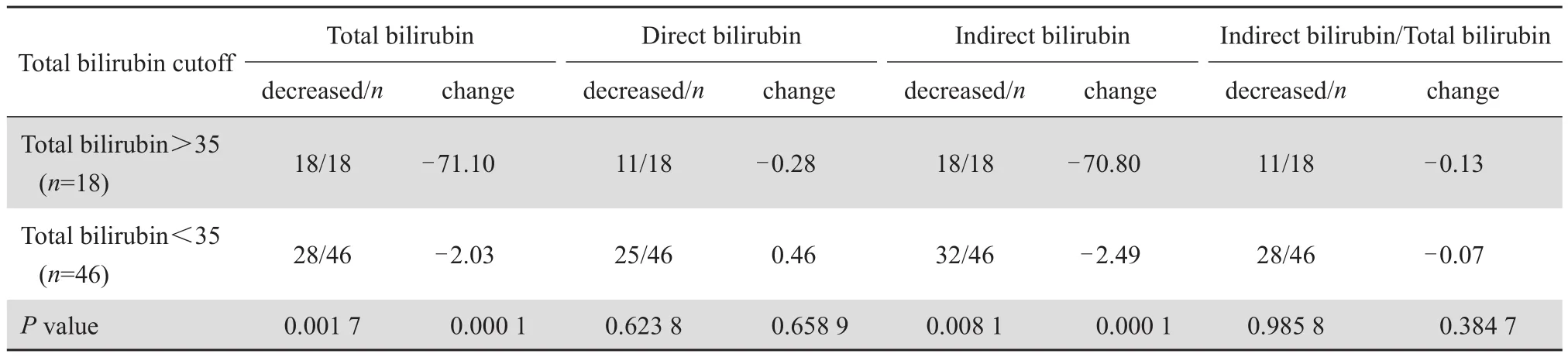
表2 64 例患兒按總膽紅素值分組用藥前后的膽紅素比較Table 2 Change of serum bilirubin levels after fusidic acid treatment in terms of total bilirubin value in 64 patients
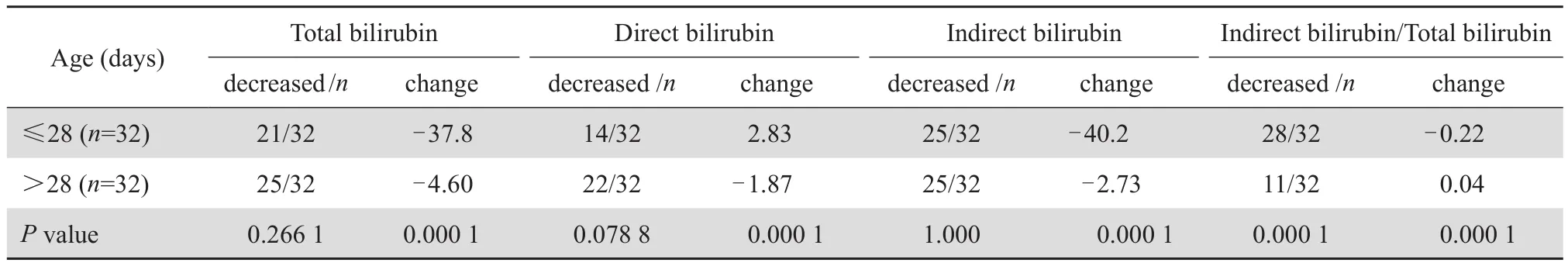
表3 64 例患兒按日齡分組用藥前后的膽紅素比較Table 3 Change of serum bilirubin levels after fusidic acid treatment in terms of patient age in 64 patients
3.1 夫西地酸對肝功能的影響
新生兒組 1 例用藥前 ALT、AST 分別為 73 U/ L、38 U/L,用藥后升高至 100 U/L、168 U/ L,達到輕度肝損傷標準,尚不確定是與藥物或病毒感染有關;1例用藥前 ALT、AST 均升高的患兒用藥后降到正常 ;其余 30例患兒用藥前后肝功能均在正常范圍。可見夫西地酸對新生兒肝臟功能無嚴重影響。
3.2 夫西地酸對血清游離膽紅素的影響
“血清游離膽紅素”并非指“未結合膽紅素(Ibil)”,而是指血清 Ibil中少量未與白蛋白結合的Ibil。實驗室血生化檢驗無法直接測定出游離 Ibil值,化驗單中的 Ibil值實際包括了“蛋白結合型Ibil”及未與白蛋白結合的“游離型 Ibil”[7]。夫西地酸在體外可競爭膽紅素與血清白蛋白結合,使血中未與白蛋白結合的 Ibil增加、與白蛋白結合的Ibil減少,最終使經肝細胞葡萄糖醛化的 Dbil減少。因此,假設夫西地酸顯著地競爭置換出膽紅素,血清中 Ibil/Tbil的比值就會明顯上升。而表1 的數據顯示,應用夫西地酸治療后的 Dbil數值并沒有顯著改變,Ibil/Tbil比值不但沒有上升、反而下降了約8%,表明“夫西地酸競爭置換出膽紅素”的情況并不明顯。
表2 和表3 的數據表明,Ibil/Tbil比值在高膽紅素組和新生兒組的下降幅度更大。這可能是因為部分新生兒組患兒治療前處于生理黃疸期,膽紅素超過了白蛋白的結合能力,從而導致治療前的 Ibil/Tbil比值偏高所致。
64 例患兒中,48 例治療前 Tbil高于正常范圍上限的患兒,治療后9例略有升高,但升高幅度小于5%。說明夫西地酸并不會顯著影響新生兒的血清游離膽紅素水平,這與體外實驗的結果并不相符,可能治療劑量的夫西地酸血藥濃度尚不足以影響血清膽紅素與白蛋白的結合。
3.3 夫西地酸導致黃疸的風險。
當血清膽紅素含量高于 34.2 μmol/L 時,肉眼可見鞏膜、黏膜、皮膚、體液等因膽紅素沉著而呈現的黃染[6]。而導致黃染的主要是游離型 Ibil。用藥的 138 例患兒中,用藥前有黃疸癥狀的 18 例患兒用藥后 4 例減輕、14 例消失 ;120 例用藥前沒有黃疸癥狀的患兒用藥后也未出現黃疸癥狀。即 使 是 用 藥 前 血 清 Tbil 高 于 35 μmol/L 的 組, 治療后也未出現皮膚黏膜黃染或黃染加重的情況,經皮測定的膽紅素值呈逐漸下降趨勢。
夫西地酸是一類抗革蘭陽性菌尤其葡萄球菌的藥物,兒童使用并不廣泛,尤其在新生兒。也有經典書籍中列入“早產兒和新生兒不推薦使用,2歲以上兒童可應用本品。”但綜合藥理學和藥物學書籍,新生兒并非使用禁忌證。本文對 64例患兒檢測了應用夫西地酸前后的血清膽紅素結果,同時對另外 74例患兒的用藥后黃疸情況進行了觀察,未發現黃疸加重或新發黃疸的情況。但由于新生兒和嬰幼兒應用夫西地酸還存在靜脈刺激和肝功能異常的報道[8-9],并不是治療感染的首選藥物,使用時還需注意觀察肝功能指標。
[1] GODTFREDSEN WO, JAHNSEN S, LORCK H, et al. Fuμsidic acid : a new antibiotic[J]. Nature,1962,193 :987-990.
[2] 陳衛東,劉雪芳 .夫西地酸鈉的藥理研究及臨床應用進展 [J].中國當代醫藥,2012,19(34):24-25.
[3] 李耘,薛峰,劉健 .夫西地酸體外抗菌活性研究 [J].中國臨床藥理學雜志,2013,29(1):34-37.
[4] CHRISTIANSEN K. Fusidic acid adverse drug reactions[J]. Int J Antimicrob Agents,1999,12(Suppl 2):s3-s9.
[5] BRODERSEN R. Fusidic acid binding to serum albumin and interaction with binding of bilirubin[J]. Acta Paediatr Scand,1985,74(6):874-880
[6] 胡亞美,江載芳,主編 .諸福棠實用兒科學 [M]. 7 版 .北京 :人民衛生出版社, 2002 :1378.
[7] 劉麗娟,樸梅花,李松 .血清游離膽紅素的相關因素的研究 [J].中國新生兒科雜志,2009,24(1):11-14.
[8] 岳林峰,張秀紅 .夫西地酸鈉致血清總膽汁酸升高 3 例 [J].實用醫學雜志,2009,25(24):4160.
[9] 余雄杰,王林霞,劉生友 .夫西地酸鈉相關肝損害 [J].藥物不良反應雜志,2010,12(2):134-135.
Effect of fusidic acid on bilirubin level in neonates and infants
YU Baodong.
(Department of Pharmacy, Qingdao Women & Children's Hospital, Qingdao Shandong 266034, China)
Objective To examine the change of bilirubin level in neonates and infants after administration of fusidic acid. Methods The data of serum bilirubin, alanine aminotransferasese (ALT), aspartate aminotransferase (AST) and adverse drug reaction were collected retrospectively in neonates and infants and compared statistically before and after administration of fusidic acid. Results Emerging jaundice or exacerbation of the existing jaundice was not found in all the 138 patients after administration of fusidic acid in this analysis. Biochemical markers were measured before and after use of fusidic acid in 64 of the patients. ALT, AST and albumin did not show significant difference before and after use of fusidic acid. However, the ratio between indirect bilirubin and total bilirubin decreased by about 8% after use of fusidic acid. Conclusions Fusidic acid did not show signif i cant effect on serum bilirubin level in the neonates and infants following fusidic acid treatment.
fusidic acid; bilirubin; adverse drug reaction; jaundice
R978.1
:A
:1009-7708 ( 2017 ) 03-0249-04
10.16718/j.1009-7708.2017.03.004
2016-03-17
2016-12-22
青島市婦女兒童醫院藥劑科,山東青島 266034。
于寶東(1972—),男,碩士,主管藥師,主要從事臨床藥學工作。
于寶東,E-mail:yubaodong2003@126.com。

