L-蘇氨酸分子印跡傳感器的制備及應用
袁愛國,李 斌,陳健平,肖麗杰,晉冠平*
(1.合肥工業大學 化學與化工學院,安徽 合肥 230009;2.汕頭市佳禾生物科技有限公司,廣東 汕頭 515021)
L-蘇氨酸分子印跡傳感器的制備及應用
袁愛國1,2,李 斌1,陳健平2,肖麗杰1,晉冠平1*
(1.合肥工業大學 化學與化工學院,安徽 合肥 230009;2.汕頭市佳禾生物科技有限公司,廣東 汕頭 515021)
采用電化學方法制備了納米銀/聚槲皮素修飾充蠟石墨電極(Ag/Qu/WGE)。以L-蘇氨酸(L-Thr)為模板分子,將一定量的殼聚糖,L-Thr和Nafion的混合液涂布在Ag/Qu/WGE上,采用恒電位法電化學清洗除去模板分子L-Thr,得到基于殼聚糖/納米銀/聚槲皮素的L-Thr分子印跡復合膜修飾電極(TMIP/WGE)。采用場發射掃描電鏡、紅外光譜分析、X射線光電子能譜和電化學技術表征了TMIP/WGE的形成。TMIP/WGE對L-Thr具有良好的電催化氧化作用,可用于L-Thr的快速、靈敏檢測,L-Thr的氧化峰電流(1.45 V)和其濃度在0.1~1.0 μmol/L范圍內呈良好的線性關系,檢出限(3σ)為0.01 μmol/L。該電極已成功用于蘇氨酸發酵液中L-Thr的檢測。
L-蘇氨酸(L-Thr);分子印跡膜;納米銀
L-蘇氨酸(L-Thr,α-氨基-β-羥基丁酸,C4H9NO3)是一種人與動物體內必需的氨基酸,具有抗潰瘍、防輻射、恢復體力和促進生長發育的作用,但動物自身不能合成,必須從食物中攝取[1-2]。目前國內外主要通過發酵法獲取蘇氨酸,蘇氨酸發酵液中主要包含蘇氨酸和其它雜質氨基酸(谷氨酸、異亮氨酸、苯丙氨酸等),以及菌體、殘糖、色素、膠體物質及其它發酵副產物[3-4]。靈敏快速地檢測發酵液中蘇氨酸含量具有重要的工業價值。
現有的測定蘇氨酸的分析方法有氨基酸分析儀測定法[4]、凱氏定氮法[4]、高效液相色譜法[5]、液相色譜-質譜聯用法[6]、液相色譜-紫外光譜聯用法[7]、氣相色譜法[8]、毛細管電泳法[9]、離子交換色譜法[7]和薄層色譜法[10]等。但上述方法存在樣品前處理復雜,氨基酸衍生化時間長,或實驗儀器價格昂貴等問題。電化學法因成本低、靈敏度高、簡便快速,已受到了廣泛關注。但是蘇氨酸分子無電化學活性,且常與其它氨基酸共存,目前為止,尚無檢測蘇氨酸的電化學傳感器報道。

圖1 L-蘇氨酸(A,L-Thr)和槲皮素(B,Qu)的結構式Fig.1 Structure formules of L-threonine(A) and quercetin(B)
L-Thr分子結構中存在羥基和胺基兩個活性基團(圖1A)。研究顯示:一定條件下,納米金屬修飾電極可電催化氧化含羥基和胺基的有機小分子[11-12]。殼聚糖和納米銀均具有良好的生物兼容性,且納米銀兼具優良的電催化活性[11]。研究采用電化學法在充蠟石墨電極上,制備了以L-Thr為模板印跡分子的殼聚糖/納米銀/聚槲皮素分子印跡復合膜修飾充蠟石墨電極(TMIP/WGE)。采用多種方法表征了電極的特性,考察了L-Thr在該電極上的電化學行為,并將該電極成功用于發酵液中L-Thr的檢測。
1 實驗部分
1.1 材料與試劑
所有電化學實驗在CHI660B(上海辰華儀器有限公司)上進行。電化學實驗采用常規的三電極系統,包括工作電極,鉑絲輔助電極,參比電極(飽和甘汞電極(SCE)或Ag/AgCl電極)。除非特別標明,本文的電位均相對于SCE。基體工作電極為本實驗室自制的充蠟石墨電極(WGE),幾何面積為0.125 cm2。JSM-600型場發射掃描電鏡(FE-SEM,日本,JEOL);ESCALAB MK2型X-射線光電子能譜儀(XPS,美國,Vg Corporation);IR 200型紅外光譜儀(IR,美國,Nicolet),H835-50 高效液相色譜(HPLC,日本日立公司)。
殼聚糖(Ch)購于上海源聚生物科技有限公司。L-蘇氨酸(L-Thr)、D-蘇氨酸、槲皮素(Qu)、硝酸銀、殼聚糖等其它試劑均購于上海化學試劑公司。0.1 mol/L磷酸鹽緩沖溶液(PBS)作為電化學實驗的支持電解質,由一定比例的磷酸、磷酸氫二鉀、磷酸二氫鉀溶液混合配制。實驗中所用藥品均為分析純。所有水溶液均用二次蒸餾水配制。實驗均在氮氣氛和室溫下進行。
1.2 Ag/Qu復合修飾電極的制備
將WGE電極依次在400,2 000及4 000目金相砂紙上研磨拋光如鏡面,然后分別在無水乙醇和二次水中超聲清洗10 min。將清潔后的WGE置于1.0 mmol/L Qu/0.1 mol/L PBS(pH 7.0)溶液中,通過循環伏安法(CV)修飾,得到聚槲皮素修飾充蠟石墨電極(Qu/WGE)[12]。將Qu/WGE電極界面在1.0 mmol/L AgNO3/0.1 mol/L LiNO3溶液中浸泡30 min后,取出在0.1 mol/L LiNO3溶液中進行CV還原,得到納米銀/聚槲皮素修飾充蠟石墨電極(Ag/Qu/WGE)。修飾好的電極保存在4 ℃水中。
1.3 TMIP/WGE的制備
將殼聚糖溶解在甲酸中制備成15 g/L的殼聚糖溶液;然后將L-Thr溶液(2 mmol/L)、殼聚糖溶液(15 g/L)和H2SO4溶液(2 mmol/L)按1∶3∶5的比例混合均勻,添加5%全氟磺酸樹脂(Nafion)10 μL,將混合溶液超聲振蕩均勻40 min。取20 μL懸濁液直接滴加在Ag/Qu/WGE電極界面上,在室溫下自然干燥,形成包含L-Thr模板分子的復合膜(MIP-Thr/WGE)。其后,將MIP-Thr/WGE在1.45 V下恒電位10 min,以洗脫L-Thr分子,得到分子印跡膜修飾電極[12],記為TMIP/WGE,保存在4 ℃的0.1 mol/L PBS(pH 7.0)溶液中。
1.4L-Thr測定
以TMIP/WGE為工作電極,鉑絲為對電極,甘汞電極為參比電極,在0.1 mol/L PBS(pH 7.0)中,電位范圍為0.9~1.5 V,掃速為50 mV/s,進行循環伏安掃描。記錄L-Thr樣品添加前后在1.45 V處的峰電流值。每次測定后,將L-Thr置于0.1 mol/L PBS(pH 7.0)溶液中,1.45 V下恒電位降解10 min以去除吸附的L-Thr。
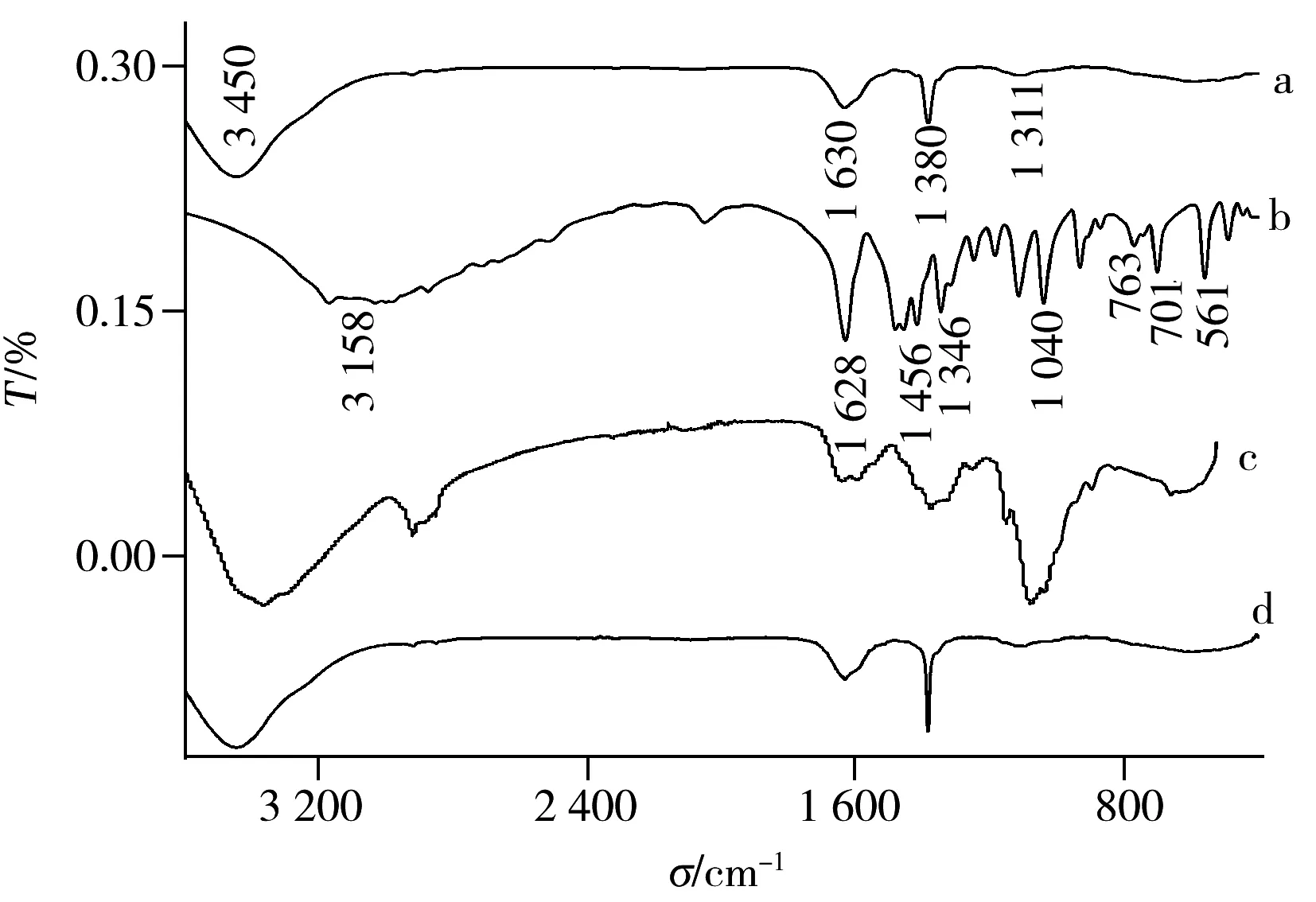
圖2 Ch/Ag/Qu/WGE(a),L-Thr(b),MIP-Thr/WGE(c)和TMIP/WGE(d)的紅外光譜圖Fig.2 IR spectra of Ch/Ag/Qu/WGE(a),L-Thr(b),MIP-Thr(c) and TMIP/WGE(d)
2 結果與討論
2.1 TMIP/WGE表征

2.1.2 FE-SEM圖 圖3A顯示電極界面上(Ag/Qu/WGE)存在大量的納米Ag粒子。將20 μL由L-蘇氨酸、殼聚糖、H2SO4和Nafion組成的懸濁液直接滴加在Ag/Qu/WGE界面上,室溫下自然干燥,制成含蘇氨酸印跡分子復合膜。圖3B為包含L-Thr模板分子的復合膜(MIP-Thr/WGE),和圖3A相比,該膜是致密和粗糙的。圖3C顯示,1.45 V下的恒電位洗脫10 min后,可使L-Thr分子從復合膜上脫落,從而形成多孔膜電極(TMIP/WGE)。

圖3 Ag/Qu/WGE(A),MIP-Thr/WGE(B)和TMIP/WGE(C)的FE-SEM圖Fig.3 FE-SEM images of Ag/Qu/WGE(A),MIP-Thr/WGE(B) and TMIP/WGE(C)
2.1.3 電化學表征 圖4A顯示了Qu在WGE上的循環伏安行為(CV),可觀察到在0.15/0.14 V處有1對氧化還原峰,其對應于 C環,而在0.78 V和1.1 V 處的兩個不可逆氧化還原峰則對應于A環中兩個羥基的氧化,在電極上產生的羥基自由基可進一步聚合成膜。隨著循環伏安的持續進行,0.78 V和1.1 V 處的兩個峰電流下降,這是由于電極上聚合物膜使傳質阻力增大所致。這一過程和酚類化合物的電化學聚合類似[11-12]。Qu兩個重要作用(圖1B):與裸WGE對Ag+的微弱吸附作用相比,可富集較多的Ag+,并得到均勻分散的納米Ag粒子;通過氫鍵吸附Ch,使Ch與膜緊密結合。圖4B為WGE(a),Qu/WGE(b)和Ag/Qu/WGE(c)在0.1 mol/L PBS(pH 7.0)溶液中的CV曲線。與曲線a相比,曲線b上0.15 V和1.10 V 處有兩個氧化峰,表明了聚槲皮素的存在。曲線c中0.15 V氧化峰明顯升高,這是由于納米銀對Qu的催化氧化。此外,在1.45 V 處出現1個氧化峰,對應于Ag→AgO→Ag2O的氧化過程[11]。表明Ag/Qu/WGE電極已形成。

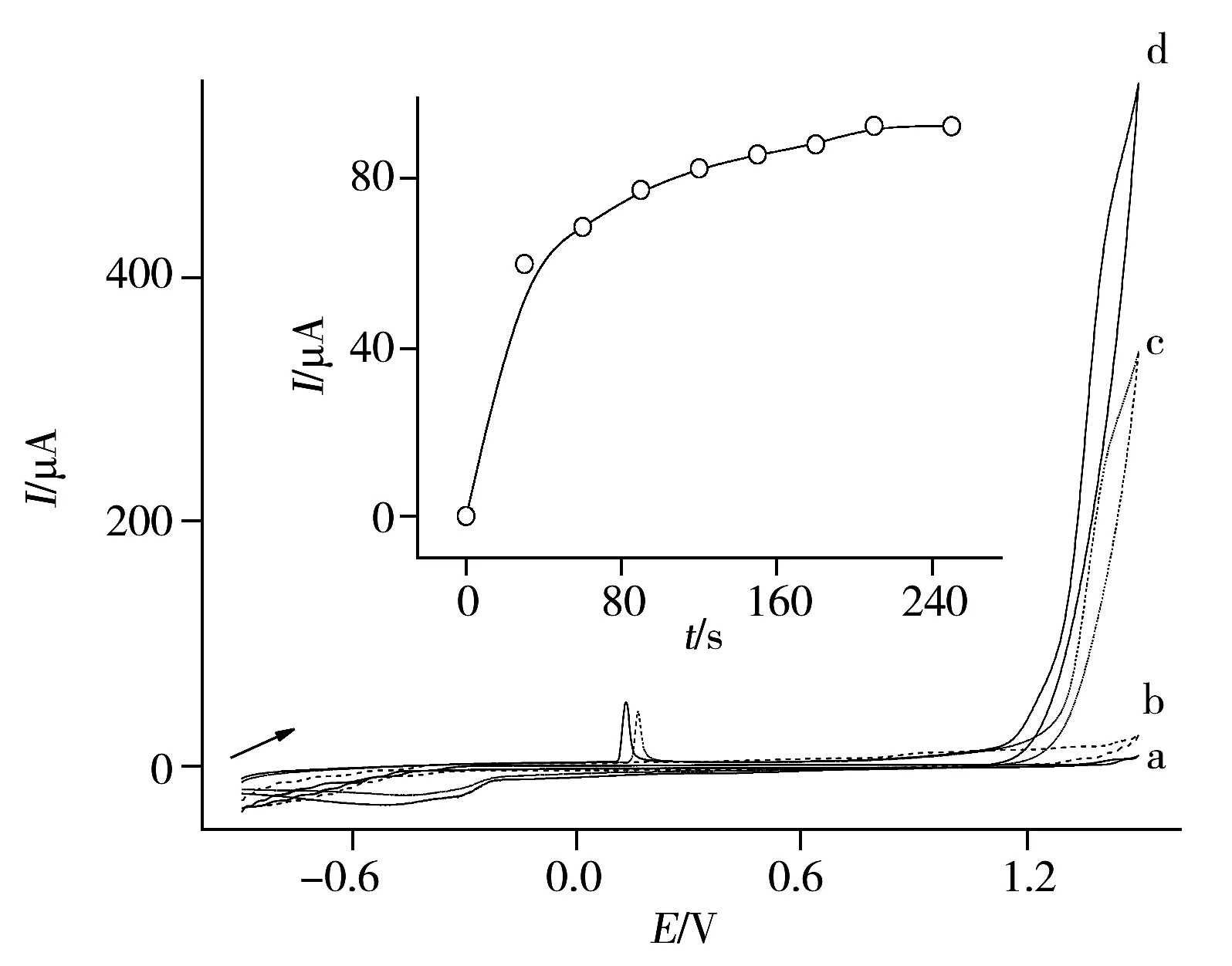
圖5 0.9 μmol/L L-Thr在WGE(a)、Qu/WGE(b)和TMIP/WGE(c)上的CV曲線,以及TMIP/WGE在PBS中的CV曲線(d)Fig.5 CVs of 0.9 μmol L-Thr at WGE(a),Qu/WGE(b),TMIP/WGE(c),and CV of TMIP/WGE in PBS buffer(d)scan rate:50 mV/s;buffer:0.1 mol/L PBS(pH 7.0)
2.2 蘇氨酸的測定
2.2.1 催化氧化機理 圖5為WGE(a),Qu/WGE(b),TMIP/WGE(c)在0.9 μmol/LL-Thr+0.1 mol/L PBS(pH 7.0)溶液中的CV曲線,曲線d為Ag/Qu/WGE在0.1 mol/L PBS(pH 7.0)中的CV曲線。可觀察到,L-Thr在WGE(a)和Qu/WGE(b)上均未出現氧化還原峰;相比于曲線d,當L-Thr存在時,0.15 V處氧化峰增高,1.45 V處氧化峰顯著升高(c),表明TMIP/WGE對L-Thr的氧化有較強的電催化作用,這為L-Thr的電化學檢測提供了依據。其可能的催化氧化機理為:L-Thr穿過印跡膜后被吸附富集在納米銀表面,納米銀降低了L-Thr分子中—NH2的活化能,在一定電位下,胺基易被催化氧化去氫[11-12],使其在1.45 V處的氧化峰升高。
2.2.2 富集時間的影響 以0.9 μmol/L的L-Thr為探針,考察了富集時間對L-Thr峰電流(1.45 V)的影響。結果顯示,隨著富集時間從0增加到120 s,L-Thr在TMIP/WGE上1.45 V處的峰電流差值(ΔI=IThr-I0)明顯增加,在200 s時達最大值,此后趨于平緩,表明吸附達到平衡。因此,本實驗選擇最佳富集時間為200 s。
2.2.3 方法的標準曲線 考察了不同濃度L-Thr在TMIP/WGE上的CV曲線。結果顯示,隨著L-Thr濃度的升高,L-Thr在1.45 V處的峰電流逐漸增大。當L-Thr的濃度為0.1~1.0 μmol/L時,其在1.45 V處的氧化峰電流差值(ΔI)與濃度呈良好的線性關系,線性方程為ΔI(μA)=43.15+116.5c(μmol/L),r=0.996 1,檢出限(3σ)為0.01 μmol/L。
2.2.4 選擇性與穩定性 以0.9 μmol/L的L-Thr為探針,研究了L-蘇氨酸發酵母液中可能共存的氨基酸[3-4],如D-蘇氨酸、谷氨酸、異亮氨酸、甘氨酸、苯丙氨酸、丙氨酸和脯氨酸對其測定的影響。結果顯示,100倍的干擾物在和L-Thr兩兩共存的情況下,L-Thr的回收率分別為8.8%,9.9 %,6.7%,3.5%,9.1%,8.0%和7.4%,L-Thr在1.45 V的峰電流回收率均小于10%,表明100倍的上述氨基酸均不干擾L-Thr的測定,即TMIP/WGE對L-Thr測定具有良好的選擇性。
以0.9 μmol/L的L-Thr為探針,研究了TMIP/WGE的穩定性和重現性。在冰箱保存7 d后,L-Thr在該電極上的電流響應為初始電流響應的96%,保存30 d后,其電流響應為初始電流響應的85%。表明TMIP/WGE具有良好的穩定性和重現性。每次測定后,將L-Thr置于0.1 mol/L PBS(pH 7.0)溶液中,1.45 V下恒電位降解10 min以去除吸附的L-Thr,其后置于4 ℃冰箱中保存。
2.3 實際樣品中L-Thr的測定
采用標準曲線法進行測定。取200 mL蘇氨酸發酵液,用陶瓷膜過濾去除較大顆粒雜質,用粒徑為0.45 μm的濾網膜過濾去除小顆粒雜質,取10.0 mL獲得的溶液,用0.1 mol/L PBS(pH 7.0)定容至500 mL(近似0.016 mol/L),作為母液。同法操作,逐步稀釋溶液,使其中L-Thr濃度約為0.5 μmol/L時,再進行電化學測定(EC),記錄1.45 V處L-Thr的峰電流差值(ΔI)。將不同體積的1.0 mol/LL-Thr標準液直接加入10.0 mL 蘇氨酸發酵液樣品中,通過標準加入法計算其中L-Thr的濃度,以計算加標回收率。結果顯示,L-Thr的氧化峰電流差值的回收率均在(100±3.0)%以內。
為了進一步驗證方法的準確性,實驗采用高效液相色譜(HPLC)[5]對蘇氨酸母液中L-Thr的含量進行檢測。由表1可見,本方法的測定結果可靠,可用于實際樣品的測定。
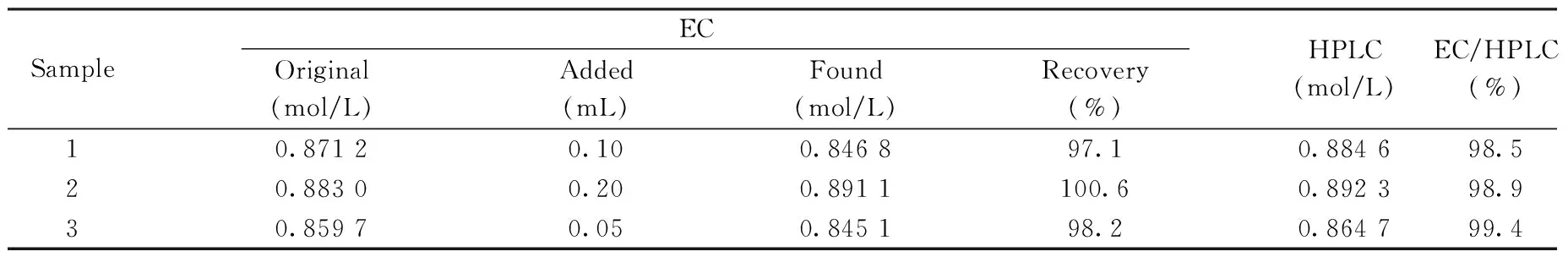
表1 電化學法測定L-Thr的回收率以及與HPLC法測定的比較Table 1 Spiked recoveries for electrochemical detection of L-Thr and comparison with method of HPLC
[1] Wang Z W,Fu J Z,Yang Z P,Sui M X,Zhang R L.Chin.Feed(王宗偉,付建中,楊志平,隋美霞,張汝雷,中國飼料),2015,12:23-26.
[2] Mastellar S L,Moffet A,Harris P A,Urschel K L.Veter.J.,2016,207:147-153.
[3] Fu Y,Wu G G,Peng Q J.Chin.J.Appl.Chem.(付勇,吳國光,彭奇均.應用化學),2007,24(4):452-456.[4] Lu W N.J.Biol.(盧偉寧.生物學雜志),2010,27(5):53-55.
[5] Zhu Y,Luo Y,Wang P,Zhao M,Li L,Hu X,Chen F.FoodChem.,2016,194:643-649.
[6] Chen R C,Chuang L Y,Tseng W L,Tyan Y C,Lu C Y.Anal.Biochem.,2013,443:187-196.
[7] Zhu F,Wang J,Zhu L,Tan L,Feng G,Liu S,Dai Y,Wang H.Talanta,2016,150:388-398.
[8] Oka K,Kimura T,Otsuka M,Ohmori S.J.Chromatogr.B,2006,830(1/2):173-177.
[9] Hamilton P B.Anal.Chem.Res.,1963,35:2055-2064.
[10] Poinsot V,Bayle C,Couderc F.Electrophoresis,2003,24:4047-4062.
[11] Zhao C,Jin G P,Chen L L,Yu B.FoodChem.,2011,129:595-600.
[12] Jin G P,Chen L L,Hang G P,Yang S Z,Wu X J.J.SolidStateChem.,2010,14(7):1163-1169.
[13] Blackwell J.MethodsinEnzymol,1988,161:430-435.
[14] Zhao X,Zhang L M,Gao W Y.Chin.J.Anal.Lab.(趙希,張黎明,高文遠.分析試驗室),2008,27:243-246.[15] Yang M.TheStudyofInfraredandRamanSpectraAminoAcidTransitionMetalComplex.Hangzhou:Zhejiang University of Technologys(楊末.氨基酸過渡金屬配合物的紅外與拉曼光譜研究.杭州:浙江工業大學),2008:56.
Preparation of a Molecularly Imprinted Film Modified Electrochemical Sensor forL-threonine Determination
YUAN Ai-guo1,2,LI Bin1,CHEN Jian-ping2,XIAO Li-jie1,JIN Guan-ping1*
(1.School of Chemistry and Chemical Engineering,Hefei University of Technology,Hefei 230009,China;2.Shantou City Jiahe Biologic Technology Co.Ltd.,Shantou 515021,China)
A nano-silver/poly quercetin composites modified paraffin-impregnated graphite electrode was prepared by electrochemical method(Ag/Qu/WGE).A mixture ofL-Thr,chitosan and Nafion was coated on the surface of Ag/Qu/WGE,L-Thr(template molecule) was removed by electrochemical cleaning using potentiostatic method.As a result,a molecular imprinted polymer modified electrode based on chitosan/nano-silver/poly quercetin composites could be obtained forL-Thr detection(TMIP/WGE).The characteristics of the modified electrode were investigated by means of field emission scanning electron microscope technique,X-ray photoelectron spectroscopy,infrared spectra and electrochemical technique.The result indicated that the TMIP/WGE displayed a good electro-catalysis towards the oxidation ofL-Thr,which could be used for sensitive and quick detection ofL-Thr.The differences of oxidation peak current ofL-Thr(1.45 V) showed a good linearity in the concentration range of 0.1-1.0 μmol/L with a detection limit(3σ) of 0.01 μmol/L.The electrode was successfully applied in the determination ofL-Thr in fermentation broth.
L-threonine(L-Thr);molecular imprinted polymer;nano-silver
10.3969/j.issn.1004-4957.2017.04.013
2016-10-09;
2016-12-30
2014廣東省協同創新與平臺環境建設專項及公益研究與能力建設專項資金(2014B0901010)
O657.1;O629.7
A
1004-4957(2017)04-0519-05
*通訊作者:晉冠平,博士,教授,研究方向:應用電化學,Tel:0551-62901450,E-mail:jgp@hfut.edu.cn

