經肛門內鏡顯微手術聯合放療治療早期直腸癌的效果分析
李青科,何立芳,耿學辰,馬國明,梁 磊,劉遠廷*(.河北省唐山市人民醫(yī)院胃腸外科,河北 唐山 063000;.河北省唐山市豐潤區(qū)人民醫(yī)院內分泌腎內科,河北 唐山 064000)
·論 著·
經肛門內鏡顯微手術聯合放療治療早期直腸癌的效果分析
李青科1,何立芳2,耿學辰1,馬國明1,梁 磊1,劉遠廷1*
(1.河北省唐山市人民醫(yī)院胃腸外科,河北 唐山 063000;2.河北省唐山市豐潤區(qū)人民醫(yī)院內分泌腎內科,河北 唐山 064000)
目的探討經肛門內鏡顯微手術(transanal endoscopic microsurgery,TEM)聯合術后放療治療早期直腸癌的的臨床效果。方法89例早期直腸癌患者術前經電子腸鏡、CT、MRI、腔內超聲等檢查證實為單發(fā)性病灶,無遠處轉移灶,無淋巴結轉移。腸壁浸潤深度為黏膜層或黏膜下層;術前病理取活組織檢查組織類型為中、高分化腺癌;術前均未行新輔助放化療。根據患者及家屬意愿分為TEM組42例和腹腔鏡下直腸癌根治術(腔鏡)組47例,分別采用TEM和腹腔鏡下直腸癌根治術;TEM組聯合術后放療。結果TEM組手術時間、住院時間、術中出血量、術后并發(fā)癥種類和例數均少于腔鏡組,差異有統(tǒng)計學意義(P<0.05)。結論TEM具有術中出血量少、手術時間短、術后并發(fā)癥少、術后恢復快、住院時間短的優(yōu)點,聯合術后放療治療早期直腸癌是安全可靠的,具有與腹腔鏡下直腸癌根治術相同的臨床療效。
直腸腫瘤;經肛門內鏡顯微手術;化放療
直腸癌是臨床最常見的消化道惡性腫瘤之一, 據2015年公布的全球癌癥統(tǒng)計結果顯示,目前直腸癌發(fā)病率男性和女性分別位居第3位,死亡人數占全部惡性腫瘤死亡總人數的8%~9%,居惡性腫瘤第4位,其發(fā)病率和病死率每年呈現上升趨勢[1]。隨著腫瘤醫(yī)學理論知識和診療技術的不斷發(fā)展,臨床上對早期直腸癌發(fā)現率逐步提高。對于早期直腸癌,外科切除仍是首選方法。但直腸癌外科切除不僅要注重是否根治性切除,還必須考慮患者術后生活質量,盡量避免術中永久性造瘺,損傷盆腔、腹下神經叢造成排便、排尿及性功能障礙。多學科聯合診治,綜合分析直腸癌患者病情,選擇合理的外科手術方式,制定安全有效的治療方案是治療直腸癌的關鍵。經肛門內鏡顯微手術(transanal endoscopic microsurgery,TEM)和腹腔鏡下直腸癌根治術都屬于微創(chuàng)手術,但是TEM為局部切除術。為了證實TEM局部切除術后聯合放療也能夠達到腹腔鏡下直腸癌根治術相同的療效,本研究對42例早期直腸癌患者采用TEM聯合術后放療,取得了較好效果,現報告如下。
1 資料與方法
1.1 一般資料 收集2013年1月—2015年1月河北省唐山市人民醫(yī)院胃腸外科收治的直腸癌患者89例,所有患者術前經電子腸鏡、CT、MRI、腔內超聲等檢查證實為單發(fā)性病灶,無遠處轉移灶,無淋巴結轉移;腸壁浸潤深度為黏膜層或黏膜下層;術前病理取活組織檢查組織類型為中、高分化腺癌;術前均未行新輔助放化療。臨床與病理分期采用美國癌癥聯合委員會TNM分期(2010版)。根據患者及家屬意愿分為TEM組42例,男性23例,女性19例,年齡42~78歲,平均(58.35±8.63)歲,腫瘤最大直徑(1.54±0.39) cm, 腫瘤距肛緣距離(5.52±1.44) cm;腹腔鏡下直腸癌根治術組(腔鏡組)47例,男性28例,女性19例,年齡45~76歲,平均(60.14±4.45)歲,腫瘤最大直徑(1.62±0.25) cm, 腫瘤距肛緣距離(5.34±1.38) cm。2組性別、年齡、腫瘤最大直徑差異均無統(tǒng)計學意義(P>0.05),具有可比性。
所有患者術前均簽署手術知情同意書。
1.2 手術器械 主要由特定的經肛直腸鏡、腹腔鏡顯像系統(tǒng)和專用手術器械組成。手術應用德國進口STORZ手術系統(tǒng)設備,特殊的直腸鏡外徑4 cm,常用長度有2種型號分別為10 cm、20 cm(圖1)。直腸鏡前端是一斜形切口,當光源通過此切口時,術者能觀察到更寬闊的視野范圍;其后端是手術操作入口平臺(圖2),此平臺上有一主接口與腹腔鏡高清顯像裝置對接作為TEM顯像系統(tǒng)(圖3),通過光源攝像,術野能夠清晰地呈現在顯示屏上。為了維持直腸腔內壓力相對恒定,在直腸鏡光源攝像裝置旁有一充氣孔,與恒量恒壓氣腹機對接,使充入腸腔內CO2壓力保持相對穩(wěn)定,一般維持在12~15 mmHg。腸腔內壓力過大會造成腸壁過度擴張,壓力過小無法使腸腔充盈建立有效的視野。另外,在操作平臺下方有專用手術器械通過的袖套式密封進口。調節(jié)雙球關節(jié)活動機械臂裝置(Martin臂)將選定型號的直腸鏡固定在手術臺上,防止脫落(圖4)。專用的手術器械包括針形高頻電刀、5 mm超聲刀、無損傷腸鉗、分離鉗、注射針、施夾器和吸凝棒等(圖5)。
1.3 手術方法 常規(guī)術前腸道準備,給予復方聚乙二醇電解質散配置成2 000 mL溫水沖服導瀉;術前30 min預防性給予抗生素。麻醉方法多采用靜脈吸入復合全身麻醉或腰硬聯合麻醉。為利于術中手術操作,在擺放患者體位時需根據腫瘤所在腸壁位置調整合適體位,使腫瘤位置完全暴露在操作視野近下方。如腫瘤位于直腸前壁,需擺成折刀位;如腫瘤位于直腸后壁,需擺放成頭低足高截石位;如腫瘤位于直腸側壁,需擺放成側臥位。體位擺放合適后,會陰肛門部常規(guī)消毒,鋪蓋無菌手術巾,充分擴肛后放置長度合適的直腸鏡,調節(jié)操作視野范圍,用Martin臂將其固定于手術臺上,防止滑脫。為擴大視野持續(xù)注入CO2(最大速率為6 L/min左右),氣壓一般控制自動調節(jié)為12~15 mmHg。確定無CO2氣體外漏后,在腔鏡顯像系統(tǒng)輔助下進行操作(圖6),距離腫瘤邊緣至少1 cm的黏膜下層注射腎上腺素鹽水(1∶200 000),用針形電刀電灼標記切除邊界,沿著預先標記線仔細切除,對T1期直腸癌行全層切除,以保證腫瘤完整切除(圖7,8)。切除后的腫瘤組織標本展平快速冰凍送病理檢查以明確病變性質及環(huán)周切緣情況。若術中切緣回報陽性或出現大出血等并發(fā)癥時,需中轉腹腔鏡下直腸癌根治術。檢查有無活動性出血,止血確切后取合適長度的3-0號可吸收線,尾端銀夾固定,給予連續(xù)縫合后再次銀夾固定或采用3-0號可吸收倒刺線連續(xù)縫合創(chuàng)面(圖9)。創(chuàng)面用蒸餾水沖洗后,關閉氣腹機,退出直腸鏡。
1.4 術后放療 患者在術后2~4周內開始輔助放療。均行盆腔三維適形放療,6 MV X線,依據腫瘤位置選擇放射野,照射范圍為瘤床、直腸系膜和盆腔淋巴引流區(qū),劑量是全盆腔DT 45~50 GY/5周。給予每日4野照射,每周5次,總共5周的放療計劃。放療過程中均未出現腸梗阻,出現的腹瀉、骨髓抑制、膀胱炎等并發(fā)癥經對癥處理后好轉。
1.5 統(tǒng)計學方法 應用 SPSS 16.0統(tǒng)計學軟件處理數據。計量資料比較采用獨立樣本的t檢驗;計數資料比較采用χ2檢驗。P<0.05為差異有統(tǒng)計學意義。
2 結 果
2.1 2組手術時間、住院時間、術中出血量比較 89例患者均成功完成手術,未出現中轉其他術式者。TEM組手術時間、住院時間、術中出血量均少于腔鏡組,差異有統(tǒng)計學意義(P<0.05),見表1。
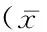
表1 2組手術時間、住院時間及術中出血量比較 ±s)
2.2 2組術后并發(fā)癥比較TEM組術后并發(fā)癥的種類和例數均少于腔鏡組,差異有統(tǒng)計學意義(χ2=11.766,P<0.05),見表2。

表2 2組術后并發(fā)癥比較 (例數)
2.3 隨訪 隨訪時間截至2016年1月,主要采用門診隨訪形式,并輔以電話隨訪。術后2年內,每3~6個月復查1次;第3年開始,每6個月復查1次。電話隨訪每月1次。復查主要包括血常規(guī)、腫瘤標志物系列、腹部盆腔CT、電子腸鏡。目前89例患者均在隨訪過程中(隨訪時間均>12個月),未出現腫瘤復發(fā)、轉移,未出現死亡病例。
3 討 論
臨床上對于已確診的直腸癌患者,在符合手術指征的情況下首選外科手術治療。經腹會陰聯合直腸癌根治術、直腸癌前切除術是臨床上治療直腸癌的常用手術方式,盡管兩者存在較高并發(fā)癥,降低患者術后生活質量(如永久造瘺,排便、排尿困難及性功能障礙等)[2-3],但是能確保腫瘤完整切除,同時清掃周圍淋巴結,預防腫瘤復發(fā),提高無瘤生存期。然而,有臨床研究顯示對于早期直腸癌采用根治術仍有過度手術治療之嫌[4],盡管其能夠清掃周圍淋巴結,但是存在較高并發(fā)癥,弊大于利。
19世紀初Lisfranc報道成功地采用局部切除術方法治療低位直腸癌(癌腫距肛緣距離≤7cm)以來,局部切除術作為一種可根治性切除腫瘤的方式或姑息性切除腫瘤的方式,在臨床上治療直腸癌逐漸被接受,越來越多的的文獻對其加以報道[5-6]。癌腫侵犯直腸黏膜的深度與淋巴結發(fā)生轉移密切相關。有學者通過研究直腸癌浸潤腸壁深度與淋巴結轉移關系,表明直腸黏膜幾乎無淋巴引流,當癌灶局限于黏膜時幾乎不會發(fā)生淋巴結轉移[7]。當病灶侵犯到黏膜下層時就會有發(fā)生淋巴結轉移的可能;當病灶侵犯到腸壁肌層時,淋巴結轉移的發(fā)生率會明顯增加。這一觀點已成為直腸癌可行局部切除術的理論基礎。研究顯示直腸癌T1、T2期病變的淋巴結轉移率分別為10.1%、23%[8]。因此有學者認為對直腸癌(病變僅侵及黏膜層)癌灶及其周圍1cm行腸壁全層切除也能達到根治的目的。
近年來,隨著人類對醫(yī)學理論和臨床實踐的不斷探索與研究,外科手術治療直腸癌的選擇上不斷更新交替,有相關文獻報道對于早期直腸癌(T1N0M0),局部切除術甚至可以代替?zhèn)鹘y(tǒng)根治性手術。TEM是一項治療直腸腫瘤較新的局部切除術式,由德國Buess首次應用于臨床,可以做到微創(chuàng)、視野暴露好、精確切除,能夠在內鏡下完整切除、止血、縫合等操作,同時兼?zhèn)鋫鹘y(tǒng)的經肛門局部切除術與內鏡下腸黏膜切除術2種術式的優(yōu)點,具有手術時間短、術中及術后并發(fā)癥少、創(chuàng)傷小、術后恢復快、住院時間短的優(yōu)勢,逐漸用于治療直腸癌[9-11]。本研究結果與文獻報道大致相仿。
局部復發(fā)與原病灶腫瘤大小、分化程度、浸潤腸壁深度及淋巴結轉移密切相關。TEM治療早期直腸癌(T1期)導致術后局部復發(fā)的危險因素包括癌腫侵犯腸壁達到黏膜下深度、環(huán)周切緣陽性、腫瘤最大直徑大小、臨床分期、有無淋巴結轉移、年齡等[12]。TEM屬于局部切除,其主要缺陷是不能清掃可能受累的淋巴結。盡管術前腔鏡超聲、盆腔MRI診斷無淋巴結轉移,但實際上對于與正常淋巴結大小相似的轉移淋巴結很難明確診斷。局部復發(fā)的主要原因是淋巴結發(fā)生轉移。直腸癌對放療敏感,通過放療殺滅亞臨床病灶和潛在轉移淋巴結,對預防局部復發(fā)有重要意義。目前尚無Ⅰ類證據證明直腸癌局部切除術后采取輔助放療是否使患者最大受益。有大量研究術后放療可有效降低直腸癌復發(fā)率,延長局部復發(fā)時間[13-14]。也有觀點認為對Ⅰ期低位直腸癌(分化程度好,未侵及脈管)患者行單純局部切除術療效可能較好,對高危者(分化程度低和侵及淋巴、血管)術后放療價值待商榷。本研究中TEM組術后均采用盆腔三維適形放療能夠降低因手術不能切除直腸系膜,留有潛在轉移淋巴結從而導致術后可能復發(fā)的風險。三維適形放療不僅可以使腫瘤靶區(qū)受到較高劑量照射,而且最大限度地保護周圍正常組織,有效提高腫瘤靶區(qū)的照射率。三維適形放療操作簡便,實用性強,與常規(guī)放療相比具有不良發(fā)應少的特點,從而提高患者生活質量。有報道顯示盆腔三維適形放療技術對放療劑量均勻性控制優(yōu)勢明顯,術后復發(fā)率低,直腸癌術后宜采用盆腔三維適形方法進行放射治療[15]。TEM術后放療,由于病理診斷明確,術中原病灶處留有銀夾,使得瘤床范圍更加準確,從而能避免過度治療,相對也減少了放療不良發(fā)應。
綜上所述,早期直腸癌患者行TEM治療,必須嚴格把握手術適應證,術前應全面檢查評估,對分化程度較好、未見淋巴結轉移等低危T1N0M0期直腸癌患者可行TEM,TEM聯合術后放療治療早期直腸癌可以最小的創(chuàng)傷使患者受益最大化。(本文圖見封三)
[1]SiegelRL,MillerKD,JemalA.Cancerstatistics,2015[J].CACancerJClin,2015,65(1):5-29.
[2]XuY,ZhuJY,ChangEI,etal.Weaklysupervisedhistopathologycancerimagesegmentationandclassification[J].MedImageAnal,2014,18(3):591-604.
[3] 姚明輝,張寧夫.直腸癌外科手術的新進展[J].中國社區(qū)醫(yī)師:醫(yī)學專業(yè),2013,15(7):6.
[4]AtallahS,NassifG,PolavarapuH,etal.Robotic-assistedtransanalsurgeryfortotalmesorectalexcision(RATS-TME):adescriptionofanovelsurgicalapproachwithvideodemonstration[J].TechColoproctol,2013,17(4):441-447.
[5]RestivoA,ZorcoloL,D'AliaG,etal.Riskofcomplicationsandlong-termfunctionalalterationsafterlocalexcisionofrectaltumorswithtransanalendoscopicmicrosurgery(TEM)[J].IntJColorectalDis,2016,31(2):257-266.
[6]OsmanKA,RyanD,AfsharS,etal.Transanalendoscopicmicrosurgery(tem)forrectalcancer:universityhospitalofnorthteesexperience[J].IndianJSurg,2015,77(Suppl3):930-935.
[7] 柯群剛,黃繼超,郝占偉,等.T1~2期原發(fā)性直腸癌患者淋巴結轉移的相關因素分析[J/CD].中華臨床醫(yī)師雜志:電子版,2015,9(14):2649-2651.
[8] 張曉路,王鑫,徐巖,等.T2期直腸癌淋巴結轉移情況的臨床病理因素分析[J].中國醫(yī)科大學學報,2014,43(2):142-145.
[9] 林國樂,邱輝忠,周皎琳,等.經肛門內鏡微創(chuàng)手術治療直腸腫瘤的臨床研究[J].中國全科醫(yī)學,2016,19(3):254-259.
[10] 任輝,宮路路,劉晶晶,等.經肛門內鏡下手術治療直腸腺瘤和早期直腸癌[J/CD].中華結直腸疾病電子雜志,2013,2(3):119-122.
[11] 黃和艮,劉飛.TEM與腔鏡治療中上段早期直腸癌臨床比較[J].結直腸肛門外科,2015,21(2):103-105.
[12] 田衍,羅華友.老年直腸癌根治術后局部復發(fā)的危險因素分析[J].中國普通外科雜志,2014,23(4):533-536.
[13] 梁博,屈國普,曾彪,等.直腸癌術后調強放療不同射野參數的劑量學對比[J].醫(yī)療裝備,2016,29(13):28-30.
[14] 高浩基,張弢,趙任,等.影響直腸癌術后局部復發(fā)的因素[J].中華胃腸外科雜志,2015,18(11):1176-1179.
[15] 劉可佳.直腸癌術后盆腔三維適形放療、簡化強調技術和適形調強放療的三維劑量學比較分析[J].中國當代醫(yī)藥,2015,22(14):60-62.
(本文編輯:許卓文)
2016-11-15;
2017-02-06
李青科(1981-),男,河北邢臺人,河北省唐山市人民醫(yī)院主治醫(yī)師,醫(yī)學碩士,從事胃腸外科疾病診治研究。
*通訊作者。E-mail:Helifang1125@126.com
R735.37
B
1007-3205(2017)04-0461-05
10.3969/j.issn.1007-3205.2017.04.022

