Box-Benhnken響應面優化銀杏葉總黃酮提取物泡騰片的制備及其質量分析
王京龍,鄭丹丹,張立華,王 飛,王占一,楚文超
(1.棗莊學院生命科學學院,山東棗莊 277160;2.鄭州大學藥學院,河南鄭州 450001)
Box-Benhnken響應面優化銀杏葉總黃酮提取物泡騰片的制備及其質量分析
王京龍1,鄭丹丹1,張立華1,王 飛1,王占一1,楚文超2
(1.棗莊學院生命科學學院,山東棗莊 277160;2.鄭州大學藥學院,河南鄭州 450001)
為制備銀杏葉總黃酮提取物泡騰片劑,本文以崩解時限、pH為評價指標,采用Box-Benhnken響應面實驗優化泡騰崩解劑配比(碳酸氫鈉:檸檬酸)、泡騰崩解劑總質量、聚乙二醇6000用量,并通過片劑重量差異、崩解時限、pH、發泡量、總黃酮的含量,對產品進行質量控制。結果表明,泡騰崩解劑最佳配比為1∶1.21,泡騰崩解劑的總量最佳質量分數為46.15%,PEG 6000的最佳質量分數為6.02%。最優工藝條件下制備的泡騰片,平均片重(500±21) mg,每片總黃酮含量為(4.80±0.08) mg,崩解時限、pH和發泡量符合藥典規定,制備的銀杏葉提取物泡騰片外觀良好,崩解迅速,溶解后溶液澄清透明、呈弱酸性。
銀杏葉提取物,泡騰片,Box-Benhnken響應面實驗,制備工藝,質量分析
銀杏(GingkobilobaL.)又叫做公孫樹、白果,是我國特有物種。2015年版《中國藥典》中記載,銀杏葉具有活血化瘀、通絡止痛、斂肺平喘、化濁降脂的功效[1]。同時,銀杏葉也常被加工成泡茶飲用,屬于“藥食同源”的范疇。銀杏葉的活性成分主要包括黃酮類、萜內酯類、多糖類、有機酸類等[2]。目前從銀杏葉中分離的黃酮類化合物有40多種,根據分子結構不同可分為黃酮、黃酮醇及其苷、雙黃酮和兒茶素等幾大類,其中黃酮(醇)苷類是主要活性成分[3]。同時,銀杏葉黃酮具有抗氧化[4]、保護心腦血管[5]、保肝[6-7]、抗腫瘤[8-9]等生理活性。
相對于傳統制劑,泡騰片具有分散快速,生物利用度高的優點[10-11],同時口感適宜,服用順從性好。目前,針對銀杏葉開發的藥品或保健食品主要有普通片劑、分散片、口服液、顆粒、丸劑、膠囊劑、注射液以及茶劑等[12],還未見有將銀杏葉開發成泡騰片的專利報道。而且,有關銀杏葉泡騰片制備工藝優化的文獻較少,僅有胡林水等人采用正交實驗對枸櫞酸、碳酸氫鈉用量以及是否采用聚乙二醇包裹進行考察[13]。
Box-Behnken中心組合設計通過二次多項式或更高次項的模型擬合,能同時進行線性、兩因素相互作用考察,從而更直觀、準確地優化得到最佳工藝條件[14]。本研究首次采用Box-Benhnken響應面優化法[15-16],以檸檬酸和碳酸氫鈉用量比例,總量以及PEG6000的量為考察因素,對銀杏葉泡騰片的制備工藝進行優化,制定工藝參數,以期制備出口感良好、食用方便、起效迅速、具有一定保健功效植物源保健品。
1 材料與方法
1.1 材料與儀器
銀杏葉 安徽亳州中藥飲片公司;蘆丁(批號:100080-201409) 中國食品藥品檢定研究院;檸檬酸、碳酸氫鈉、無水乙醇 天津市福晨化學試劑廠;聚乙二醇6000、甘露醇、乳糖 天津市風船化學試劑科技有限公司;亞硝酸鈉等試劑 均為分析純。
UV-4802雙光束紫外-可見分光光度計 上海尤尼柯儀器有限公司;PHS-3C pH計、FA1104電子分析天平 上海儀電科學儀器股份有限公司;DHG-9246A電熱鼓風干燥箱 上海精宏實驗設備有限公司;VH-2精品實驗用混合機 常州市龍湖干燥工程有限公司;YK60小型實驗室顆粒機 長沙市楚泰制藥機械設備有限公司;2P-5A旋轉式壓片機 青州市精誠醫藥裝備制造有限公司;片劑四用測定儀 上海黃海藥檢儀器有限公司。
1.2 實驗方法
1.2.1 銀杏葉提取物的制備 準確稱取銀杏葉粉45.0 g,8%氫氧化鈉溶液調節pH至10,回流提取(溫度95 ℃,料液比1∶40,煎煮時間60 min),粗濾,4000 r·min-1離心25 min,上清液用稀鹽酸調節pH至3.5,靜置24 h抽濾,沉淀物水洗至中性[17],60 ℃烘箱中烘干得干浸膏,研磨過80目篩,即得銀杏葉總黃酮提取物(總黃酮質量分數為22.32%)。
1.2.2 銀杏葉提取物泡騰片的制備工藝 稱取PEG6000適量,60 ℃左右恒溫水浴鍋中水浴融化,加入處方量碳酸氫鈉,快速攪拌直到完全熔融,冷卻后變成固體,研磨,過80目篩制成分散體。采用濕法制粒將分散體、檸檬酸、銀杏葉提取物、乳糖/甘露醇(8∶1)按照處方混合均勻,以95%乙醇作為粘合劑制軟材,制粒,顆粒在50 ℃左右烘干,20目篩整粒,控制空氣相對濕度在30%以下,進行顆粒壓片。
1.2.3 銀杏葉提取物泡騰片處方優化單因素實驗 銀杏葉片收載于《中國藥典》2015年版一部,規定每片含總黃酮不少于9.6 mg,參照此標準,結合本實驗泡騰片的質量(規格:0.5 g),模擬計算可知,固定銀杏葉提取物在處方中的比例為4.3%,每2片銀杏葉泡騰片可相當于1片普通銀杏葉片來使用。
為優化泡騰片制備工藝,固定銀杏葉提取物的質量分數4.3%,以泡騰片崩解時限、pH作為評價指標,考察泡騰崩解劑配比、泡騰崩解劑質量分數、PEG 6000用量三個因素對泡騰片質量的影響。另外,選擇乳糖與甘露醇作為稀釋劑,二者的吸濕性都較低,同時,在本制劑中銀杏葉提取物有苦味,可以起到矯味的作用。由于甘露醇具有較強的利尿作用,不宜過多,所以在實驗中選擇乳糖和甘露醇的比例為6∶1、7∶1、8∶1、9∶1、10∶1進行優化,結果在乳糖∶甘露醇為8∶1時,口感、泡騰效果最好。
1.2.3.1 泡騰劑堿酸比單因素實驗 固定泡騰崩解劑質量分數為45%,PEG 6000用量6%,選擇碳酸氫鈉∶檸檬酸質量比為1∶0.6、1∶0.8、1∶1.0、1∶1.2、1∶1.4,按1.2.2項下方法制備銀杏葉泡騰片,測定其崩解時限、溶解后溶液的pH(n=3),以篩選泡騰劑的酸堿比。
1.2.3.2 泡騰崩解劑總質量單因素實驗 同法,固定碳酸氫鈉:檸檬酸質量比為1∶1.2,PEG6000用量6%,選擇崩解劑質量分數為30%、35%、40%、45%、50%,按1.2.2項下方法制備銀杏葉泡騰片,篩選泡騰崩解劑的總質量。
1.2.3.3 PEG6000用量單因素實驗 同法,固定碳酸氫鈉:檸檬酸質量比為1∶1.2,泡騰崩解劑質量分數為45%,選擇PEG 6000用量為2%、3%、4%、5%、6%、7%、8%,篩選PEG 6000用量。
1.2.4 響應面法優化銀杏葉泡騰片制備工藝 結合單因素實驗結果,選擇泡騰崩解劑配比、泡騰崩解劑總質量、PEG6000用量三個因素作為Box-Benhnken設計中的考察對象,以崩解時限為評價指標,對泡騰片的處方進行優化,實驗因素和水平見表1。
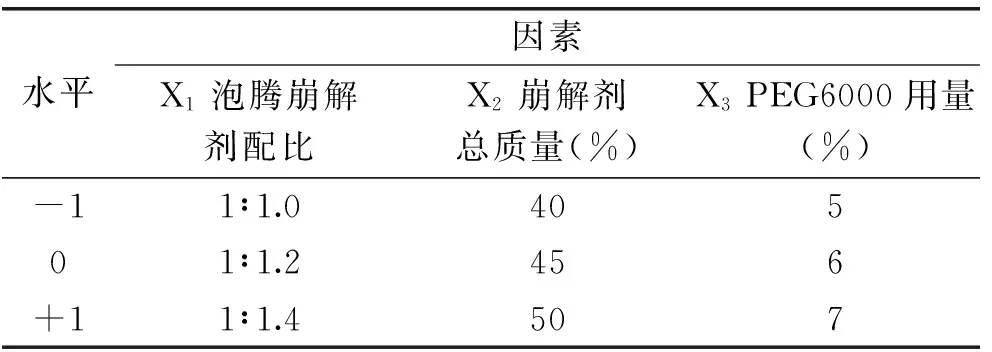
表1 Box-Benhnken實驗設計因素水平
1.2.5 工藝驗證 按1.2.4項下所得優化工藝條件制備泡騰片3批,以崩解時限為指標進行工藝驗證。
1.2.6 銀杏葉提取物泡騰片的質量分析
1.2.6.1 重量差異測定 取自制泡騰片20片,精密稱定重量,超出片重差異限度的不得多于2片,并不得有1片超出限度1倍。
1.2.6.2 崩解時限的測定 取本品1片,置于盛有200 mL溫水(約20 ℃)的燒杯中,待片劑周圍氣體停止逸出時,片劑應在5 min內溶散完全無殘留(n=6)。
1.2.6.3 pH測定 取泡騰片6 片,分別分散于100 mL、20 ℃蒸餾水中,測定各溶液的pH。
1.2.6.4 發泡容量檢查 采用質量損失法,取泡騰片1片,研磨,精密稱取片粉適量(1 g左右),置于已精密稱質量的含水燒杯中,待其發泡完全,再精密稱定燒杯及溶液總質量,計算CO2的體積(n=6)。CO2氣體生成越多,此配方泡騰效果就越好。
1.2.6.5 泡騰片中總黃酮的含量 制備0.20 mg/mL的蘆丁對照品溶液,再精密量取1、2、3、4、5、6 mL,置25 mL容量瓶中,分別加水至6 mL,加入5%亞硝酸鈉溶液1 mL,搖勻后靜置5 min;加入10%硝酸鋁溶液1 mL,搖勻后靜置6 min;加入4%氫氧化鈉溶液10 mL,用蒸餾水定容至刻度,搖勻后靜置15 min顯色。同法制備空白對照溶液,立即在500 nm波長下用紫外-可見分光光度計測定吸光度[18],并以吸光度(A)為縱坐標,蘆丁濃度(C)為橫坐標,進行線性回歸,得回歸方程A=11.261C-0.0135(R2=0.9980)。
稱取自制泡騰片20片,搗碎,取1.5 g粉末,95%乙醇溶液溶解,搖勻,定容至100 mL,作為供試品溶液。精密吸取供試液5 mL,同法測定,計算銀杏葉泡騰片中總黃酮的含量。
1.3 統計分析方法
使用SPSS 20.0數據統計軟件對結果進行分析。
2 結果與分析
2.1 銀杏葉提取物泡騰片處方優化單因素實驗結果
2.1.1 泡騰劑配比單因素實驗結果 預實驗中,對酸源(檸檬酸、酒石酸、富馬酸)進行了初步篩選,酒石酸所制泡騰片泡騰效果較好,但泡騰后的水溶液易顯渾濁或沉淀,影響色澤觀感和口感;富馬酸所制泡騰片泡騰效果不好,崩解時限最慢;相比前二者,檸檬酸的泡騰效果較佳,口感、色澤也較好。表2為泡騰劑配比對片劑崩解時限和pH的影響,結果顯示,當碳酸氫鈉∶檸檬酸質量比為1∶1.2時,泡騰片崩解時限最短。口感方面,如果堿源比例過大,泡騰片溶液容易發澀,酸源比例過大,pH太小,也不利于口感。綜合考慮,選取泡騰崩解劑配比在1∶1.0~1∶1.4范圍內進行響應面實驗。
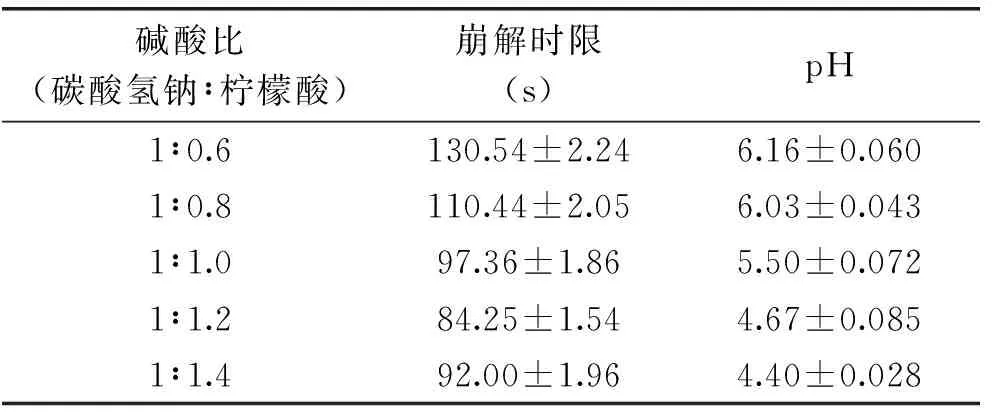
表2 泡騰劑配比對片劑崩解時限和pH的影響
2.1.2 泡騰崩解劑總質量單因素實驗結果 表3為泡騰劑總量對片劑崩解時限和pH的影響,結果顯示,當崩解劑總質量分數在45%時,泡騰片崩解時限最短,崩解劑總質量分數對pH的影響不大。綜合考慮,選取泡騰崩解劑配比在40%~50%范圍內進行響應面實驗。
2.1.3 PEG 6000用量單因素實驗結果 在制粒壓片過程中,PEG 6000用量為2%、3%、4%時制成的顆粒較松散,壓片不易成片;PEG 6000用量為8%時,由于PEG 6000用量較多,所形成的分散體呈塊狀不易研磨,易造成損失。PEG 6000用量為6%時,泡騰片崩解時限最短。綜合考慮,PEG 6000質量分數在5%~7%范圍內進行響應面實驗。
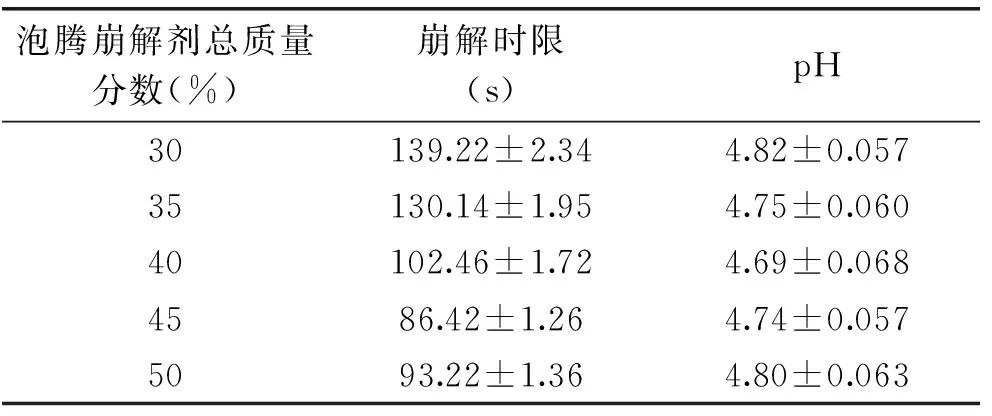
表3 泡騰劑總量對片劑崩解時限和pH的影響
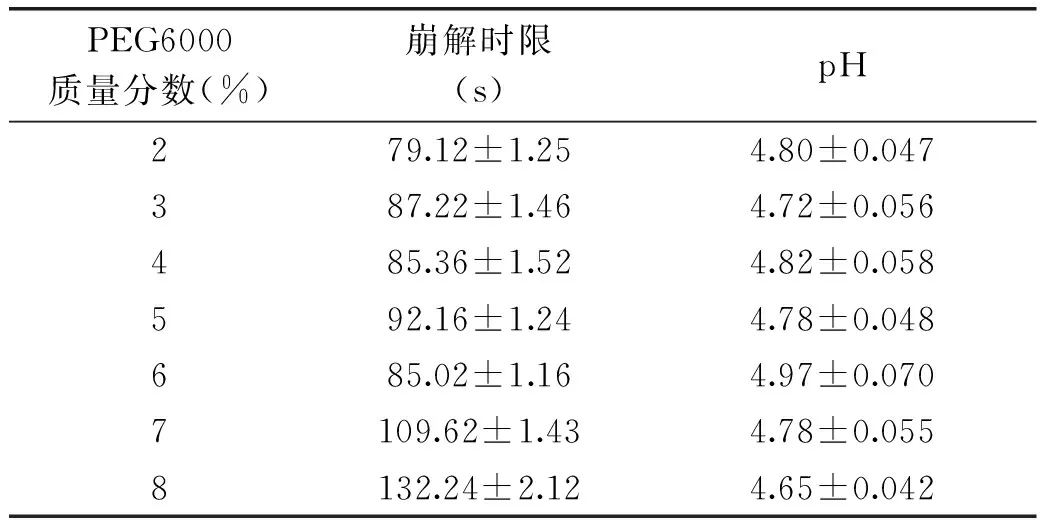
表4 PEG6000用量對片劑崩解時限和pH的影響
為了提高泡騰片的穩定性,在制備銀杏葉泡騰片過程中采用PEG 6000包裹碳酸氫鈉的方法制備分散體。在實驗過程中曾實驗用PEG 6000包裹檸檬酸用于減少碳酸氫鈉和檸檬酸的接觸,但是PEG 6000與檸檬酸混合后出現低共融現象,二者一起熔融后不能冷卻成固體。
2.2 Box-Benhnken設計響應面實驗結果
在進行單因素實驗時,選取了pH和崩解時限作為雙重評價指標,但結果顯示,除堿源和酸源的比例對pH影響較大外,另外兩個因素的變化對pH的影響不具有顯著性,進行響應面實驗設計時,如果將pH作為考察指標,二次回歸和多次回歸擬合意義不大。而且,《中國藥典》中,對泡騰片水溶液的pH并沒有明確規定,本實驗中,通過單因素實驗發現,pH在4.40~6.16之間,符合弱酸性要求,同時能保證口感。所以,只選擇崩解時限作為指標進行回歸分析。
以泡騰崩解劑總質量分數(%)、碳酸氫鈉∶檸檬酸的比例、PEG6000用量為考察因素,應用Box-Benhnken設計三因素三水平的實驗,以泡騰崩解時限作為評價指標對泡騰片制備工藝進行優化,實驗結果見表5。
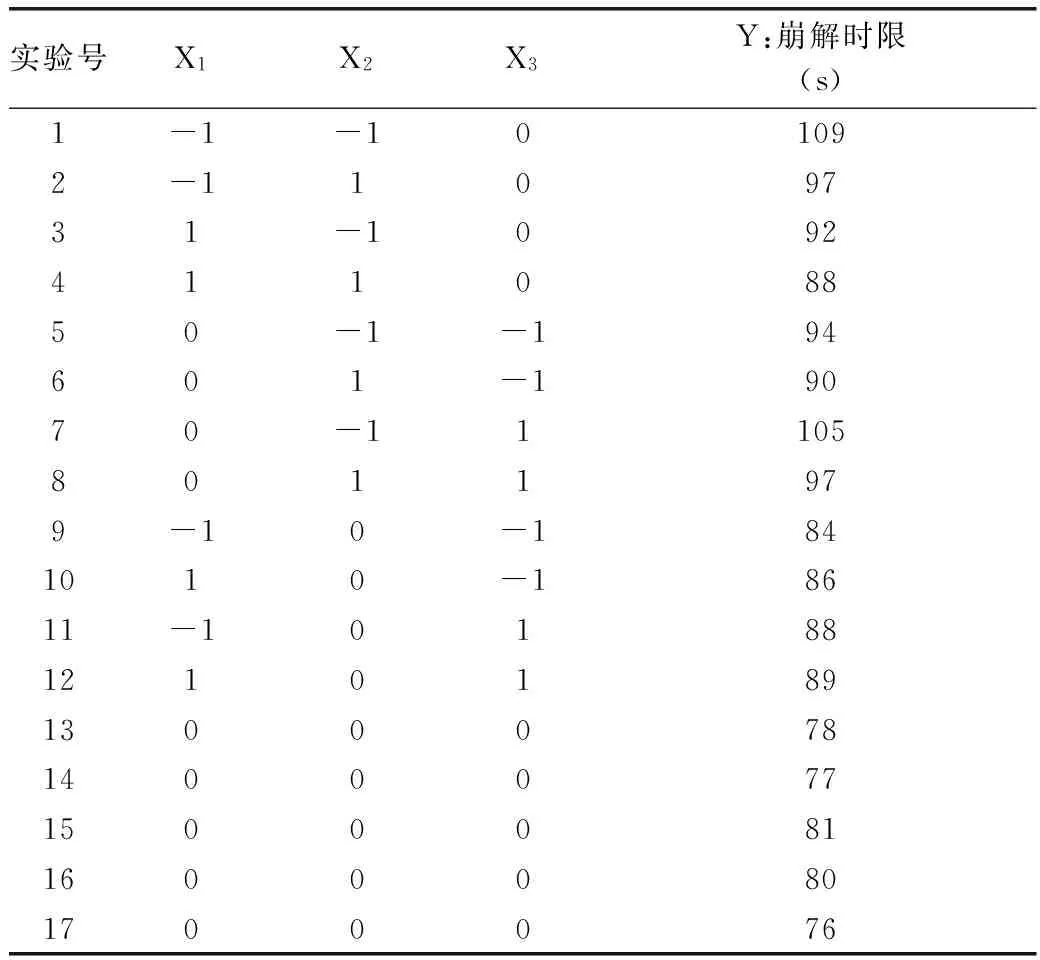
表5 Box-Benhnken設計表及結果
對響應值和各因素進行回歸擬合,得到回歸方程如下:Y=65.20-2.62X1-3.75X2+0.13X3+1.00X1X2+0.25X1X3-1.50X2X3+17.27X12+8.02X22+5.28X32,相關系數R2=0.9663,說明因變量和自變量之間線性關系顯著,方程擬合度好。由表6可知,模型F值為22.28,p=0.0002<0.05,表現為極顯著;失擬項p=0.1274>0.05,表現為不顯著,說明模型精度高,能很好的對響應面進行預測,適用于銀杏葉泡騰片制備工藝優化分析。
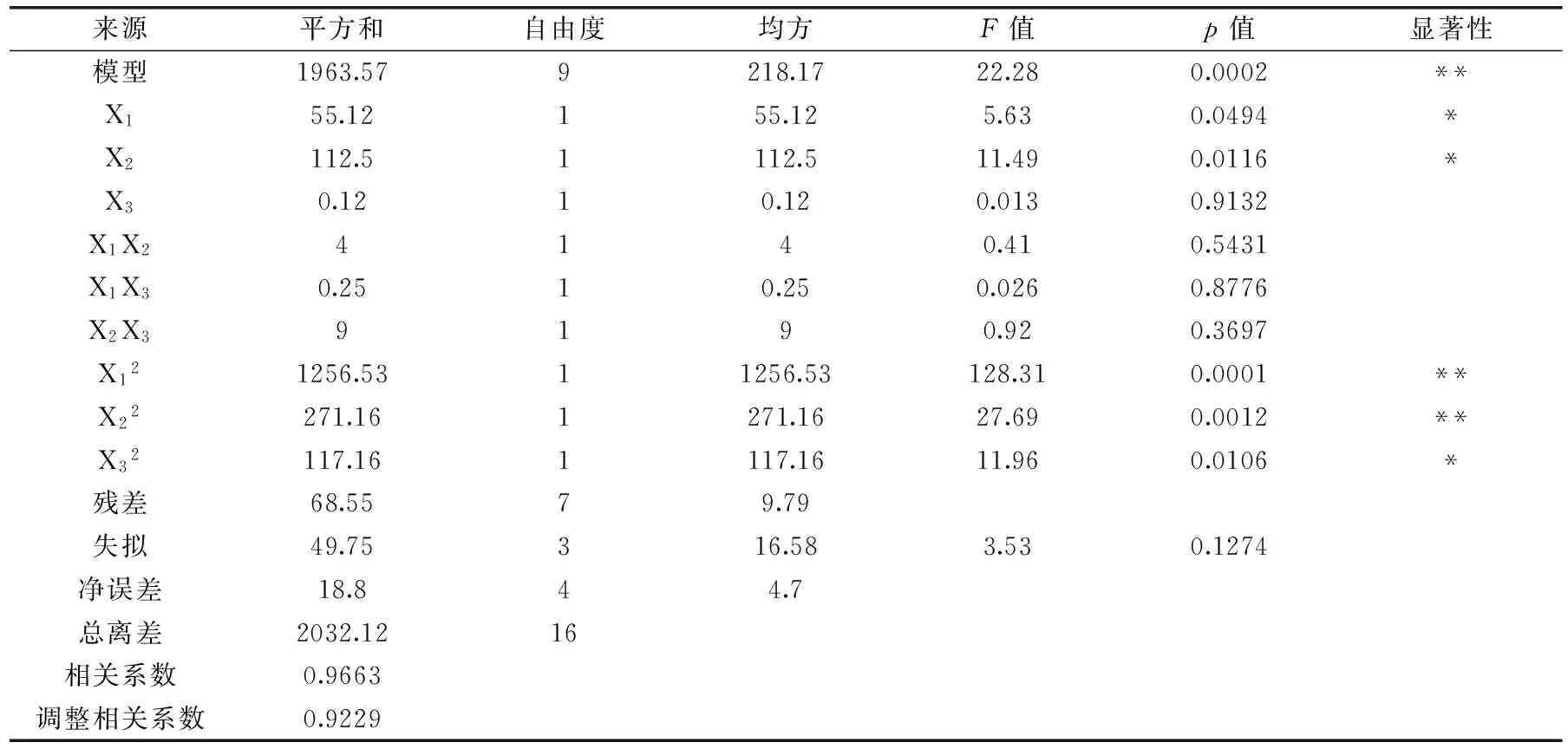
表6 響應面實驗方差分析
注:**表示影響極顯著(p<0.01),*表示影響顯著(p<0.05)。
由表6可知,3個因素對泡騰片質量的影響順序為泡騰崩解劑總量>泡騰崩解劑配比>PEG6000用量,X1、X2、X32影響顯著(p<0.05),X12、X22的影響極顯著(p<0.05),但泡騰崩解劑總量、泡騰崩解劑配比以及PEG6000用量之間交互作用不顯著。
2.3 影響因素的響應面曲線圖
交互作用的響應面曲線圖能直觀地反映各因素對響應值的影響,在所選的范圍內分析響應面的最低點可以看出有最優值存在,曲面圖中若曲面坡度陡峭,表示兩個因素結合在一起對實驗結果影響較大,相反表示影響較小。從三組響應面圖1可知,曲線圖中崩解時限隨泡騰崩解劑配比(X1)的變化而變化,而PEG6000(X3)用量對曲線圖變化幾乎無影響,同時泡騰崩解劑總質量(X2)對曲線圖變化影響較小,所以X1X3兩因素交互作用幾乎不存在,X1X2兩因素交互作用較小。圖1的曲線圖中崩解時限隨泡騰崩解劑總質量(X2)的變化而變化,同時PEG6000(X3)用量對曲線圖變化影響較大,所以X2X3兩因素存在交互作用;綜合分析上述三組圖可知,因素之間交互作用大小為X2X3>X1X2>X1X3。響應面優化實驗得出最優條件為:泡騰崩解劑配比(碳/檸)1∶1.21、泡騰崩解劑總量46.15%、PEG6000用量6.02%,此條件下模型預測泡騰片崩解時限為79.67 s。
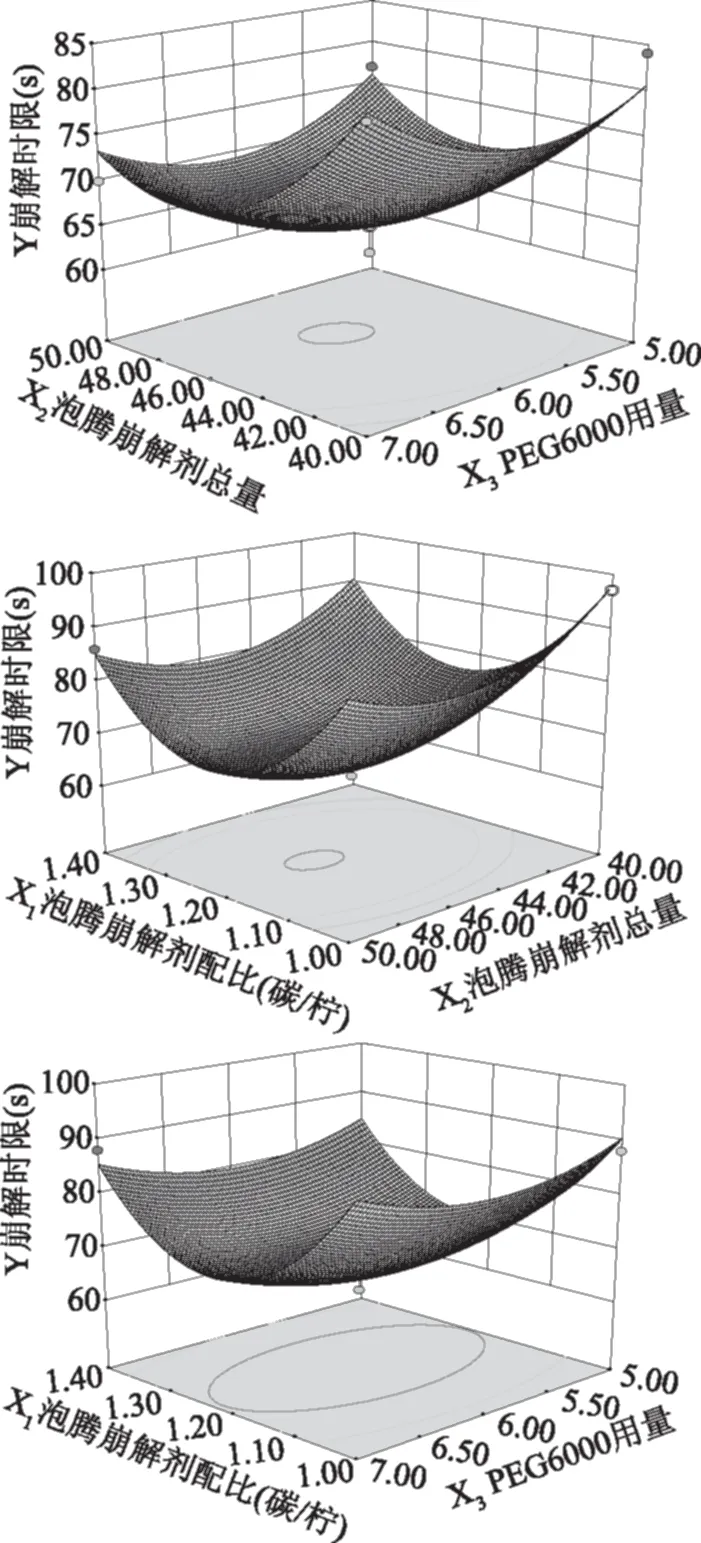
圖1 各因素交互作用對崩解時限的影響曲面圖Fig.1 The response surface figure of three factors interaction effect on disintegration time limit
按所得最佳工藝條件制備銀杏葉提取物泡騰片3批,進行工藝驗證,測得崩解時限為(79.14±1.24) s。經過數據分析,所得方程擬合度高,因素影響顯著性高,銀杏葉提取物泡騰片的崩解時限預測值79.67 s,驗證實驗結果顯示,其崩解時限79.14 s,與預測值接近,數據模型合理、可信。
2.4 銀杏葉總黃酮提取物泡騰片的質量分析
采用本工藝制備的銀杏葉提取物泡騰片,外觀整潔,沖泡后所得溶液澄清透明,口感佳。平均片重為(500±21) mg,未發現片重超限,全部在5 min內崩解,符合《中國藥典》2015年版的相關規定。所得溶液均呈弱酸性,1 g泡騰片粉平均可產生CO2氣體(10.25±0.22) mL(RSD=2.14%)。按1.2.6.5項下方法求得,銀杏葉提取物泡騰片中總黃酮的含量為(4.80±0.08) mg/片(RSD=1.67%),每片按0.5 g計算。模擬設計給藥方案,每天3次,每次2片,可以達到市場上銷售的銀杏片總黃酮當量。
3 結論
本研究旨在將銀杏葉進行二次開發,制備成口感好,易吸收的泡騰片劑。泡騰崩解劑最佳配比為1∶1.21,泡騰崩解劑的總量最佳質量分數為46.15%,PEG 6000的最佳質量分數為6.02%。最優工藝條件下制備的泡騰片,平均片重(500±21) mg,每片總黃酮含量為(4.80±0.08) mg,崩解時限、pH和發泡量符合藥典規定,制備的銀杏葉提取物泡騰片外觀良好,崩解迅速,溶解后溶液澄清透明、呈弱酸性。
目前,銀杏葉被廣泛開發成藥品或保健食品,用于心腦血管疾病病人的治療或養生與保健。本研究將銀杏葉中的總黃酮提取物開發成了口感好,利于服用的泡騰片,具有良好的市場前景。在以后的工作中,還應在體內藥代動力學方面[19-20]和藥效學等方面繼續深入研究,并與現有制劑比較,以考察本研究所制備泡騰片在生物利用度和藥效方面的優勢。
[1]國家藥典委員會.中華人民共和國藥典(一部)[S].北京:中國醫藥科技出版社,2015.
[2]李芳,石吉勇,張德濤,等. 銀杏葉中黃酮含量的葉面分布檢測研究[J]. 食品工業科技,2015,36(9):270-272.
[3]聶黎行,戴忠,魯靜,等.銀杏葉、銀杏葉提取物及其制劑質量控制研究進展[J].中國藥事,2011,25(2):171-173.
[4]何鋼,劉嵬,李會萍,等 銀杏葉多糖分離純化、結構鑒定及抗氧化活性研究[J]. 食品工業科技,2015,36(22):81-86.
[5]宋貴櫟.銀杏葉注射液治療冠心病心絞痛的臨床療效及安全性[J].中國當代醫藥,2013,20(7):66-67.
[6]孟愛紅,陳芝蕓,嚴茂祥,等.銀杏葉提取物對肝纖維化大鼠肝組織COX-2表達的影響[J].中華中醫藥學刊,2013,31(8):1698-1700.
[7]王樹芳,徐海英,李萌,等.銀杏葉提取物對急性肝衰竭大鼠FADD表達的影響[J].中國現代醫學雜志,2012,22(22):23-26.
[8]Kang JW,Kim JH,Song K,et al.Kaempferol and quercetin,components ofGinkgobilobaextract(EGb761),induce caspase-3-dependent-apoplosis in oral cavity cancer cells[J].Phytother Res,2010,24(1):S77-82.
[9]Dias MC,Rodrigues MA,Reimberg MC,et al.Protective effects ofGinkgobilobaagainst rat liver carcinogenesis[J].Chem Biol Interact,2008,173(1):32-42.
[10]ELAD S,ZEEVI I,FINKE J,et al. Improvement in oral chronic graft-versus-host disease with the administration of effervescent tablets of topical budesonide—an open,randomized,multicenter study[J]. Biology of Blood and Marrow Transplantation,2012,18(1):134-140.
[11]肇麗梅,韓峰超,邱楓,等.阿司匹林維生素C泡騰片的體內過程及生物等效性[J].中國藥學雜志,2004,39(2):135-138.
[12]程心旻,雷海民,劉偉.全球銀杏制劑專利概況[J].中國中藥雜志,2013,38(17):2889-2893.
[13]胡林水,鄭珺,邵勝榮.銀杏葉提取物泡騰片的研制及質量考察[J]. 中藥材,2005,28(1):52-54.
[14]陳潔,戴衍朋,孫立立,等. Box-Behnken 設計-效應面法優選甘草切制工藝[J].中草藥,2013,44(12):1579-1583.
[15]沈秀娟,周倩,孫立立,等. Box-Benhnken設計效應面法優選黃芪切制工藝[J].中國中藥雜志,2014,39(13):2498-2503.
[16]李潔,楊小明,王云飛,等 響應面法優化銀杏葉聚戊烯乙酸酯水解工藝[J]. 食品工業科技,2013,34(7):256-259.
[17]劉金香,王水興,范青生.堿溶酸沉法提取銀杏葉總黃酮[J].安徽農業科學,2008,36(26):11386-11388.
[18]鄭丹丹,王京龍,張立華,等. 竹葉提取物泡騰片的制備工藝優化及其質量分析[J].食品科學,2016,37(8):39-44.
[19]張穎,劉建勛,林力,等. HPLC-ECD法測定大鼠血漿中銀杏葉黃酮成分及藥代動力學研究[J]. 藥物分析雜志,2011,31(1):10-14.
[20]Ude C,Paulke A,Noldner M,et al.Plasma and brainlevels of terpene trilactones in rats after an oral singledose of standardizedGinkgobilobaextract EGb 761(R)[J].Planta Medica,2010,77(3):259-264.
Preparation ofGinkgobilobaleaves flavonoids extract effervescent tablets with Box-Benhnken response surface experiments and its quality analysis
WANG Jing-long1,ZHENG Dan-dan1,ZHANG Li-hua1,WANG Fei1,WANG Zhan-yi1,CHU Wen-chao2
(1.College of Life Sciences,Zaozhuang University,Zaozhuang 277160,China;2.Department of Pharmacy,Zhengzhou University,Zhengzhou 450001,China)
To prepareGinkgobilobaleaves extracts effervescent tablets,Box-Benhnken response surface experiments was used to optimize the formulation,including the usage of matrix(polyethylene glycol 6000,PEG 6000),the proportion and amount of effervescent agent(sodium bicarbonate and citric acid),with pH value and disintegration time limit as the evaluation index. Then the optimized effervescent tablets were analyzed by main drug content,frothing volume,pH value,disintegration time limit and the weight variation. The optimum proportion of effervescence disintegrants(sodium bicarbonate,citric acid)was 1∶1.21,the mass fraction of effervescence disintegrants was 46.15%,and mass fraction of PEG 6000 was 6.02%. The average weight of the tablets was(500±21) mg,and the content of flavonoid was(4.54±0.08) mg. The disintegration time,pH and foaming quantity also meet the requirements of pharmacopoeia. The obtained effervescent tablets displayed good appearance,rapid disintegration,clear solution and no precipitation.
Ginkgobilobaextracts;effervescent tablets;Box-Benhnken response surface experiments;preparation;quality analysis
2016-08-16
王京龍(1988-),男,博士,講師,研究方向:中藥新藥研發與中藥炮制原理,E-mail:jlwang8121@163.com。
山東省自然科學基金項目(ZR2013BL018)。
TS202.1
B
1002-0306(2017)06-0288-05
10.13386/j.issn1002-0306.2017.06.046

