氨基酸雜多酸鹽在模擬汽油催化氧化脫硫中的應用研究
石榮榮
(南京科技職業學院,江蘇南京210048)
氨基酸雜多酸鹽在模擬汽油催化氧化脫硫中的應用研究
石榮榮
(南京科技職業學院,江蘇南京210048)
分別以甘氨酸(Gly)、丙氨酸(Ala)和谷氨酸(Glu)為陽離子,磷鎢酸和磷鉬酸為陰離子,合成了氨基酸雜多酸鹽[Gly]3PW12O40、[Ala]3PW12O40、[Glu]3PW12O40和[Glu]3PMo12O40。以氨基酸雜多酸鹽為催化劑、離子液體1-甲基-3-辛基咪唑六氟磷酸鹽([Omim]PF6)為萃取劑、過氧化氫為氧化劑,考察了模擬汽油催化氧化脫硫效果。其中,[Glu]3PW12O40-[Omim]PF6-H2O2催化氧化脫硫體系的脫硫效果最好,采用該體系考察了脫硫條件對模擬汽油脫硫率的影響。結果表明,當n(過氧化氫)∶n(硫)∶n(催化劑)=100∶25∶1、反應時間為60min、反應溫度為50℃、V([Omim]PF6)∶V(模擬汽油)=1∶5時,模擬汽油中二苯并噻吩(DBT)的脫除率可達98.5%,重復使用5次脫硫率仍高于95%。
氨基酸;雜多酸;離子液體;模擬汽油;氧化脫硫
近些年,環境污染問題引起人們普遍關注,特別是空氣污染問題,而汽車尾氣的大量排放是空氣污染重要來源,尤其是燃油燃燒過程中排放的SOx會帶來很多危害,并危及人體健康[1]。為控制燃油中硫化物危害,世界各國都制定了嚴格的燃油硫含量標準,相應地燃油脫硫技術的開發成為研究重點[2]。加氫脫硫是應用最為成熟的脫硫技術,但是該工藝通常需要在高溫(>300℃)和高壓(3~10MPa)條件下進行,且存在投資和運行成本高、需要消耗大量氫氣、對噻吩及其衍生物脫除效果較差和辛烷值降低等缺點[3]。研究者們陸續開發了一些新的非加氫脫硫技術,如吸附脫硫、萃取脫硫、生物脫硫、烷基化脫硫和氧化脫硫等[4]。其中,氧化脫硫技術具有反應條件溫和、不消耗氫氣、能夠有效脫除噻吩及其衍生物、能夠生產低硫甚至無硫油品和不影響油品辛烷值等優點,成為深度脫硫技術的研究熱點[5]。氧化脫硫技術包括氧化階段和萃取階段,氧化階段氧化劑多為H2O2,一般需要采用催化劑用于催化氧化過程的進行。氧化脫硫技術的核心技術是開發新型高效的催化劑和萃取劑,進而提高脫硫效果。
雜多酸(鹽)是一種新型環境友好型催化劑,具有酸性可調、催化活性高、使用條件溫和和“假液相”等優點,在催化領域有廣泛的應用[6-7],用作催化氧化脫硫過程也體現出優良的催化性能[8]。離子液體是指在室溫或室溫附近呈液態、完全由陰陽離子組成的一類物質的總稱,具有可設計、飽和蒸汽壓低和穩定性高等優點,在諸多領域都有廣泛的應用[9]。尤其是用于油品脫硫時,離子液體是一種性能優良的萃取劑,相對于有機溶劑萃取劑,其具有操作簡單、萃取選擇性高和重復使用性能好等優點,且不存在交叉污染[10]。雜多酸鹽用于油品催化氧化脫硫已有不少報道,但是使用的雜多酸鹽催化劑多以有機陽離子和雜多酸陰離子復合而成,而有機陽離子以咪唑或吡啶居多[11-12],使得此類催化劑制備成本較高,且制備過程較為繁雜。筆者以價格低廉、環境友好的氨基酸與雜多酸反應制備了以氨基酸為陽離子、雜多酸為陰離子的有機-無機復合雜多酸鹽,以此作為催化劑、離子液體[Omim]PF6作為萃取劑,構建了雜多酸-離子液體-H2O2催化氧化脫硫體系,考察了其對模擬汽油的脫硫效果,并考察了脫硫體系的重復使用能力。
1 實驗部分
1.1 試劑與儀器
試劑:甘氨酸、L-谷氨酸、DL-丙氨酸,均為生化試劑;磷鎢酸、磷鉬酸、二苯并噻吩、N-甲基咪唑、溴代正辛烷、六氟磷酸鉀、乙酸乙酯、正辛烷、質量分數為30%的H2O2,均為分析純。儀器:SHZ-D(Ⅲ)型循環水式真空泵;DF-101S型恒溫加熱磁力攪拌器;DZ-1A型真空干燥箱;RE-52A型旋轉蒸發儀。
1.2 離子液體[Omim]PF6制備
參照文獻[13]合成離子液體[Omim]PF6。1)稱取0.2mol N-甲基咪唑于三口燒瓶中,取稍過量溴代正辛烷0.21mol,通過恒壓滴液漏斗緩慢加入上述三口燒瓶中。升溫至70℃,恒溫回流反應30 h,并不斷磁力攪拌。反應結束后,反應液用乙酸乙酯洗滌3次,然后轉移到旋轉蒸發儀中除去乙酸乙酯。洗滌后的產物置于真空干燥箱中干燥備用,即為離子液體中間體1-甲基-3-辛基咪唑溴鹽[Omim]Br。合成反應方程式見式(1)。
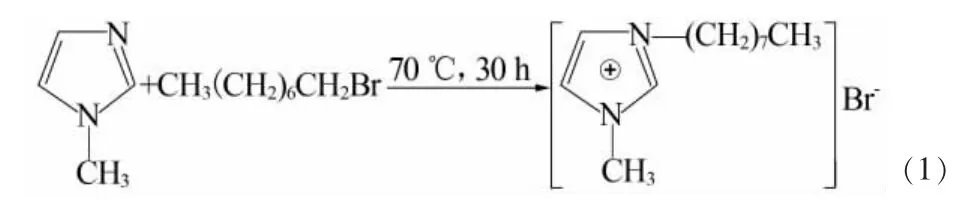
2)稱取0.1mol六氟磷酸鉀溶于適量蒸餾水中配成溶液,取0.1mol離子液體中間體[Omim]Br于圓底燒瓶中,通過恒壓滴液漏斗將六氟磷酸鉀溶液緩慢加入圓底燒瓶中,并不斷攪拌。反應體系在室溫下磁力攪拌反應12 h。反應結束后靜置分層,下層產物在旋轉蒸發儀中除去未反應完全的原料,然后用蒸餾水反復洗滌。洗滌后的產物在真空干燥箱中干燥至質量恒定,即得目標離子液體[Omim]PF6。合成反應方程式見式(2)。
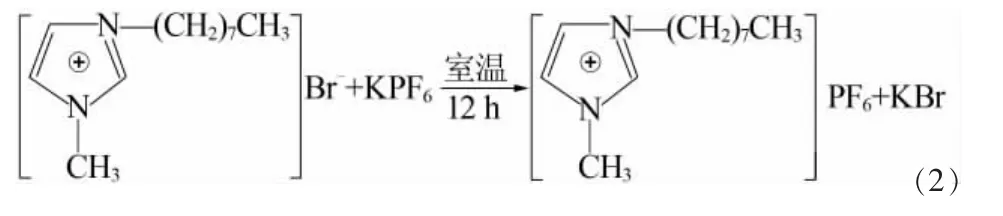
1.3 氨基酸雜多酸鹽制備
參照文獻[14]合成氨基酸雜多酸鹽,以[Glu]3PW12O40制備過程為例來說明氨基酸雜多酸鹽合成過程。以物質的量比為1∶3稱取磷鎢酸和谷氨酸并溶于適量蒸餾水制成溶液,將磷鎢酸水溶液滴加到谷氨酸溶液中,并不斷磁力攪拌。待反應體系由澄清變混濁,停止攪拌,靜止片刻有白色物質析出,產物用蒸餾水洗滌3次,而后置于真空干燥箱中干燥至質量不再變化,即得[Glu]3PW12O40。合成反應方程式見式(3)。

1.4 催化氧化脫硫實驗
實驗汽油為模擬汽油,選用正辛烷為模擬汽油芳烴本體、DBT為模型硫化物,模擬汽油中DBT質量分數為500μg/g。取5mL模擬汽油和1mL[Omim]PF6于三口燒瓶中,另取一定量氨基酸雜多酸鹽和質量分數為30%的H2O2分別作為催化劑和氧化劑置于三口燒瓶中。反應體系在一定溫度下磁力攪拌反應,反應結束后靜置分層,上層為脫硫后模擬汽油。取脫硫后模擬汽油測定其硫含量,根據脫硫前、后模擬汽油中硫含量計算脫硫率。
2 結果與討論
2.1 不同種類催化劑的脫硫效果
在 n(H2O2)∶n(S)∶n(催化劑)=100∶25∶1、反應時間為60min、反應溫度為50℃、萃取劑用量為V([Omim]PF6)∶V(模擬汽油)=1∶5條件下,分別以[Gly]3PW12O40、[Ala]3PW12O40、[Glu]3PW12O40、[Glu]3PMo12O40為催化劑,考察催化劑對模擬汽油的催化氧化脫硫效果,結果見圖1。由圖1可知,以不同的氨基酸雜多酸鹽作催化劑時模擬汽油的脫硫率不同。其中[Gly]3PW12O40、[Ala]3PW12O40、[Glu]3PW12O40具有相同的陰離子,但是陽離子分別為甘氨酸、丙氨酸、谷氨酸,以[Glu]3PW12O40作催化劑時模擬汽油的脫硫率最高。可能是因為,甘氨酸和丙氨酸中都只含有一個—COOH,而谷氨酸中含有 2個—COOH,谷氨酸具有較強的酸性,使得[Glu]3PW12O40的酸性最強,促進了H2O2氧化DBT反應的進行,使得脫硫率增大。對于[Glu]3PW12O40、[Glu]3PMo12O40,當陽離子均為谷氨酸、陰離子分別為磷鎢酸和磷鉬酸時,以[Glu]3PW12O40作催化劑時模擬汽油的脫硫率較高。所以,選取[Glu]3PW12O40作為催化劑。
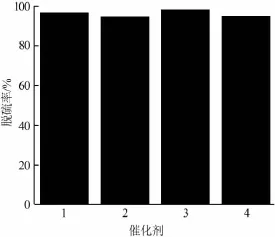
圖1 不同種類催化劑對模擬汽油的脫硫效果
2.2 雙氧水用量對脫硫率的影響
在反應時間為 60 min、反應溫度為 50℃、V([Omim]PF6)∶V(模擬汽油)=1∶5、n([Glu]3PW12O40)/ n(S)=0.04時,考察了不同n(H2O2)/n(S)時模擬汽油脫硫率,結果見圖2。由圖2可知,隨著雙氧水用量增大,模擬汽油脫硫率逐漸增大。按照DBT氧化反應化學計量關系,1molDBT被完全氧化成二苯并噻吩砜(DBTO2)需要消耗2molH2O2。但是,當n(H2O2)/ n(S)=2時脫硫率僅為81.4%。這是因為,反應體系中不可避免地存在雙氧水自身分解反應,雙氧水并不能完全起到氧化劑作用。隨著雙氧水用量增加,有利于氧化階段DBT氧化反應進行,模擬汽油脫硫率增大。當n(H2O2)/n(S)=4時,繼續增加雙氧水用量,脫硫率不再明顯增加。可能是因為,雙氧水用量過大,其自身分解速率增大,雙氧水利用率降低。因此,最佳雙氧水用量為n(H2O2)/n(S)=4。
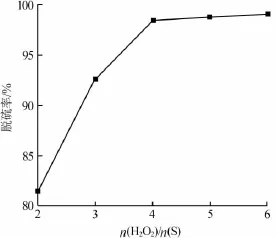
圖2 雙氧水用量對模擬汽油脫硫率的影響
2.3 反應溫度和反應時間對脫硫率的影響
在 n(H2O2)∶n(S)∶n([Glu]3PW12O40)=100∶25∶1、 V([Omim]PF6)∶V(模擬汽油)=1∶5條件下,考察了反應溫度和反應時間對模擬汽油脫硫率的影響,結果見圖3。由圖3可知,在相同溫度時,隨著反應時間延長,脫硫率不斷增加,且脫硫率增加趨勢逐漸變緩,最后趨于穩定。這是因為,反應時間延長,萃取階段和氧化階段都能充分地進行;隨著反應時間的繼續延長,模擬汽油中硫化物濃度降低,脫硫率增加趨勢變緩。當反應時間為60min時,繼續延長反應時間脫硫率增加不明顯,可以認為脫硫過程已達到平衡狀態。所以,選取反應時間為60min。
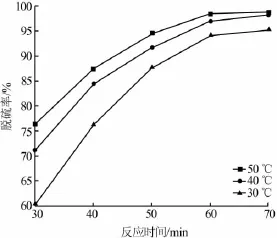
圖3 反應溫度和反應時間對模擬汽油脫硫率的影響
當反應溫度從30℃增加到50℃時,模擬汽油脫硫率不斷增加。這是因為,溫度升高離子液體黏度降低,促進硫化物萃取進入離子液體相,有利于萃取階段的進行。另外,溫度升高DBT氧化反應速率增大,有利于氧化階段的進行。并且,氧化階段的順利進行使得油相和離子液體相中硫化物濃度差增大,進一步促進萃取階段的進行。由于H2O2易分解,溫度過高會使得H2O2大量分解,氧源利用效率降低。因此,選取反應溫度為50℃。
2.4 催化劑用量對脫硫率的影響
在V([Omim]PF6)∶V(模擬汽油)=1∶5、n(H2O2)/ n(S)=4、反應時間為60min、反應溫度為50℃條件下,考察了[Glu]3PW12O40用量對模擬汽油脫硫率的影響,結果見圖4。由圖4可知,隨著催化劑用量增大,模擬汽油脫硫率不斷增加。這是因為,催化劑用量增加,反應體系活性中心數量增加,DBT氧化反應速率增加,脫硫率增大。當 n([Glu]3PW12O40)/ n(S)=0.04時脫硫率可達98.5%,繼續增加催化劑用量脫硫率不再明顯增加。因此,最佳催化劑用量為n([Glu]3PW12O40)/n(S)=0.04。

圖4 [Glu]3PW12O40用量對模擬汽油脫硫率的影響
2.5 催化氧化脫硫體系重復使用性能
為考察催化氧化脫硫體系重復使用性能,在n(H2O2)∶n(S)∶n([Glu]3PW12O40)=100∶25∶1、反應時間為60min、反應溫度為50℃、V([Omim]PF6)∶V(模擬汽油)=1∶5條件下進行催化氧化脫硫實驗。脫硫過程結束后靜置分層,分離出下層離子液體相,經過簡單再生后加入一定比例30%H2O2和模擬汽油,在相同條件下進行脫硫實驗,結果見圖5。由圖5可知,[Glu]3PW12O40-[Omim]PF6-H2O2催化氧化脫硫體系具有較好的重復使用能力,重復使用5次后,模擬汽油脫硫率僅有少量降低,脫硫率仍高于95%。脫硫率的降低可能是因為,一方面離子液體在重復使用過程中有損失,不能完全回收;另一方面離子液體再生效果不徹底,其中仍有硫化物的氧化物殘留,直接影響新一輪脫硫時的脫硫效果。
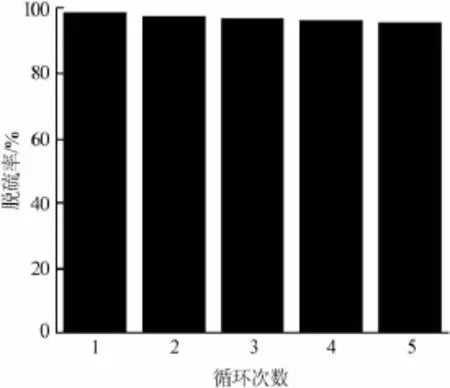
圖5 脫硫體系重復使用能力
3 結論
以氨基酸為原料,制備了4種氨基酸雜多酸鹽[Gly]3PW12O40、[Ala]3PW12O40、[Glu]3PW12O40和[Glu]3PMo12O40,相比于咪唑和吡啶類雜多酸鹽,氨基酸雜多酸鹽具有原料經濟性好、制備過程簡單、不需要使用有機溶劑等優點。將氨基酸雜多酸鹽用于催化氧化模擬汽油脫硫研究,其中[Glu]3PW12O40-[Omim]PF6-H2O2體系具有最好的脫硫效果。當n(H2O2)∶n(S)∶n([Glu]3PW12O40)=100∶25∶1、反應時間為60min、反應溫度為50℃、V([Omim]PF6)∶V(模擬汽油)=1∶5時,模擬汽油中DBT脫除率可達98.5%,重復使用5次后脫硫率仍高于95%。
[1] Stanislaus A,Marafi A,Rana M S.Recent advances in the science and technology of ultra low sulfur diesel(ULSD)production[J]. Catal.Today,2010,153:1-68.
[2] 付輝,李會鵬,趙華,等.WO3-ZSM-5/MCM-41催化劑的合成及其催化氧化脫硫研究[J].無機鹽工業,2014,46(7):75-78.
[3] Zhang H X,Gao JJ.Removal of thiophenic sulfurs using an extractiveoxidative desulfurization processwith threenew phosphotungstate catalysts[J].Ind.Eng.Chem.Res.,2012,51:6658-6665.
[4] 林燕,王芳,張志慶,等.離子液體綠色脫硫機理及應用進展[J].化工進展,2013,32(3):549-557.
[5] Zhang J,Wang A.Oxidative desulfurization ofdibenzothiopheneand dieselover[Bmim]3PMo12O40[J].J.Catal.,2011,279(2):269-275.
[6] Martin A,Armbruster U,Atia H.Recent developments in dehydration of glycerol toward acrolein over heteropolyacids[J].Eur.J.Lipid Sci.Tech.,2012,114(1):10-23.
[7] 趙忠奎,李宗石,王桂茹,等.雜多酸催化劑及其在精細化學品合成中的應用[J].化學進展,2004,16(4):620-630.
[8] 張海燕,代躍利,蔡蕾.雜多酸催化劑催化氧化脫硫研究進展[J].化工進展,2013,32(4):809-815.
[9] Guo F,Zhang SJ,Wang JJ,etal.Synthesisand applicationsof ionic liquids in clean energy and environment:a review[J].Curr.Org. Chem.,2015,19(5):455-468.
[10] 胡華玲,楊浩,喬聰震,等.燃油深度脫硫用離子液體研究進展[J].化學研究,2014,25(1):104-110.
[11] 安瑩,陸亮,李才猛,等.磷鉬雜多酸離子液體催化氧化脫硫[J].催化學報,2009,30(12):1222-1226.
[12] 丁永萍.基于雜多酸的咪唑類離子液體的合成、表征及催化性能研究[D].沈陽:遼寧大學,2011.
[13] 關衛省,李宇亮,茹靜,等.1-丁基-3-甲基咪唑六氟磷酸鹽離子液體合成[J].應用化工,2010,39(6):818-822.
[14] 劉靜,黃小文,趙小平,等.氨基酸功能化雜多酸鹽的制備及其在無溶劑條件下催化正十二醇與乙酸酯化反應性能[J].石油學報:石油加工,2013,29(3):383-389.
聯系方式:Rain_shi@126.com
Application of am ino acidsheteropolyacid salt in catalytic oxidative desulfurization of simulated gasoline
ShiRongrong
(Nanjing Polytechnic Institute,Nanjing 210048,China)
Amino acids heteropoly acid salts[Gly]3PW12O40,[Ala]3PW12O40,[Glu]3PW12O40,and[Glu]3PMo12O40were synthesized with glycine,alanine,and glutamic acid as cations,and phosphorus acid and phosphomolybdic acid as anions.The catalytic oxidative desulfurization effectwas investigatedwith ionic liquid[Omim]PF6asextractive agentand H2O2asoxidant. In which,the catalytic oxidative desulfurization system[Glu]3PW12O40/[Omim]PF6/H2O2performed the best desulfurization property,and the effect of conditions on the sulfur removalwas investigated.Result showed that the sulfur removal of DBT could be 98.5%under the conditions n(H2O2)∶n(S)∶n(Catalyst)=100∶25∶1,reaction timewas 60min,reaction temperature was50℃,and V([Omim]PF6)/V(modeloil)=1∶5.After reused five times,the sulfur removalofDBT stillexceeded 95%.
amino acids;heteropoly acid;ionic liquid;simulated gasoline;oxidative desulfurization
TQ032
A
1006-4990(2017)03-0077-04
2016-09-18
石榮榮(1980— ),女,碩士,講師,研究方向為工業催化和化學工程。

