提高多重耐藥菌防控措施執行力對降低多重耐藥菌醫院感染的影響
李 穎,許 文,戈 偉,慕彩妮,曹小琴,范珊紅
(第四軍醫大學唐都醫院,陜西 西安 710038)
·論著·
提高多重耐藥菌防控措施執行力對降低多重耐藥菌醫院感染的影響
李 穎,許 文,戈 偉,慕彩妮,曹小琴,范珊紅
(第四軍醫大學唐都醫院,陜西 西安 710038)
目的 了解提高多重耐藥菌(MDRO)預防控制措施依從率對重癥監護病房(ICU)MDRO傳播的影響。方法 選擇2014年3—6月某院5個ICU 的所有患者,2014年3月1日—4月30日為基線調查階段,2014年5月1日—6月30日為干預階段(采取綜合干預措施),比較干預前后5個ICU MDRO患者接觸隔離措施落實情況、醫護人員MDRO相關知識知曉情況。結果 干預后醫務人員對MDRO傳播方式、接觸隔離措施和轉科告知知曉率(分別為100.00%、98.89%、93.33%),均高于干預前(分別為67.22%、61.11%、45.56%);除單間隔離外,其他防控措施(隔離醫囑、床旁隔離、穿隔離衣、掛隔離標志)的依從率(>70%)均高于干預前(<50%)(均P<0.01)。 干預后MDRO的檢出率為7.16%(90/1 257),低于干預前9.65%(117/1 212)(χ2=5.00,P=0.03)。結論 采取綜合干預措施,可以提高醫務人員MDRO防控措施的執行力度,減少MDRO的傳播。
多重耐藥菌; 預防控制; 干預措施; 執行力
[Chin J Infect Control,2017,16(2):126-129]
根據2007年歐洲疾病控制與預防中心(ECDC)和歐洲藥品評估局(EMEA)的數據分析,歐盟由于多重耐藥菌(multidrug-resistant organism,MDRO)感染而導致死亡人數約為25 000例/年[1],由 MDRO感染所產生的額外醫療費用和生產力損失至少1.5億/年[1]。美國疾病控制與預防中心(CDC)制定了預防和控制病原體醫院感染傳播的相關指南[2]。有證據顯示,CDC的防控措施可有效控制醫院感染[3-4],但控制措施的依從性相對較低。我國對MDRO醫院感染傳播的防控措施也日趨完善,但由于防控措施的執行力度相對較低,各種MDRO醫院感染暴發事件仍然層出不窮。本研究旨在提高MDRO預防控制措施執行力度,降低MDRO醫院感染。
1 資料與方法
1.1 一般資料 監測2014年3—6月某醫院5個重癥監護病房(ICU),包括神經外科、胸腔外科、神經內科、呼吸內科和麻醉科ICU的所有患者,重點監測診斷為MDRO感染/定植的患者,并收集患者的相關資料。
1.2 研究方法
1.2.1 研究階段與內容 本研究分為兩個階段:2014年3月1日—4月30日為基線調查階段,2014年5月1日—6月30日為干預階段。通過查詢微生物檢驗室登記的MDRO,獲得MDRO感染/定植患者名單,每日對前一日臨床標本檢出MDRO的患者(除外標本污染引起的陽性結果)進行現場查看,觀察患者的各項接觸隔離措施的落實情況,同時分別在基線調查階段和干預階段對該病區的醫務人員進行MDRO防控知識問卷調查。
1.2.2 干預措施 對MDRO感染/定植患者采取綜合性干預措施,包括(1)MDRO專項知識培訓。利用科室集體學習活動的機會,取得科室主任、護士長的配合,進行MDRO相關知識培訓,并在查看科室相關措施落實情況時進行隨機提問。(2)加強手衛生督查。在完善各科室的手衛生設施與手衛生用品的基礎上,加強手衛生依從性暗訪和考核頻率,提問手衛生的五個重要時刻,并抽查六步洗手法完成情況。(3)監督隔離醫囑的下達與執行。明確隔離醫囑醫護責任分工(醫生未下達接觸隔離醫囑,責任為醫生;醫生下達了接觸隔離醫囑,而護士未執行接觸隔離措施,責任為護士),醫生或護士隔離醫囑完成情況均與科室每月的醫護質量考核評分直接相關。(4)建立MDRO交班制度。將患者的微生物培養結果作為病房交接班的一項內容,每日交接班時,匯報本病區臨床標本中檢出MDRO情況。
1.3 MDRO定義與判斷標準 指對臨床使用的3類或3類以上抗菌藥物同時呈現耐藥的細菌。具體判斷標準按照李春輝[5]翻譯的《MDR、XDR、PDR多重耐藥菌暫行標準定義——國際專家建議》進行判斷。
1.4 統計分析 應用SPSS 13.0統計軟件進行統計分析,計數資料以率或構成比表示,率或構成比的比較采用卡方檢驗,P≤0.05為差異有統計學意義。
2 結果
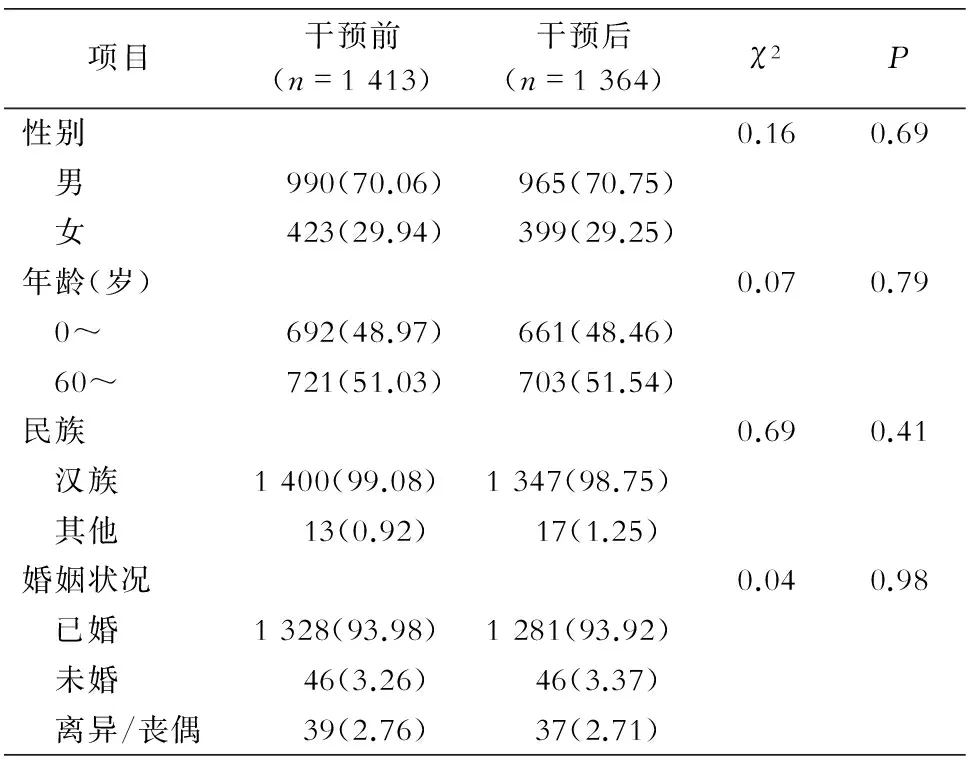
2.1 一般情況 5個ICU共有97張床位,其中單間隔離病房6間,醫生24名,護士156名。基線調查階段5個ICU出院患者共計 1 413例,平均住院日3.69 d,84例患者檢出MDRO 126株(其中污染菌株9株),其中男性51例,女性33例,年齡21~91歲;干預階段出院患者1 364例,平均住院日3.76 d,75例患者檢出MDRO 95株(其中污染菌株5株), 其中男性47例,女性28例,年齡16~87歲。干預前后患者人口學特征均衡可比,見表1。
表1 干預前后患者人口學特征比較[例數(%)]
Table 1 Comparison of patients’ demographic characteristics before and after intervention (No. of cases[%])
項目干預前(n=1413)干預后(n=1364)χ2P性別0.160.69 男 990(70.06) 965(70.75) 女 423(29.94) 399(29.25)年齡(歲)0.070.79 0~ 692(48.97) 661(48.46) 60~ 721(51.03) 703(51.54)民族0.690.41 漢族1400(99.08)1347(98.75) 其他 13(0.92) 17(1.25)婚姻狀況0.040.98 已婚1328(93.98)1281(93.92) 未婚 46(3.26) 46(3.37) 離異/喪偶 39(2.76) 37(2.71)
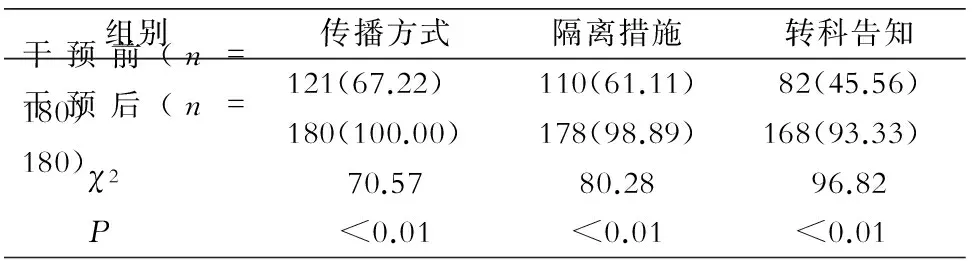
2.2 醫務人員MDRO防控措施知識掌握情況 干預后醫務人員對MDRO傳播方式、接觸隔離措施和轉科告知知曉率均高于干預前,詳見表2。
表2 干預前后醫務人員MDRO防控知識知曉情況比較[人數(%)]
Table 2 Comparison of knowledge about MDRO prevention and control among HCWs before and after intervention (No. of HCWs[%])
組別傳播方式隔離措施轉科告知干預前(n=180)121(67.22)110(61.11)82(45.56)干預后(n=180)180(100.00)178(98.89)168(93.33) χ270.5780.2896.82 P<0.01<0.01<0.01
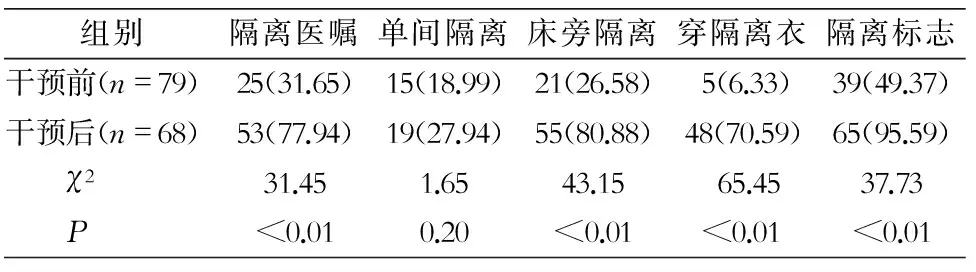
2.3 MDRO患者接觸隔離措施依從性 除去臨床標本污染引起的陽性結果和微生物培養及藥敏結果完成時已出院或死亡的患者,對檢出MDRO患者(干預前79 例,其中轉科15例;干預后68例,其中轉科47例)進行接觸隔離措施現場查看。查看轉科患者轉科告知,干預前轉科告知率13.33%(2/15),干預后提升至72.34%(34/47)(χ2=16.26,P<0.01)。干預前查看醫護人員手衛生876人次(醫生239人次,護士637人次),合格479人次,依從率54.68%;干預后查看醫護人員手衛生921人次(醫生257人次,護士664人次),合格786人次,依從率85.34%,干預后醫務人員手衛生依從率高于干預前(χ2=202.54,P<0.01)。干預前后5個ICU均做到診療儀器(包括聽診器和體溫計等)專人專用,干預前后其他措施落實情況見表3。
表3 干預前后醫務人員各項措施依從性比較[例數(%)]
Table 3 Comparison of HCWs’ compliance to various measures before and after intervention (No. of HCWs[%])
組別隔離醫囑單間隔離床旁隔離穿隔離衣隔離標志干預前(n=79)25(31.65)15(18.99)21(26.58)5(6.33)39(49.37)干預后(n=68)53(77.94)19(27.94)55(80.88)48(70.59)65(95.59) χ231.451.6543.1565.4537.73 P<0.010.20<0.01<0.01<0.01
2.4 標本類型及MDRO檢出情況
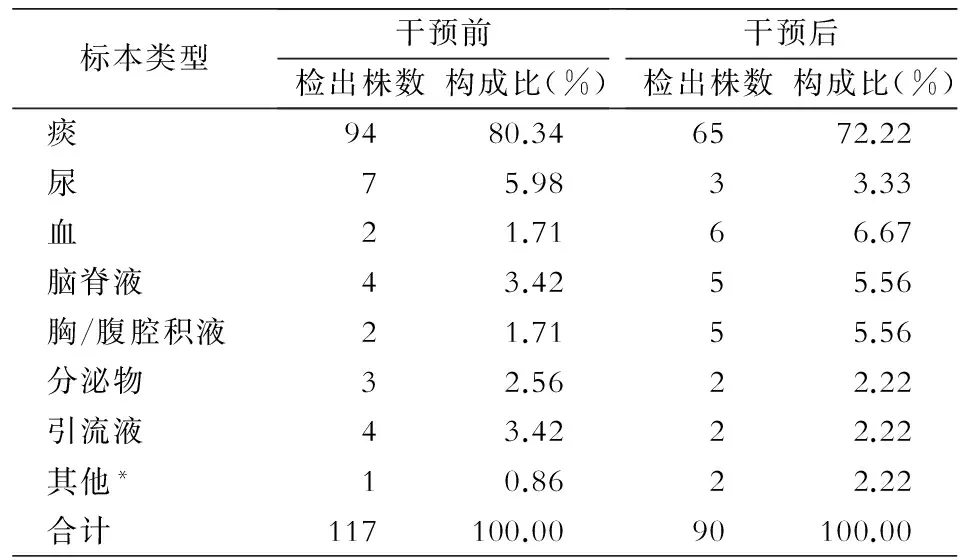
2.4.1 標本類型 除去標本污染引起的陽性結果和同種標本多次培養出的相同菌株,干預前檢出MDRO標本類型構成比居前四位的分別為痰、尿、腦脊液和引流液;干預后居前四位的分別為痰、血、腦脊液和胸/腹腔積液。干預前后檢出MDRO的標本類型構成比較,差別無統計學意義(χ2=8.03,P=0.32),見表4。
表4 干預前后5個ICU檢出MDRO的標本類型
Table 4 Specimen types of MDROs detected in 5 ICUs before and after intervention
標本類型干預前檢出株數構成比(%)干預后檢出株數構成比(%)痰9480.346572.22尿75.9833.33血21.7166.67腦脊液43.4255.56胸/腹腔積液21.7155.56分泌物32.5622.22引流液43.4222.22其他*10.8622.22合計117100.0090100.00
*:其他包括穿刺液、導管、骨髓和組織
2.4.2 MDRO檢出情況 干預后MDRO的檢出率為7.16%(90/1 257),低于干預前9.65%(117/1 212)(χ2=5.00,P=0.03)。干預前后檢出MDRO革蘭陰性菌以鮑曼/溶血不動桿菌和銅綠假單胞菌所占比例最高,革蘭陽性菌則以耐甲氧西林金黃色葡萄球菌(MRSA)和屎腸球菌所占比例最高,干預前后檢出MDRO病原菌構成比較,差異無統計學意義(χ2=13.76,P=0.74)。
2.5 MDRO定植/感染情況 干預前MDRO定植/感染發病率和例次發病率分別為5.94%(84/1 413)、8.28%(117/1 413),干預后分別為5.50%(75/1 364)和6.60%(90/1 364),干預前后比較,差異均無統計學意義(均P>0.05)。
3 討論
據美國國家醫療安全網絡(NHSN)報道,美國2006—2007年與MDRO有關的感染占整個醫院感染的16%[6]。住院患者感染MDRO的現象越來越普遍,而且目前有效的抗菌藥物相對較少[7],MDRO感染引起的死亡人數不斷增加[8-9]。CDC推薦在護理MDRO定植/感染的住院患者過程中,應嚴格遵守接觸隔離預防措施[2],但是目前這些措施的依從性并不高。
Gammon等[10]研究顯示,接觸隔離措施依從率低的主要原因為可利用的時間不足、缺乏隔離衣、工作量大、風險認知不足、缺乏相關知識和健忘。本研究基線調查MDRO感染防控措施執行率低的原因主要有:(1)對MDRO防控相關知識缺乏;(2)對MDRO傳播風險認知不足;(3)人員責任分工不明確。針對以上幾個問題,干預階段采取了一系列促進防控措施落實的管理制度。對醫護人員進行MDRO防控知識專項培訓,經過相關培訓后,醫務人員對MDRO傳播方式知曉率(100.00%)、隔離措施知曉率(98.89%)和患者轉科告知率(93.33%)均高于干預前(分別為67.22%、61.11%和45.56%),為提高醫務人員執行防控措施奠定理論基礎。
醫務人員的手是MDRO感染最主要的傳播媒介[11-12]。CDC推薦醫務人員和探視者在接觸患者前后、接觸患者醫療設備或周圍環境后應進行手衛生[2],否則可能會使病原菌經醫務人員的手傳播給其他患者引起交叉感染。本研究干預階段在完善科室的手衛生設施與手衛生用品的基礎上,加強手衛生依從性暗訪和考核頻率,手衛生依從率從干預前的54.68%提高至干預后的85.34%。
干預前MDRO定植/感染的患者中僅31.65%有隔離醫囑。醫生未下達隔離醫囑,導致責任護士不知曉患者有MDRO感染/定植,在護理過程中未采取相應的接觸隔離措施,非常容易造成MDRO交叉傳播。干預階段加強對接觸隔離醫囑的監督,明確醫護責任分工(如MDRO感染/定植患者未進行接觸隔離措施,若醫生未下達隔離醫囑,則責任為主管醫生;如隔離醫囑已下達,但無接觸隔離措施,則責任為主管護士),并將責任與考核直接相關。通過此項干預措施,隔離醫囑下達率達77.94%。另外,每日各病區晨交班時強調患者MDRO檢出情況,使醫護人員進一步明確患者的MDRO定植/感染情況,從而做好接觸隔離措施。除單間隔離外,其他防控措施(隔離醫囑、床旁隔離、穿隔離衣、掛隔離標志)的依從率均明顯提高。
賈會學等[13]一項多中心研究顯示,通過對MDRO進行綜合干預后,同種病原體隔離、懸掛隔離標志、手衛生、物品專用依從率均有所提高,MDRO醫院感染發病率明顯下降,但單間隔離依從率無明顯改善,與本研究結果一致。因此,無單間隔離條件的醫療機構,如果做好其他各項接觸隔離措施和標準預防措施也同樣能夠有效地預防和控制MDRO的傳播。
本研究結果顯示,采取綜合干預措施后MDRO檢出率降低,但是干預前后患者MDRO定植/感染發病率、例次發病率差異無統計學意義,可能與本研究觀察時間較短、樣本量偏少有關。因此,建議擴大樣本量、延長觀察時間,進一步研究干預措施執行力的提高對MDRO定植/感染發病率的影響。
[1] Kanerva M, Ollgren J, Hakanen AJ, et al. Estimating the burden of healthcare-associated infections caused by selected multidrug-resistant bacteria Finland, 2010[J]. Antimicrob Resist Infect Control, 2012, 1(1): 33.
[2] Siegel JD, Rhinehart E, Jackson M, et al. 2007 Guideline for isolation precautions: preventing transmission of infectious agents in health care settings[J]. Am J Infect Control, 2007, 35(10 Suppl 2): S65-S164.
[3] Slota M, Green M, Farley A, et al. The role of gown and glove isolation and strict handwashing in the reduction of nosocomial infection in children with solid organ transplantation[J]. Crit Care Med, 2001, 29(2): 405-412.
[4] Safdar N, Marx J, Meyer NA, et al. Effectiveness of preemptive barrier precautions in controlling nosocomial colonization and infection by methicillin-resistantStaphylococcusaureusin a burn unit[J]. Am J Infect Control, 2006, 34(8): 476-483.
[5] 李春輝, 吳安華. MDR、XDR、PDR多重耐藥菌暫行標準定義——國際專家建議[J]. 中國感染控制雜志, 2014, 13(1):62-64.
[6] Hidron AI, Edwards JR, Patel J, et al. NHSN annual update: antimicrobial-resistant pathogens associated with healthcare-associated infections: annual summary of data reported to the National Healthcare Safety Network at the Centers for Disease Control and Prevention, 2006-2007[J]. Infect Control Hosp Epidemiol, 2008, 29(11): 996-1011.
[7] Boucher HW, Talbot GH, Bradley JS, et al. Bad bugs, no drugs: no ESKAPE! An update from the Infectious Diseases Society of America[J]. Clin Infect Dis, 2009, 48 (1): 1-12.
[8] Peleg AY, Seifert H, Paterson DL.Acinetobacterbaumannii: emergence of a successful pathogen[J]. Clin Microbiol Rev, 2008, 21(3): 538-582.
[9] Gaynes R, Edwards JR. National Nosocomial Infections Surveillance System. Overview of nosocomial infections caused by gram-negative bacilli[J]. Clin Infect Dis, 2005, 41(6): 848-854.
[10] Gammon J, Morgan-Samuel H, Gould D. A review of the evidence for suboptimal compliance of healthcare practitioners to standard/universal infection control precautions[J]. J Clin Nurs, 2008,17(2): 157-167.
[11] Albrich WC, Harbarth S. Health-care workers: source, vector or victim of MRSA?[J]. Lancet Infect Dis, 2008, 8(5): 289-301.
[12] Duckro AN, Blom DW, Lyle EA, et al. Transfer of vancomycin-resistant enterococci via health care worker hands[J]. Arch Intern Med, 2005, 165(3): 302-307.
[13] 賈會學,胡必杰,吳安華,等.多重耐藥菌感染干預效果多中心研究[J].中國感染控制雜志,2015,14(8):524-529.
(本文編輯:孟秀娟)
Effect of improving compliance to multidrug-resistant organism prevention and control measures on reducing MDRO healthcare-associated infection
LIYing,XUWen,GEWei,MUCai-ni,CAOXiao-qin,FANShan-hong
(TangduHospital,FourthMilitaryMedicalUniversity,Xi’an710038,China)
Objective To understand the effect of improving compliance rate to multidrug-resistant organism (MDRO) prevention and control measures on reducing MDRO transmission in the intensive care unit (ICU). Methods All patients in 5 ICUs of a hospital in March-June 2014 were chosen, March 1-April 30, 2014 was baseline survey stage, May 1-June 30, 2014 was intervention stage (comprehensive intervention measures were taken), the implementation of patients contact isolation measures, as well as awareness of MDRO-related knowledge among health care workers(HCWs) in 5 ICUs before and after intervention were compared respectively. Results HCWs’ awareness rates of MDRO transmission modes, contact isolation measures, and informing of department transfer after intervention were all higher than before intervention(100.00% vs 67.22%, 98.89% vs 61.11%, 93.33% vs 45.56%, respectively); except single-room isolation,compliance rates to other prevention and control measures(including doctor’s advice on isolation, bedside isolation, wearing isolation gowns, adding isolation logo) were all higher than before intervention(>70% vs <50%, allP<0.01). Detection rate of MDROs after intervention was lower than before intervention (7.16%[90/1 257] vs 9.65%[117/1 212],χ2=5.00,P=0.03). Conclusion Comprehensive intervention measures can improve HCWs’ compliance to prevention and control measures on MDROs, and reduce the transmission of MDROs.
multidrug-resistant organism; prevention and control; intervention measure; compliance
2016-06-15
陜西省科學技術研究發展計劃項目(2012K18-01-05);第四軍醫大學唐都醫院科技創新發展基金臨床研究項目(2014LCYJ006)
李穎(1984-),女(漢族),陜西省渭南市人,公共衛生醫師,主要從事醫院感染預防與控制研究。
范珊紅 E-mail:fanshanhong_001@163.com
10.3969/j.issn.1671-9638.2017.02.006
R181.3+2
A
1671-9638(2017)02-0126-04

