痛風方聯合非布司他對痛風高尿酸血癥患者IL-6及IL-12的影響研究※
劉 歡 舒建龍 龐學豐 蒙宇華 吳燕紅
(廣西中醫藥大學附屬瑞康醫院風濕免疫科,廣西 南寧 530011)
痛風方聯合非布司他對痛風高尿酸血癥患者IL-6及IL-12的影響研究※
劉 歡 舒建龍 龐學豐△蒙宇華 吳燕紅
(廣西中醫藥大學附屬瑞康醫院風濕免疫科,廣西 南寧 530011)
目的 觀察痛風方聯合非布司他對痛風高尿酸血癥患者外周血白細胞介素6(IL-6)及IL-12水平的影響。方法 將66例痛風高尿酸血癥患者隨機分為2組,對照組33例予非布司他治療,治療組33例在對照組治療基礎上加痛風方治療,2組療程均為12周。檢測2組治療前后血清IL-6、IL-12水平變化,以及腎功能指標血肌酐(SCr)、血尿素氮(BUN)、血尿酸(BUA)水平變化。結果 2組治療后IL-6、IL-12水平均較本組治療前明顯下降(P<0.05),且治療組低于對照組(P<0.05)。治療后2組SCr、BUA及治療組BUN均較本組治療前下降(P<0.05),且治療組BUA較對照組下降明顯(P<0.05)。結論 痛風方聯合非布司他能明顯降低痛風高尿酸血癥患者IL-6、IL-12、及BUA水平,對腎功能有一定的保護作用,值得臨床推廣。
痛風;高尿酸血癥;中西醫結合療法;白細胞介素類
痛風是尿酸鈉結晶沉積在關節導致的炎性疾病,與高尿酸血癥密切相關[1],好發于40歲以上男性及絕經后女性[2]。研究表明,高尿酸血癥患者中大約有10%的患者尿酸以鈉鹽的沉積形式引起組織炎癥反應,引發痛風發作[3]。治療痛風高尿酸血癥最重要的措施是降低尿酸。臨床報道,非布司他能降低血尿酸水平,阻止腎功能衰退,對合并腎功能不全的高尿酸血癥伴痛風患者存在長遠利益[4]。近年來大量臨床報道中醫藥治療痛風、降低尿酸有顯著的療效[5]。本研究采用痛風方聯合非布司他治療痛風高尿酸血癥33例,并與非布司他治療33例對照,觀察對患者血清炎癥因子白細胞介素6(IL-6)及IL-12的影響,結果如下。
1 資料與方法
1.1 病例選擇
1.1.1 診斷標準 符合美國風濕病學會制訂的痛風性關節炎診斷標準[6],且男性血尿酸(BUA)>420 μmol/L,女性BUA>375 μmol/L。
1.1.2 納入標準 符合診斷標準;年齡18~75歲;經飲食控制后,男性BUA> 420 μmol /L,女性BUA>375 μmol /L;近2周無痛風發作;患者知情同意,并簽署知情同意書。
1.1.3 排除標準 孕期或哺乳期婦女;肝腎功能不全者;貧血等血液系統疾病者;近1周內使用過降尿酸藥物者;有嚴重肺、肝、腦等惡性腫瘤者;近1年有活動性消化性潰瘍病史者;對研究用藥不能耐受者;慢性彌漫性結締組織病患者。
1.2 一般資料 選取2015-01—2016-04我院風濕免疫科住院(47例)以及門診(19例)患者66例,運用隨機數字表法分為2組。治療組33例,男31例,女2例;年齡20~71歲,平均(46.57±7.48)歲;病程0.3~5年,平均(2.62±1.96)年。對照組33例,男30例,女3例;年齡22~74歲,平均(44.13±9.62)歲;病程0.5~6年,平均(2.95±1.74)年。2組一般資料比較差異無統計學意義(P>0.05),具有可比性。
1.3 治療方法
1.3.1 對照組 予非布司他片(江蘇恒瑞醫藥股份有限公司,國藥準字H20130082)40 mg,每日1次口服;服用2周后,BUA仍>360 μmol/L者,可調整劑量至80 mg,每日1次口服。
1.3.2 治療組 在對照組治療基礎上加痛風方。藥物組成:蒼術15 g,黃柏10 g,牡丹皮10 g,桂枝8 g,澤瀉10 g,附子10 g,山茱萸12 g,益母草10 g,黃芪20 g,當歸10 g,芡實12 g,玉米須15 g,貓須草15 g,澤蘭12 g,三棱10 g,莪術10 g,大腹皮10 g,半邊蓮10 g,車前子10 g,甘草6 g。每日1劑,水煎取汁300 mL,分早、晚2次溫服。
1.3.3 療程 2組療程均為12周。
1.4 檢測指標 采用全自動生化分析儀檢測2組治療前后腎功能指標血肌酐(SCr)、血尿素氮(BUN)、BUA水平變化情況。采用酶聯免疫吸附測定法(ELISA)檢測2組治療前后血清IL-6、IL-12水平,并進行統計學比較,試劑盒購自武漢博士德生物工程有限公司。

2 結 果
2.1 2組治療前后SCr、BUN及BUA水平比較 見表1。
表1 2組治療前后SCr、BUN及BUA比較


組 別n治療前治療后治療前組間比較檢驗值P值治療前后組內比較檢驗值P值治療后組間比較檢驗值P值SCr(μmol/L)治療組33102.51±18.4492.59±19.08t=0.7100.240>0.05t=2.1480.018<0.05t=0.4530.326>0.05對照組3399.14±20.0790.47±18.92t=1.8060.038<0.05BUN(mmol/L)治療組336.74±1.296.14±1.55t=0.2780.391>0.05t=1.7090.046<0.05t=0.6670.254>0.05對照組336.82±1.036.38±1.37t=1.4750.073>0.05BUA(μmol/L)治療組33586.42±85.64328.91±79.08t=0.2310.490>0.05t=12.6900.000<0.01t=1.9340.029<0.05對照組33591.27±84.71366.85±80.30t=11.0450.000<0.05
由表1可見,2組治療前SCr、BUN及BUA比較差異均無統計學意義(P>0.05)。治療后,2組SCr、BUA及治療組BUN均較本組治療前下降(P<0.05),對照組BUN無明顯變化(P>0.05)。治療后治療組BUA低于照組(P<0.05),但2組BUN、SCr水平無統計學差異(P>0.05)。
2.2 2組治療前后IL-6及IL-12水平比較 見表2。
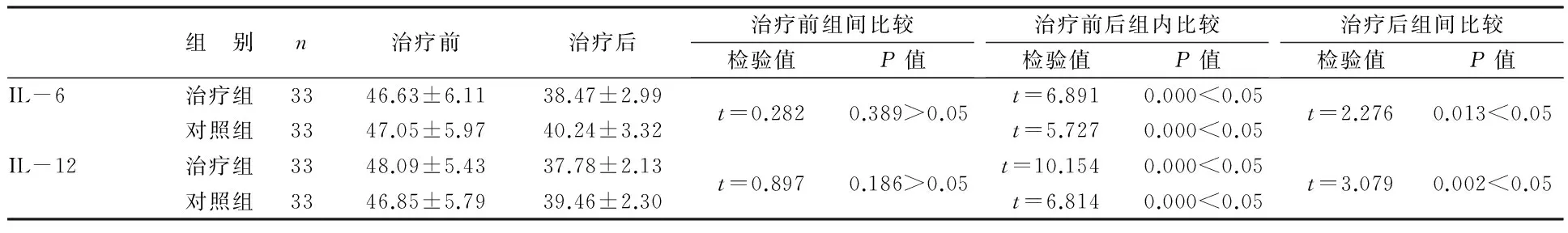
表2 2組治療前后IL-6及IL-12水平比較

組 別n治療前治療后治療前組間比較檢驗值P值治療前后組內比較檢驗值P值治療后組間比較檢驗值P值IL-6治療組3346.63±6.1138.47±2.99t=0.2820.389>0.05t=6.8910.000<0.05t=2.2760.013<0.05對照組3347.05±5.9740.24±3.32t=5.7270.000<0.05IL-12治療組3348.09±5.4337.78±2.13t=0.8970.186>0.05t=10.1540.000<0.05t=3.0790.002<0.05對照組3346.85±5.7939.46±2.30t=6.8140.000<0.05
由表2可見,治療前2組IL-6及IL-12水平比較差異無統計學意義(P>0.05)。治療后2組IL-6、IL-12水平均較本組治療前明顯下降(P<0.05),且治療組低于對照組(P<0.05)。
3 討 論
現代醫學認為,痛風的重要生化基礎是高尿酸血癥,高尿酸血癥是引起痛風的一個重要危險因素[7]。尿酸是一種弱酸,是超過溶解度的尿酸鹽析出的針狀結晶,是人嘌呤代謝的產物,在人體內每日的生成量和排泄量大約是相等的。當體內嘌呤代謝紊亂或攝入嘌呤過多導致體內嘌呤含量過高時,就會尿酸過多或者尿酸排泄減少,造成尿酸升高。尿酸過高,沉積在溫度較低的遠端肢體和酸度較高的關節腔中的尿酸鹽結晶被吞噬細胞、白細胞吞噬, 可破壞細胞的溶酶體等細胞器, 釋放出蛋白水解酶、激肽、組胺、趨化因子等物質,引起局部血管擴張、滲透性增加、血漿滲出、白細胞集聚、炎癥因子釋放等炎癥反應,周圍組織被溶解侵蝕,從而發生痛風性關節炎癥反應[8]。美國風濕病學會和歐洲抗風濕病聯盟建議BUA水平<360 μmol/L是治療痛風和持續高尿酸導致痛風反復發作、痛風石沉積和關節破壞的最理想指標,能最終停止甚至逆轉尿酸鹽結晶沉積和臨床癥狀、體征[9]。理論上,通過飲食控制最多只能降低人體內20%的尿酸,所以藥物干預對部分明顯的痛風高尿酸血癥患者來說是十分有必要的[10]。
非布司他是一種新型非嘌呤類黃嘌呤氧化酶(XO) 選擇性抑制劑,能夠高效且同時地抑制還原型和氧化型黃嘌呤氧化酶,具有明確的降BUA作用,且作用較別嘌醇更強[11]。非布司他口服給藥后吸收迅速,1 h血藥濃度達到80%以上,49%通過腎臟排泄、45%通過糞便排泄,屬于雙通道排泄[12],與蛋白結合率有關的藥物相互作用的可能性較小,對于諸如布洛芬、華法林、吲哚美辛以及萘普生等藥代動力學無影響。多項隨機、對照臨床試驗證實,年齡、性別對非布司他的藥代動力學、藥效學及安全性無顯著影響,對痛風高尿酸血癥的治療具有很好的療效及安全性[13-16]。
中醫學認為,痛風高尿酸血癥屬痹證、熱痹、歷節病、白虎歷節等范疇[17]。發病機制為稟賦不足、年高體衰,脾腎不足,精不化氣,脾運化水濕功能、腎陽蒸騰氣化功能失常,濕濁內生,蘊結生熱,濕濁熱毒趨下為患;或飲食不節,過食膏粱辛辣厚物,礙脾滯胃,釀生濕濁,難以排泄,久滯脈中,隨氣血鼓動,留滯關節,阻礙氣血。由此可見,濕熱、痰濁、瘀血痹阻為痛風高尿酸血癥發病的重要病理因素。治宜清利濕熱,化痰通絡,活血定痛。本研究所用痛風方是由《丹溪心法》中的痛風方加減而成,方中蒼術燥濕健脾,祛風散寒,黃柏清下焦濕熱,功擅清熱、解毒、燥濕,與蒼術共為君藥;澤蘭、牡丹皮、當歸、三棱、莪術活血化瘀,通絡止痛,為臣藥;佐以桂枝溫通血脈,附子溫腎助陽化氣,益母草、澤瀉、車前子、大腹皮、玉米須、半邊蓮、貓須草利濕泄濁,山茱萸、黃芪、芡實補氣健脾祛濕;使以甘草調和諸藥。諸藥合用,共奏清利濕熱、化痰通絡、活血定痛之功。現代藥理研究表明,蒼術、黃柏可抗炎、解熱、鎮痛,降低毛細血管通透性,改善局部酸性環境以利于痛風石溶解[18],黃柏還能降低尿酸性腎病大鼠的BUA,抑制相關炎性反應[19];潘志等[20]研究表明,黃柏、蒼術水提物可以抑制次黃嘌呤氧化酶和黃嘌呤氧化酶活性。澤蘭、當歸可抑制尿酸合成,澤瀉、車前子有降壓、促進尿酸排泄等作用[21]。由此可見,現代藥理研究也證實,痛風方對痛風高尿酸血癥患者的治療具有積極意義。
研究表明,炎性細胞因子在關節炎性疾病中大量存在,且作用廣泛,與痛風性關節炎有著密切的關系[17]。國外研究顯示,IL-2、IL-6等炎性細胞因子能夠誘導關節軟骨細胞外基質降解并破壞軟骨,促進前列腺素E2(PGE2)的合成、白細胞與單核細胞的趨化和吞噬能力及尿酸在關節局部的沉積[22-23]。IL-6主要由T 淋巴細胞和單核-巨噬細胞產生,是體內多種有核細胞產生的前炎癥因子。國內相關研究顯示,IL-6在高尿酸狀態下(關節損害的早期)具有致炎作用,在痛風急性期呈明顯高表達,與痛風性關節炎的骨破壞有關系,可作為判斷痛風性關節炎病情活動性和嚴重程度的指標[24-26]。IL-12是促炎性細胞因子,具有促進干擾素產生、提高自然殺傷細胞的細胞毒作用和痛風炎癥反應等作用[27-28]。因此,痛風高尿酸血癥的治療不要忽略了降低致炎性細胞因子的作用。本研究結果表明,痛風方聯合非布司他治療痛風高尿酸血癥SCr、BUA及BUN均較本組治療前下降(P<0.05),且BUA較對照組下降更明顯(P<0.05);2組IL-6及IL-12均降低(P<0.05),且治療組較對照組效果顯著(P<0.05)。提示降低炎癥細胞因子水平對保護腎功能、降低BUA有一定的益處,值得臨床應用。
[1] 張貴江.非布司他和別嘌醇治療痛風有效性和安全性的meta分析[J].中國醫藥指南,2015,13(36):73-74.
[2] Lawrence RC,Felson DT,Helmick CG,et al. Estimates of the prevalence of arthritis and other rheumatic conditions in the United States.Part II[J].Arthritis Rheum,2008,58(1):26-35.
[3] 韓瑩,朱翊,傅得興.非布司他治療高尿酸血癥伴痛風的藥理與臨床評價[J].中國新藥與臨床雜志,2010,29(8):635-638.
[4] 楊婷,路敏,周穎,等.非布司他和別嘌醇治療痛風有效性和安全性的Meta分析[J].中國臨床藥理學雜志,2015,31(2):122-126.
[5] 佟穎,文慧麗,李一平,等.痛風及高尿酸血癥近年來的中醫治療研究進展[J].風濕病與關節炎,2015,4(11):66-69.
[6] 何培根.風濕性疾病的診斷標準[J].臨床內科雜志,1995,12(3):13-14.
[7] Zhu Y,Pandya BJ,Choi HK.Prevalence of gout and hyperuricemia in the US general population:the National Health and Nutrition Examination Survey 2007-2008[J].Arthritis Rheum,2011,63(10):3136-3141.
[8] 張劍勇,王輝,謝靜靜,等.痛風泰顆粒對急性痛風大鼠IL-1、IL-6及TNF-α含量的影響[J].新中醫,2016,48(12):201-203.
[9] Sarawate CA,Patel PA,Schumacher HR,et al.Serum urate levels and gout flares:analysis from managed care data[J].J Clin Rheumatol,2006,12(2):61-65.
[10] 陳翔,蔡嚇明,陳國勇.非布司他治療痛風伴高尿酸血癥療效觀察[J].中外醫學研究,2015,13(34):34-36.
[11] 孫兆姝,張卉卉,包永睿,等.二妙丸對痛風癥大鼠血清炎癥介質的影響研究[J].遼寧中醫雜志,2016,43(2):412-414.
[12] 魏斐菲.對痛風伴高尿酸血癥患者采取非布司他治療的效果研究[J].中國現代藥物應用,2016,10(21):84-85.
[13] 張彩香,林章梅,梁艷玲,等.高尿酸血癥患者血清白介素-6和轉化生長因子-β1水平及應用非布司他治療前后的變化[J].中國糖尿病雜志,2016,24(3):250-253.
[14] 任慶杰,張旭環,陳鐵霽,等.非布司他治療痛風伴高尿酸血癥、腎功能不全患者的療效觀察[J].現代實用醫學,2016,28(9):1174-1176.
[15] Frampton JE.Febuxostat:a review of its use in the treatment of hyperuricaemia in patients with gout[J].Drugs,2015,75(4):427-438.
[16] 韓鳳.非布司他治療痛風伴高尿酸血癥的臨床效果[J].中國當代醫藥,2015,22(33):81-82.
[17] 陸玉鵬,李義凱,李益軍,等.痛風定膠囊聯合非布司他對高尿酸血癥患者炎性因子的影響及其療效[J].中國生化藥物雜志,2016,36(1):59-61.
[18] 樂楓,錢耀明,顧寶妹.急痛湯治療急性痛風110例療效觀察[J].河北中醫,2003,25(2):108.
[19] 劉睿,胡家才.黃柏對尿酸性腎病大鼠的影響及機制[J].武漢大學學報:醫學版,2011,32(2):180-182.
[20] 潘志,段富津,王穎航,等.黃柏與蒼術提取物對高尿酸血癥小鼠血尿酸的影響[J].時珍國醫國藥,2008,19(1):112-113.
[21] 李娟,紀偉.中醫藥治療痛風性關節炎的研究進展[J].實用中醫藥雜志,2009,25(2):134-135.
[22] Perez-Ruiz F,Calabozo M,Herrero-Beites AM,et al.Improvement of renal function in patients with chronic gout after proper control of hyperuricemia and gouty bouts[J].Nephron,2000,86(3):287-291.
[23] Terkeltaub R,Sundy JS,Schumacher HR,et al.The IL-1 inhibitor rilonacept in treatment of chronic gouty arthritis: results of a placebo-controlled, monosequence crossover, nonrandomized, single-blind pilot study[J].Ann Rheum Dis,2009,68(10):1613-1617.
[24] 羅進林,羅紅彤,羅利飛.當歸拈痛湯對急性痛風性關節炎患者血漿炎癥細胞因子的影響[J].福建中醫藥,2012,43(5):17-18.
[25] 姜春曉.當歸拈痛湯聯合苯溴馬隆對急性痛風性關節炎患者血清炎癥因子水平的影響及療效觀察[J].新中醫,2015,47(11):99-100.
[26] 劉圳奮,馬紅霞,李秀寧,等.痛風性關節炎與高尿酸血癥炎性細胞因子水平比較[J].西部中醫藥,2014,27(8):157-158.
[27] 王小茜,邢陳,黎燕,等.IL-12家族在自身免疫性疾病中的免疫調節作用[J].軍事醫學,2015,39(8):637-640.
[28] 樸成玉,房城,安柏松,等.丹溪痛風膠囊對大鼠急性痛風性關節炎IL-12及COX-2表達的影響[J].中醫藥信息,2012,29(4):91-92.
(本文編輯:曹志娟)
10.3969/j.issn.1002-2619.2016.11.018
※ 項目來源:廣西高校中青年教師基礎能力提升項目(編號:KY2016YB232)
劉歡(1981—),男,主治醫師,碩士。研究方向:風濕病的防治。
R589.706;R446.122
A
1002-2619(2016)11-1676-04
2016-06-08)
△ 通訊作者:廣西中醫藥大學附屬瑞康醫院風濕免疫科,廣西 南寧 530011

