有關烴類燃燒重要規律剖析
■寧夏回族自治區固原一中 李曉峰
?
有關烴類燃燒重要規律剖析
■寧夏回族自治區固原一中 李曉峰
一、關于氣態烴類燃燒前后氣體體積變化規律
1.燃燒后生成水為液態(即t<100 ℃)時的規律。

結論:如果生成水為液態時,氣態烴燃燒后氣體體積減小,且減小值與烴中的氫原子數目有關,與碳原子數目無關。
2.燃燒后生成水為氣態(即t≥100 ℃)時的規律。
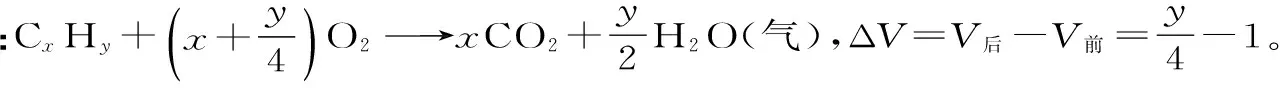
結論:(1)當ΔV>0時,y>4, 即y>4時,燃燒后氣體體積增大。
(2)當ΔV<0時,y<4, 即y<4時,燃燒后氣體體積減小。
(3)當ΔV=0時,y= 4, 即y= 4時,燃燒后氣體體積不變。

例1 兩種氣態烴以任何比例混合,在105 ℃時1 L該混合烴與9 L氧氣混合,充分燃燒后恢復到原狀態,所得氣體體積仍為10 L。下列各組烴中不符合條件的是( )。
A.CH4C2H4B.CH4C3H6
C.C2H4C3H4D.C3H6C2H2
解析:由題意知:兩種氣態烴無論以任何比例混合,燃燒前后ΔV=0(t=105 ℃),即要求符合:烴分子(或烴的平均化學式)中氫原子數為4,則選項A、C符合題意,選項B始終不符合,其平均化學式中氫原子數始終大于4,而D中只有當n(C2H6)∶n(C3H6)=1∶1混合時,才符合題意,所以不符合條件的是B、D。
例2 120 ℃時,在密閉容器中,下列烴各1 mol與氧氣充分燃燒后,溫度恢復到120 ℃,壓強保持原狀,其體積增大最大的是( )。
A.CH4B.C2H2
C.C2H6D.C4H8

二、關于烴類燃燒時耗氧量規律
1.等物質的量的烴完全燃燒耗氧量規律。
2.等質量的烴完全燃燒耗氧量規律。
(1)等質量的烴完全燃燒,H的質量分數越大,則耗氧量越多,生成H2O的量越多,生成CO2的量越少(因為12 g C消耗1 mol O2, 12 g H消耗3 mol O2)
例3 等質量的下列烴完全燃燒耗氧量由大到小的順序是____。
(1)C2H6(2)C2H4(3)C3H8(4)聚乙烯 (5) C4H6

例4 1 mol CxHy(烴)完全燃燒需要5 mol O2,則x與y之和可能是( )。
A.x+y=5 B.x+y=7
C.x+y=11 D.x+y=9

三、關于烴類完全燃燒后生成物量值的大小關系規律
1.單一烴類完全燃燒生成物量值的大小關系。

結論:n(CO2) 結論:n(CO2)=n(H2O) 。 結論:n(CO2)>n(H2O),CO2比H2O多1 mol。 結論:n(CO2)>n(H2O),CO2比 H2O多3 mol。 利用上述規律,可由生成物量值的大小關系初步推斷單一烴的類型,也可綜合分析兩類烴的組成情況。 例5 某烴完全燃燒后,生成的物質的量之比為n∶(n-1),此烴可能是( )。 A.烷烴 B.單烯烴 C.炔烴 D.苯的同系物 解析:借助上述通式分析,由生成CO2和H2O 的關系式知,本題正確答案為C。 2.混合烴類完全燃燒生成物量值的大小關系與混合烴種類關系。 (1)當n(CO2) 烴,其組成可能有:烷烴,烷烴和烯烴,烷烴和炔烴,烷烴、烯烴和炔烴。在前兩種情況下,則有:n(烷)=n(H2O)-n(CO2);在后兩種情況中,則有:n(烷)-n(炔)=n(H2O)-n(CO2)。 (2)當n(CO2)=n(H2O)時,其組成可能有:烯烴,烷烴和炔烴,烷烴、烯烴和炔烴。在后兩種情況中,則有:n(烷)=n(炔)。 (3)當n(CO2)>n(H2O)時,其情況較為復雜,如果肯定無芳香烴,其組成可能有:炔烴,烯烴和炔烴,烷烴、烯烴和炔烴。在前兩種情況下,則有:n(炔)=n(CO2)-n(H2O);在后兩種情況中,n(烷)-n(炔)=n(H2O)-n(CO2)。 例6 由兩種烴組成的混合物,已知其中之一為烯烴,燃燒1 mol該混合物,測得產生CO24.0 mol,H2O 4.4 mol,試求混合物的組成情況。 解析:因為n(H2O)>n(CO2),說明另一烴一定為烷烴,又因為烯烴燃燒后,生成物n(H2O)=n(CO2),所以混合物中n(烷)=n(H2O)-n(CO2)=4.4-4.0=0.4 mol,則烯烴為0.6 mol。設烷烴CxH2x+2,烯烴為CyH2y,則有如下關系:0.4x+0.6y=4,即2x+3y=20。則有:(1)x=1時,y=6,即為甲烷、己烯。(2)x=4時,y=4,即為丁烷、丁烯。(3)x=7時,y=2,即為庚烷、乙烯。 例7 任取兩種烴,混合后點燃,如果生成的CO2的物質的量大于生成H2O的物質的量,則兩種烴的組合不可能是( )。 A.烷烴和烯烴 B.烷烴和炔烴 C.烯烴和炔烴 D.炔烴和苯的同系物 解析:由上述各類烴燃燒后產物量值關系知:烷烴n(CO2) (責任編輯 謝啟剛)


