鹽水濃度對鑄造鋁合金腐蝕行為的影響*
陳 林,石偉和,劉春柳
(百色學院材料科學與工程學院,廣西 百色 533000)
?
鹽水濃度對鑄造鋁合金腐蝕行為的影響*
陳林,石偉和,劉春柳
(百色學院材料科學與工程學院,廣西百色533000)
鋁合金材料的表面氧化薄膜很容易受到氯離子的腐蝕從而減少其使用壽命。試驗采用浸泡法研究了鑄造鋁合金A356.2在低濃度NaCl溶液中的腐蝕行為,通過不同濃度NaCl溶液腐蝕情況進行對比,隨著濃度的增加,腐蝕會逐漸加劇,而在2%~4%NaCl濃度下,腐蝕較為平緩,沒有因為濃度的增加而產生明顯的加劇腐蝕,在4%濃度后會有明顯的腐蝕加劇現象。
鋁合金A356.2;點腐蝕;NaCl濃度
鋁產業的發展和汽車的發展息息相關,如今汽車鋁化率日益提高,對鋁合金車輪的耐腐蝕性能、輕量化要求也邁上了新的臺階,特別是在中國[1-2]。腐蝕是一種自發進行的現象,具體表現為材料和周圍的環境發生反應而被破壞[7]。腐蝕對我們的經濟有著巨大的危害,帶來的損失遠比想象中的多。調查顯示:腐蝕造成的經濟損失是非常嚴重的,基本上占各國國民經濟總產值的1%~5%,是自然災害損失總和的6倍。腐蝕就像是金屬材料在“患病”,要想控制或者減少金屬的腐蝕損失,就必須要了解金屬腐蝕行為是如何進行的,通過了解金屬的腐蝕行為從而應用防腐蝕知識和技術可以將腐蝕的損失減少25%~30%。
環境污染日益嚴重,對汽車的使用環境要求也日益提高,汽車的使用環境也會變得較為惡劣,對于輪轂鋁合金耐腐蝕性能的研究鮮有報道,因此有必要探究鹽水對鋁合A356.2的腐蝕行為影響,這將有助于汽車車輪在鹽堿地帶、沿海地區、海洋大氣環境下使用壽命的評估,對保障汽車的安全使用有重要的意義。
1 實 驗
鋁合金A356.2,主要化學成分(w%)為:Si 6.5~7.5、Ti 0.10~0.20、Sr 0.01~0.02、Mg 0.25~0.40、余量Al[19]。把試驗材料切割成塊,然后用金相打磨機和拋光機把材料打磨成試驗需要的尺寸8 mm×4 mm×2 mm。鋁合金輪轂腐蝕主要發生在鹽堿地、海洋氣候、沿海地區,Cl-離子濃度一般較低,故腐蝕溶液的濃度區間定為2%~6%(ω),而微量的雙氧水則是為了加速腐蝕。輪轂在戶外使用過程中由于摩擦、陽光的暴曬等原因,都會使得車輪的溫度高于氣溫,所以把腐蝕的溫度定為45℃,腐蝕時間為48 h。腐蝕試驗采用浸泡法,腐蝕介質分為5組,由不同濃度的NaCl和一定濃度的H2O2組成,成分含量如表1所示。分別在8 h、16 h、24 h、32 h、40 h和48 h將試樣取出,用超聲波清洗儀清洗腐蝕樣品,然后用電子天平稱量質量測量腐蝕損失狀況并用金相顯微鏡觀察腐蝕表面。

表1 腐蝕溶液化學成分
2 結果與討論
圖1中a、b、c分別是e、f、g的腐蝕前的金相圖,e為在2%NaCl濃度下的腐蝕后的金相圖,可以發現腐蝕坑點并不是很多,f是在5%NaCl濃度下的腐蝕金相圖,相對于2%濃度下腐蝕坑點分布得更為廣泛,坑點大小沒有明顯的區別,g是在6%NaCl濃度下的腐蝕后金相圖,腐蝕坑點明顯的變大,腐蝕坑得數目也開始變多變密集,說明其對低濃度的鹽水的腐蝕有一定的抵抗能力。由金相圖可以推斷鋁合金A356.2在低濃度Cl-的腐蝕下是以點腐蝕為主,其他腐蝕形態暫時沒有出現。
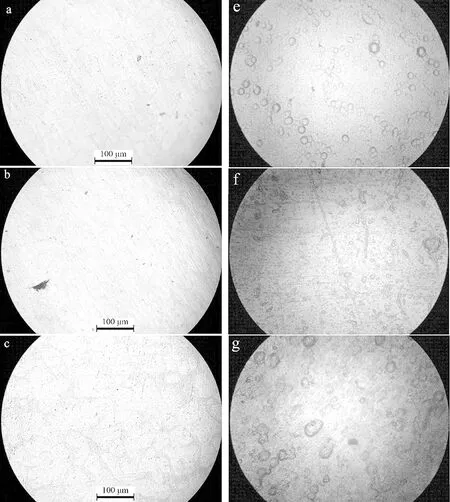
圖1 腐蝕前后金相圖
試樣的失重作為評價腐蝕程度主要參考標準,并以此標準來研究溶液對試樣腐蝕行為的影響,各個濃度下的試樣失重與時間的關系曲線如圖2所示。
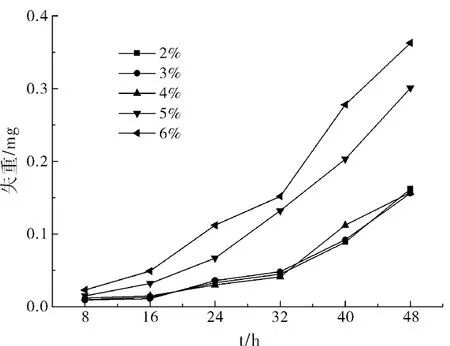
圖2 失重曲線
由圖2可以看出在32 h前,由于鋁合金表面氧化薄膜的關系,腐蝕的速率比較緩慢,在32 h以后由于Cl-和Al(OH)3發生反應生成AlCl3,而AlCl3的水解則會使溶液的pH變越來越低,使得腐蝕速率增加。在同一時間內5%和6%濃度下的試樣腐蝕速率明顯高于4%以下的腐蝕速率,說明了Cl-的濃度是決定腐蝕速率的關鍵因素。
經過48 h的腐蝕后,試樣經過處理后稱量得到溶液濃度與試樣的腐蝕速率關系如圖3所示。
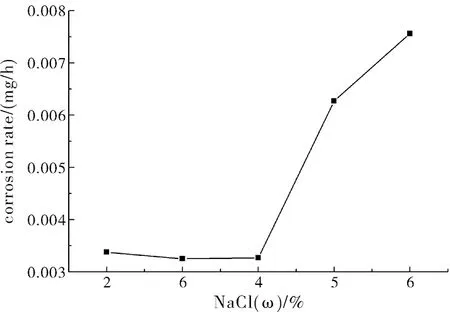
圖3 鋁合金A356.2的腐蝕速率曲線
由圖3可以看出來在4%濃度前腐蝕的速率和腐蝕失重都相差不大,在4%之后腐蝕的速率和腐蝕失重都有明顯的提升,說明4%濃度是鋁合金A356.2腐蝕的一個臨界點。再結合金相圖e表明鋁合金的氧化薄膜在低濃度鹽水下發揮出了很好的防腐蝕作用,高于4%之后鋁合金的抗腐蝕能力會變的相當弱,使得鋁合金的基體遭到破壞。
不管是在溶液還是大氣環境下,鋁合金發生點腐蝕的主要原因都是和Cl-發生反應,在鋁合金發生腐蝕的產物中硫酸鹽腐蝕排在第一,而氯化產物就排在第二,足以說明Cl-在鋁合金腐蝕中的作用。在大氣環境下,Cl-主要是通過氣相的HCl、含氯的的有機氣體、海鹽等通過降雨進入江水、湖水,然后與鋁合金發生接觸產生點腐蝕,如果有應力的作用下會使得點蝕坑內產生晶間腐蝕[3]。而鋁合金發生點腐蝕的最初一步是液膜中Cl-在鋁合金的表面的活性位發生吸附,在鋁合金氧化膜不完整和缺陷的地方這種現象會被增強,接下來吸附的離子會和氧化膜發生進一步的化學反應,使得鋁合金的氧化膜被削弱而進一步的直接溶解[4]。
Cl-的存在會使氧化膜被滲透,氧化膜會被破壞,因此Al3+會向外遷移。鋁合金的表面活化,點腐蝕從此開始。在點腐蝕坑處,陽極會溶解為Al3+,而在電力場的作用下Cl-會進一步向合金內部遷移。腐蝕產物中以AlCl3為主,其只要原因是Al(OH)3經過一系列的綠化步驟形成的,Al(OH)nCl3-n則是OH-和Cl-在鋁合金表面的氧化膜競爭吸附形成的產物,其反應情況如下:
(1)
腐蝕產物AlCl3的水解會使得腐蝕坑中的pH降低,使得腐蝕作用進一步的增強[5]。雙氧水的加入則是考慮到了實驗時間的問題,雙氧水會和鋁合金發生以下反應:
(2)
而Al(OH)3則會和Cl-上述式(1)的反應,故而會加速鋁合金的腐蝕,從而縮短實驗的時間,因為鋁合金的的鹽水腐蝕實驗想要得出比較明顯的實驗結果需要長達幾個月甚至上年的時間,在有雙氧水的條件下時間要短上很多。
3 結 論
鑄造鋁合金A365.2在較低濃度的NaCl溶液中的腐蝕程度很小,具有一定的抵抗能力;但是當鹽水濃度高于4%時,合金的腐蝕速率會快速的增長,這說明鋁合金的點腐蝕行為受
Cl-濃度增加影響,當Cl-離子濃度達到一個極限值后其抵抗腐蝕的能力幾乎被完全破壞,使得合金組織被腐蝕。
[1]宋鴻武,李昌海,常海平,等.高強韌鋁合金輪轂的輕量化鑄旋新工藝[J].稀有金屬,2012,4(5):630-635.
[2]姜玉波.鋁合金材料在汽車輕量化中的應用分析[J].試驗技術與試驗機,2004,44(3):31-34.
[3]徐火平,劉慧叢,朱立群,等.鹽水環境下高強鋁合金暴露面積對腐蝕行為的影響[J].材料工程,2010(05):41-46.
[4]陳文敬.高強鋁合金應力條件下的腐蝕行為及其電化學行為研究[D].長沙:中南大學,2008.
[5]Nguyen T H,Foley R T.chemical nature of aluminum corrosion -3.the dissolution mechanism of aluminum oxide and aluminum powder in various electrolytes.[J].Journal of the Electrochemical Society,1980,127(12):2563-2566.
Effect of Salt Concentration on the Corrosion of Cast Aluminium Alloy*
CHEN Lin,SHI Wei-he,LIU Chun-liu
(School of Materials Science and Engineering,Baise University,Guangxi Baise 533000,China)
The performance of surface oxide film of aluminum alloy is susceptible to corrosion of chlorine ion and reduced the service life of aluminum alloy.Alloy A356.2 were immersion in different concentrations of NaCl,the corrosion rate increased with the concentration,when the NaCl concentration was 2%to 4%,the corrosion was gentle,but when the concentration ≥4%,the phenomenon of corrosion were very evident.
A356.2 aluminum alloy; corrosion; NaCl concentration
廣西高校科學技術研究重點資助項目(2013ZD070);廣西高校科學技術研究項目(YB2014387、KY2015LX384);白色學院校級一般項目(2015KBN04);2015 年地方高校國家級大學生創新創業訓練計劃項目(201510609004)。
陳林(1987-),男,碩士,主要研究方向高性能鋁合金材料。
TG172.6+3
A
1001-9677(2016)06-0040-03

