氨基酸自動分析儀測定燕窩氨基酸組成
◎黃永連,陳曉嘉,韓秋珍(1.廣東省食品工業研究所,廣東 廣州 510308;2.廣東省質量監督食品檢驗站,廣東 廣州 510308)
氨基酸自動分析儀測定燕窩氨基酸組成
◎黃永連1,2,陳曉嘉1,2,韓秋珍1,2
(1.廣東省食品工業研究所,廣東 廣州 510308;2.廣東省質量監督食品檢驗站,廣東 廣州 510308)
本文通過鹽酸水解法處理燕窩樣品,通過日立L-8900氨基酸自動分析儀測定氨基酸含量,分析不同燕窩中氨基酸的含量及其組成。結果顯示:干燕窩的氨基酸總含量大概在43 g/100 g~49 g/100 g,新鮮的冷凍燕窩在8 g/100 g左右,燕窩中氨基酸組成相對穩定,其氨基酸比值的極差均小于1.0%。因此,氨基酸含量和氨基酸比值可為建立系統的氨基酸監測技術體系提供理論依據。
燕窩;氨基酸;氨基酸自動分析儀
多年以來,燕窩一直被認為是高檔滋補品,在一些燕窩出產地區,由于對燕窩的采摘,造成金絲燕瀕臨滅絕,加上現在環境破壞,燕子種類和數量都在減少,燕窩產量也就越來越少,物以稀為貴,造成燕窩價格高,為了牟取更多利益,有些商家在燕窩中摻雜使假、以次充好,使燕窩質量參差不齊,給市場和消費者造成了一定的混亂[1-4]。因此,有必要建立一個有效的手段對燕窩品質進行監控。
由于氨基酸是組成蛋白的基本單位,相同類型的物質蛋白和氨基酸具有相似性,通過檢測燕窩中的氨基酸,分析其中的規律建立質控的方法。氨基酸自動分析儀測定不同產地燕窩中氨基酸組成的方法的研究,本法操作簡單、靈敏度高、專一性強,可適用性強[5-7]。
1 材料與方法
1.1儀器與試劑
日立L-8900氨基酸自動分析儀、AG204電子天平、HHS-2電熱恒溫水浴鍋以及電熱恒溫干燥烘箱等。濃鹽酸、苯酚、茚三酮等:均為分析純。
1.2色譜條件
色譜柱規格:4.6×60 mm,填料為3 μm磺酸型陽離子樹脂分離柱,泵1流速0.40 mL/min,泵2流速0.35 mL/min,柱溫57 ℃,檢測器溫度135 ℃,檢測波長:第一通道570 nm,第二通道440 nm,進樣量20 μL,每個樣品分析時間約53 min。
1.3實驗方法-氨基酸的測定
(1)樣品前處理。準確稱取0.5 g(精確至0.000 1 g)燕窩樣品于水解管中,加6 mol/L鹽酸10~15 mL(視試樣蛋白質含量而定),加入新蒸餾的苯酚3~4滴,再將水解管放入冷凍劑中,冷凍3~5 min,再接到真空泵的抽氣管上,抽真空(接近0 Pa),然后充入高純氮氣;再抽真空充氮氣,重復3次后,在充氮氣狀態下封口,將已封口的水解管放在(110±1)℃的恒溫干燥箱內,水解22 h后,取出冷卻。
打開水解管,將水解液過濾后,用去離子水多次沖洗水解管,將水解液全部轉移到50 mL容量瓶內用去離子水定容。吸取濾液2 mL于50 mL燒杯中,水浴蒸干,殘留物用1~2 mL水溶解,再干燥,反復進行兩次,最后蒸干,用10 mL pH 2.2的緩沖液溶解,混勻壓濾,供儀器測定用。
(2)定量分析。準確吸取0.200 mL混合氨基酸標準,用pH 2.2的緩沖液稀釋到5 mL,此標準稀釋液濃度為2.0 nmol/20 μL,作為上機測定用的氨基酸標準,用氨基酸自動分析儀以外標法測定試樣測定液的氨基酸含量。
2 結果與分析
2.1標準曲線繪制
精確吸取18種氨基酸混合標準溶液(2.5 μmol/mL)20、40、80、160 μL和320 μL分別加入到5 mL容量瓶中,用0.02 mol/L鹽酸溶液定容至刻度,氨基酸分析儀分析,以峰面積和濃度繪制標準曲線可知:以蛋氨酸(Met)為例,線性回歸方程y=1.5×106x+15 848;相關系數:R2=1.000 0。其他16種氨基酸相關系數R2均在0.999 0~1.000 0。在氨基酸濃度為0.2~3.2 nmol/20 μL范圍內,氨基酸的質量濃度與峰面積之間具有良好的線性關系,其最低檢出限為10 pmol(見圖1)。
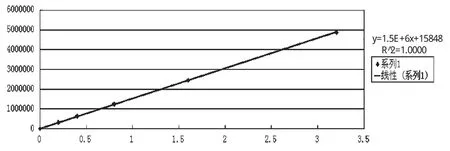
圖1 蛋氨酸(Met)濃度與峰面積曲線圖
2.2儀器精密度
配制氨基酸標準溶液2.0 nmol/20 μL,連續進樣6次。峰面積RSD%均≤1.02%,符合儀器要求。
2.3試驗方法精密度
取適量的燕窩樣品,按1.3的方法處理,分別測定其氨基酸的含量,結果見表1。
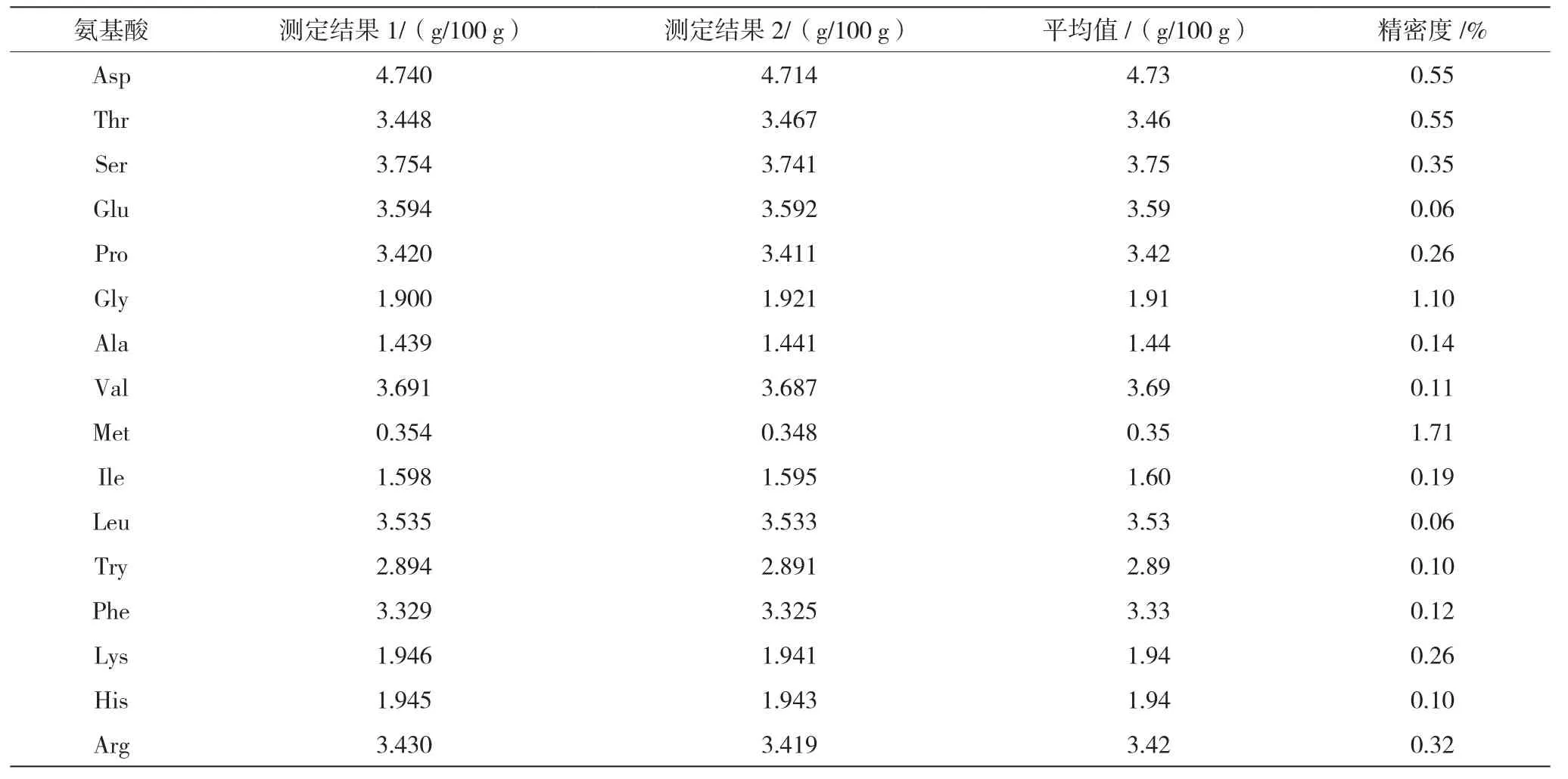
表1 精密度實驗表
2.4燕窩中氨基酸的分析研究
先對燕窩樣品進行酸水解,再通過氨基酸自動分析儀對天冬氨酸(Asp)、蘇氨酸(Thr)、絲氨酸(Ser)、谷氨酸(Glu)、脯氨酸(Pro)、甘氨酸(Gly)、丙氨酸(Ala)、纈氨酸(Val)、蛋氨酸(Met)、異亮氨酸(Ile)、亮氨酸(Leu)、酪氨酸(Try)、苯丙氨酸(Phe)、賴氨酸(Lys)、組氨酸(His)和精氨酸(Arg)等16種氨基酸進行測定,并算出氨基酸總量。圖中VIS2(440 nm)用于檢測脯氨酸,VIS1(570 nm)用于檢測除脯氨酸以外的其他氨基酸(見圖2和圖3)。
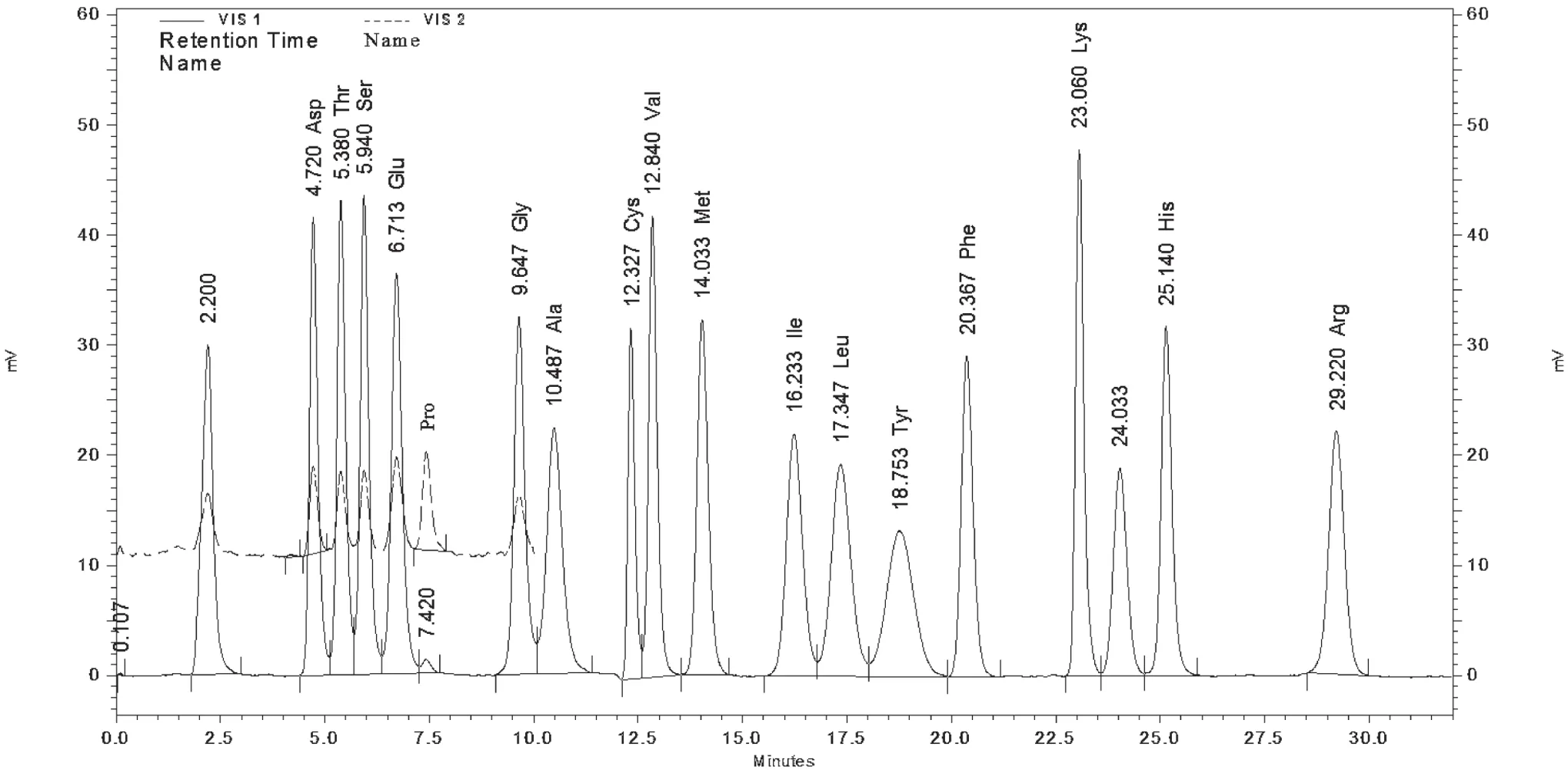
圖2 18種氨基酸混標的分離色譜圖
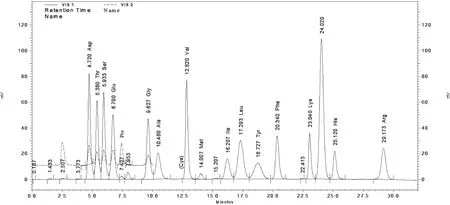
圖3 燕窩中各氨基酸的分離色譜圖
在圖2中,將原裝氨基酸液體混標稀釋后直接上機測定,可使其中的18種氨基酸(包括NH3)在32 min內得到十分理想的分離效果。在圖3中,燕窩經鹽酸水解后,其待測液中幾乎沒有雜質干擾,且各氨基酸的峰形良好,出峰時間與峰形與標準均較一致,且各種氨基酸的分離效果良好,說明此法可以較準確地獲得各種水解氨基酸含量。利用氨基酸自動分析儀對鹽酸水解后的8個樣品進行分析測定,對其獲得的結果進行整理,得到燕窩中各種氨基酸含量占氨基酸總量的比值及比值范圍,干燕窩的氨基酸含量大概在43 g/100 g~49 g/100 g,新鮮的冷凍燕窩在8 g/100 g左右。在各氨基酸組分中,天冬氨酸的含量最高,約占總量的11%;蛋氨酸的含量最低,約占0.8%;其他氨基酸的含量均在3%~9%的范圍里[5](見表2和表3)。
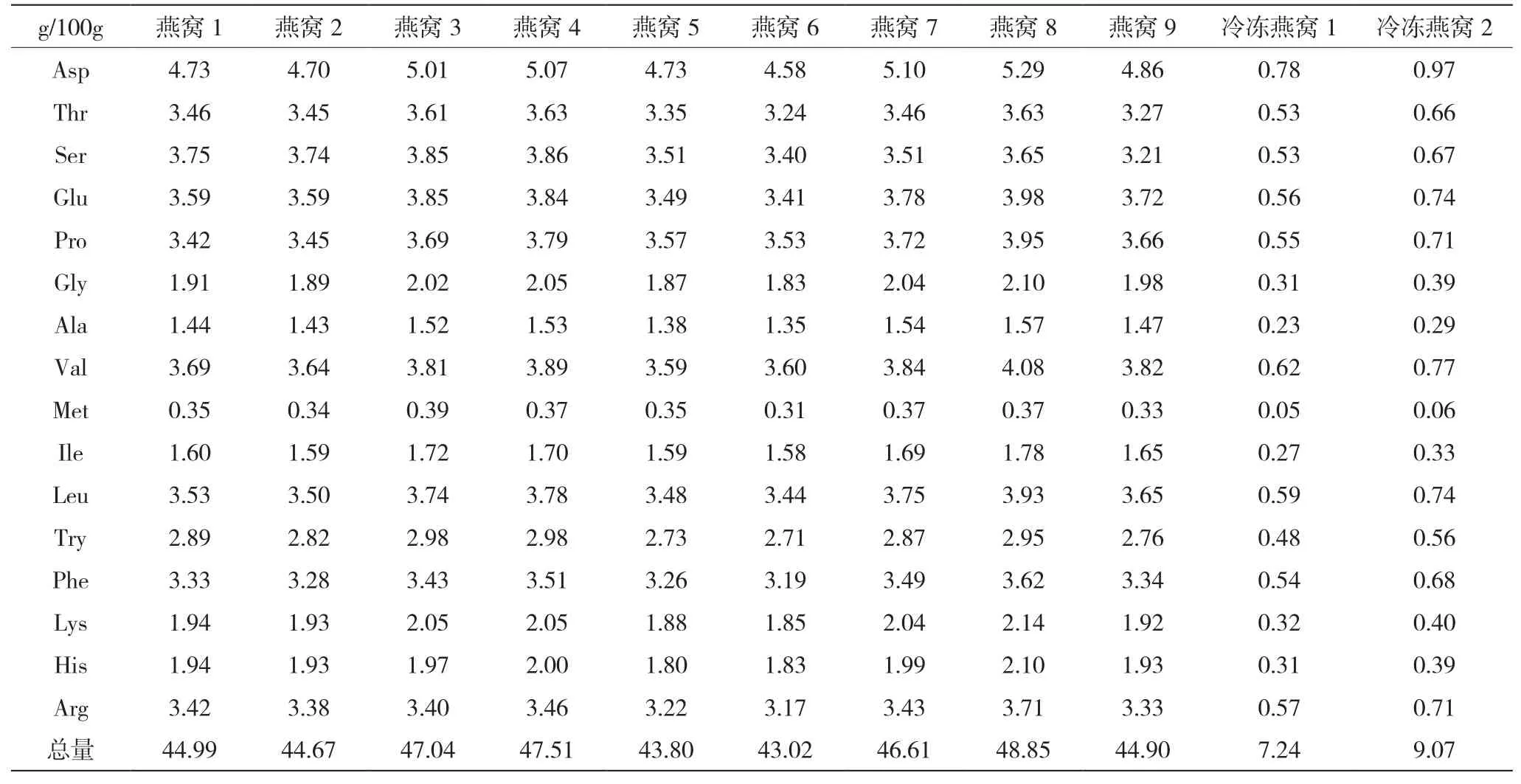
表2 燕窩樣品中各氨基酸含量及總量表
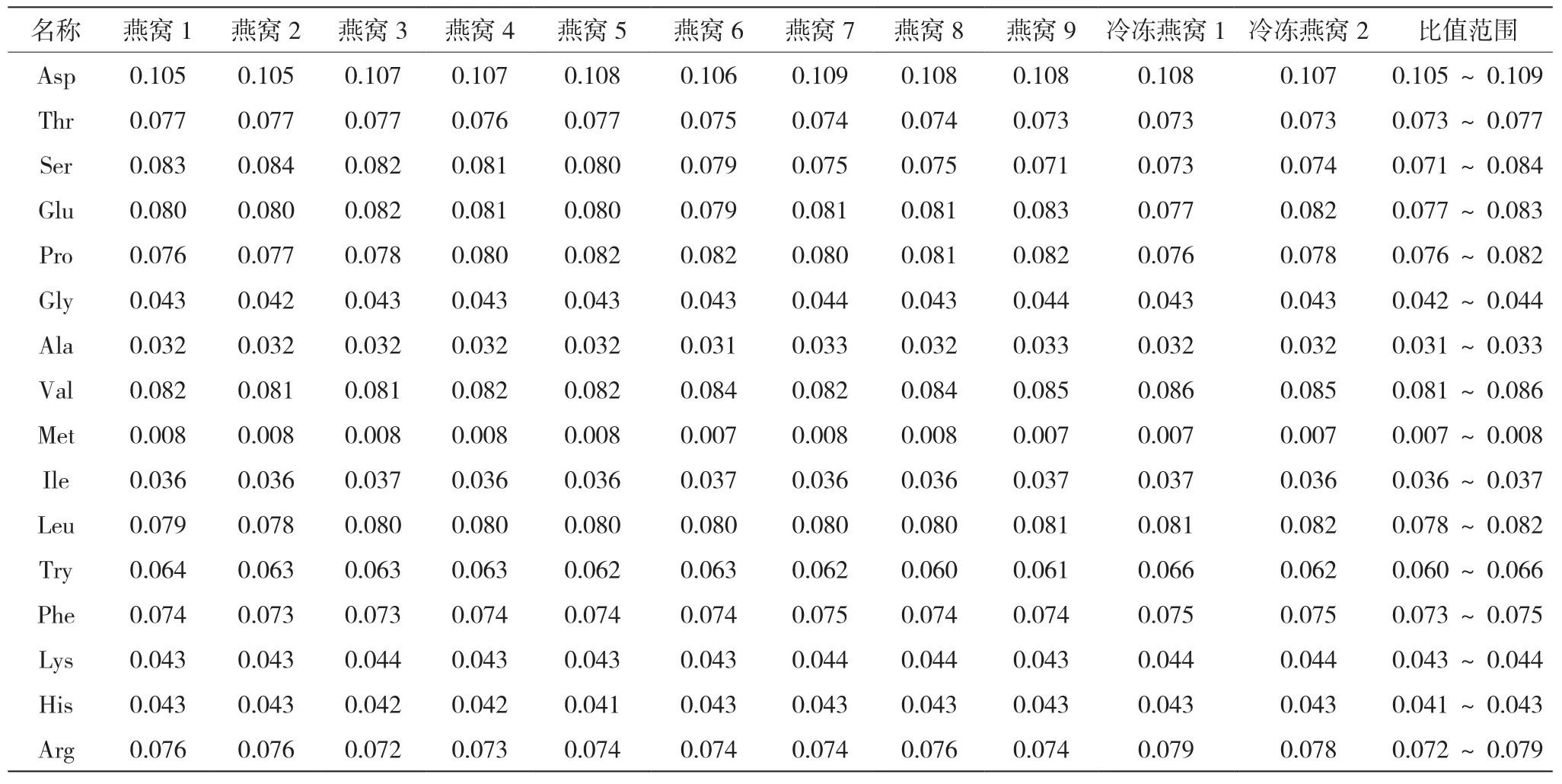
表3 燕窩樣品中各氨基酸含量占氨基酸總量的比值及范圍表
3 結論
干燕窩的氨基酸總含量大概在43~49 g/100 g,新鮮的冷凍燕窩在8 g/100 g左右,因此可以通過檢測燕窩中氨基酸的含量初步判斷燕窩中是否添加非蛋白成分,過低或過高的含量都說明存在異常情況。燕窩中各氨基酸比值的極差均小于1.0%,說明燕窩中氨基酸組成相對穩定。因此可以根據燕窩中各氨基酸的比值判斷燕窩中是否添加其他氨基酸或者蛋白質成分。
[1]中華人民共和國衛生部.GB/T 5009.124-2003 食品中氨基酸的測定[S].北京:中國標準出版社,2003.
[2]馮志強,周興起,莊俊鈺.氨基酸分析儀測定含乳飲料中游離甘氨酸的方法研究[J].現代食品科技,2007,23(7):89-91.
[3]王洪健,周興起,馮志強,等.氨基酸自動分析儀測定食品中牛磺酸的方法建立[J].現代食品科技,2012,28(3):348-350.
[4]林潔茹,周 華,賴小平.燕窩研究概述[J].中藥材,2006,29(1):85-90.
[5]朱春紅,雍 韋,徐 厲,等.燕窩真假鑒定技術研究[J].中國食品衛生雜志,2007,19(3):206-208.
[6]馮志強,許銀葉,黃永連,等.氨基酸自動分析儀測定膠原蛋白保健品中羥脯氨酸的含量[J].食品工業,2014,35(5):248-250.
[7]林 丹,莊俊鈺,黃永連,等.白燕窩的氨基酸指紋圖譜構建及識別研究[J].食品工業,2014,36(7):269-272.
Comparative Studies of Protein and Amino Acid Composition in the Cubilose
Huang Yonglian1,2, Chen Xiaojia1,2, Han Qiuzhen1,2
(1.Guangdong Food Industry Institute, Guangzhou 510308, China;2.Guangdong Food Quality Supervision and Inspection Station, Guangzhou 510308, China)
This article through the hydrochloric acid hydrolysis method to deal with samples of the cubilose by Hitachi L-8900 automatic amino acid analyzer to determine the amino acid content, analysis of different amino acid content in the cubilose and its composition. The res μLts showed that the total amino acid content of dry cubilose around 43 g/100 g ~49g/100 g, fresh frozen cubilose is controlled in 8 g/100 g,cubilose is relatively stable, the amino acid composition of the amino acid ratio, the poor are less than 1.0%. Therefore, the amino acid content and amino acid ratio can provide theoretical basis for the establishment of the system of amino acid monitoring technology system.
Amino acid; Protein; Cubilose
TS252.7
10.16736/j.cnki.cn41-1434/ts.2016.12.036

